人参皂苷Rg1对疲劳小鼠骨骼肌中TFAM和NRF-1基因表达的影响
孔凡秀,杨 琪,董佳萍,谢琳琳,王鹤霖,迟晓星
(黑龙江八一农垦大学 食品学院,黑龙江 大庆 163319)
人参皂苷Rg1是一种重要的人参皂苷单体,目前在多领域都有对人参皂苷单体的功能性研究[1-4],但在其抗疲劳作用方面的研究相对较少[5]。疲劳的产生伴随着能量的大量消耗,其中包括血糖与肌/肝糖原的消耗,同时伴随着疲劳产物的积累,机体调节协同机能失调等。
线粒体作为人体主要的产能场所,大量运动后机体内氧化磷酸化形成超氧化物等活性氧簇,这些活性氧簇的产生使线粒体机能衰退,导致膜活性下降,影响了线粒体电子的传递和氧化磷酸化的进行,导致ATP合成不足,造成机体运动能力下降,诱发运动性疲劳的发生。线粒体的功能结构与骨骼肌的功能密切相关[6],线粒体转录因子A(TFAM)为线粒体DNA的上游调节基因[7-8],TFAM能够与线粒体DNA相结合,形成一种类核复合体结构,此结构能够保护线粒体DNA(mtDNA)免受活性氧簇的损伤。作为一种由细胞核基因编码的线粒体蛋白质,除可参与线粒体的转录、复制及形成拟核结构等生物合成方面的功能外,还可以保护线粒体免受氧化损伤。核呼吸因子-1(NRF-1)参与多种核编码基因和TFAM等的表达[9]。NRF-1和TFAM等组成的信号通路在线粒体生物合成中起着重要的调节作用,参与mtDNA的转录和复制[10]。
作者通过强制小鼠力竭游泳造成小鼠疲劳运动模型,观察不同剂量人参皂苷Rg1对骨骼肌中抗氧化指标以及与线粒体生物合成密切相关的转录因子TFAM和NRF-1基因表达的调节作用,以期发现人参皂苷Rg1的抗疲劳作用及可能的作用途径。
1 材料与方法
1.1 材料与仪器
1.1.1 主要试剂人参皂苷Rg1(纯度98%):南京斯道夫生物科技有限公司产品;环磷酰胺:江苏盛迪医药有限公司产品;乳酸脱氢酶(LDH)、丙二醛(MDA)、肝/肌糖原、蛋白质定量试剂盒:南京建成生物工程研究所产品。
1.1.2 主要仪器5424高速离心机:美国Eppendorf公司产品;紫外可见分光光度计:上海INESA公司产品;酶标仪:BioTec公司产品;恒温培养箱:DRP-9162上海森信公司产品;ABI-7300 Real-time检测仪:ABI公司产品。
1.2 动物与分组
雄性BALB/c小鼠70只,2月龄,体质量18~21 g,辽宁长生生物技术有限公司提供。小鼠按体质量随机分7组,每组10只,灌胃给药前,除空白静止和空白运动组外,其他组小鼠注射环磷酰胺制作免疫抑制模型。
人参皂苷Rg1用生理盐水溶解,Rg1低(L)、中(M)、高(H)剂量组的灌胃剂量分别为12.5、25、50 mg/kg[11];空白静止组(BSG)、空白运动组(BEG)和模型组(MG)按体质量以等量生理盐水灌胃,阳性对照组(P)生理盐水溶解贞芪扶正颗粒,连续灌胃21 d。小鼠在温度为(20±2)℃、相对湿度为40%~60%、光/暗循环12 h环境下饲养。
1.3 小鼠免疫疲劳模型的建立
免疫低下和疲劳密不可分,免疫低下个体更易形成疲劳模型。将健康小鼠随机分组后,除BSG与BEG组腹腔注射生理盐水外,其余组腹腔注射环磷酰胺造模,根据文献[13-14]确定环磷酰胺剂量为30 mg/kg,连续7 d可造成小鼠免疫低下模型。每周两次进行无负重游泳训练,如出现直立性游泳、眼鼻渗血等不能顺利完成游泳者被淘汰。各实验组小鼠置于水中互不接触,不停驱赶使之不停游泳,游泳结束后尽快擦干小鼠皮毛。训练时间为20 min,周期为21 d。
1.4 小鼠负重力竭游泳实验
疲劳模型建立之后,除空白静止组外,小鼠进行负重游泳试验,末次灌胃半小时后,将小鼠尾巴根部绑紧其自身体质量5%的铅皮,放入水深35 cm、水温为(25±1)℃的游泳箱中,用秒表记录时间,沉没后10 s仍不能浮出水面,该时间为小鼠的力竭游泳时间[15-17]。
1.5 指标测定
1.5.1 疲劳和抗氧化生化指标测定小鼠处死后取肝脏、骨骼肌等组织,生理盐水漂洗后滤纸吸干,按试剂盒说明测定丙二醛(TBA法)、乳酸脱氢酶(微量酶标法)、肌/肝糖原(比色法)等生化指标。
1.5.2 小鼠骨骼肌中TFAM mRNA和NRF-1 mRNA表达水平测定取骨骼肌组织,提取总RNA,RT-PCR测定小鼠骨骼肌中TFAM mRNA和NRF-1 mRNA表达水平。
1)基因序列
管家基因引物序列:

目的基因引物序列:
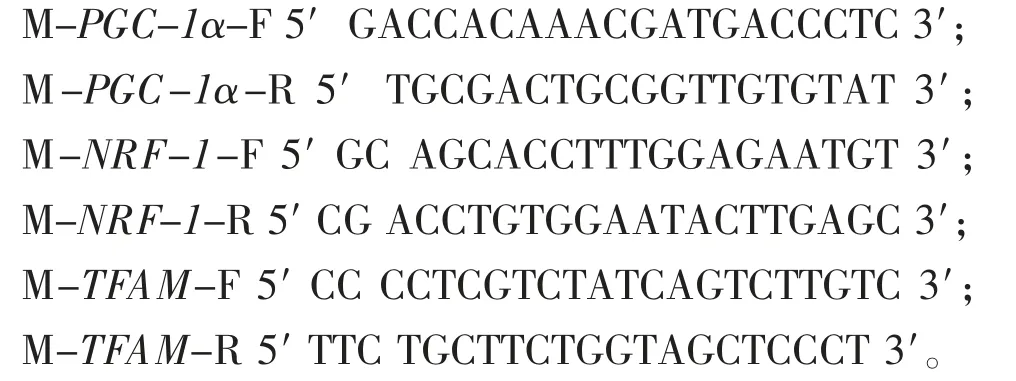
2)骨骼肌RNA提取和鉴定 取小鼠骨骼肌100 mg,加TRIZOL提取RNA。通过变性琼脂糖凝胶电泳确定RNA完整性,并在紫外分光光度计测定RNA的质量浓度及纯度。
3)逆转录反应 取3μg RNA,以oligo(dT)为引物进行反转录,进行cDNA合成。20μL体系中含有5×RT缓冲液4μL,2.5 mmol/L dNTP混合液4μL,1μL RNA酶抑制剂,MMLV反转录酶1 μL,3.5μmol/L oligo(dT)引物1μL,RNA 3 pg,反应条件:37℃1 h,然后95℃保持5 min,冰上放置5 min,备用。
4)荧光定量PCR反应 样品按以下反应体系进行:10×PCR缓冲液2.5μ,MgCl2溶液3 pL,dNTP混合液3 pL,Taq聚合酶3 U,0.25 X Sybergreen,上游引物F(20 pmol/L)0.5 pL,下游引物R(20μmol/L)0.5 pL,cDNA 1μL,加ddH2O至总体积为25μL。反应条件为:95℃反应20 s,60℃反应20 s,72℃反应20 s,87℃反应10 s,共40个循环。反应结束后,电脑自动分析荧光信号并将其转换为Ct值。结合RNA浓度,将荧光定量PCR定量结果进行换算,得出待测样本的RNA表达量。
5)PCR产物定量分析的校正 采用Beta-actin作为内参照。将TFAM、NRF-1和内参基因Ct值之间的差值来计算基因表达差异。
1.6 数据处理
数据采用SPSS 20.0进行单因素方差分析,采用LSD法进行多重比较,数据均以均值±标准差(x±s)表示,以组间方差分析P<0.05为具有统计学意义。
2 结果与分析
2.1 小鼠负重游泳的力竭时间
从表1可以看出,与空白组相比,各剂量组小鼠负重游泳的力竭时间均有不同程度的延长,尤以中剂量组效果最为明显。与空白组和模型组相比,中剂量(25 mg/kg)的人参皂苷Rg1可显著延长小鼠的力竭游泳时间,增长率为271.4%,差异有显著性(P<0.01)。
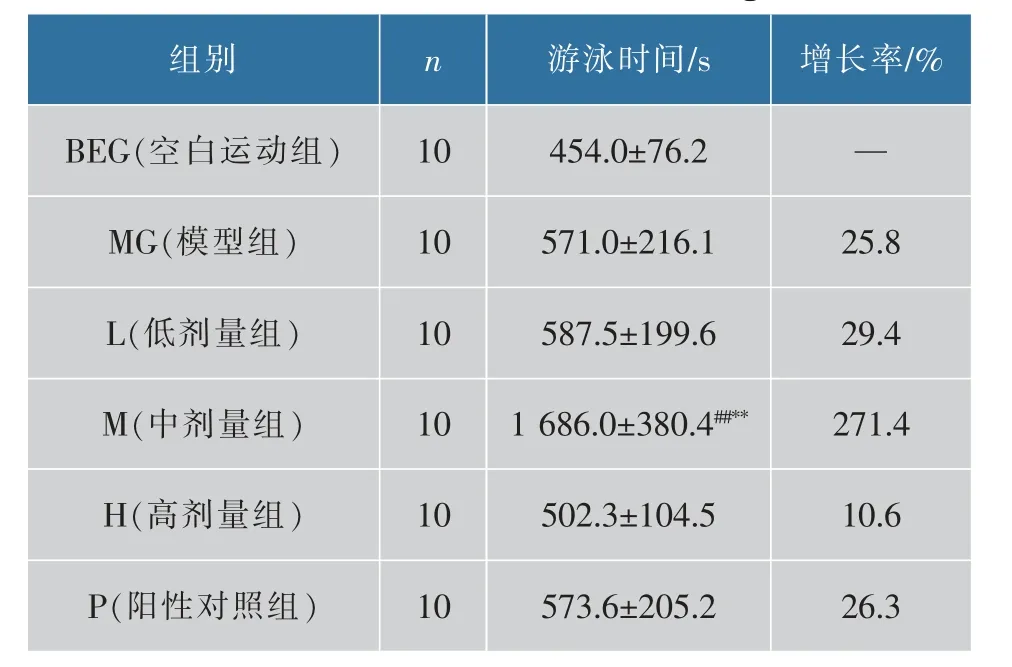
表1 小鼠负重游泳力竭时间Table 1 Exhausted time of mice swimming with load
2.2 小鼠肝脏和骨骼肌中糖原水平
如图1所示,各组间肌糖原浓度无显著差异性。与模型组比较,中剂量人参皂苷Rg1组可明显增加小鼠肝糖原浓度(P<0.05),说明在中剂量时人参皂苷Rg1增加疲劳小鼠肝糖原的效果较好。

图1 人参皂苷Rg1对小鼠肝糖原和肌糖原浓度的影响Fig.1 Effects of ginsenoside Rg1 on glycogen levels of liver and skeletal muscle of mice
2.3 小鼠骨骼肌中MDA、LDH的水平
如图2所示,与MG组比较,人参皂苷Rg1各剂量组小鼠骨骼肌中MDA质量摩尔浓度均明显下降,差异具有显著性(P<0.01)。与空白静止组相比,模型组、空白运动组和低剂量组骨骼肌中LDH活性下降明显(P<0.01);与模型组和空白组相比,中、高剂量组小鼠骨骼肌中LDH活性增加显著(P<0.01)。
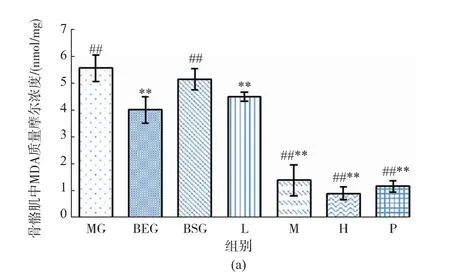
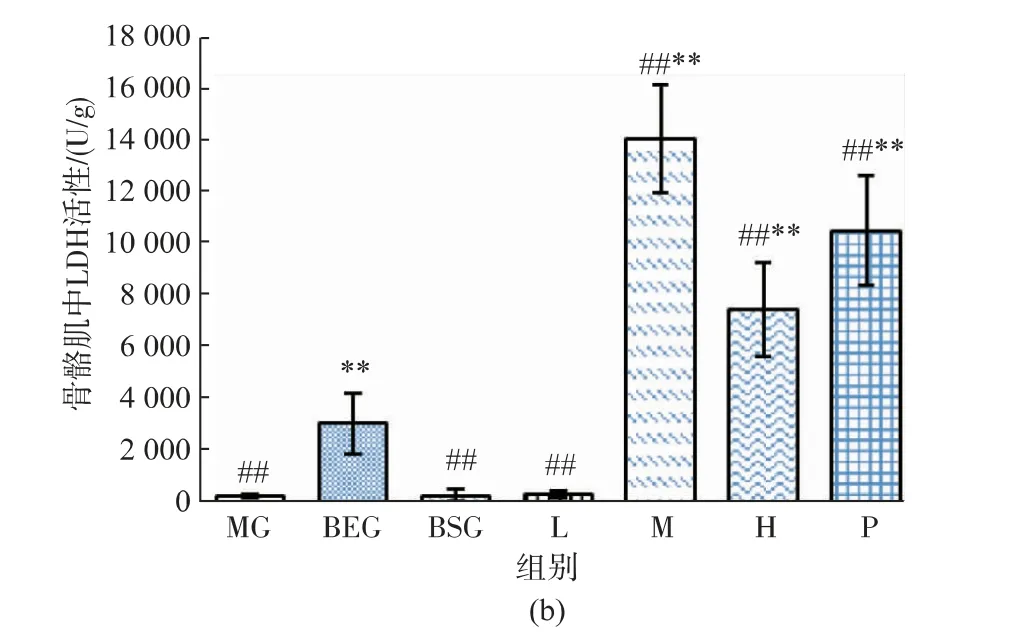
图2 人参皂苷Rg1对小鼠骨骼肌中MDA和LDH的影响Fig.2 Effects of ginsenoside Rg1 on MDA and LDH content in skeletal muscle of mice
2.4 小鼠骨骼肌中TFAM和NRF-1基因表达水平
从图3可以看出,与模型组相比,中剂量人参皂苷Rg1可显著增加小鼠骨骼肌中TFAM mRNA和NRF-1 mRNA表达水平,说明人参皂苷Rg1在25 mg/kg的剂量下,对骨骼肌中线粒体相关因子的调节作用最好,从而提高线粒体的生物合成,使线粒体氧化供能增强。
3 结 语
目前已有研究发现,人参皂苷Rg1主要是通过加速自由基清除率、增强体内抗氧化物酶活性、维持血糖水平、促进糖原合成等方面共同协作发挥抗疲劳作用。疲劳的产生通常伴随着能量的大量消耗,其中包括血糖与肌/肝糖原的消耗,同时伴随着疲劳产物的积累,机体调节协同机能失调等[18]。本研究结果显示,中剂量的人参皂苷Rg1显著增加了小鼠肝糖原浓度,可有效减少能量消耗。有学者通过实验证实,小鼠灌胃人参提取物后可延长力竭负重游泳时间,具有抗疲劳作用。宋姌和刘涛[19]研究发现,人参皂苷Rg1可明显降低慢性疲劳综合征大鼠脂质过氧化物丙二醛的含量,同时增强抗氧化酶SOD的活性,说明人参皂苷Rg1能够提高抗氧化酶系统活性并减轻脂质过氧化代谢产物的堆积,具有良好的抗疲劳作用。王莹等研究表明,人参皂苷Rg1能显著延长小鼠力竭游泳时间,降低血清中尿素氮水平,同时维持血糖水平,增加肌糖原和肝糖原储备,显著降低小鼠运动后血乳酸浓度,以上研究结果与本实验结果基本一致。在本实验中,小鼠游泳运动后与正常运动组小鼠比较,肝和骨骼肌中MDA质量摩尔浓度并无显著性差异。在给予人参皂苷后,各剂量组的人参皂苷对骨骼肌组织中的MDA质量摩尔浓度均有降低作用。
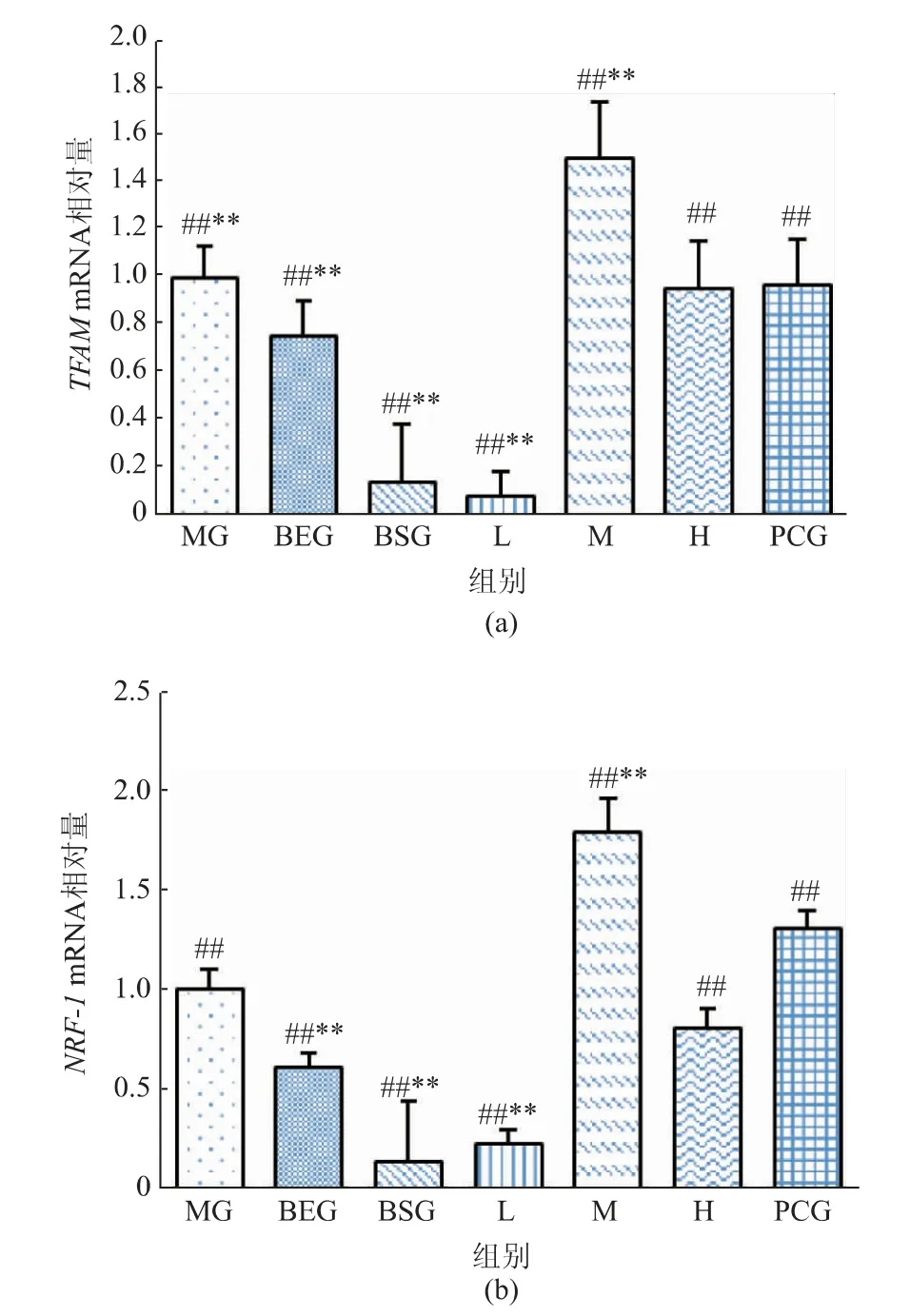
图3小鼠骨骼肌中TFAM mRNA和NRF-1 mRNA表达水平Fig.3 Expression of TFAM mRNA and NRF-1 mRNA in skeletal muscle of mice
TFAM基因的启动子上具有多种调节因子的识别位点,其中NRF-1占主导位置,二者与DNA结合后可增高其mRNA的表达及升高TFAM的蛋白质合成,从而增加线粒体进行生物合成[9]。NFR-1的主要作用是调控mtDNA的表达,包括线粒体转录因子A(TFAM),其中TFAM在调控mtDNA表达及线粒体基因组复制中起重要作用。TFAM是mt DNA复制转录的直接调控子[21],学者通过敲除了TFAM基因的大鼠发现,mtDNA的复制明显减少,并且线粒体电子传递能力受到损伤[22]。线粒体功能的改善可能与TFAM的大量表达相关联,其作用还有参与调节线粒体的转录机制[20]。NRF-1能调控多种线粒体蛋白质的表达[12]。TFAM可在NRF-1的作用调节下激活,对mtDNA的复制与转录起着重要的调控作用。赵婷婷等研究证实,一次长时间大鼠游泳后能促进骨骼肌中PGC-1α与TFAM mRNA的共同表达,黄芪丹参复合物可通过p38MAPK-PGC-1α-NRF-1-TFAM途径促进线粒体生物发生。实验结果显示:不同剂量的人参皂苷Rg1可同时上调NRF-1和TFAM基因的表达,以中剂量组(25 mg/kg)效果最明显,说明人参皂苷Rg1可激活NRF-1在线粒体转录因子A(TFAM)启动子上的转录功能,而TFAM是线粒体生物合成的直接调控因子,因此证明人参皂苷Rg1可改善线粒体功能和修复肌细胞的损伤,对骨骼肌肌细胞产生保护作用。
人参皂苷Rg1对疲劳模型小鼠的疲劳相关指标肝/肌糖原以及骨骼肌中抗氧化指标有很好的调节作用,并能有效调节骨骼肌中线粒体合成过程中的重要因子的表达水平,从而起到抗疲劳的作用。

