线粒体通透性转换孔在锌缺乏模型大鼠心肌缺血/再灌注损伤中的作用
连 婷,张瑞君,熊晓兰,张小雅,余 涛,张世忠
(三峡大学医学院 生理与病理学系,湖北 宜昌 443002)
锌是人体中重要且必不可少的微量元素,在生化、免疫和临床功能中均起着重要作用[1]。锌缺乏是一个世界性的医学问题,特别在发展中国家锌缺乏尤为严重,锌缺乏可使消化系统、中枢神经系统、免疫系统和生殖系统等功能受损[2]。在心血管系统中,锌缺乏还与心脏相关疾病有关,例如动脉粥样硬化、心力衰竭[3]。研究表明,心肌缺血/再灌注(ischemia-reperfusion,I/R)可损害心脏中锌稳态[4],缺血性心肌病患者的锌水平较低[5]。这些研究结果提示锌缺乏与心肌I/R损伤密切相关。但是,目前现尚不清楚锌缺乏导致心肌I/R损伤的确切机制。
线粒体通透性转换孔(mitochondrial perme-ability transition pore,mPTP)位于线粒体内膜中,其开放会导致线粒体肿胀、破裂,细胞色素C释放,最终导致细胞死亡[6],大量研究报道了mPTP在心肌I/R损伤中发挥重要作用[7-8],但是mPTP是否也参与锌缺乏相关的心肌I/R损伤,现尚不清楚。
本实验建立大鼠心肌I/R损伤模型,观察mPTP开放在缺锌大鼠心肌I/R损伤中的作用。
1 材料与方法
1.1 材料
1.1.1 实验动物:清洁级雄性SD大鼠,体质量(250±5)g[三峡大学实验动物中心,合格证号:SCXK(鄂)2017-0012],大鼠在实验过程中的处理符合动物伦理学的要求。
1.1.2 主要试剂:缺锌饲料和标准饲料(南通特洛菲饲料科技有限公司);Masson染色试剂盒(武汉赛维尔生物科技有限公司);氯化三苯四氮唑(2,3,5-triphenyl-tetrazolium,TTC)(Sigma-Aldrich公司);乳酸脱氢酶(lactate dehydrogenase,LDH)试剂盒(南京建成生物有限公司)。
1.2 方法
1.2.1 缺锌动物模型的建立:将大鼠随机分为2组:对照组(control):饲喂含100 mg/(kg·d)锌的标准饲料;缺锌组(zinc deficiency):饲喂含1.2 mg/(kg·d)锌的缺锌饲料,连续喂养6周。在整个实验过程中定时监测每只大鼠的行为和体质量变化。
1.2.2 血浆锌含量的测量:用肝素作为抗凝剂采集大鼠血样,在4 ℃、3 500 r/min离心10 min,获得血浆,血浆锌水平用原子吸收分光光度计测量,锌水平以mg/L表示。
1.2.3 Masson染色观察心肌纤维化:参照Masson染色试剂盒进行染色。正常心肌组织染成红色,胶原纤维染成蓝色,显微镜下采集图像。
1.2.4 Langendorff灌流离体心脏准备及各组大鼠心脏灌流方案:给大鼠腹膜注射10%水合氯醛(3.5 mL/kg)麻醉后迅速取出心脏,经主动脉逆行插管固定在Langendorff装置上,以恒压5.59 mmHg(1 mmHg=0.133 kPa)、恒温37 ℃的条件下用K-H缓冲液(以95% O2及5% CO2混合气体饱和,pH为7.3~7.4)灌注。连续监测左心室发展压力(Left ventricular developed pressure,LVDP)、左心室舒张末期压力(left ventricular end-diastolic pressure,LVEDP)、左心室压力的最大上升/下降速度(±dp/dtmax)。冠脉流量通过使用校准管按固定间隔定时收集流出液进行测量,并以mL/min表示。各组大鼠心脏具体灌流方案为:1)对照组大鼠离体心脏灌流平衡20 min,全心缺血30 min,然后再灌注120 min;2)缺锌组方法同对照组;3)zinc deficiency+CsA组在再灌注开始时先用0.2 μmol/L mPTP特异性抑制剂环孢霉素A(cyclosporin A,CsA)灌流10 min,其余同对照组;4)control+CsA组方法同(zinc deficiency+CsA)组。
1.2.5 测量梗死面积:心脏再灌注120 min后,在-20 ℃冷冻后横向切成2 mm厚的切片,1% TTC的溶液中孵育(2~5)min,然后固定在10%甲醛10 min心脏切片经TTC染色后,未梗死危险区域,活组织被染成红色,梗死组织为白色。使用Image/J(NIH)软件测定梗死区域和危险区域。以梗死区占危险区的百分比表示心肌梗死程度。
1.2.6 冠脉流出物中LDH的测定:在再灌注5 min时收集来自离体灌注心脏的冠状流出物,并用分光光度法测定LDH活性,以U/L表示。
1.2.7 线粒体的准备:用含有160 mmol/L KCl、10 mmol/L EGTA(乙二醇-双四乙酸,pH 7.4)和0.5%不含脂肪酸的BSA缓冲液对心脏组织进行匀浆,将匀浆液在2 ℃、1 000×g离心10 min,取上清液在2 ℃、8 000×g离心10 min,将沉淀重悬于悬浮缓冲液(320 mmol/L蔗糖和10 mmol/L Tris-HCl,pH 7.4)中,并在2 ℃、8 000×g离心10 min,获得纯化的线粒体,并用考马斯亮蓝对线粒体蛋白进行了定量。
1.2.8 电镜检测线粒体:将分离的线粒体固定在1%四氧化锇的0.1 mol/L甲藻酸酯缓冲液中,于(0~4)℃固定120 min。然后,将样品冲洗、脱水并包埋在Epon 812中。在超薄切片机上切下切片,用乙酸铀酰和柠檬酸铅染色,并在H-600透射电子显微镜下检查确定。
1.2.9 mPTP开放的测量:为了测量mPTP的开放度,将分离的心脏线粒体重悬于溶胀缓冲液(含有120 mmol/L KCl、10 mmol/L Tris-HCl、20 mmol/L MOPS、5 mmol/L KH2PO4,pH 7.4)中,使其最终浓度为0.25 g/L,加入CaCl2(200 μmol/L)引发线粒体肿胀,于520 nm处检测线粒体吸光度(A)来确定mPTP的开放度,mPTP开放程度以线粒体最大溶胀率表示。
1.3 统计学分析
2 结果
2.1 血浆中的锌水平
与对照组相比,大鼠缺锌饮食喂养3及6周后,缺锌大鼠的血浆锌含量明显降低(P<0.01)(表1)。

表1 血浆锌含量
2.2 锌缺乏症状
缺锌组大鼠的体质量和心脏增重明显低于对照组(P<0.05)(图1A,B)。缺锌组大鼠背部、腹部和口腔均出现严重的脱毛溃烂,大鼠活动明显减少,精神状态较差(图1C)。

*P<0.05 compared with control
2.3 心脏组织的病理变化
Masson染色结果所示,对照组大鼠心肌纤维排列整齐,细胞之间只有少量蓝色胶原纤维,而缺锌组大鼠心肌纤维断裂且排列混乱,细胞间有大量胶原纤维沉积(图2)。

图2 大鼠心肌组织Masson染色图
2.4 心功能变化
与对照组相比,缺锌大鼠心肌缺血/再灌注30 min时,LVDP、±dp/dtmax显著降低(P<0.01),LVEDP明显升高(P<0.05)。mPTP特异性抑制剂CsA(0.2 μmol/L)可以减轻锌缺乏大鼠心肌缺血/再灌注引起的LVDP、±dp/dtmax降低(P<0.05)和LVEDP升高(P<0.05)(表2)。
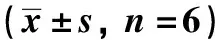
表2 心功能各个指标的改变
2.5 心肌梗死面积和LDH
与对照组相比,缺锌大鼠心肌缺血/再灌注损伤引起的梗死面积和冠状流出物中LDH释放明显增加(P<0.05)。CsA可减小缺锌缺乏大鼠心肌缺血/再灌注损伤的梗死面积以及心肌冠脉流出液LDH含量(P<0.05)(图3)。
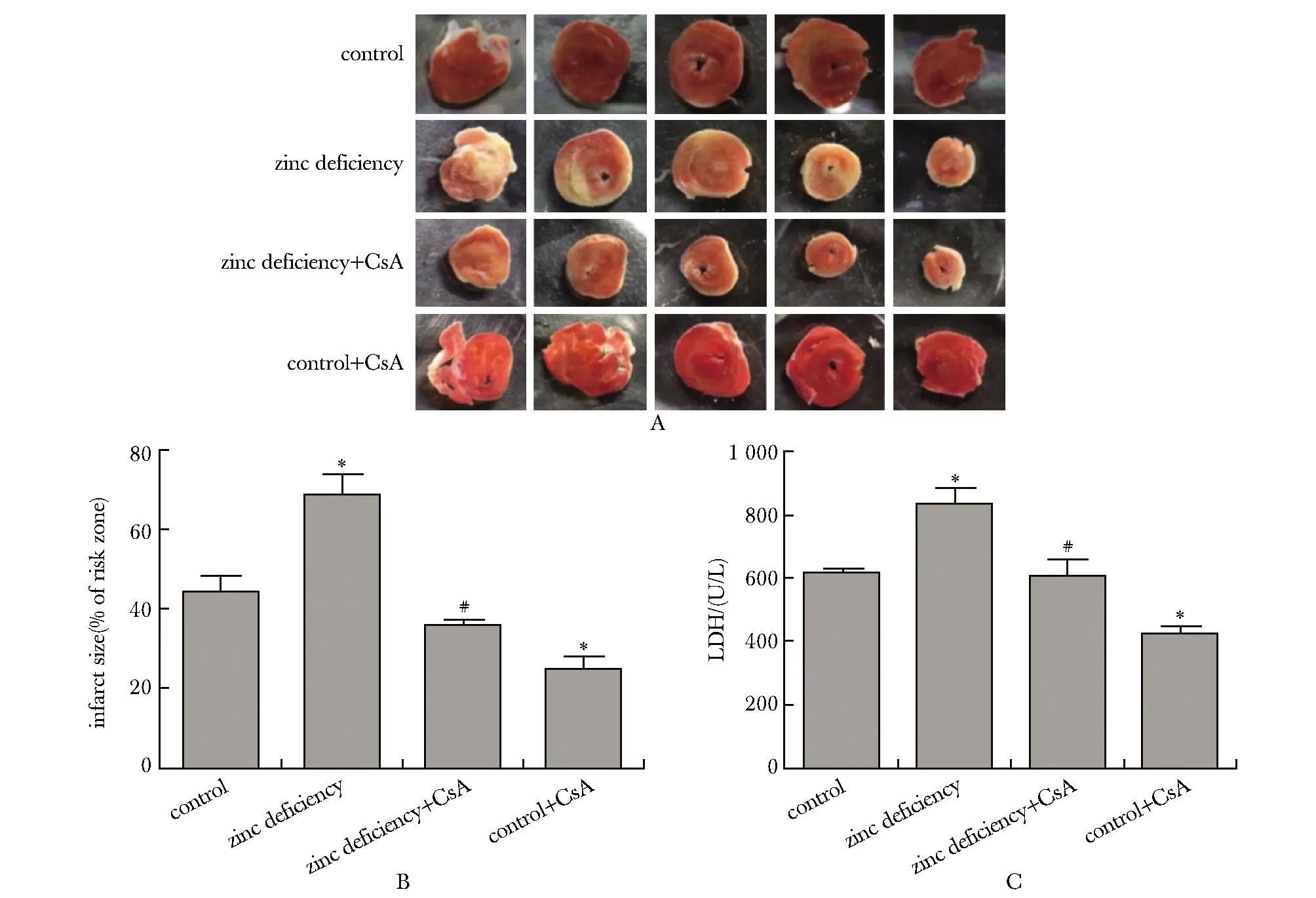
*P<0.05 compared with control; 0.05 compared with zinc deficiency
2.6 线粒体的形态
在电子显微镜下,线粒体在肿胀(mPTP开放)之前显示完整的膜和致密的基质空间(图4A),但是在Ca2+引起的肿胀(mPTP开放)之后,外膜的破坏和嵴的消失很明显(图4B)。
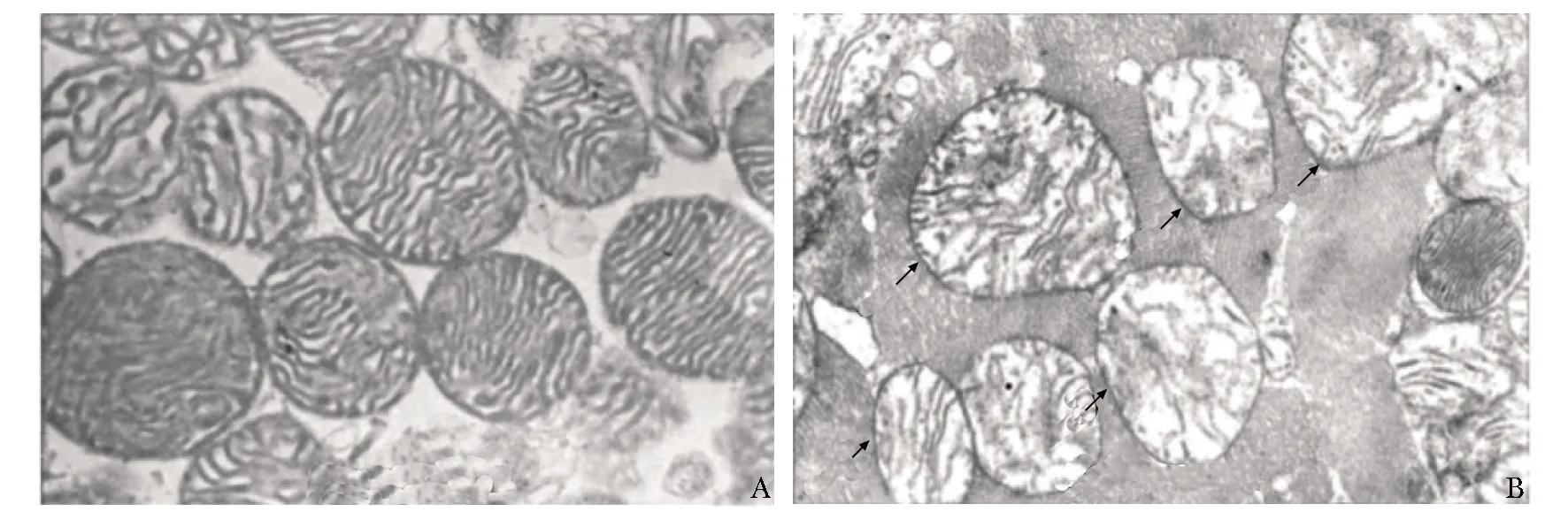
A.fixation was performed following isolation; B.following exposure to 200 μmol/L CaCl2; the mitochondia were swollen(indicated by arrows)
2.7 锌缺乏对mPTP开放的影响
与对照组相比,缺锌大鼠缺血前心脏线粒体的mPTP开放显著降低(P<0.05),但是在缺血30 min后,mPTP开放显著增加(P<0.05)(图5)。

A.mPTP opening in mitochondrial was measured by spectrophotometric monitoring of the decrease in absorbance at 520 nm(A520)after addition of CaCl2(200 μmol/L); B.maximal swelling rates of mitochondria; *P<0.05 compared with control(before isc); #P<0.05 compared with zinc deficiency(before isc); isc.ischemia
3 讨论
锌在蛋白质结构、细胞功能调节中起着重要作用,在心血管系统的病理生理过程中发挥重要作用[2-3]。心脏I/R导致心肌组织中锌的流失,并且在再灌注期间补充锌可减轻心脏损伤[9]。缺血性心肌病患者的锌水平也较低[5]。但是,现尚不清楚锌缺乏时,锌缺乏症患者在发生心肌I/R时是否会遭受更严重的心脏损伤。本实验研究结果表明,与对照组相比,缺锌6周后大鼠具有明显的缺锌症状,且体质量和心脏重量明显降低,此时心肌纤维排列紊乱,胶原纤维大量沉积,锌缺乏严重。与锌水平正常的大鼠相比,锌缺乏大鼠心肌I/R损伤更加严重,提示低锌水平的患者可能更容易遭受更严重的心肌I/R损伤。
mPTP是位于线粒体内膜上的非特异性孔,其开放会导致细胞色素C的释放,从而引起心肌细胞的凋亡,而锌的添加会减少mPTP的开放[6]。已有研究发现,mPTP参与了心肌I/R损伤[8]。为了验证mPTP是否与锌缺乏相关的心肌I/R损伤有关。本实验在心脏缺血前线粒体中,发现缺锌大鼠的mPTP开放比对照大鼠明显减少,提示mPTP开放的减少可能是预防缺锌所致伤害的补偿,但其潜在机制有待于进一步阐明。为了进一步观察mPTP在心肌I/R过程中的作用,本实验检查了心脏缺血30 min后mPTP的开放程度,结果表明mPTP开放度在缺血后显著高于缺血前,这表明mPTP的开放增强可能是导致缺锌大鼠心脏I/R损伤增加的主要原因。为了进一步证实这一推测,本实验使用了mPTP特异性抑制剂CsA来抑制再灌注期间mPTP的开放,结果表明,与对照组相比,心肌I/R损伤明显减轻,这很好地解释了本实验研究结果,即为什么缺锌大鼠在心肌缺血复灌后比正常锌水平的大鼠有更严重的心脏损伤。活性氧在心肌I/R损伤的发病机制中起着关键作用,即可触发mPTP的开放[10],而锌是超氧化物歧化酶的组成部分,可提供抗氧化作用,稳定细胞膜结构[11]。因此,本实验推测缺锌可能会导致细胞抗氧化能力的降低,增加了mPTP开放,进一步导致心肌I/R损伤的加重。
本研究表明锌缺乏可通过诱发心肌I/R期间mPTP的开放增加,从而介导锌缺乏大鼠心脏I/R损伤。

