通过预设和纠正错误示范培养“变量控制”科学方法
陈秀荣
江苏省丰县中学(221700)
“变量控制”是一种重要的科学方法,《普通高中化学课程标准(2017年版2020年修订)》明确把“能运用变量控制的方法探究并确定合适的反应条件”作为高中学生学业质量水平的要求[1],人教版化学必修第二册教材在显眼位置以“方法引导”栏目专门介绍变量控制方法。同时,变量控制作为设计化学实验时的常用方法,贯穿学生整个化学学习过程,也是科学探究的核心能力[2]。
但在实际教学中,学生对变量控制方法的学习主要是在教师的明确指引下进行的,缺少独立的设计,尤其难以识别可能存在的“未控制”变量导致结果不可靠的情况[3]。为了强化控制变量科学方法的培养,本文提出可以预设错误的(未控制变量的)实验示范,引导学生寻找其中未被控制的额外变量,并重新设计实验进行纠正。
1 初识方法:感受变量控制的价值
人教版教材中第一次专门介绍变量控制的方法,是在必修第二册“化学反应的速率与限度”一节的“方法引导”部分。在常规的教学设计中,教师一般会先介绍变量控制的方法,再应用这个方法设计“影响化学反应速率的因素”探究实验来体现实验设计中的控制变量思想。但是,这样的“顺序”设计不容易让学生感受到控制变量方法的必要性和价值,因此本文提出一种“倒序”的教学设计。
教师进行如下演示实验,在试管中倒入5 mL 10% H2O2溶液,然后滴加2滴10% CuSO4溶液,发现溶液中缓慢地形成一个个的小气泡,说明此时反应速率较慢。过1~2 min后,教师往原试管中继续滴加2滴10% FeCl3溶液,溶液中快速冒出了许多气泡,说明此时反应速率较快。随后,师生就实验现象展开讨论。
教师:从实验现象中,你发现什么因素影响了过氧化氢分解的速率?
学生1:催化剂种类。FeCl3比CuSO4的催化效果更好,反应速率更快。
教师:这个实验可以证明这一点吗?
学生2:可以,因为加FeCl3的时候,过氧化氢已经反应掉一部分了,理论上反应速率应该更慢,但加FeCl3之后反应速率却变快了,可以证明FeCl3确实催化效果更好。
教师:从这个角度看,反应物浓度这个变量虽然没有被控制,但不影响结果的可信度。那其他方面呢,有没有同学有不同意见?
学生3:我觉得结果不可信。因为加FeCl3之后,催化剂的量也改变了,也许4滴催化剂的反应速率本来就比2滴催化剂要快。
教师:这位同学的质疑很值得关注,因为催化剂的量和催化剂的种类都有可能导致反应速率加快,在刚刚的实验中,这两个变量都改变了,我们不知道反应速率加快到底是哪个变量导致的,又或者是两个变量共同作用导致的。除此以外,你还能找到实验中没有被控制的变量吗?
提出这个问题后,学生沉默思考,但久久没有发言。教师播放了“铝片与氢氧化钠溶液的反应”实验视频,视频中,铝片与氢氧化钠反应初期速率缓慢,但过一会后突然剧烈反应,溶液快速沸腾,气泡快速生成,夹杂着白雾升腾而起。学生想到,这个反应是放热反应,随着温度的不断升高,反应速率也不断加快,导致温度继续升高,速率进一步加快……联想到刚刚的实验,过氧化氢分解也是放热反应,也可能出现类似的现象,即反应放热导致的温度升高最终导致反应速率加快。这样,学生找到了原始实验第3个未被控制的额外变量——温度。
通过上述的教学过程,学生深刻认识到,如果不经过精心的实验设计,即便得到了感觉上可靠的实验结果,也未必是科学严谨的。因为有一些未被控制的额外变量可能干扰实验结果,让人无法区分究竟哪个变量才是导致结果发生的真正原因(又或者这些变量都是原因)。至此,教师顺理成章地引出了“变量控制”的科学方法的教学,并让学生感受到这个方法的必要性和重要价值。
2 迁移方法:应用变量控制的实践
在学习了变量控制方法之后,教师在“化学能转化成电能”的复习课上训练学生将控制变量方法迁移应用到实验探究活动中(参考人教版必修二的实验活动6)。教师进行预设的演示实验(错误示范)如图1所示。该实验的目的是探究电极种类(铜、碳)对原电池电流的影响,在2个烧杯中放入等浓度等体积的硫酸,用2个相同的锌片分别作为2个原电池的负极,用铜片作为第1个原电池的正极,用碳棒作为第2个原电池的正极,负极、正极均用导线相连并串联电流表,比较电流表示数大小。教师在即将搭建好实验装置时,针对装置是否实现了“变量控制”的问题展开讨论。

图1 未控制变量的探究电极种类对电流的影响的演示实验
教师:同学们认为这样的实验装置实现“变量控制”了吗?
学生1:电解质浓度和用量都一样,控制了。
学生2:这里的变量很多……
教师:这个实验中变量确实很多,需要仔细梳理,请同学们填写表1来识别变量,然后检查额外变量是否被控制(表1中的“变量名称”和“额外变量是否被控制”需要学生自己填写)。
学生2:我发现,一个是铜片,一个是碳棒,形状不一样,这样2种电极与溶液的接触面积可能是不同的。

表1 实验中的变量
教师:很好,你发现了这个实验的设计缺陷。同学们可以根据变量控制的方法,自己改进实验吗?(学生小组讨论,形成方案。)
经过讨论,不同学生小组大致形成了2种方案。
学生方案一:测量浸入溶液的铜片的长、宽,计算其表面积;测量碳棒的直径,计算其表面积;比较两者的面积,如果不一致,把铜片剪成合适大小,使其表面积与碳棒一致。
学生方案二:把铜片换成与碳棒直径相同的粗铜丝(见图2),浸入溶液时,确保与碳棒浸入深度相同。
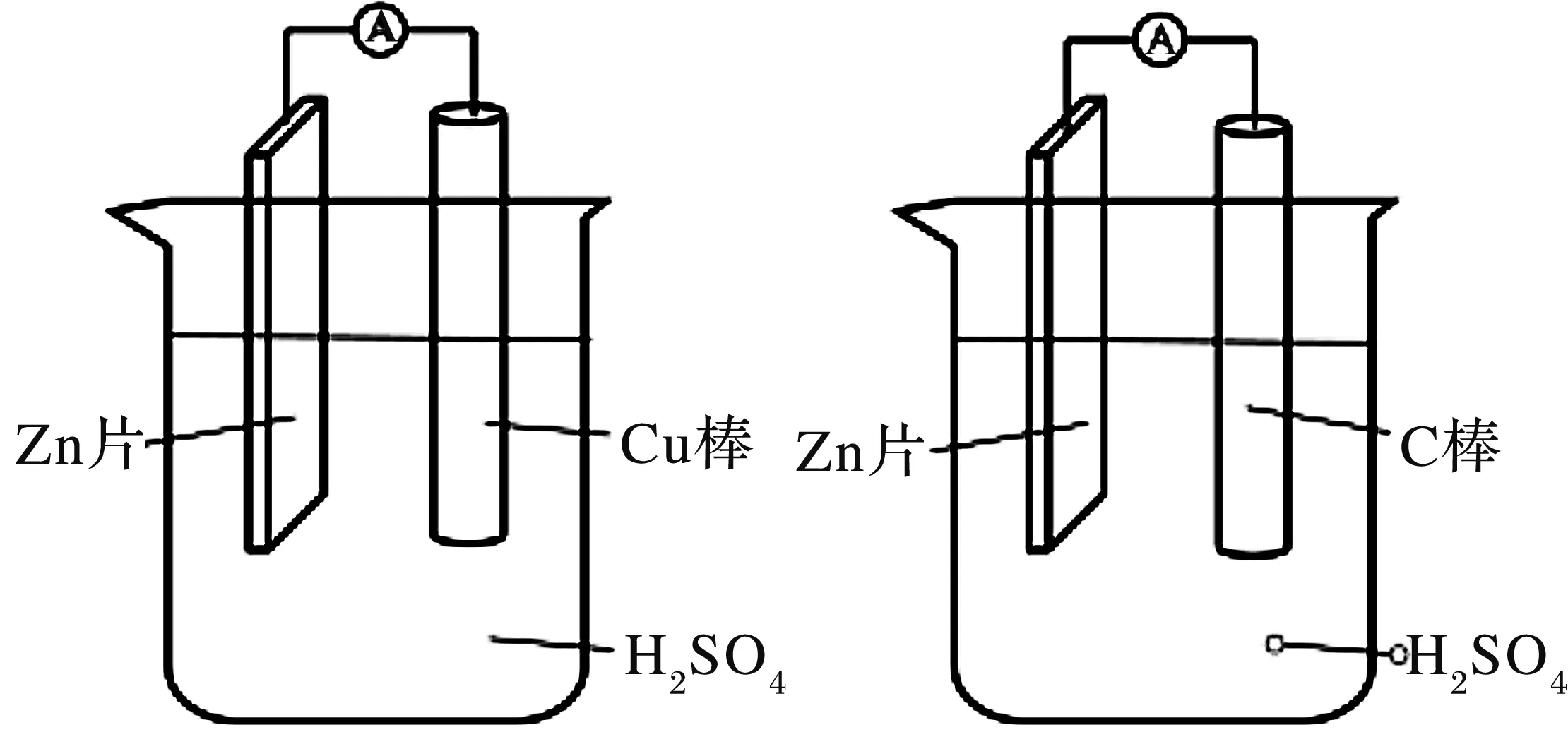
图2 改进后的学生方案
教师:大家觉得哪种方案更好?
学生3:我觉得方案二更好,因为方案一还有电极的形状这一变量没有被控制。平面的铜片靠近负极的那个面明显生成的气泡更多,另一面的气泡很少。
经过进一步的讨论,大家同意学生3的观点,最终采用方案二进行了后续的实验。在这个教学过程中,学生把已学的变量控制方法应用到批判性评价实验方案的严谨性、科学性上,并进一步用其设计新的实验方案,这是对科学方法的迁移应用。制的方法,久而久之可能会形成定势思维,过分追
3 拓展方法:多因素变量控制与综合应用
学生在必修阶段接触的主要是单因素变量控求单因素的最优条件,而忽略了系统的最优条件。实际上,化学现象、化工生产是复杂的,存在许多自变量都能导致因变量(结果)的变化,要兼顾全局,考虑最优的条件。
例如,在“探究原电池电流的影响因素”的实验中,学生发现“电极与溶液的接触面积越大,电流越大”,因此过分地追求将这单一变量最优化。教师适时给予引导。
学生:能不能用一个很大的锌片和铜片,让电池电流更大呢?
教师:但是这样烧杯就装不下了。
学生:那就可以换一个更大的烧杯。
教师:在现实生活中,如果给你一个特别大的烧杯电池,你会愿意吗?
学生:不愿意……看来锌片和铜片也不能特别“占地方”。
教师:在这个实验中,“电极与溶液的接触面积”只是众多变量中的一种,我们应该找到尽可能多的变量,然后考虑实际情况,优先改进更安全、更经济、更方便的变量,达到综合情况的最优化。
实际上,电极种类、电解质种类、电解质浓度、电极间距等众多变量都能影响“烧杯电池”的电流,学生为了变量控制常常要把多因素问题转化为单因素问题单独实验和分析,但最后还需要综合考虑,才能更好地解决实际问题。

