钙-磷系自固化材料改性研究进展
李 航,廖建国,马婷婷,冯锦伦
(河南理工大学材料科学与工程学院,焦作 454000)
0 引 言
临床上绝大多数骨缺损是不规则的,定型的骨修复材料不易与周围骨组织紧密接触,从而影响修复效果,所以集成型和修复一体的骨水泥被广泛应用于骨科微创手术。骨水泥主要分为生物惰性的聚甲基丙烯酸甲酯(polymethylmethacrylate, PMMA)骨水泥、生物活性的磷酸钙水泥(calcium phosphate cement,CPC)和其他复合骨水泥[1]。PMMA骨水泥力学强度高,在临床应用中使用最广泛,但其不可降解,聚合过程放热量大,易杀死周围正常细胞,且未聚合单体具有细胞毒性[2-4]。CPC由两种或两种以上磷酸钙粉末与液相溶液混合制备而成。CPC经溶解-沉淀反应生成的水化产物透钙磷灰石或磷灰石(羟基磷灰石或缺钙型羟基磷灰石),与骨的主要无机成分相似,将CPC植入体内后不会引起抗原反应,骨水泥能与骨直接结合,形成强骨-材料界面,成为新骨生长的模板,为新骨生长提供细胞附着增殖场所[5-7]。与PMMA骨水泥相比,CPC水化过程放热量低,可降解,无细胞毒性,生物相容性好,可促进新骨再生[8-9]。然而,CPC力学强度低,不能用于承重部位,降解速度缓慢,诱导成骨细胞增殖分化和血管生长能力有待提高,与临床应用需求仍存在一定的差距,所以国内外研究者对其进行了大量的改性研究[10-12]。本文从CPC的理化性能和生物学性能两方面综述了其改性研究进展。
1 CPC的理化性能
1.1 力学强度
CPC固化反应是溶解-沉淀的过程,当水泥固相颗粒与液相溶液混合后,固相颗粒逐渐溶解,颗粒周围溶液过饱和,生成细晶和微晶,细晶和微晶相互缠绕,随着时间推移,晶体不断生长,晶体缠绕网络逐渐致密,致使CPC具有一定力学强度。CPC可用于人体非承重部位,如牙周疾病治疗、颅骨-颌面外科重建等,不能用作承重部位骨修复材料。目前,增强CPC力学性能方法主要分为三类:(1)颗粒增强;(2)纤维增强;(3)优化制备条件。
1.1.1 颗粒增强
当颗粒作为增强体均匀分布在CPC基体中后,填充了基体内部孔隙,材料结构致密,同时在外加载荷作用下,颗粒会阻碍基体位错运动,位错密度增加从而强化了基体,CPC强度得到提高。Zhang等[13]在CPC中加入粒径小于106 μm的掺铜磷酸三钙颗粒,改性后的骨水泥抗压强度提高了30%。Xia等[14]以纳米氧化铁颗粒填充CPC基体,降低了CPC内部孔隙率和孔隙体积,其抗折强度增加了一倍。Lin等[15]将纳米磷酸铜颗粒与CPC复合,纳米颗粒填充了水泥颗粒空隙,提高了结构密实度,抗压强度提高。
1.1.2 纤维增强
纤维通过桥接、裂纹挠度和摩擦滑动等增强机制可对CPC基体进行力学增强。当水泥基体产生裂纹时,纤维桥接裂纹,阻止裂纹继续扩展并改变裂纹扩展方向;纤维引起裂纹挠曲延长裂纹扩展距离,消耗能量;纤维在被拔过程中与水泥基体发生摩擦滑动,会进一步消耗来自应力的能量,从而提高水泥的抗断裂性能。Zhang等[16]选用细菌纤维素(BC)纤维增强CPC,纤维表面的OH键与CPC表面Ca2+发生配位反应,形成纤维-基体强界面(见图1),掺入2%(质量分数)BC纤维后抗压强度提高了两倍。Li等[17]发现2%(质量分数)玄武岩纤维可显著提高了CPC的韧性,同时,抗折和抗压强度也得到提高,但随着纤维含量的增加,增强效果降低。Petre等[18]发现当CPC中加入5%(质量分数)聚乙烯醇纤维后,其断裂功为(8.7±2.5)kJ/m2,达到皮质骨最低韧度值(1.5~15 kJ/m2)。
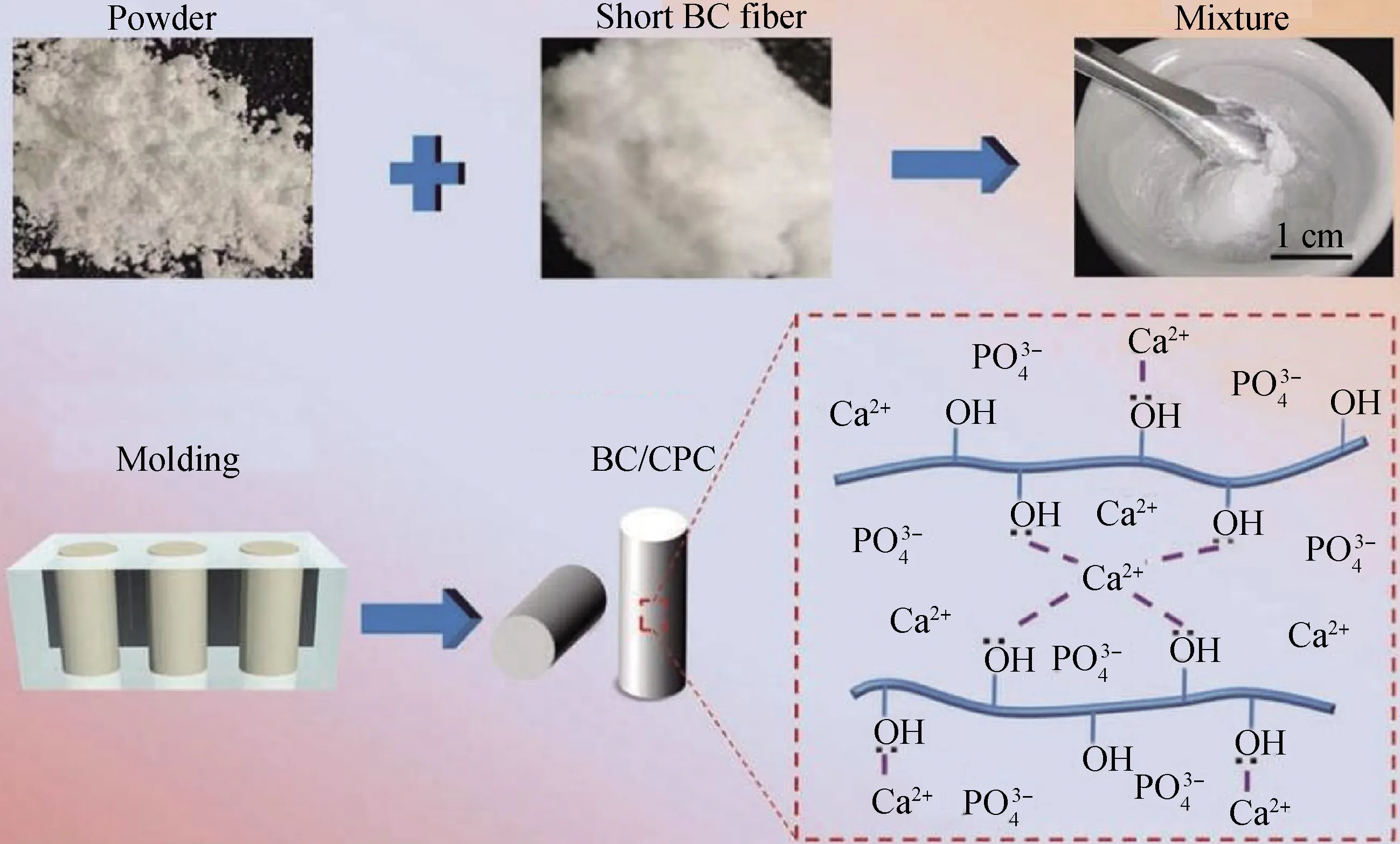
图1 BC纤维与CPC界面反应的制备方法和机理[16]
1.1.3 优化制备条件
CPC粉体颗粒粒径会影响其力学强度,颗粒越小,颗粒比表面积越大,与液相接触面积越大,磷灰石晶体生成速率越快,会形成大量细晶和微晶,晶体密集缠绕使CPC力学强度增加。黄萍等[19]采用球磨技术对CPC粉末进行机械活化处理,原料粉末比表面积增大,原料反应活性提高,致使水泥固化后的水化产物黏结更加紧密,提高了水泥结构密实度,结果表明,原料经过球磨处理后的CPC抗压强度约为未处理的两倍。
当CPC固化的时候外部环境发生改变时,水泥性能会发生变化。Wang等[20]将石墨烯(RGO)/碳纳米管(CNTs)增强的CPC在微波环境下进行固化反应,微波有助于离子扩散,加速固化反应,会促进RGO、CNTs和基体界面结合紧密,与未处理的复合CPC相比,微波处理后的复合CPC力学强度增高且先达到最大值。
1.2 可注射性
可注射骨水泥常用于填补骨质疏松引起的骨折损伤、骨折原位固定和肿瘤等疾病治疗的微创手术中[21],是手术成败的关键因素之一。CPC的可注射性是指在骨水泥注射过程中能够保持均匀性的能力。当前,表征骨水泥可注射性的方法主要为:(1)使用万能试验机对注满骨水泥的注射器进行外力加载,加载速度固定,计算骨水泥被挤出部分重量与初始重量的百分比;(2)对装满骨水泥的注射器进行固定的外力加载,计算骨水泥注射后的质量残余率;(3)测试定量的骨水泥被完全注射所需要的注射力[22-25]。CPC原料颗粒内部分散度和浆料黏度显著影响CPC浆料可注射性。
Hurle等[23]通过加入植酸(IP6)对CPC进行改性(见图2),随着IP6量增加,CPC基体中Ca2+与IP6中磷酸基团螯合产生的螯合物含量增加,使游离Ca2+含量降低,水泥浆体固化时黏度增加,固化反应速度延缓。但IP6加入提高了CPC表面电荷量,可有效分散水泥颗粒,使水泥浆体能有效通过注射器,在混合10 min后CPC仍保持良好的可注射性。Nezafati等[24]在以磷酸四钙(TTCP)为主要成分的CPC中加入微乳化明胶颗粒(GMs)得到可注射骨水泥(GMs/CPC),随着GMs用量增加,GMs/CPC凝结时间延长,注射时间增加;GMs/CPC的可注射率高于纯CPC;其中,含10%(质量分数)GMs的骨水泥可注射性最佳。Amirian等[25]将海藻酸(ALG)-透明质酸(HA)微珠(ALG/HA)掺入CPC后,与CPC对比,在注射位移12 mm时所需注射力更低,且两种骨水泥在注射过程中无裂缝出现(见图3)。
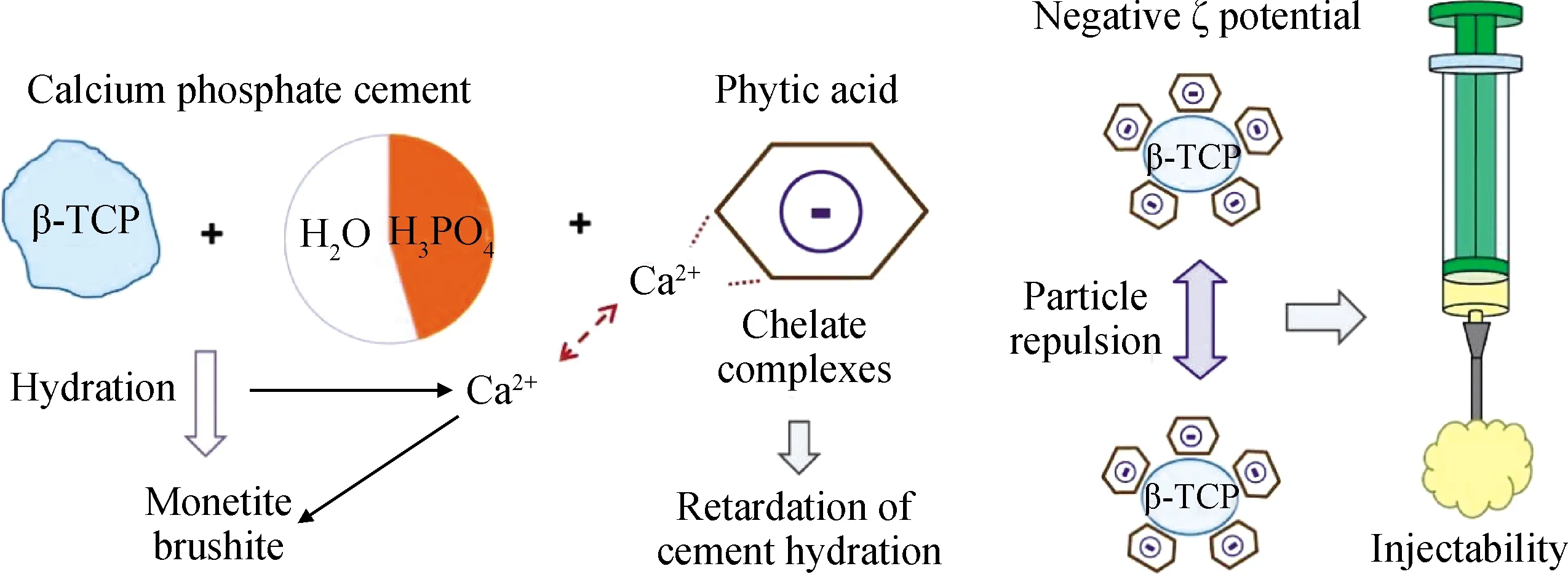
图2 植酸与CPC粉体结合形成可注射CPC[23]

图3 CPC和CPC/ALG-HA水泥的可注射性分析[25]
1.3 抗溃散性
在体内液体环境下,未固化完全的CPC浆体易受到周围组织液体侵蚀,发生材料解体溃散,溃散的水泥颗粒易进入血管中随血液流动,容易使血管堵塞,若溃散的水泥颗粒随血液流动进入器官中,会引起肺栓塞等严重术后并发症[26],因此,抗溃散性是CPC重要的性能之一。
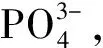

图4 KGM/GG共混物的加入显著提高了CPC的抗冲刷性能[28]
1.4 放射不透明性
在微创手术中,为及时掌握骨水泥注射情况,避免骨水泥渗漏或注射不足,骨水泥注射过程需要在放射显影器下进行。但CPC与骨成分相似,X射线照射下两者对比度低,难以区分,会影响手术操作判断,因此需要提高CPC在X射线下的显影效果。添加造影剂于骨水泥中可提高其放射不透明性,常用的造影剂主要为原子量高、比重大的高密度造影剂,如BaSO4和碘制剂等。
Liu等[31]把造影剂BaSO4引入玉米淀粉(starch)-CPC中,通过在大鼠皮下注射和股骨注射评价复合水泥放射不透明性,结果发现,掺有20%(质量分数)玉米淀粉的磷酸钙复合骨水泥(CPS)与自体骨有相似的放射不透明性,而添加20%(质量分数)BaSO4和20%(质量分数)玉米淀粉-磷酸钙复合骨水泥(CSB)、添加30%(质量分数)BaSO4的PMMA放射显影密度均高于自体骨,能呈现出清晰的X射线对比影像(见图5)。
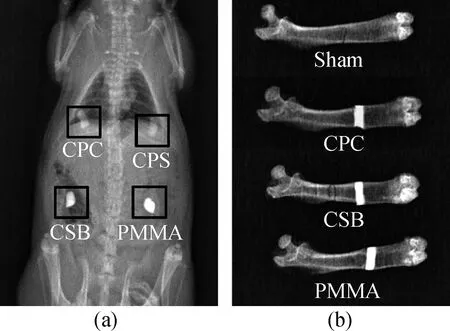
图5 骨水泥X射线影像片(a)皮下植入和(b)股骨植入(CPC:磷酸钙水泥;CPS:20%(质量分数)玉米淀粉-磷酸钙复合水泥;CSB:添加20%(质量分数)BaSO4和20%(质量分数)玉米淀粉-磷酸钙复合水泥;PMMA:添加30%(质量分数)BaSO4的聚甲基丙烯酸甲酯水泥;Sham为自体骨)[31]
碘比醇(iobitridol)为非离子型溶于水的含碘造影剂,性能稳定,渗透压低,耐受性好,Le Ferrec等[32]将水溶性碘化造影剂碘比醇与CPC结合,当碘比醇含量在水泥中达到70 mg/mL时,CPC能快速释放定量造影剂,且掺入碘比醇并不影响骨水泥的可注射性、力学强度和生物相容性。
在市场经济条件下,各企业之间的竞争愈演愈烈,各企业在面对如此激烈的竞争时,往往会采用各种各样的手段来提高企业的效益,诸如采用赊销的办法来刺激企业产品的输出,减少产品的滞留,也能够使顾客更加愿意去购买相应企业的商品。然而,赊销政策的实施,虽有利于促进销售,但也往往会带来客户拖欠款的现象。企业收不回应收账款,会给企业带来一定的资金危机,从而使企业不能够持续稳定地发展。因此,市场上商业竞争过大也是企业应收账款制度现存的一个大问题。
铋是一种不透光元素,毒性低。Wu等[33]加入铝酸铋(BiA)来增强CPC辐射透明度,随着BiA含量的增加,CPC的对比度提高,放射不透明度得到显著改善,BiA-CPC也具有良好的细胞相容性。
2 CPC生物学性能
2.1 成骨活性
骨移植物的基本特性包括骨传导、骨诱导、骨形成和结构支撑[34]。对于CPC,可通过改性促进其骨诱导、骨形成和成血管化等提高成骨活性。常用的改性方法主要为两种:添加生物活性因子和添加生物活性离子。
2.1.1 添加生物活性因子
生长因子可以调控成骨细胞和破骨细胞基因表达,促进骨细胞分化,诱导血管生长。在CPC中加入生长因子后,可诱导新骨和血管生长,进一步促进骨损伤部位愈合。蛋白质基本组成单位氨基酸可促进骨髓间充质干细胞(BMSCs)增殖分化[35],赖氨酸为骨骼代谢重要的氨基酸,Shi等[36]将赖氨酸引入CPC,实验发现对BMSCs成骨分化有显著性改善,促进了纤维连接蛋白的固定。
降钙素基因相关肽(CGRP)可以刺激血管皮内细胞增殖[37],通过促进血管生长,为骨生长传输营养物质,从而促进骨生长。Lv等[38]将CGRP与壳聚糖-Sr-CPC相复合后,释放的CGRP可增强人脐静脉内皮细胞增殖,显著上调血管内皮生长因子(vascular endothelial growth factor, VEGF)基因表达和蛋白分泌,改善血管生成。
2.1.2 添加生物活性离子
微量元素在骨生长过程中发挥着重要作用,可促进骨质矿化和胶原合成,刺激成骨细胞增殖,诱导BMSCs分化为成骨细胞,抑制破骨细胞活性,刺激血管内皮生长基因表达促进血管生长,优化骨免疫调节特性。与生长因子成本高、半衰期短、释放不稳定不易控制,仅适用于短期骨愈合相比,生物活性微量元素离子可通过多种方式储于CPC中,且相对生物活性因子更容易调控其释放速率。目前,在CPC中掺杂具有生物活性的微量元素离子,如Zn、Si、Cu和Sr等,成为一种提高骨水泥成骨活性的新型有效策略。

图6 0% ZS/PLGA/CPC和10% ZS/PLGA/CPC复合材料分别植入4周(a)、8周(b)和16周(c)后的代表性组织学切片和新骨定量结果(d)(NB:新骨;M:材料)[43]
据报道[45],Cu2+刺激BMSCs增殖并分化为诱导矿化的成骨细胞,可调节VEGF,刺激新血管生长,有助于新骨生长。Zhang等[13]将合成的掺铜磷酸三钙(Cu-TCP)颗粒,与由部分结晶磷酸钙和无水磷酸二钙组成的CPC混合制成Cu-CPC,Cu2+与CPC表面生成的羟基磷灰石(hydroxyapatite, HAp)晶体相结合导致Cu2+离子释放量相对较低,小鼠BMSCs和人脐静脉内皮细胞在Cu-TCP/CPC上均有良好的活性,骨和血管相关基因表达上调,Cu-CPC对血管化新骨再生具有促进作用。Lin等[15]用CuP纳米颗粒作为Cu2+载体引入CPC中,结果表明,释放的Cu2+刺激成骨分化基因和血管相关基因表达,从而促进血管生长和BMSCs增殖分化。
Sr元素具有双重作用,一方面能刺激成骨细胞分化,另一方面又抑制破骨细胞活性,在骨质疏松治疗中起着关键作用[46]。Schumacher等[47]研究了Sr-CPC对人间充质干细胞体外增殖和成骨分化的影响,结果表明,由Sr-CPC处理的人间充质干细胞中ALP活性高,Sr-CPC促进人间充质干细胞增殖和成骨分化。Schumacher等[48]研究了Sr-CPC对破骨细胞的影响,结果表明,Sr-CPC在体外不能抑制破骨细胞形成,但能显著降低破骨细胞对骨基质的吸收。Lode等[49]采用SrCO3取代 α-TCP基骨水泥粉体中的CaCO3组分,制备了Sr-CPC,Sr掺杂增强了CPC的骨原细胞增殖和成骨分化,在人尸体脊柱手术中证实了Sr-CPC在球囊后凸成形术具有适用性。
2.2 生物可降解性
CPC水化产物HAp溶解度较低,导致CPC在体内降解缓慢,难以与新骨生长同步。此外,CPC水化晶体之间存在孔隙,但孔径微小导致新生骨组织仅限于生长在表面,无法渗透进入结构内部[50]。为了提高CPC降解速度,同时增大其内部孔隙体积,目前主要采用的策略是在CPC中引入致孔剂。致孔剂在CPC内部可以发生快速溶解或降解,使水泥内部产生大孔,大孔可传递营养成分,允许成骨细胞、破骨细胞和成血管相关细胞进入孔隙内生长[51],同时,致孔剂降解引起的孔隙会增加体液接触面积,提高骨水泥在体液中的溶解性,促进水泥颗粒降解,从而有助于骨修复重建。
Yamamoto等[52]将粒径为200~500 μm具有不同热处理历史的低内毒素GMs分散在CPC中,与CPC相比,GMs/CPC更易降解和吸收,并伴随着新骨生成(见图7);GMs/CPC的溶解速率与GMs热处理温度相关,通过调节GMs预热处理温度可控制CPC体内吸收速率和降解速率,其中383 K下GMs热处理24 h的复合CPC降解性最佳。Smith等[53]把葡萄糖微粒(GMPs)和PLGA微粒作为CPC的双致孔剂;体外降解8周后,GMPs和PLGA微粒几乎完全降解,复合水泥孔隙率显著增加;同时,GMPs的加入提高CPC早期孔隙率,促进PLGA降解产物扩散,减轻了PLGA降解物造成局部酸性。Grosfeld等[54]GMPs作为CPC的致孔剂,将GMPs/CPC植入大鼠股骨缺损两周后出现明显降解,且骨生成量显著增加。Lodoso-Torrecilla等[30]在CPC中掺入PLGA和PVP颗粒,发现低分子量的PVP加入可影响骨水泥早期降解性,PLGA在CPC中内部水解降解产生的酸性单体,对CPC的充分降解有利。
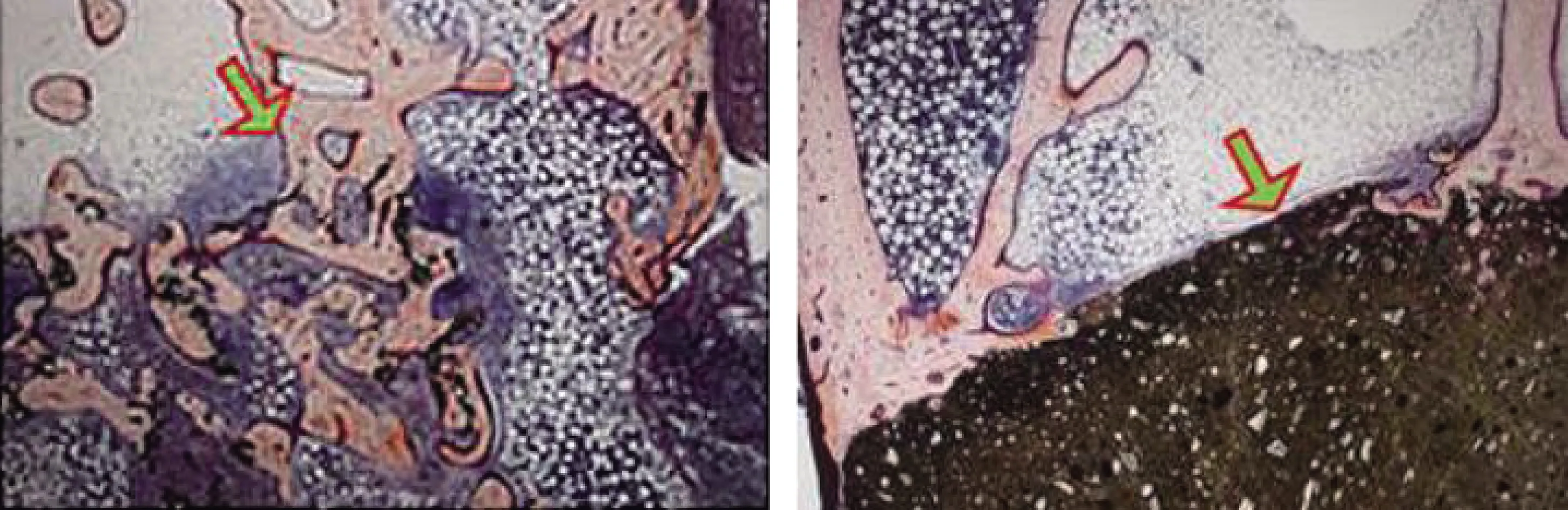
图7 明胶微粒进行适当热处理分散,使磷酸钙骨水泥迅速吸收并伴随骨形成[52]
2.3 载药性
以CPC为载体的药物缓释体系是一种比较先进的给药体系,药物可以与CPC的固相或液相结合,附着在CPC表面或孔隙内,负载药物的CPC复合体系具有载药稳定性,可在骨缺损部位进行持续药物释放,使药物维持在有效浓度范围内,提高了药物利用率,同时降低了药物对于其他器官部位的刺激副作用。
Montazerolghaem等[55]在预混合酸性CPC中载入不同剂量的辛伐他汀发现,辛伐他汀可抑制破骨细胞分化和骨再吸收,但并不影响细胞增殖和生存能力。吴建煌等[56]用可降解的PLGA微球包裹利福平(RFP)药物,与CPC复合得到RFP-PLGA-CPC发现,其固化体断面孔隙比未改性的CPC多,有利于提高成骨性,且药物可持续稳定局部释放。Ghosh等[57]以含量不同的无定形晶态HAp作为CPC的固相,将万古霉素和环丙沙星掺入固相中,研究发现,前体CPC组分中HAp处于初生沉淀无定形状态时间越久,药物扩散释放越活跃,而凝结速率与药物释放速率和无定形HAp的含量成反比。
Prokopowicz等[58]将合成的介孔二氧化硅(CaP@MSi)与CPC制成双相复合材料,用作盐酸阿霉素(DOX)的给药系统,结果表明,复合提高了CPC的成骨细胞活性,延长了DOX的释放时间。Lucas-Aparicio等[59]将Si-β-TCP陶瓷粉末与微胶囊相变材料(MPCM)制备Si-CPC并负载万古霉素,结果发现,Si-CPC具有零级释放动力学,与负载的药物浓度无关,能有效地调整药物释放动力学,抑制金黄色葡萄球菌的生长。Filippo等[60]将硫酸庆大霉素作为模型药物,分别采用药物微粒直接与CPC混合、负载药物的固体脂质微粒与CPC混合、药物直接与CPC和固体脂质微粒复合等三种方式进行性能对比,结果显示,药物微粒与CPC复合的效果较优,能抑制菌株及分离株活性,可长期缓慢释放抗菌活性药物,且其物理性能没有减弱。
3 结语与展望
CPC具有良好生物活性和生物相容性,能任意塑形,自行固化,但是CPC性能与临床所需仍有一定差距。
与天然骨相比,CPC脆性大,力学强度低,不能应用于承重部位,所以其力学性能改善一直被重点研究。根据颗粒和纤维增强机制,将纳米颗粒和纤维引入CPC中,可使其内部结构致密,抗压强度增大,同时纤维在内部承担部分外界冲击应力,可提高其韧性和抗冲击能力。在体内植入环境下,CPC由于处于复杂的体液环境容易发生溃散,预设结构遭到破坏,颗粒冲散分布到其他部位,容易引起血管堵塞等并发症,研究者们通过增强水泥颗粒内部黏聚力来提高CPC的抗溃散能力,防止其植入体内发生溃散。从临床应用角度而言,CPC的可注射能力和放射不透明性都应引起重点关注,增强其可注射性有助于手术操作,而通过改善CPC的放射不透明性,使其与自体骨影像在放射条件下呈现不同程度亮度,便于操作人员观察骨水泥注射进度,防止发生骨水泥渗漏和填充不足。
CPC降解缓慢,不能诱导成骨细胞增殖分化和新血管生长,其生物学性能亦被重点关注。生物活性因子和生物活性离子在成骨过程发挥着重要作用,将它们引入CPC中,植入体内后可刺激成骨相关基因,参与成骨过程,促进新血管产生。CPC植入体内后,细胞逐渐长入水泥内部,在其内部发生增殖分化,同时与周围组织相结合,CPC应逐渐降解,最终新生骨组织取代CPC,骨缺损部位愈合。由于结构致密,内部大孔隙少,CPC降解速度缓慢,无法与骨生长速度相匹,将致孔剂掺入其中,促使内部产生大孔隙,可加速骨水泥降解。此外,CPC作为单一骨修复材料具有一定局限性,如何将其与药物相结合成为了研究热点;理想状态下,药物与CPC结合,随着CPC在体内降解,药物缓慢释放,植入部位可持续保持一定的药物浓度,使骨愈合和靶向治疗能够同步进行。总之,CPC理化性能和生物学性能如何综合改性以满足临床应用需求,成为CPC未来研究的新挑战。

