慢性髓系白血病ABL激酶区突变患者格列卫联合阿糖胞苷的疗效及预后分析*
杨 欢,刘 扬,陈相言,文 明,刘 徽
(四川省广安市人民医院风湿免疫与血液内科 638000)
慢性髓系白血病(chronic myeloid leukemia,CML)是一种克隆性恶性疾病,目前临床上一般采用干扰素、白消安等药物进行治疗,但治疗效果并不明显。虽然在临床上CML并不常见,但是倘若发病就会严重威胁患者的生命[1]。有研究显示,格列卫和阿糖胞苷可能对CML具有较好的治疗效果[2]。格列卫属于人工合成的酪氨酸激酶抑制剂,可使表达BCR/ABL的造血细胞停止凋亡。阿糖胞苷属于嘧啶类抗代谢药物,当细胞处于增殖期时,可直接作为DNA聚合酶的竞争性抑制剂,从而对DNA的合成产生抑制作用,影响白血病细胞增殖。考虑到此药物具有较好的耐受性和温和作用[3],本文将阿糖胞苷联合格列卫用于治疗CML ABL激酶区突变患者,观察治疗后的临床效果及对患者生存预后的影响,以期为临床治疗CML ABL激酶突变提供有利依据。
1 资料与方法
1.1 一般资料
选取2020年2月至2021年6月本院收治的271例CML ABL激酶区突变患者作为研究对象。纳入标准:(1)均符合《血液病诊断及疗效标准》[4];(2)未合并严重的心、脑、肝、肾功能损伤和其他系统性疾病;(3)对本文所使用的药物具备耐受性;(4)所有患者或家属均已签署知情同意书。排除标准:(1)药敏检查显示对本研究所使用的药物过敏;(2)哺乳期或妊娠者;(3)患有精神疾病或者意识不清的患者。将患者分为3组,格列卫组69例患者,其中男34例,女35例,年龄24~76岁,平均(40.26±6.51)岁;阿糖胞苷组91例患者,其中男45例,女46例,年龄26~77岁,平均(42.29±5.32)岁;联合组111例患者,其中男51例,女60例,年龄25~76岁,平均(41.39±6.19)岁。本研究已通过医院伦理委员会批准。
1.2 方法
格列卫组:使用格列卫治疗,在治疗初期口服格列卫,每天400 mg,分2次服用,之后根据患者的个人临床症状及生化指标随时调整用药。阿糖胞苷组:使用阿糖胞苷治疗,在治疗初期静脉滴注阿糖胞苷,按照1 kg体重2 mg阿糖胞苷的剂量,每天1次,连续使用14 d之后,根据患者的临床症状调整用药,当患者的临床症状得到缓解之后,按照1 kg体重1 mg阿糖胞苷的剂量,每天1次,连续使用7 d。联合组:同时使用两种药物,在治疗初期时患者口服格列卫,每天服用400 mg,分2次服用,同时静脉滴注阿糖胞苷,按照1 kg体重2 mg阿糖胞苷,每天1次,持续治疗14 d后依据患者生化检测指标调整药物使用剂量。
1.3 观察指标
3组患者随访12个月,记录随访期间骨髓细胞遗传学和血液学的缓解率。(1)完全血液学缓解(CHR)为白细胞计数<10×109,血小板计数<450×109,无不成熟细胞;(2)细胞遗传学缓解(MCyR)为中期分裂相细胞中1%~<35%表达PH染色体;(3)完全细胞遗传学缓解(CCyR)为中期分裂相细胞无PH染色体;(4)分子生物学缓解(MMR)为较治疗前血小板降低超过50%,但血小板计数<450×109,且脾脏较治疗前缩小50%;(5)完全分子生物学缓解(CMR)为中期分裂相细胞中35%~90%表达PH染色体;上述缓解情况使用实时定量聚合酶链反应检测。同时记录3组患者随访12个月期间血液学、细胞遗传学、分子遗传学的复发情况和不良反应发生率等。随访12个月期间观察3组患者死亡率和死亡时间、死亡原因(包括疾病进展、脑出血和心力衰竭)。
1.4 统计学处理
2 结 果
2.1 观察随访期间3组患者细胞遗传学和血液学缓解情况
接受6个月、12个月治疗后,联合组患者CHR、MCyR、CCyR、MMR及CMR明显高于格列卫组和阿糖胞苷组患者,差异有统计学意义(P<0.05),见表1。
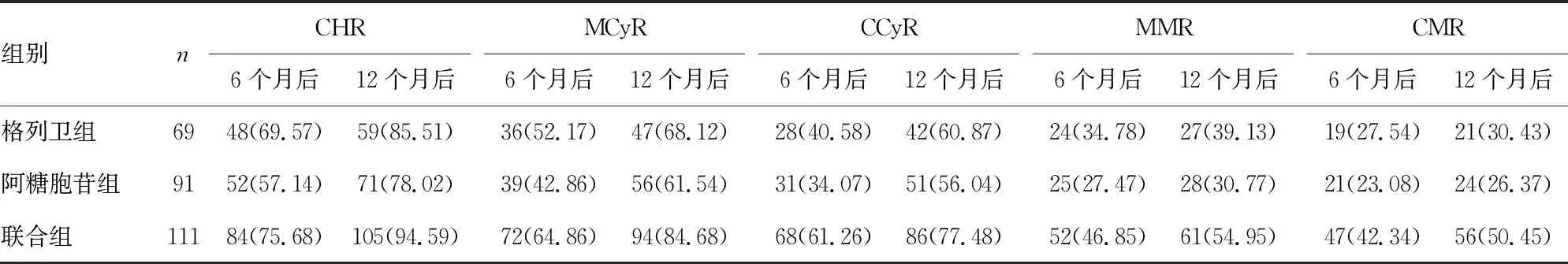
表1 3组患者血液学和细胞遗传学缓解情况[n(%)]
2.2 3组患者的复发情况
格列卫组和阿糖胞苷组患者的复发率比较差异无统计学意义(P>0.05),联合组复发率明显低于格列卫组和阿糖胞苷组(P<0.05),见表2。
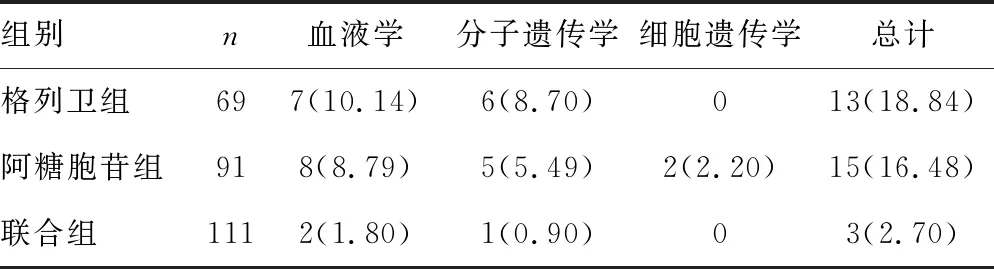
表2 3组患者在随访期间的复发率[n(%)]
2.3 随访12个月时3组患者的不良反应发生率
格列卫组药物不耐受、胸腔积液、血小板减少、中性粒细胞减少、皮疹、头痛、感染、肝功能异常和恶性、呕吐等不良反应发生率明显高于联合组和阿糖胞苷组(P<0.05),且联合组的不良反应发生率低于格列卫组和阿糖胞苷组(P<0.05),见表3。

表3 3组患者在随访期间发生的不良反应情况
2.4 3组患者的生存情况
统计随访结束后各组患者的生存情况,发现格列卫组患者的死亡率最高(7.24%),其次为阿糖胞苷组(6.59%),但是两组相比差异无统计学意义(P>0.05);联合组患者在随访期间的死亡率(1.80%)明显低于格列卫组和阿糖胞苷组(P<0.05),见表4。
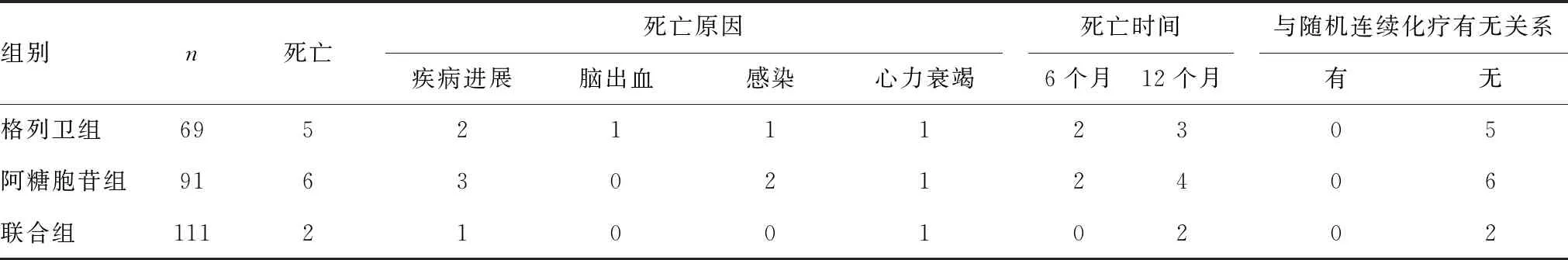
表4 3组患者在随访结束后的生存情况(n)
3 讨 论
CML在临床上属于恶性克隆性疾病,全球发病率为1.6~2.0/10万,且我国CML发生率较西方国家更加年轻化,中位发病年龄为45~50岁,而西方国家为67岁。临床将CML分为慢性期、无症状期、加速期和急变期4个时期,而多数CML患者发病时多为慢性期,主要症状为脾大、多汗、食欲不振和上腹部不适等情况,若未得到及时治疗进入急性期会威胁患者生命,对患者的健康造成严重影响[5-8]。目前临床主要采用酪氨酸激酶抑制剂(TKI)类药物治疗CML或采用造血干细胞移植、放射治疗或脾切除等,但进入急性期的患者应按照急性期白血病治疗方案治疗,但此时的缓解率较低[9-10]。有研究发现,CML患者发病过程中,ABL激酶区会发生突变,对治疗效果造成了严重影响,从而加重了病情的恶化[11]。研究显示,格列卫联合阿糖胞苷治疗CML,可对BCR/ABL起到明显抑制作用,抑制ABL激酶区的突变,从而提高治疗效果,改善临床预后[12-13]。
本研究发现,联合组治疗6个月、12个月时患者CHR、MCyR、CCyR、MMR及CMR明显高于格列卫组和阿糖胞苷组,与上述报道结果相似。本研究显示,联合组在随访6、12个月期间细胞遗传学、分子遗传学和血液学的复发率明显低于格列卫组和阿糖胞苷组,且联合组的不良反应发生率也明显低于单独用药的两组,说明格列卫联合阿糖胞苷治疗CML ABL可有效降低疾病的复发率,提高治疗效果。本研究还发现,联合组患者不良反应发生率明显低于单独用药的两组,而3组患者均出现不良反应,但联合组患者不良反应发生率低。由此可见,格列卫联合阿糖胞苷治疗能够显著降低患者的不良反应发生率,提高患者的生存质量。
本研究显示,格列卫组患者在随访期间的死亡率最高,为7.24%,与阿糖胞苷组(6.59%)比较无差异,但联合组患者的死亡率仅为1.80%,与其他两组比较有明显差异;此外,格列卫组死亡的5例患者中,2例死因为疾病进展、1例为脑出血、1例为感染、1例为心力衰竭。阿糖胞苷组死亡的6例患者中,3例死因为疾病进展、2例为感染、1例为心力衰竭。联合组2例患者的死因分别是疾病进展和心力衰竭。由此可见,格列卫联合阿糖胞苷治疗能够显著提高患者的生存率。由于死于疾病进展的患者较多,临床医师应当密切观察患者的临床症状,定期检测患者的临床指标,一旦发现患者有异常的情况发生,应该立即对患者采取相应的急救措施,挽救患者的生命[14-17]。
综上所述,格列卫联合阿糖胞苷治疗CML ABL激酶区突变患者能够显著提高其生存质量和生存率,值得推广应用。

