慢性肾脏病患者肾小球滤过率与甲状腺素指标的相关性及并发甲状腺功能异常的危险因素分析
王 洁,杨 勇,余 君
(1.浙江省湖州市第一人民医院肾脏内科 313000;2.湖北科技学院医学部健康医学院,湖北咸宁 437100)
慢性肾脏病(chronic kidney disease,CKD)是指由多种原因(如高血压、糖尿病、肾小球肾炎等)导致的慢性肾脏结构和功能障碍[1],其肾脏损害病史一般大于3个月[2]。CKD的全球患病率约14.3%,我国患病率约10.8%,且每年以8%的速度上升,该病预后差,治疗成本高,是一个全球性的公共卫生问题[3]。甲状腺激素是一组由甲状腺滤泡上皮细胞合成的碘甲腺原氨酸,主要包括三碘甲状腺原氨酸(triiodothyroxine,T3)和四碘甲状腺原氨酸(tetraiodothyroxine,T4),具有促进生长发育、维持正常新陈代谢和神经系统功能等作用[4]。研究认为甲状腺激素水平异常可能与CKD的发生和发展有关,肾功能障碍可能改变甲状腺激素合成、代谢和调节,降低机体甲状腺激素水平[5]。而甲状腺功能减退又会降低肾小球滤过率(glomerular filtration rate,GFR),增加CKD发生和发展的风险[6]。本研究通过检测不同CKD分期患者血清甲状腺功能指标水平,分析GFR与甲状腺功能指标之间的关系,探讨CKD并发甲状腺功能障碍的危险因素,为促进CKD的预防和治疗,改善预后,提供科学依据,报道如下。
1 资料与方法
1.1 一般资料
选取2020年5月至2021年5月在湖州市第一人民医院住院治疗的CKD患者152例。患者均符合美国肾脏基金会的CKD临床实践(K/DOQI)指南[7]中关于CKD的相关诊断标准,均无甲状腺疾病史。其中男91例,女61例;年龄27~89岁,平均(63.13±14.39)岁;病程0~41年,平均(14.08±5.27)年。患者签署知情同意书,本研究获得医院医学伦理委员会批准。
1.2 方法
患者入院时,收集临床基本资料,包括年龄、性别、身高、体重、血压(收缩压和舒张压)、吸烟史、饮酒史以及最早确诊时间(计算病程)等指标,同时采集患者空腹静脉血,分离血清,使用雅培CIL6200全自动生化分析仪检测血尿素氮(BUN)、血肌酐(Scr)和血尿酸(SUA);使用美国雅培i2000全自动化学发光免疫分析仪检测血清中总三碘甲状腺原氨酸(total triiodothyroxine,TT3)、游离三碘甲状腺原氨酸(free triiodothyroxine,FT3)、总甲状腺素(total tetraiodothyroxine,TT4)、血清游离甲状腺素(free tetraiodothyroxine,FT4)及促甲状腺激素(thyroid stimulating hormone,TSH)的水平。
1.3 观察指标及评价标准
采用改良MDRD公式[8-10]估算肾小球滤过率(glomerular filtration rate,GFR),并参照GFR值将慢性肾脏病分为5期[2],G1期:GFR≥90 mL·min-1·1.73 m-2,肾功能正常或增高;G2期:GFR 60~<90 mL·min-1·1.73 m-2,肾功能轻度降低;G3期:GFR 30~<60 mL·min-1·1.73 m-2,肾功能中度降低;G4期:GFR 15~<30 mL·min-1·1.73 m-2,肾功能重度降低;G5期:GFR<15 mL·min-1·1.73 m-2,肾衰竭。甲状腺功能的判定[11-13]:TT3、FT3、TT4、FT4和TSH 5项指标均在正常范围内则为甲状腺功能正常,有1项或1项以上指标不在正常范围内则为甲状腺功能异常。TT3的正常范围0.83~2.45 nmol/mL,FT3的正常范围2.63~5.70 pmol/L,TT4的正常范围62.68~150.80 nmol/L,FT4的正常范围9.01~19.05 pmol/L,TSH的正常范围0.35~4.94 mIU/L。
1.4 统计学处理

2 结 果
2.1 一般资料比较
不同CKD分期患者性别、年龄、病程、体重指数(BMI)和SUA差异无统计学意义(P>0.05),而Scr、BUN和GFR差异有统计学意义(P<0.05),Scr和BUN水平呈递增趋势,GFR呈递减趋势,见表1。

表1 不同CKD分期患者基本资料比较
2.2 各组患者甲状腺功能异常率和甲状腺素水平比较
不同CKD分期患者的甲状腺功能异常率差异有统计学意义(P<0.05),G5期最高,为39.1%,G1期最低,为8.3%;不同CKD分期患者血清TSH水平差异无统计学意义(P>0.05),而血清TT3、FT3、TT4和FT4水平差异有统计学意义(P<0.05),其中TT3随G1~G5期呈递减趋势,TT4和FT4呈先增后减趋势,见表2。

表2 不同CKD分期患者的甲状腺功能和甲状腺素水平比较
2.3 CKD患者甲状腺功能正常组与异常组的甲状腺素水平比较
与甲状腺功能正常组比较,甲状腺功能异常组的TT3、FT3、TT4和FT4水平下降,而TSH水平上升(P<0.05),见表3。

表3 CKD患者甲状腺功能正常组与异常组的甲状腺素水平比较分析
2.4 CKD患者GFR与甲状腺激素水平的相关性分析
使用Spearman秩相关检验分析患者GFR与甲状腺激素水平之间的相关性。CKD患者GFR与血清TT3、FT3水平呈正相关(P<0.05),其线性散点图见图1、2;与血清TSH水平呈负相关(P<0.05),其线性散点图见图3;与血清TT4、FT4水平无直线相关关系(P>0.05),其线性散点图见图4、5。
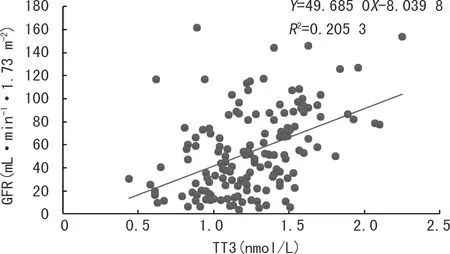
图1 CKD患者GFR与TT3的相关性散点图

图2 CKD患者GFR与FT3的相关性散点图

图3 CKD患者GFR与TSH的相关性散点图

图4 CKD患者GFR与TT4的相关性散点图
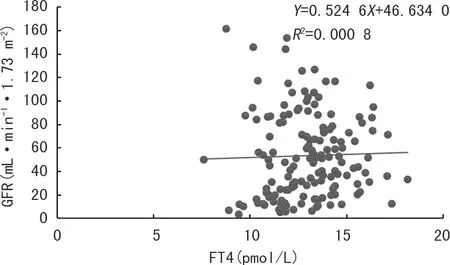
图5 CKD患者GFR与FT4的相关性散点图
2.5 CKD患者甲状腺功能异常的单因素分析
不同性别CKD患者甲状腺功能异常率有统计学差异,女性高于男性(P<0.05);不同CKD分期患者甲状腺功能异常率有统计学差异,G3、G4和G5期显著高于G1和G2期(P<0.05);而不同年龄、病程、体重、吸烟、饮酒和高血压特征的CKD患者甲状腺功能异常率无统计学差异(P>0.05),见表4。

表4 CKD患者甲状腺功能异常的单因素分析

续表4 CKD患者甲状腺功能异常的单因素分析
2.6 CKD患者甲状腺功能异常的多因素logistic回归分析
经二元logistic回归分析,发现CKD分期为G3~G5期和女性是CKD患者出现甲状腺功能异常的危险因素,差异有统计学意义(P<0.05);而年龄、病程、体重、是否吸烟、是否饮酒以及是否为高血压等特征不是导致CKD患者甲状腺功能异常的因素,差异无统计学意义(P>0.05),见表5。

表5 CKD患者甲状腺功能异常的多因素logistic回归分析
3 讨 论
甲状腺激素与人体代谢密切相关,可调节细胞糖类、脂类和蛋白质的合成与分解,具有促进细胞生长、组织形态分化等重要作用[14]。甲状腺激素T3和T4由甲状腺上皮细胞合成。生理状态下,进入血液循环的TT3和TT4大部分(99%以上)会与血浆蛋白(甲状腺素结合球蛋白)结合,而少部分以FT3和FT4的形式发挥激素作用,到达体细胞与特定受体结合(如甲状腺素运载蛋白)发挥生理作用[15]。甲状腺激素和肾脏二者之间相互作用并相互影响:一方面,甲状腺激素可调节肾脏早期的生长发育、肾小球和肾小管重要功能;另一方面,肾脏又可调节甲状腺激素的新陈代谢及消除[16]。当肾功能正常时,与血浆蛋白结合的甲状腺激素不会被肾小球滤过,当发展为CKD时,肾小球滤过膜受损,血浆清蛋白滤过肾小球,机体大量丢失清蛋白,不仅影响甲状腺激素的合成,还会降低原本合成的甲状腺激素,最终导致血液甲状腺激素水平下降[5,17]。本研究结果显示,随着GFR的下降,TT3和FT3呈逐渐下降的趋势,且GFR与TT3、FT3均呈负相关,甲状腺功能异常组的TT3、FT3、TT4和FT3均显著降低。原因是CKD会影响甲状腺功能,持续性肾功能不全可能导致甲状腺功能减退[18]。在CKD的特殊类型中,如微小变异性肾病综合征、局灶性节段性肾小球肾炎和膜性肾病,由于患者肾小球滤过膜受损,通常会出现大量蛋白尿,以至于甲状腺激素可能会漏入尿液丢失[19];同时大量的血浆蛋白丢失会影响甲状腺激素的合成和储存;CKD患者肾脏排泄功能出现障碍,会降低无机碘的清除率,过量的碘可经Wolff-Chaikoff效应降低甲状腺激素的合成[18]。本研究结果与胡蓉等[20]、REINHARDT等[21]和LI等[22]的结果很相似。
TSH被认为是一般人群中最敏感和最特异的甲状腺功能减退的一项指标[18]。TSH由垂体腺分泌,可调节甲状腺激素T3、T4的合成和分泌。当血中T3、T4水平降低时,通过反馈作用垂体细胞合成和分泌TSH,进而促进T3、T4的合成[15]。研究表明,即使在正常甲状腺激素水平下,FT3和FT4水平下降及TSH水平上升可能增加肾病发生的风险[23]。本研究各CKD分期组患者TSH与GFR呈负相关关系,且TSH水平随GFR的降低而呈升高趋势,甲状腺功能异常组的TSH水平显著上升。TSH水平原因可能是患者肾小球滤过膜受损,体内TT3、FT3漏入尿液丢失、水平下降,进而反馈促进垂体细胞合成TSH;另外患者TSH糖基化不良,失去昼夜节律,生物活性受损也是原因之一;此外,TSH浓度增加还可能和TSH对促甲状腺激素释放激素(thyrotropin-releasing hormone,TRH)的反应迟钝,TSH和TRH清除率下降有关[24-25]。本研究结果与胡爱娥[26]、LI等[22]的研究结果相似。虽然本研究患者CKD各分期TSH水平无统计学差异,但是TSH随CKD进展呈增加趋势,无统计学差异原因是本次观察的样本含量较少,加上个体间TSH值波动性大,采用正态性检验发现TSH值呈偏态分布,只能采用非参数秩和检验,导致检验效能不如参数检验,因此在今后的研究中要进一步增加样本量,提高检验效能。
年龄、性别和CKD进展被认为是患者出现甲状腺功能异常重要因素[18]。YUASA等[19]的研究显示,CKD患者的年龄、GFR与甲状腺功能减退相关,甲状腺功能减退组患者的年龄显著大于对照组,而GFR则显著低于对照组;多因素分析结果显示,高年龄(OR=1.04,95%CI:1.01~1.07)是CKD患者并发甲状腺功能减退的危险因素,但是较高的GFR(OR=0.96,95%CI:0.95~0.99)是保护因素。HUANG等[27]的研究表明,55岁及以上的人群中,患有甲状腺功能减退症的人更容易患CKD,甲状腺功能低下(OR=1.59,95%CI:1.52~1.66)和甲状腺功能减弱(OR=1.12,95%CI:1.08~1.16)是CKD的危险因素。本研究未发现55岁及以上CKD患者甲状腺功能异常率显著高于55岁以下,原因可能是55岁以下患者人数偏少(44例),存在一定的选择偏倚。一般认为,女性甲状腺功能减退的发病率高于男性[28]。CHUANG等[29]的回顾性队列研究表明,女性亚临床甲状腺功能减退与CKD风险增加相关(HR=1.22,95%CI:1.08~1.39)。本研究女性CKD患者甲状腺功能异常率高于男性,与相关研究报道一致。CKD的进展与甲状腺功能障碍有关。KHATIWADA等[30]的横断面研究结果表明,CKD 4期和5期CKD患者发生甲状腺功能障碍的风险明显高于3期患者,多因素分析结果显示4期(OR=2.1,95%CI:1.28~3.42)和5期(OR=3.64,95%CI:1.94~6.85)CKD患者是甲状腺功能障碍的危险因素。本研究发现CKD 3~5期是甲状腺功能障碍的危险因素,与KHATIWADA等[30]的结果很相似。
多项临床流行病学研究结果提示,不同程度甲状腺功能异常与肾功能异常的发生、发展密切相关[31-33]。甲状腺功能的下降可能会对CKD患者的肾脏造成进一步的损害。甲状腺激素不足会影响蛋白质合成和细胞发育,导致肾脏变小[6]。另外,甲状腺激素不足还可能降低肾脏血流量,进而诱发一系列并发症,例如肾小球出现基底膜增厚、毛细血管压增高和滤过膜损伤,以及肾小管排泄功能受损等问题[17]。甲状腺功能异常在不需要长期透析治疗的CKD患者中比较普遍,在不需要肾脏替代治疗的CKD患者中,亚临床甲状腺功能减退和临床甲状腺功能减退的发生率约为18%~20%[18,34]。本研究CKD患者的甲状腺功能总异常率为23.7%,其中G5期患者高达39.1%,甲状腺功能异常发生率较高,说明CKD患者的甲状腺功能异常是临床常见并发症,提示临床医生和护士应及时关注患者的甲状腺功能,观察甲状腺激素水平波动对观察患者病情进展的影响,结合患者游离T3和TSH情况进行干预,必要时进行营养干预,再考虑甲状腺素补充治疗。
本研究有一定的局限性,首先,这是一项横断面研究,因此无法确定因果关系;其次,研究数据不是全面筛查所得,因此可能高估了CKD患者中甲状腺功能异常的真实患病率;最后,本研究缺乏关于CKD患者甲状腺功能异常可能病因的详细信息(如抗甲状腺抗体、尿蛋白等)的测量,在解释具体的发生机制方面缺乏证据。因此,今后可开展前瞻性队列研究,阐明甲状腺素与肾小球滤过率之间的作用关系,并更好地了解CKD患者中甲状腺功能异常的真实患病率。
综上所述,不同分期CKD患者血清甲状腺功能指标可出现不同程度改变,CKD女性患者更易出现甲状腺功能异常。建议临床医生密切监测CKD患者血清甲状腺功能指标的水平,研究患者肾功能与甲状腺功能之间的相互关系,未来使用更多明确的证据证实甲状腺激素替代治疗甲状腺功能减退能否改善CKD预后。

