磷酸盐尿性间叶性肿瘤影像学表现及文献回顾
岳梦情,张家雄
磷酸盐尿性间叶性肿瘤(phosphateuria mesenchyal tumor,PMT)是一种罕见的间叶源性肿瘤,多数为良性肿瘤,临床上首发症状常表现为全身骨痛、佝偻病、骨质疏松、骨质软化、病理骨折等,而原发瘤隐蔽,因此常导致误诊、漏诊。本研究回顾性分析4例PMT,结合其临床、影像、病理及相关文献等进行分析总结,提高对该病的认识。
材料与方法
回顾性分析2019年-2021年4例与骨质疏松、骨软化相关的经手术病理证实为PMT的患者的病例资料。其中男3例,女1例;年龄38~56岁。3例有2~6年全身多发骨关节疼痛病史,进行性加重,且伴骨质疏松、畸形或病理性骨折病史;1例无明显全身症状,仅在头部外伤后行MR检查时偶然发现颅内颞部肿瘤。
结 果
4例PMT,位于臀部软组织1例,肱骨1例,胫骨1例,颅内1例。
3例有全身骨质疏松软化,伴多发陈旧性病理性骨折、畸形,常规影像上原发瘤征象不太明确;1例颅内肿瘤患者原发瘤影像征象明确,但无明显骨质疏松软化征象。
血磷降低3例,1例血磷正常;碱性磷酸酶升高3例,1例正常;4例血钙均正常。3例血磷降低患者,肿瘤切除术后,血磷逐渐恢复正常,碱性磷酸酶较术前有降低。全身骨痛症状逐渐减轻。
3例病理诊断为磷酸盐尿性间叶源性肿瘤;1例右臀部肿物为纤维硬化性脂肪瘤(纤维瘤样脂肪瘤)。
病例1,男,38岁。2年前无明显诱因出现双髋部、胸部及腰背部疼痛、活动受限,在当地医院就诊,诊断为“双股骨近端骨折”;因症状持续,近期进行性身高下降,躯干出现挛缩,驼背、鸡胸,双下肢及胸背部疼痛、活动受限加重,来本院就诊。查体:体温36.7℃ ,心率106次/分钟,呼吸20次/分钟,血压122/98 mmHg,蹒跚步态,躯干畸形,驼背、鸡胸,双竖棘肌紧张,压痛(+),腰部活动受限,双髋内翻畸形,“4”字试验(±),髋关节活动受限,双下肢肌力正常。右臀部可见一大小约1 cm×1 cm×1 cm肉色肿物,无压痛,边界清楚;外院PET-CT示该部位局部高代谢灶。
实验室检查:术前血磷0.42 mmol/L(正常值0.81~1.65 mmol/L),血钙2.28 mmol/L(正常值2.03~2.54 mmol/L);碱性磷酸酶344.8 U/L(正常值53.0~128.0 U/L)。甲状旁腺激素及甲状腺功能三项正常;类风湿因子、HLA-B27、风湿病自身免疫性抗体谱定量阴性;肝肾功能、血沉、血常规、尿常规及大便常规正常。
影像学表现:全身多部位骨质疏松、软化;多发胸腰椎椎体“双凹状”变扁,双侧多发肋骨和双侧股骨上端陈旧性骨折畸形愈合或骨不连(图1a~c)。
治疗与转归:在局麻下行右臀部肿物切除术。术后病理结果(图1d):(右臀部肿物)纤维硬化性脂肪瘤(纤维瘤样脂肪瘤)。术后1周复查碱性磷酸酶有下降(321.6 U/L),半年以后复查碱性磷酸酶正常(84.7 U/L);术后血磷逐渐恢复正常(术后1周血磷0.52 mmol/L,术后约2周血磷1.82 mmol/L)。

图1 男,38岁。a)双侧多发肋骨陈旧性骨折;b)多发胸腰椎不同程度双凹状变扁;c)右股骨颈、左股骨粗隆间、双侧耻骨上下支陈旧性骨折;股骨颈和粗隆间骨折成角畸形、骨不连;d)镜下见纤维脂肪组织,纤维组织玻璃样变,脂肪组织部分坏死(HE,×100)。
病例2,男,56岁,全身骨痛进行性加重6年,曾在外院多次行颈椎内固定、双髋关节置换术等。发现右胫腓骨骨折。双能骨密度检查:腰椎骨密度降低、前臂1/3桡骨骨密度降低,符合严重骨质疏松症。临床考虑低磷性骨软化症可能。
实验室检查:术前血磷0.42 mmol/L;血钙2.23 mmol/L;碱性磷酸酶333.0 U/L。甲状旁腺激素及甲功三项正常;类风湿因子、HLA-B27、风湿病自身免疫性抗体谱定量阴性;肝肾功能、血沉、血常规、尿常规及大便常规正常。
影像学表现:CT上可见右肩关节骨质疏松,肱骨大结节邻近见局限性小片状骨密度增高,密度不均,边界较清(图2a)。X线片见全身多发骨质明显疏松;双侧多发肋骨陈旧性骨折、畸形;右侧胫腓骨下端陈旧性骨折、畸形(图2b~c)。外院PET-CT(奥曲肽)检查:右肱骨大结节髓腔内小结节,DOTA-TATE代谢异常增高。
治疗与转归:手术凿开右肱骨大结节下骨皮质清除颜色较深病灶组织,植入异体骨。术后病理结果(图2d):结合临床实验室检查及免疫组化,符合骨磷酸盐尿性间叶性肿瘤(肿瘤性骨软化症)。

图2 男,56岁。a)CT平扫冠状面示右肱骨大结节小片高密度影,密度不均,边界较清;b)X线片示右胫腓骨下端陈旧性骨折、成角畸形、骨不连;c)X线片示双侧多发肋骨陈旧性骨折畸形愈合;d)病理图(HE,×100)镜下骨小梁间见梭形、卵圆形纤维母细胞样细胞增生,间质见丰富的厚壁血管,大部分血管出现管周肌性改变。
术后第3、4天查血磷分别为0.52 mmol/L、0.61 mmol/L,碱性磷酸酶289.0 U/L。术后1周血磷1.26 mmol/L。
病例3,女,46岁,6年前无明显诱因下出现全身多处疼痛,以左髋部疼痛伴左下肢疼痛、活动受限为主,曾在外院治疗;近1年来病情加重,遂到本院就诊。查体:左髋部轻压痛,髋关节内收内旋活动轻受限,双下肢肌力3级。
实验室检查:术前血磷0.58 mmol/L,血钙2.15 mmol/L,碱性磷酸酶274.5 U/L。甲状旁腺激素及甲状腺功能三项未见异常;类风湿因子、HLA-B27、风湿病自身免疫性抗体谱定量阴性;肝肾功能、血沉、血常规、尿常规及大便常规正常。
影像学表现:X线片示全身多发骨质明显疏松;双侧多发肋骨陈旧性骨折、畸形;左腓骨上段、双侧耻骨上下支和双侧股骨颈陈旧性骨折。左胫骨上端骨密度高低不均(图3a~d)。外院PET-CT检查提示:左胫骨上端局限性高代谢灶。
治疗及转归:左胫骨平台外侧凿开骨皮质,行病灶刮除、灭活、植骨术。术后病理结果(图3e):结合临床,免疫组化报告,(左胫骨)符合磷酸盐尿性间叶性肿瘤(骨软化症相关性间叶肿瘤)。术后服用服用维生素D2片及骨化三醇软胶囊。术后第2、3、5天复查血磷分别为0.87 mmol/L、0.70 mmol/L、1.20 mmol/L。术后1个月骨痛症状逐渐缓解。术后约2个月血磷1.53 mmol/L,碱性磷酸酶231.0 U/L。

图3 女,46岁。a、b)X线片示左腓骨上段陈旧性骨折、愈合不良,胫骨上端骨结构模糊,密度不均;c)X线片示双侧耻骨上下支和双侧股骨颈陈旧性骨折愈合后表现;d)X线片示双侧多发肋骨陈旧性骨折愈合后表现;e)病理图镜下见纤维钙化性病变,镜下瘤组织主要由梭形、卵圆形细胞构成,夹杂多灶絮凝状、软骨样钙化性基质,另见少许多核巨细胞及含铁血黄素沉积(HE,×100)。
病例4,男,56岁,1年前车祸后影像学检查偶然发现颅内左颞部肿物,近1年来肿物逐步增大,偶有头痛,可自行缓解,无呕吐、四肢抽搐等不适。
实验室检查:术前血磷1.21 mmol/L,血钙2.44 mmol/L,碱性磷酸酶61.8 U/L。肝肾功能、血沉、血常规、尿常规及大便常规正常。
影像学表现:MR平扫+增强:左侧中颅底肿块,T1稍低混杂信号,T2稍高混杂信号,增强见肿块明显不均匀强化,边界清;颞骨、颧骨等骨质破坏。CT 平扫:左侧颞部稍高密度肿块,边界较清,密度不均,肿块内见斑点状钙化灶,颞骨、颧骨等骨质破坏。胸部X线片未见明显骨质疏松软化征象(图4a~f)。
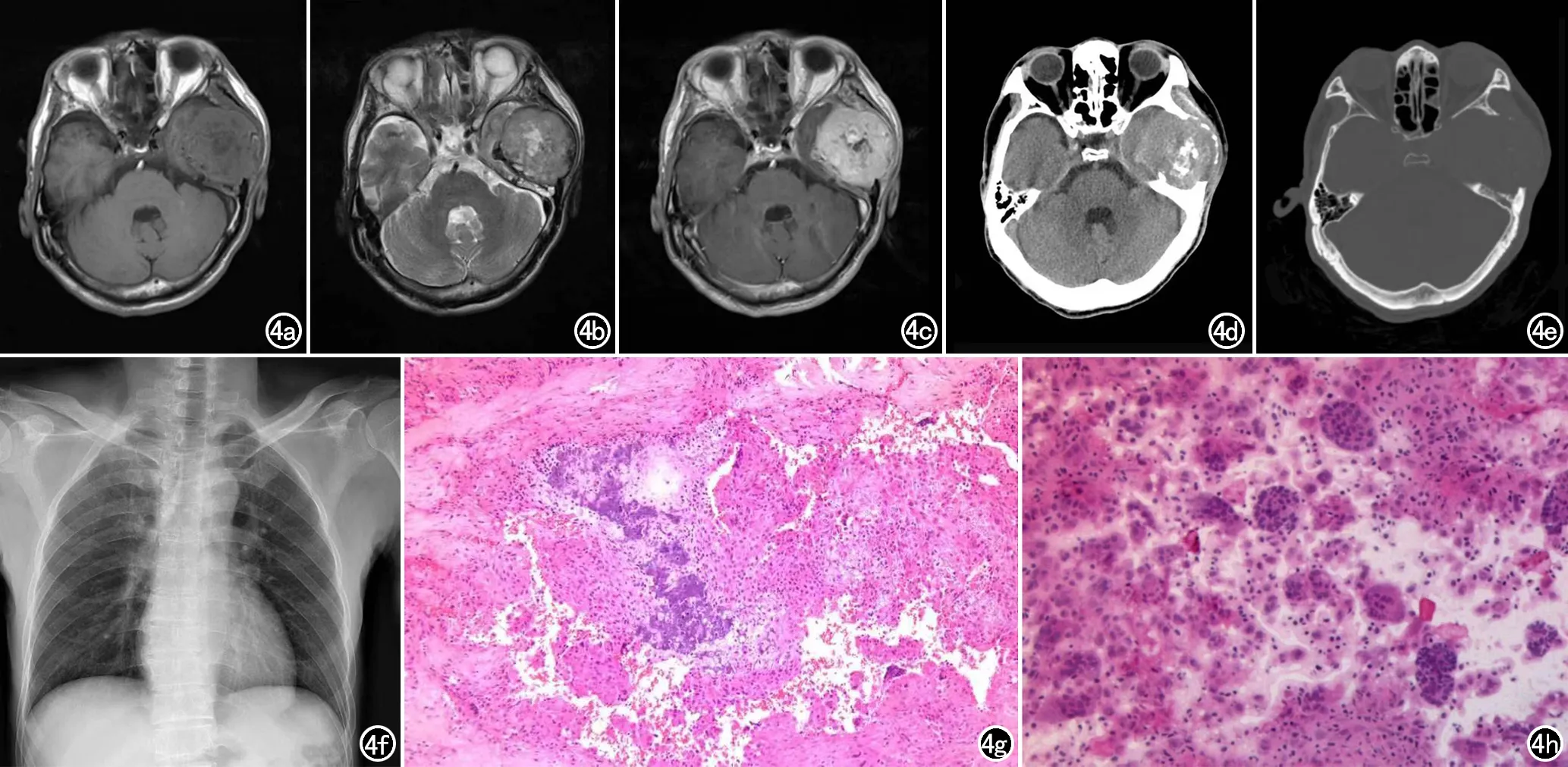
图4 男,56岁。a)T1示左侧中颅窝肿块呈稍低混杂信号;b)T2示病灶呈稍高混杂信号;c)MR增强示肿块明显不均匀强化,边界清;d、e)CT平扫示左侧颞部稍高密度肿块,边界较清,密度不均,肿块内斑点状钙化灶,颞骨、颧骨等骨质破坏,未见明确骨膜反应;f)胸部X线片各骨未见明显异常;g)镜下见肿瘤主要由卵圆形细胞组成,未见明显核分裂,夹杂散在破骨样多核巨细胞及微囊形成,部分区域呈纤维组织细胞瘤样,间质较多烟熏样基质及絮凝状钙化灶穿插,可见粘液囊性变,瘤体内血管丰富(HE,×100);h)免疫组化:瘤组织Vim(+)、EMA散在少量(+)、Fli-1散在(+)、ERG散在(+)、SMA及MSA(+)、CD56局灶(+)、D2-40局灶(+)、SATB2小灶(+)、F8、CD31及CD34标记血管内皮、AE1/AE3(-)、S100(-)、GFAP(-)、PR(-)、Ki-67热点区约5%(+)、CD63散在(+)、CD68标记多核巨细胞。
治疗及转归:切开左侧额颞部头皮,颅骨破坏,见灰白色类圆形肿物,包膜完整,伸入中颅窝,颞骨、颧骨侵蚀破坏,完整切除肿瘤。术后病理结果:形态学结合影像表现及免疫组化,考虑为颅内磷酸盐尿性间叶性肿瘤(图4g~h)。术后服用维生素D2片及骨化三醇软胶囊。术后第2、7天复查血磷分别为1.34 mmol/L、1.22 mmol/L,血钙分别为2.04 mmol/L、2.24 mmol/L。
讨 论
肿瘤性骨软化症(tumor-induced osteomalacia,TIO)是一种由原发肿瘤特征性地分泌纤维母细胞生长因子(fibroblas growth factor 23,FGF-23),抑制肾重吸收磷,使得25-羟维生素D-1a羟化酶调节能力下降,从而使尿磷排泄增多,导致骨骼矿化障碍、骨质软化的少见的副瘤综合征,临床上表现为进行性肌无力、肌肉痛和骨痛及反复性骨折,实验室检查以低血磷、低血1,25二羟维生素D为特点,血钙、甲状旁腺激素和25-羟维生素D表现正常[1]。TIO少数情况下与某些肿瘤有关(例如有文献报道,结肠腺癌、卵巢浆液性癌、肾透明细胞癌、前列腺癌、肺小细胞癌、甲状腺间变性癌中,均可能出现TIO样表现,包括血清FGF23水平升高导致肾磷丢失的骨软化症临床表现),但大部分是软组织或骨组织的间叶性肿瘤所致,以往认为,所有类型间叶性肿瘤都可以导致骨质软化症,但近些年研究表明,不同类型的间叶性肿瘤几乎都属于一种形态学和遗传学具有独特之处的肿瘤,即PMT。1947年,McCance等[2]报道了第一例股骨肿瘤所致的骨软化症,1959年Prader等[3]阐述了间叶性肿瘤与骨质软化的关系;直至1987年Weidner等[4]才首次将骨质软化症相关间叶性肿瘤命名为“磷酸盐尿性间叶性肿瘤-混合组织亚型”。1991年Folpe等提出PMT四种亚型,包括混合结缔组织型、骨母细胞样型、非骨化性纤维样型及骨化性纤维样型,其中以混合结缔组织亚型最为常见[5]。按照肿瘤发生部位可分为骨组织及软组织来源,发生在软组织的相对较多[6]。WHO(2013)软组织肿瘤分类中,PMT首次被收录[7]。PMT肿瘤细胞一般表现为形态温和的纺锤状、卵圆形或星状细胞,间质富于血管且常呈微囊性改变,还可发现破骨细胞样巨细胞、脂肪细胞,软骨样、类骨样或钙化基质,可见出血区域[8]。
既往文献报道引起骨软化的原发性肿瘤主要为间叶性肿瘤,如:胸膜外脂肪瘤样型孤立性纤维性肿瘤、腓骨头纤维血管瘤、鼻腔血管外皮瘤、血管球周皮细胞瘤、血管内皮瘤、纤维血管瘤、 腱鞘巨细胞瘤、腱鞘纤维瘤、梭形细胞瘤、去分化脂肪肉瘤、下颌骨肌纤维母细胞等。
结合文献及本组病例,PMT具有以下临床及影像学的特点:①PMT好发于成年人,以40~60岁最为常见,偶发生于儿童引起佝偻病[9],隐匿起病;②临床表现为四肢乏力,进行性骨痛,骨痛以四肢及负重关节为主,常伴骨折,身高进行性下降等;③无家族性佝偻病或骨软化史;④辅助检查提示低血磷;⑤影像学表现为全身骨质疏松,部分伴病理性骨折的骨软化表现及骨或软组织原发瘤。原发瘤CT可表现为软组织肿块或骨骼溶骨性破坏或混合性骨破坏等;MR根据瘤内成分不同,表现为T1呈等信号或混杂信号,T2呈高或高低混杂信号,增强扫描可呈轻-中度强化;放射性核素扫描在寻找软组织隐匿性PMT的检测中往往有较高的价值,作为代谢活性肿瘤,可通过99mTc-MIBI SPECT、18F-FDG PET/CT发现隐匿性PMT肿瘤分布[10]。
PMT的诊断因原发瘤影像学上无特征性、而且往往较隐蔽,其主要依据实验室检查(低血磷,高尿磷、血碱性磷酸酶升高、FGF-23等)和影像学上骨质疏松、软化征象,CT、MR或放射性核素扫描找到原发瘤等综合分析可作出诊断。但有些软组织和骨来源的肿瘤会有PMT的形态学特点,且有FGF23的表达,但无明确的骨软化症,这类肿瘤近些年研究已明确为非高磷酸盐尿性的亚型,本文颅内肿瘤病例可能属于此亚型。对于非高磷酸盐尿性的亚型这类患者,无骨质疏松、软化,无血磷降低表现,术前要作出PMT的诊断则非常困难。
该疾病需与其他原因所致骨质疏松、骨软化的疾病相鉴别:①常染色体显性低磷性佝偻病:常见于儿童,有家族病史;骨质密度降低、干骺端杯口状及毛刷状等佝偻病表现,生长缓慢;颅骨、胸廓、脊柱、关节等畸形。②X连锁显性低磷性佝偻病:常见于儿童,女性多于男性;长管状骨弯曲畸形,干骺端不规则,呈杯口样毛刷状等佝偻病表现,生长缓慢;下肢异常较上肢明显,以股骨下端变形及距骨颈短缩、距骨穹窿扁平改变常见;颅骨、胸廓、脊柱、关节等畸形。③甲状旁腺功能亢进骨病:普遍性骨质疏松,单发或多发骨质破坏;发生在脊椎可呈夹心面包征改变,可伴棕色瘤形成;骨膜下骨吸收破坏:最常见于第二、三指中节指骨桡侧皮质缘呈花边状、虫蚀状改变;软骨下骨吸收:常累及锁骨远端、骶髂关节和耻骨联合。④成骨不全症:临床表现为反复骨质脆性骨折史、蓝巩膜、进行性听力下降;颅骨、脊柱畸形,椎体双凹征改变;长骨纤细、多发骨折可致弯曲变形。⑤除了上述疾病之外,还需要注意与骨髓瘤、贫血(如地中海贫血、镰状细胞贫血等)、慢性白血病等所致全身骨质疏松、破坏等疾病相鉴别,结合临床和实验室检查鉴别不难。对于发生在骨组织的原发病灶,结合病理镜下成分鉴别意义更大,当某病例出现骨样基质、软骨样基质、多核巨细胞及不规则钙化时,需要考虑到骨肉瘤、软骨类肿瘤(软骨母细胞瘤、内生软骨瘤等)及骨的富于巨细胞肿瘤(如骨巨细胞瘤、巨细胞修复性肉芽肿)并进行鉴别:①对于本文病例2,需要考虑到骨样骨瘤及骨母细胞瘤,病灶可发生在椎体、附件及长骨,表现为骨质破坏,典型者破坏区内可有钙化或骨化,骨母细胞瘤肿瘤范围大于骨样骨瘤,当病灶部位出现夜间痛明显,服用水杨酸可缓解为骨样骨瘤特点。②对于某些发生在骨组织中,出现片絮样、边界模糊或大量钙化、骨样基质肿瘤需要与骨肉瘤鉴别,如本文病例3,胫骨上端出现片絮状高密度影,边界不清,需要考虑到不典型骨肉瘤。典型原发性骨肉瘤多见于青少年,患处肿痛、皮温升高,好发于股骨下端及胫骨上端,骨质破坏明显或有成骨表现,出现肿瘤骨、软组织肿块形成,可出现Codman三角骨膜反应。对于原发病灶位于颅内的肿瘤,例如,本文病例4,该病例最容易误诊为脑膜瘤,典型脑膜瘤与硬脑膜或颅骨以宽基底相连,CT呈等或稍高密度,密度常较均匀,少有囊变坏死,可以沙砾样钙化;MRI上呈T1WI等或稍低信号,T2WI稍高信号,增强扫描较均匀明显强化,可有脑膜尾征,周围水肿轻,邻近骨质常出现骨质增生硬化。对于其他原发病灶位于软组织的肿瘤,应根据不同部位好发肿瘤的不同临床、影像及病例特点进行相应考虑并与之鉴别。
综上所述,当成年人出现乏力、骨痛、骨密度降低、进行性身高下降等骨质软化症状,生化检查呈现低血磷、高尿磷的特点,要考虑磷酸盐尿性间叶性肿瘤性骨软化症的可能。