进展性脑梗死动脉粥样硬化相关危险因素分析
董书宇 田永芳 陈巍巍 谢志远 鹿寒冰 周生奎▲
1.江苏省徐州市中心医院神经内科,江苏徐州 221000;2.江苏省徐州市中心医院胃肠外科,江苏徐州 221000
急性脑梗死又称急性缺血性脑卒中(acute ischemic stroke,AIS),是由于动脉粥样硬化等原因使脑动脉供血障碍造成的脑组织损伤及脑功能异常[1],其发病率高且近年来日趋年轻化。进展性脑梗死(progressive ischemic stroke,PIS)是AIS在早期阶段(时间大多在6 h至1周内)症状持续性进展加重的临床亚型,其在AIS各分型中最为严重且难治,约占全部脑梗死患者的26%~43%,病情凶险,病死率、致残率极高,给社会和家庭造成巨大负担[2-3]。AIS主要病因为动脉粥样硬化,动脉粥样硬化斑块形成、血管内炎症反应与感染等因素均对动脉粥样硬化发生发展起重要作用。本研究对2019—2020年度病历资料进行回顾性分析,探讨可能影响PIS发生的动脉粥样硬化相关危险因素,为其临床治疗提供依据。
1 资料与方法
1.1 一般资料
收集徐州市中心医院2019年1月至2020年12月的146例AIS患者的临床资料并分组。其中,进展组(PIS组)患者84例(57.53%),年龄48~84岁;非进展组(NPIS组)患者 62例(42.47%),年龄52~90岁。纳入标准:符合《中国急性缺血性脑卒中诊治指南2018》[4]中AIS的诊断标准,通过颅脑CT平扫或MRI确诊为脑梗死。排除标准:混合性脑卒中者;合并急性心血管事件、周围血管闭塞性疾病者;近1月有手术或外伤史者;合并肿瘤、风湿、血液系统疾病者;严重脏器功能不全者;近1周内使用糖皮质激素者;合并心房颤动者、可能存在栓塞者;有精神疾病者。PIS组于发病后6 h至1周内,积极治疗后神经功能缺失症状仍加重,美国国立卫生研究院卒中量表(NIHSS)评分较前增加3分以上[3]。本研究已经医院医学伦理委员会审批。
1.2 方法
记录两组性别、年龄、吸烟史、饮酒史、高血压病、糖尿病、冠心病、颅内或颈动脉狭窄[5]、低回声斑块、卒中相关肺部感染(stroke-associated pneumonia,SAP)等一般情况,记录并计算载脂蛋白B和载脂蛋白A1比值(apolipoprotein B/A1 ratio,ApoB/ApoA1)、单核细胞和高密度脂蛋白胆固醇比值(monocyte/high density lipoprotein ratio,MHR)、同型半胱氨酸(homocysteine,HCY)水平、脂蛋白相关磷脂A2(lipoprotein associated phospholipid A2,Lp-PLA2)水平。其中,颅内或颈动脉狭窄均为颅脑MRA/头颈CTA确诊,低回声斑块行颈部血管彩超明确,SAP通过胸部CT平扫证实,生化指标均为患者入院24 h内常规抽取的肘静脉血检测,实验室结果包括血细胞分析、血脂水平、HCY、Lp-PLA2。
1.3 统计学处理
采用SPSS 23.0软件对数据进行统计学分析处理,计量资料用均数±标准差()表示,采用独立样本t检验,计数资料用[n(%)]表示,采用χ2检验,对单因素分析有意义的因素继续采用logistic回归分析,P< 0.05为差异有统计学意义。
2 结果
2.1 影响AIS患者PIS发生的单因素分析
两组部分一般情况(包括性别、年龄、吸烟史、饮酒史、高血压病、糖尿病、冠心病)比较,差异无统计学意义(P> 0.05);PIS组的颅内或颈动脉狭窄、低回声斑块、SAP占比及ApoB/ApoA1、MHR、HCY、Lp-PLA2水平明显高于NPIS组,差异有统计学意义(P< 0.05),见表1。

表1 影响AIS患者PIS发生的单因素分析[n(%)]
2.2 影响AIS患者PIS发生的多因素分析
颅内或颈动脉狭窄、低回声斑块、SAP、高ApoB/ApoA1、高 MHR、高 HCY、高 Lp-PLA2是影响 PIS发生的独立危险因(P< 0.05),见表 2~3。
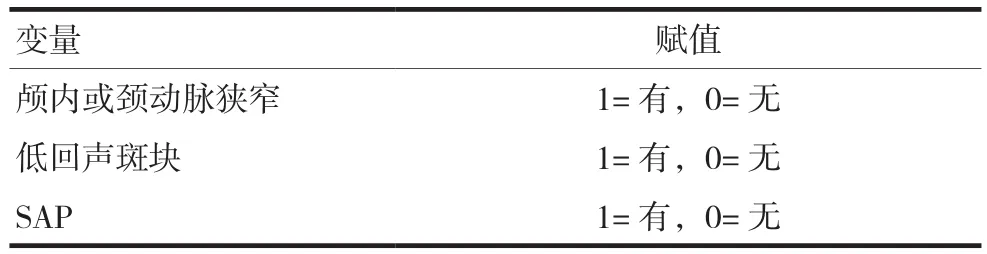
表2 赋值表
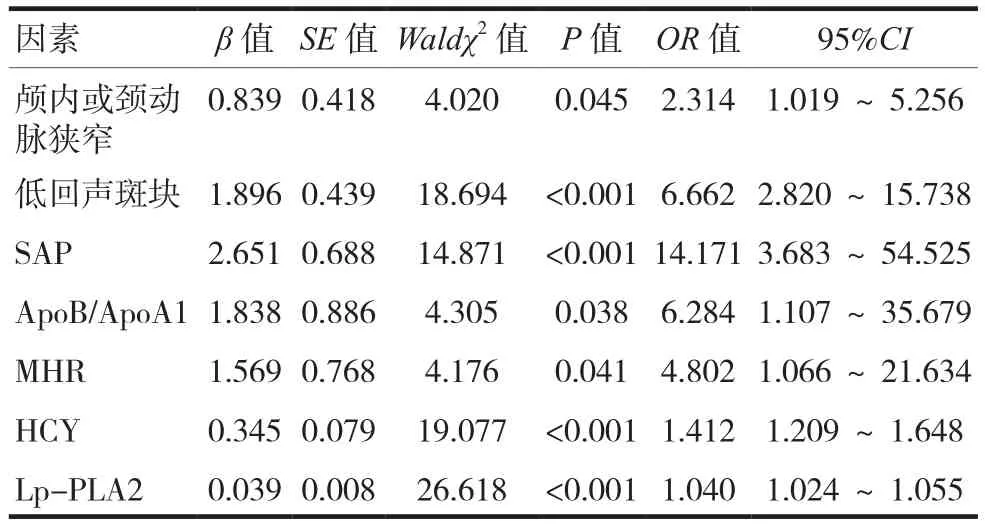
表3 影响AIS患者PIS发生的多因素分析
3 讨论
PIS是AIS的一种典型类型,是导致AIS患者预后不佳的重要因素[2],其机制至今仍未完全阐明。目前,临床上提倡“早发现,早治疗”的防治理念,对于病情转归具有十分重要的意义。
颅内或颈动脉狭窄和低回声斑块与动脉粥样硬化发生密切相关,均可推进PIS发展。产生机制可能是颅内或颈动脉狭窄后,脑灌注急剧下降、血栓负荷加重,引发神经缺损症状,同时低回声斑块的破裂脱落可加剧血栓形成,进一步影响血供,从而发生PIS。血脂异常也可推动动脉粥样硬化进展。ApoB主要作用是诱发动脉粥样硬化,可诱导泡沫细胞生成;ApoA1主要作用是抵抗动脉粥样硬化,并具有一定抗炎作用。多项研究表明,ApoB/ApoA1升高是短暂性脑缺血发生的危险因素之一,且其对评估脑血管病危险程度较测定单个血脂指标更有意义[5]。该指标越高,反映颅内供血动脉粥样硬化发生发展趋势越明显,发生PIS可能性越大。
有文献指出,炎症与感染是AIS进展的重要危险因素[6]。当AIS发生后,脑血管发生狭窄、闭塞可致脑组织细胞缺血、缺氧,可加重炎症因子释放及氧化应激过程,进一步加重脑组织、血管内皮功能损伤,从而导致PIS发生[6]。MHR是一项新发现的炎症相关指标[7],与心脑血管不良事件、动脉粥样硬化型斑块的稳定性、高血压并发AIS密切相关[8]。本研究结果显示,高MHR对于预测PIS发生有一定意义。其机制可能是:①单核细胞活化释放大量炎症因子推进炎症反应,降低斑块稳定性形成游离栓子,游离栓子数量增加导致PIS发生;②高密度脂蛋白胆固醇(HDL-C)下降时,对内皮细胞保护作用减弱,抗动脉粥样硬化作用减弱,更易发生PIS。
SAP是最常见的AIS并发症之一[6,9],且其大多合并发热。发生SAP后,机体内环境中性粒细胞百分比升高,可促进炎症反应、释放活性物质,增加脑细胞缺血坏死面积,可致神经功能缺损程度加重。除此之外,受发热因素影响,缺血、缺氧所致坏死的脑组织可进一步发生酸中毒,加速PIS进程。本研究结果显示,SAP与PIS的发生密切相关,故SAP的早期发现、防治工作,对于改善PIS预后有重大意义。
Lp-PLA2及HCY均可作为心脑血管疾病的预测指标[10-12]。Lp-PLA2参与血栓形成及急性炎症反应等过程并发挥重要作用[13-14]。AIS发生后,Lp-PLA2水平升高,可加速动脉粥样硬化进展,不稳定斑块数量增多、稳定性下降,从而引起PIS。HCY是促进血管内皮细胞凋亡、血管壁损伤、功能异常的内源性物质[15],可加速动脉粥样硬化进展,最终导致脑血管疾病的发生发展。但关于两者对PIS预测价值的报道数量有限,本研究通过多因素回归分析验证,其均为 PIS发生的独立危险因素(P< 0.05),与既往文献[9-10]结论一致,为其应用提供更多依据。
本研究就动脉粥样硬化相关危险因素展开比较、研究和探讨,针对性更强,对动脉粥样硬化型的PIS防治更有指导意义。但本研究样本量有限,有待后续扩大,另在未来的研究中可纳入其他分型的PIS相关危险因素进行研究,以期进一步提高研究结果的科学性。
综上,颅内或颈动脉狭窄、低回声斑块、SAP、高 ApoB/ApoA1、高 MHR、高 HCY、高 Lp-PLA2是影响PIS发生的独立危险因素。上述检验指标基于常规血液检验,具有更高的实用性及推广前景。临床上可根据上述指标,早期识别PIS,及时调整治疗方案,以降低PIS发生率,改善AIS患者预后。

