影响安罗替尼对晚期非小细胞肺癌临床疗效的多因素分析
沈旦 陈澄 朱晔 曾大雄 黄建安 石建
在全球范围内肺癌是常见的恶性肿瘤之一,预后并不理想[1]。自从1971年Jodah Folkman教授提出抗血管生成治疗理论以来,该治疗目前已成为抗肿瘤治疗中一个很有前途的手段[2-3]。安罗替尼是一种新型小分子多靶点酪氨酸激酶抑制剂(tyrosine kinase inhibitor,TKIs),可以作用于血管内皮生长因子(VEGF),成纤维细胞生长因子(FGF),血小板衍生生长因子(PDGF)的受体以及c-Kit等靶点,具有抗肿瘤血管生成和抑制肿瘤生长的双重作用[4-6]。ALTER0303的主要研究成果使安罗替尼在2018年首次被批准用于NSCLC的三线治疗[7],因安罗替尼对NSCLC三线之前治疗的临床疗效影响因素的研究目前仍较少,故本研究通过回顾性分析经过安罗替尼治疗的晚期NSCLC患者的临床指标,探索影响安罗替尼临床疗效的因素。
资料与方法
一、研究对象
选取2019年1月1日—2021年4月30日于苏州大学附属第一医院呼吸与危重症医学科治疗的晚期NSCLC患者,入选标准:1)治疗方案为安罗替尼单药或安罗替尼联合方案;2)Ⅲ/Ⅳ期无手术机会的NSCLC患者。排除标准:1)有严重肝肾功能或凝血功能异常。2)近期有不可控制的出血事件。3)使用安罗替尼后因严重不良反应被迫停药的。4)不能遵照医嘱定期服药及复查评估的患者。将符合标准的患者纳入研究,随访记录性别、年龄、吸烟史、病理类型、临床分期、转移情况、治疗线数、PS评分、治疗方案等资料。本研究通过医院伦理委员会批准(伦理号:(2022)伦研批第090号)。
二、疗效评价
患者至少完成1周期(12mg,每日1粒,连续口服2周,停用1周)的安罗替尼治疗,采用胸部CT评估治疗效果。参照RECIST 1.1版标准进行评价,分为4个等级:a.完全缓解(complete response,CR)所有目标病灶完全消失。b. 部分缓解(partial response,PR):所有目标病灶的直径总和低于基线≥30%。c. 疾病进展(progressive disease,PD):所有目标病灶直径之和较基线≥20%。d. 疾病稳定(stable disease,SD):靶病灶减小或增加的程度既未达到PR,也未达到PD。
疗效评价:主要评估DCR和PFS。DCR=(CR+PR+SD)/(CR+PR+SD+PD)×100%。PFS定义为患者当天首次服用安罗替尼到出现肿瘤进展的时间。
三、统计学分析
采用SPSS 25.0进行数据分析,借助Graphpad prism 8.0作图。对相关影响因素分别进行单因素分析、多因素Logistic回归模型分析、Cox比例风险模型分析,采用Kaplan-Meier法制作生存曲线,用Log-rank检验生存曲线差异。P<0.05表示差异具有统计学差异。
结 果
一、研究对象的特点
截止至2021年4月30日,共收集使用了安罗替尼的NSCLC患者141例,36例因未再返院复查,无法评估疗效故剔除,105例纳入本研究,临床特征如下(见表1)。

表1 患者临床特征
二、DCR及影响因素分析
所有105例患者中,有85例患者达到疾病控制,总DCR为81.0%,其中单药使用安罗替尼的DCR为56.8%,安罗替尼联合治疗的DCR为94.1%。
将可能影响DCR的因子进行单因素分析(表2),结果提示,肝脏转移、心包转移、联合用药、PS评分可能为DCR的独立影响因子,将其纳入Logistic回归模型分析提示:联合用药为提高DCR的独立保护因素,PS评分2分以上、心包转移为DCR的独立危险因素,肝脏转移不能做为DCR的独立影响因子(表3)。
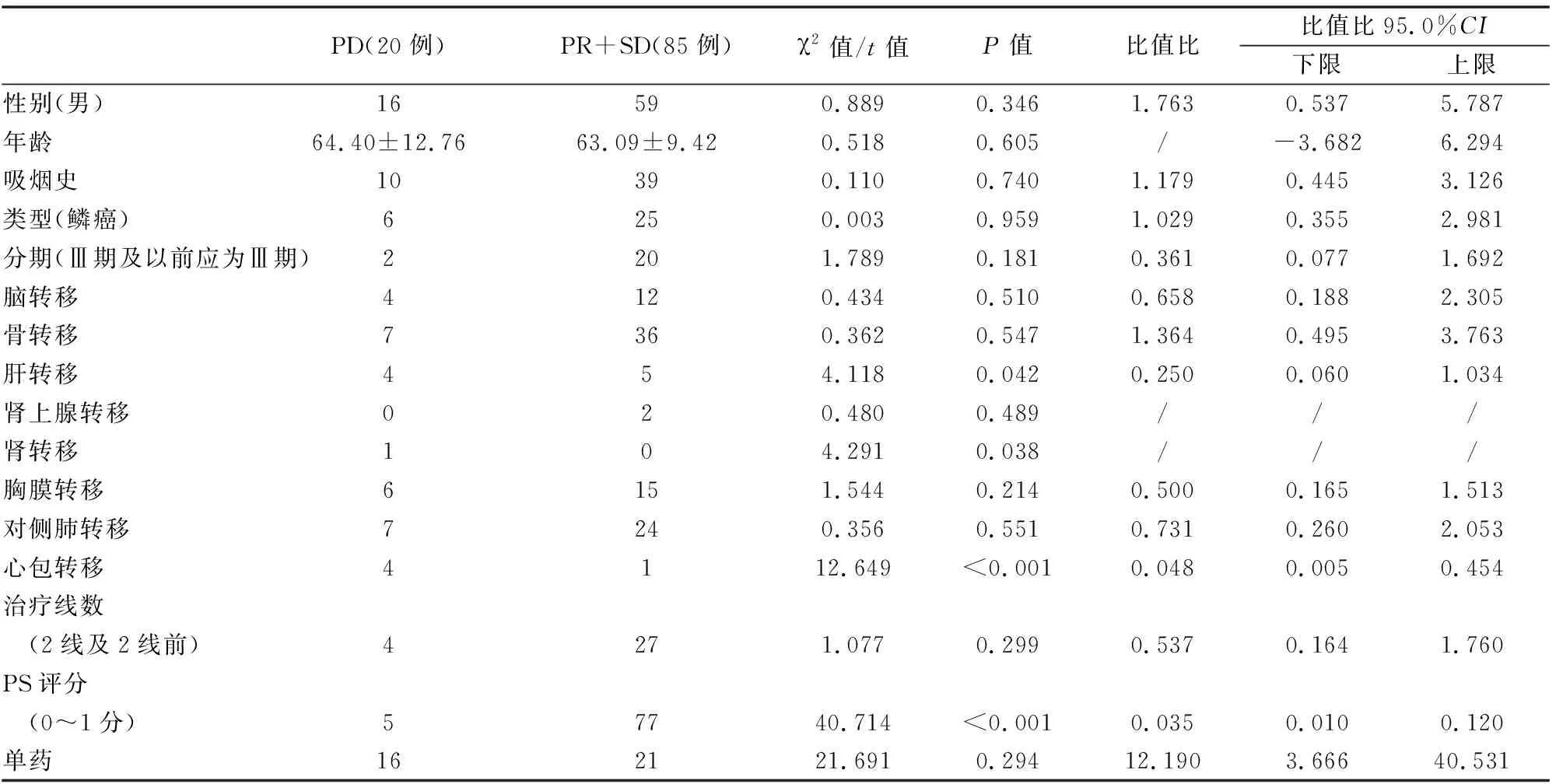
表2 DCR的单因素分析
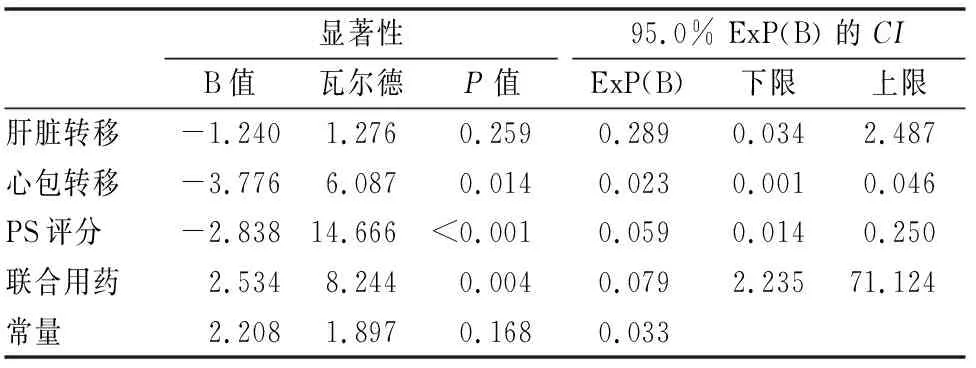
表3 多因素Logistic回归模型分析DCR
三、PFS及影响因素分析
所有105例患者中,中位PFS时间为12.2月(95%CI:9.99~13.52),PS评分0~1分患者为13.87月(95%CI:12.00~15.73),PS评分2分以上为2.83月(95%CI:1.59~4.06),联合用药患者中位PFS时间14.41月(95%CI:12.39~16.43),单药使用为5.35月(95%CI:3.73~6.96)。采用Cox比例风险模型探索影响安罗替尼PFS的因素,结果发现:PS评分和是否联合用药与安罗替尼的PFS相关,结果有统计学差异,而未发现其它因素与安罗替尼的PFS相关(见表4)。

表4 Cox比例风险模型分析安罗替尼PFS
以KaPlan-Meier法做生存分析,PS评分0~1分患者中位PFS时间较PS评分2分以上明显延长,结果有统计学差异(χ2=51.194,P<0.001)。安罗替尼联合用药患者中位PFS时间高于单药使用,结果有统计学差异(χ2=27.619,P<0.001)(见图1)。

图1 安罗替尼的PFS
四、安罗替尼联合用药的DCR和PFS时间
在联合用药的患者中,有35位患者联合使用了化疗方案,DCR为94.3%,中位PFS时间为11.06(95%CI:8.76~13.36)月,25位患者联合使用了免疫治疗,DCR为96%,中位PFS时间为14.77(95%CI:11.88~17.65)月,16位患者联合使用了靶向治疗,DCR为93.8%,6位患者同时联合使用了化疗及免疫治疗方案,DCR为83.3%,因后两组患者大多尚未进展,故暂时无法得出其准确的中位PFS时间(见图2)。

图2 安罗替尼不同联合用药方案的中位PFS时间
讨 论
近年来随着肺癌靶向和免疫治疗的广泛使用,部分患者取得了良好的疗效,然而,随着时间的推移,继发耐药及不良反应日益突出。安罗替尼作为一个小分子多靶点TKi,临床上使用越来越多。
本研究显示,安罗替尼对晚期肺癌具有较好的DCR,81.0%的患者在使用安罗替尼后疾病可以得到控制,特别是联合用药后,患者的DCR可以达到94.1%。而即使是单药使用安罗替尼,DCR也可达到56.8%,这一结果与ALTER0303的结果相仿[7],且安罗替尼本身为口服制剂,服用方便,这使得很多中晚期不愿意进行或无法耐受放化疗的患者有了新的药物选择。心包转移为患者DCR的独立危险因素,但由于本研究中,心包转移患者仅5例,这一结论尚需大样本资料进一步证实。本研究发现,影响安罗替尼DCR和PFS的因素仅与患者PS评分和是否与其它药物联合使用有关,与患者性别、年龄、吸烟史、肺癌病理类型、除心包以外的其他转移部位、几线使用并无相关性,且本研究中无一线使用安罗替尼的患者,故是否一线二线使用安罗替尼,目前并没有明显的证据支持。
值得一提的是,除了心包转移外,其它部位的转移均既不影响患者安罗替尼治疗的DCR,也不影响PFS,特别是对于颅内转移患者。既往都认为肺癌一旦出现颅内转移,将大大降低患者的生活质量和生存期,而在本研究中,颅内转移患者的DCR和PFS,并没有统计学差异,说明对于颅内转移患者,安罗替尼同样有良好的疗效。Jiang等纳入437例出现颅内转移的NSCLC患者发现,与安慰剂组相比,安罗替尼组患者有更长的无颅内病灶进展时间[8]。
本研究发现安罗替尼联合用药后,无论是DCR还是中位PFS时间均远高于单药使用。本研究中,安罗替尼的联合治疗模式包括联合化疗(35例)、联合免疫治疗(25例)、联合靶向治疗(16例)和同时联合化疗及免疫治疗(6例),DCR分别为94.3%,96%,93.8%,83.3%。目前有关安罗替尼联合治疗疗效的研究大多为探索性研究,鉴于贝伐珠单抗[9]和雷莫芦单抗[10]联合化疗对NSCLC患者疗效优于单纯化疗,安罗替尼早期联合化疗的疗效同样值得期待。RELAY研究发现,雷莫芦单抗联合厄洛替尼治疗初治EGFR突变的晚期NSCLC的PFS时间,显著高于厄洛替尼单药治疗[11]。最近两项研究评估了安罗替尼联合程序性死亡受体-1(programmed cell death-1,PD-1)单抗治疗晚期NSCLC的安全性和有效性,均显示这种治疗方案具有良好的耐受性和抗肿瘤活性[12-13]。不仅安罗替尼,其他抗血管生成药物,如重组人血管内皮抑素[14]、阿帕替尼[15]等药物,在晚期肺癌的治疗中,同样取得了不错的效果,提示在晚期肺癌的治疗中,联合抗血管生成药物,或许可以成为一个不错的选择。
本研究初步探索了影响安罗替尼疗效的临床因素,由于所收集的患者均来自于临床真实世界,患者返院复查时间控制不严格,PFS时间或许有少许偏差。另外直至本研究终点时,大多患者仍然存活,故目前无法评估总生存时间(overall survival,OS)。未来仍需收集更大的样本量,观察更长的时间以探索安罗替尼治疗晚期NSCLC的最佳治疗策略。

