十枣汤凝胶膏剂处方药味提取工艺优化研究
黄 群,刘蔚雯,陈 丹
(福建中医药大学药学院,福建 福州 350122)
十枣汤是张仲景治疗水饮、峻下逐水的代表方,主要由芫花、大戟、甘遂组成,配以10 枚大枣,方中芫花、大戟、甘遂为君药,大枣为佐药。大戟、甘遂、芫花3 味药配伍用于攻逐水饮,因药力过于峻猛,易伤脾胃,故用大枣相辅[1-2],临床上多用于治疗胸腔积液和肝硬化腹水等疾病,功效甚佳,但内服易伤脾胃。近年来,十枣汤外用贴敷剂在临床上的应用越来越广泛[3-6],多将十枣汤作为基础方加减调配,饮片研磨成粉,用醋调成糊状敷于患处。但该法需临用前调制生药,贴敷时黏性差、易污染衣物、易染菌。为改善患者临床用药的依从性,降低胃肠道的不良反应,增加载药量,提高治疗效果,课题组将十枣汤改剂,研制经皮给药制剂十枣汤凝胶膏剂,外用贴敷于腧穴或患处。十枣汤中大戟、甘遂泻水逐饮、消肿散结的主要药效成分大戟二烯醇为三萜类化合物[7-9],芫花的主要药效成分芫花素为黄酮类化合物[10]。因此,本实验以芫花中芫花素、甘遂和大戟中大戟二烯醇含量结合得膏率作为综合评价指标,对十枣汤凝胶膏剂的处方药味芫花、大戟及甘遂的提取工艺开展优化研究,采用L9(34)正交试验法,考察提取溶剂、提取次数、提取时间及料液比4 个因素对提取工艺的影响,筛选适用于十枣汤凝胶膏剂处方药味的最佳提取工艺,为后续凝胶膏剂的制备奠定原料基础。
1 仪器与试药
1.1 仪器 LC-20AT 液相色谱仪、SPD-M20A 二极管阵列检测器、CTO-20A 柱温箱(日本岛津公司);NewclassicMF 十万分之一电子天平(梅特勒-托利多仪器上海有限公司);FA604N 型电子天平(上海精天电子仪器有限公司);RE-52AA 旋转蒸发器(上海亚荣生化仪器厂);HH-2 数显恒温水浴锅(常州国华电器有限公司);KQ-500E 超声波清洗器(昆山市超声仪器有限公司);超纯水仪(美国Millipore 公司)。
1.2 试药 芫花饮片(产地安徽,批号:20190901)、甘遂饮片(产地安徽,批号:20190602)、京大戟饮片(产地江苏,批号:20190901)均购自安徽亳州药材市场,经福建中医药大学药学院中药鉴定教研室车苏容副教授鉴定,均符合2020 年版《中华人民共和国药典(一部)》规定;大戟二烯醇对照品(成都普思生物科技股份有限公司,批号:PS010984,纯度>98%);芫花素对照品(上海源叶生物科技有限公司,批号:R13A8F33981,纯度>98%);甲醇(色谱纯,批号:20200217)、乙腈(色谱纯,批号:20200303)均购自国药集团化学试剂有限公司;甲酸(色谱纯,上海麦克林生化有限公司,批号:64-18-6);水为超纯水;其余试剂均为分析纯。
2 方法与结果
2.1 十枣汤处方药味的提取制备及得膏率计算 按处方量称取芫花粗粉(过2 号筛)、甘遂中粉(过4 号筛)、京大戟中粉(过4 号筛)各等量,每份6 g,混匀,按照设定的提取次数、料液比、乙醇浓度、提取时间,加入适量提取溶剂乙醇,先浸泡0.5 h,再于80 ℃水浴中回流提取一定时间,提取2 次;合并各次提取滤液,将所得滤液减压浓缩,至恒重,得十枣汤提取液浸膏。将十枣汤提取液浸膏置于105 ℃干燥箱中干燥3 h,再移至干燥器中冷却0.5 h,快速精密称定干膏重量,按2020 年版《中华人民共和国药典(四部)》[11]中“0831”项下干燥失重法测定得膏率。
得膏率=干膏质量/饮片质量×100%
2.2 提取液中多指标成分的含量测定
2.2.1 对照品溶液的制备 精密称取芫花素对照品0.58 mg 置于10 mL 量瓶中,用甲醇溶解并稀释至刻度,制成浓度为0.058 mg/mL 的芫花素对照品溶液,备用。精密称取大戟二烯醇对照品1.5 mg 置于10 mL 量瓶中,加入甲醇溶解并用甲醇稀释至刻度,制成浓度为0.150 mg/mL 的大戟二烯醇对照品溶液,备用。
2.2.2 供试品溶液的制备 精密称取按“2.1”项下制得的十枣汤提取液浸膏约1.00 g,置于25 mL 量瓶中,用甲醇溶解并稀释至刻度,0.45 μm 微孔滤膜滤过,即得供试品溶液。
2.2.3 阴性对照溶液的制备 精密称取缺芫花处方药味,按照“2.1”与“2.2.2”项下同法操作,制备缺芫花阴性对照溶液;精密称取缺大戟和甘遂处方药味,按照“2.1”与“2.2.2”项下同法操作,制备缺大戟和甘遂阴性对照溶液。
2.2.4 芫花素色谱条件 Dimonsil C18色谱柱(4.6 mm×250 mm,5 μm);流动相为甲醇∶0.8 %冰醋酸=65∶35;流速 1 mL/min;柱温30 ℃,检测波长338 nm。
2.2.5 大戟二烯醇色谱条件 Neptune C8色谱柱(4.6 mm×150 mm,5 μm);流动相乙腈∶0.1 %甲酸=86∶14;流速 1 mL/min;柱温为30 ℃,检测波长210 nm。
2.2.6 标准曲线的制备及线性关系的考察 分别精密吸取芫花素对照品溶液4、6、8、10、12、15 μL,按“2.2.4”项下色谱条件测定,以芫花素色谱峰的峰面积(Y1)为纵坐标,进样量(X1)为横坐标,进行线性回归。结果表明:芫花素在0.058~2.900 μg 浓度范围呈良好的线性关系,回归方程为Y1=6.886 0×106X1+1.080 4×105(r=0.999 9)。分别精密吸取大戟二烯醇对照品溶液8、10、12、14、16、18 μL,按“2.2.5”项下色谱条件测定,以大戟二烯醇色谱峰的峰面积(Y2)为纵坐标,进样量(X2)为横坐标,进行线性回归。结果表明:大戟二烯醇在0.150~7.500 μg 浓度范围呈良好的线性关系,回归方程为Y2=2.133 5×105X2-7.616 6×10(3r=0.999 9)。
2.2.7 专属性试验 分别精密吸取芫花素对照品溶液、供试品溶液和缺芫花阴性对照溶液各10 μL,按“2.2.4”项下色谱条件测定,结果见图1。分别精密吸取大戟二烯醇对照品溶液、供试品溶液和缺大戟和甘遂阴性对照溶液各10 μL,按“2.2.5”项下色谱条件测定,结果见图2。结果表明:阴性对照无干扰,方法专属性良好。
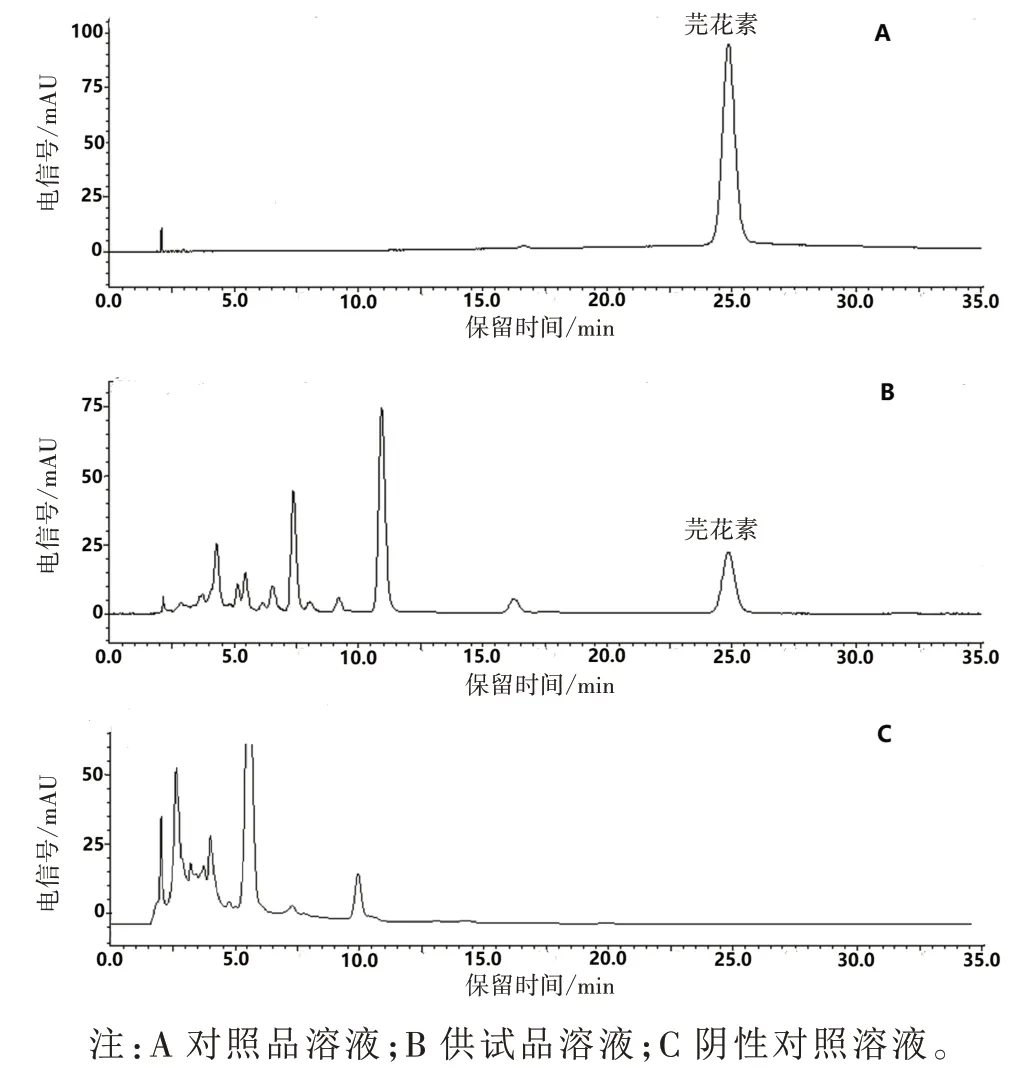
图1 十枣汤提取液中芫花素的高效液相色谱图
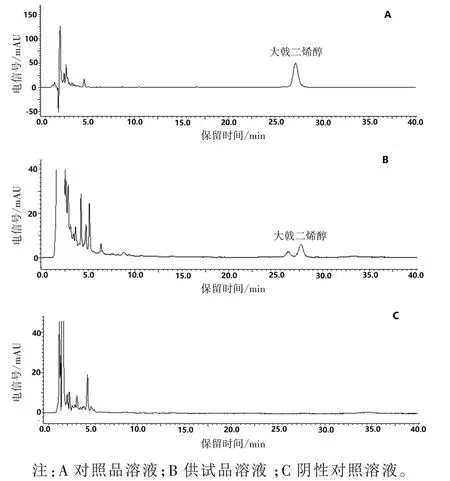
图2 十枣汤提取液中大戟二烯醇的高效液相色谱图
2.2.8 精密度试验 精密吸取芫花素对照品溶液,按“2.2.4”项下色谱条件,分别连续进样10 μL 测定6 次,计算得芫花素峰面积的RSD 为0.312 %;精密吸取大戟二烯醇对照品溶液,按“2.2.5”项下色谱条件,分别连续进样10 μL 测定6 次,计算得大戟二烯醇峰面积的RSD 为1.04%。结果表明:仪器精密度良好。
2.2.9 重复性试验 分别平行制备6 份供试品溶液,分别按照“2.2.4”与“2.2.5”项下色谱条件,分别进样供试品溶液、对照品溶液各10 μL 测定,计算。结果表明:芫花素含量的RSD 值为0.518%,大戟二烯醇含量的RSD值为3.492%,说明方法重复性良好。
2.2.10 稳定性性试验 取供试品溶液,分别在0、2、4、6、8、10、12 h 按照“2.2.4”与“2.2.5”项下色谱条件进样10 μL 测定,计算。结果表明:芫花素含量的RSD 值为0.31%,大戟二烯醇含量的RSD 值为1.81%,说明供试品溶液12 h 内稳定性良好。
2.2.11 加样回收率试验 分别精密称取6 份十枣汤提取液浸膏约0.50g,分别加入芫花素对照品溶液1 mL(浓度0.177 6 mg/mL)、大戟二烯醇对照品溶液3 mL(浓度0.152 0 mg/mL),制备供试品溶液,分别按照“2.2.4”与“2.2.5”项下色谱条件进样10 μL测定,计算。结果表明:芫花素平均回收率为96.73%,RSD 为 1.37%(n=6);大戟二烯醇平均回收率为99.03%,RSD为2.67%(n=6),说明方法准确度较高。
2.3 正交试验优化十枣汤提取工艺
2.3.1 正交试验设计 根据预实验和单因素试验考察结果,提取温度为80 ℃时提取效率较高,提取溶剂乙醇的浓度(A)、料液比(B)、提取时间(C)、提取次数(D)4 个因素为提取工艺的主要影响因素,故实验采用L9(34)正交试验设计,每个因素选取3 个水平,以提取液中芫花素和大戟二烯醇含量结合得膏率作为综合考察指标,优选最佳十枣汤提取工艺。正交试验因素水平见表1。
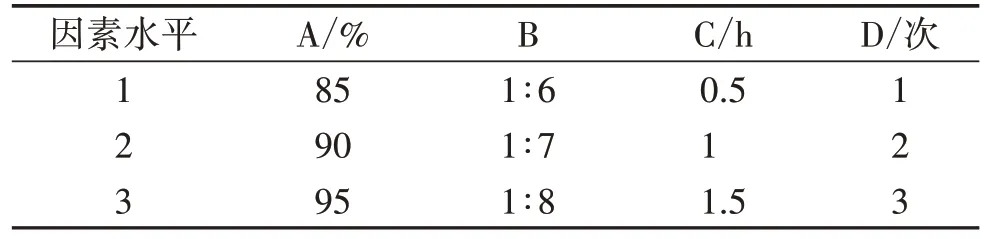
表1 正交试验因素水平
2.3.2 正交实验样品的制备 按处方量分别称取芫花、甘遂、大戟各2 g,共9 份,分别按“2.1”项下同法提取十枣汤凝胶膏剂处方药味,并制成提取液浸膏;分别按“2.2”项下HPLC 法测定芫花素和大戟二烯醇的含量。综合评分(Y)=Y1+Y2+Y3,其中设定权重计算Y1=(20/最大得膏率)×得膏率(X1),Y2=(40/最大大戟二烯醇含量)×大戟二烯醇含量(X2),Y3=(40/最大芫花素含量)×芫花素含量(X3)。结果见表2、表3。
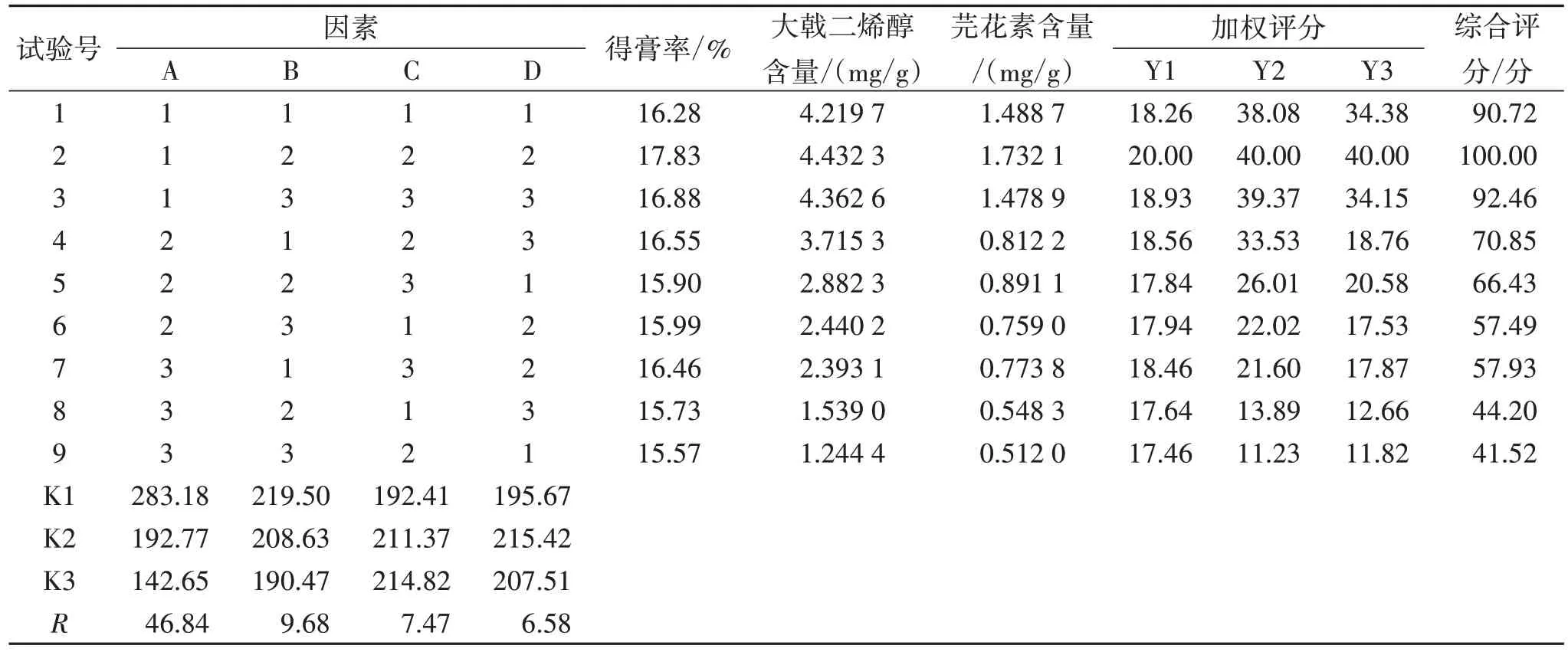
表2 十枣汤提取工艺正交试验结果
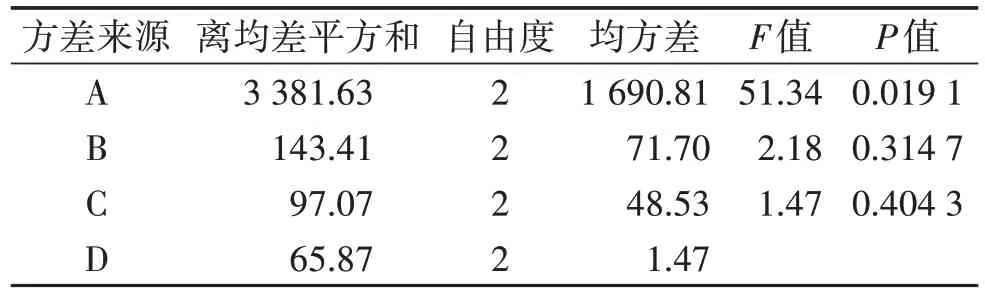
表3 正交试验方差分析结果
2.3.3 正交试验结果分析 表2 直观分析结果显示:4 个因素对十枣汤提取结果影响大小依次为:A>B>C>D,即乙醇浓度>料液比>提取时间>提取次数,且 A1>A2>A3,B1>B2>B3,C3>C2>C1,D2>D3>D1,故最佳提取工艺是A1B1C3D2。表3 方差分析结果表明:因素A 乙醇浓度对芫花素和大戟二烯醇含量有显著性影响(F=51.34,P<0.05),料液比、提取时间、提取次数对正交试验结果的差异无统计学意义(P>0.05),因此,优化筛选的提取工艺为A1B1C3D2。综合考虑提取效率、降低成本等因素,确定最佳提取工艺为:取处方药味饮片适量,按料液比1∶6,用85%乙醇为溶剂,浸泡0.5 h,于80 ℃下回流提取2 次,提取时间每次1.0 h,提取液压榨过滤,合并2 次滤液,减压浓缩,制成浸膏。
2.3.4 提取工艺验证 分别称取处方量的饮片各3 份,平行试验3 批,按照正交试验优选的最佳工艺提取,即按料液比1∶6,加85%乙醇提取溶剂,浸泡0.5 h 后,80 ℃回流提取 2 次,每次 1.0 h,过滤,浓缩,制成浸膏。精密称取浸膏,每批分别按“2.3.2”项下同法平行测定3 次,计算得膏率、提取液中芫花素及大戟二烯醇含量,按“2.3.2”项下公式计算综合评分。最佳工艺验证试验结果表明:该提取工艺综合评分在95.89~99.10 分,RSD=1.82%~2.43%,说明优化的最佳提取工艺稳定、可行,适用于十枣汤凝胶膏剂处方药味的提取。结果见表4。

表4 最佳提取工艺验证试验结果
3 讨 论
3.1 提取溶剂及提取方法的选择 十枣汤处方药味芫花含有以芫花素为代表的黄酮类化合物,难溶于水,易溶于甲醇、乙醇等有机溶剂中,大戟和甘遂主要含有以大戟二烯醇为代表的萜类化合物,难溶于水,易溶于甲醇、乙醇等有机溶剂,故基于主要有效成分的溶解特性及预实验结果,选择价廉易得且相对安全的乙醇为提取溶剂。预实验曾比较了超声提取与传统的加热回流提取法,后者提取液的主要有效成分含量更高,相对提取效率较高,在中药材提取中应用也较多,故选用乙醇为溶剂、加热回流提取十枣汤中的有效成分。
3.2 正交试验评价指标的选择 经典名方十枣汤方中芫花、大戟、甘遂均为君药。2020 年版《中华人民共和国药典(一部)》规定芫花项下含量测定成分为芫花素,京大戟和甘遂项下含量测定成分为大戟二烯醇[12],故实验采用HPLC 法测定十枣汤凝胶膏剂处方药味提取液中芫花素及大戟二烯醇的含量作为提取效率评价指标,设权重各占40%。此外,考虑到中药提取液浓缩至浸膏对提取效率也具有一定的意义,提取得膏率可以反映中药提取是否完全,与制剂质量有密切关系,故将得膏率权重设为20%。实验通过芫花素、大戟二烯醇含量结合得膏率作为正交试验的综合评价指标,较为全面地考察优化提取工艺,确保十枣汤凝胶膏剂原料的质量[13]。
3.3 正交试验设计 根据预实验结果,饮片经浸泡后提取效率较佳,浸泡0.5 h 和1 h 提取效率无差异,故选择浸泡0.5 h 后提取。单因素试验曾分别考察了不同浓度乙醇提取溶剂、提取次数、不同料液比、提取时间、提取温度等对提取效率的影响,结果表明提取温度80 ℃时综合分值最佳;而乙醇浓度、料液比、提取次数、提取时间是提取效率的较重要的影响因素,故实验设计以这4 个因素为变量,开展四因素三水平正交试验,进一步优化提取工艺。结果显示:十枣汤凝胶膏剂处方药味饮片最佳提取工艺为取处方饮片适量,以85%乙醇按料液比1∶6,浸泡 0.5 h 后,于 80 ℃下回流提取 2 次,每次1.0 h,提取液过滤、浓缩制成浸膏。经工艺验证,优化的提取工艺操作简单,方法稳定可行,适用于十枣汤凝胶膏剂处方药味的提取,并为后续十枣汤凝胶膏剂的原料生产奠定了可靠的基础。

