去除无细胞百日咳疫苗丝状血凝素纯化液中内毒素TritonX-114液相分离法的建立及其效果评价
温嘉纳,王虓宇,张光贤,陈林涛,张晓华,赵宸,李娜,孙明波,梁疆莉
中国医学科学院北京协和医学院医学生物学研究所,云南昆明 650118
百日咳疫苗生产过程中,细菌会产生大量内毒素,内毒素是革兰阴性细菌细胞壁中的一种成分,该成分称为脂多糖,破碎细菌获得蛋白抗原的同时,细胞壁的内毒素会释放至蛋白溶液中。《欧洲药典》8.0版中规定,无细胞百白破-脊髓灰质炎联合疫苗的内毒素含量应<100 EU/剂[1],根据该要求推算百日咳疫苗中丝状血凝素(filamentous hemagglutinin,FHA)、百日咳毒素(pertussis toxin PT)及69 kD外膜蛋白(pertactin,PRN)3种原液的内毒素含量应均<100 EU/mg,因此必须采取合理有效的方法去除内毒素。
通常去除内毒素的方法有化学萃取法(如TritonX-114液相分离法)和离子交换层析法(如离子交换层析)[2-3]。TritonX-114液相分离法经济高效,已广泛应用于生物制品中内毒素的去除[4-5]。1990年,AIDA等[6]采用Triton X-114液相分离法去除重组蛋白溶液中的内毒素,随后有研究采用该方法去除其他生物制品中的内毒素,效果均较好[7-8]。TritonX-114是一种非离子型表面活性剂[9-11],在低温时成水溶性,温度升高后变为脂溶性,具有较低的临界胶束浓度,于4℃可与水溶液互溶,并与脂多糖分子结合;25℃以上能携带脂多糖分子从水相中析出。利用TritonX-114的特性,本研究建立适合于百日咳疫苗FHA纯化液去除内毒素的TritonX-114液相分离法,并评价其去除效果。
1 材料与方法
1.1 纯化液 无细胞百日咳疫苗FHA纯化液(批号:20200901-01、20201101-01、20201101-02、20201101-03)由中国医学科学院医学生物学研究所制备。
1.2 主要试剂TritonX-114及Lowry蛋白测定试剂盒均购自北京Solarbio公司;内毒素鲎试剂购自湛江安度斯生物有限公司。
1.3 正交试验FHA纯化液(20200901-01)中加入一定浓度的TritonX-114,4℃振荡混匀,37℃静止分层,经16 743×g离心后,含有内毒素的液相位于下层,提取上层液相,去除下层液相,达到去除内毒素目的。根据TritonX-114液相分离法所需条件,设计4因素[TritonX-114加入量(A)、4℃混匀时间(B)、37℃分层时间(C)、25℃16 743×g离心时间(D)]及3水平,共12组正交试验,见表1和表2。以纯化液回收率作为因变量确定各因素的最佳值。应用SPSS 17.0软件进行数据正交设计、线性模型单变量分析、主体间效应检验、四因素同回收率检验,依据纯化液蛋白回收率及P值结果,确定最佳内毒素去除条件(以P<0.05为差异有统计学意义)。

表1 正交试验因素及水平Tab.1 Factors and levels in orthogonal test
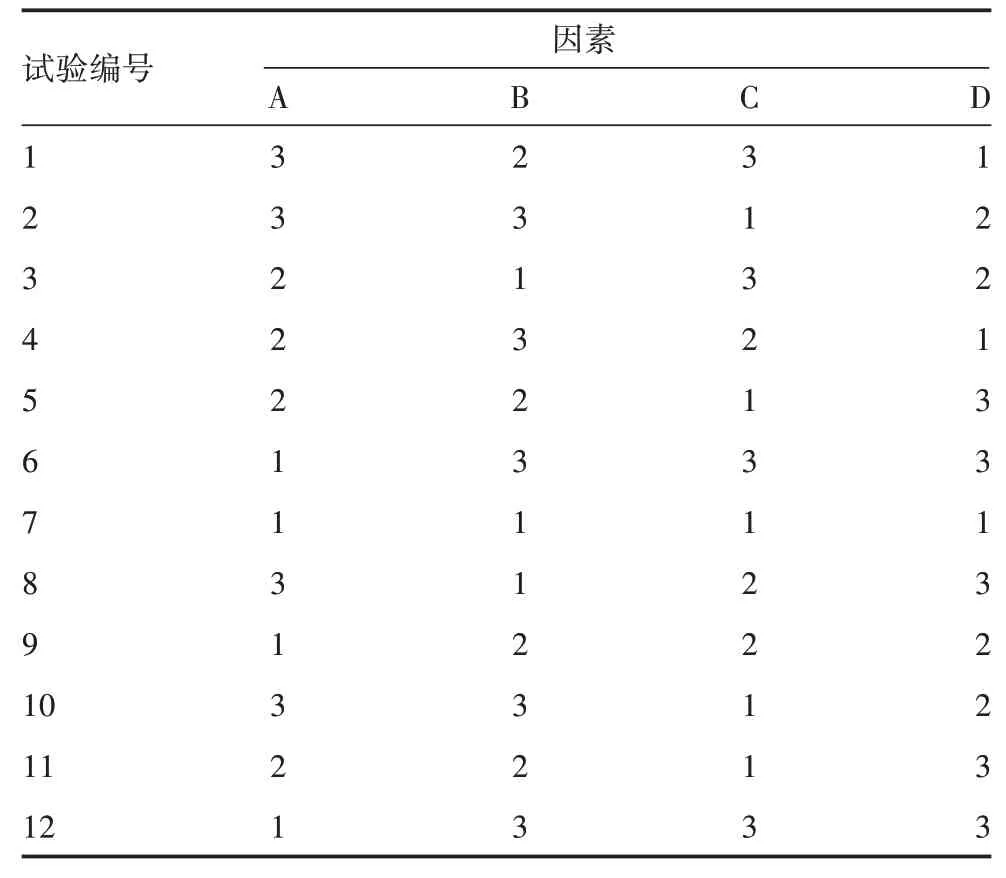
表2 正交试验设计Tab.2 Design of orthogonal test
1.4 内毒素去除效果的评价 以正交试验确定的最佳条件去除3批无细胞百日咳疫苗FHA纯化液(批号:20201101-01、20201101-02、20201101-03)的内毒素,检测去除内毒素后纯化液的FHA蛋白含量、内毒素含量及TritonX-114残留量。同时将去除内毒素前后的FHA纯化液进行10%SDS-PAGE分析。
1.5 内毒素及FHA蛋白含量的检测 分别按照《中国药典》三部(2015版)中细菌内毒素检测凝胶法及Lowry蛋白检测法进行检测[12]。
1.6 TritonX-114残留量检测 参照文献[13]的浊度法检测样品的TritonX-114残留量,其原理为TritonX-114与苯酚反应可产生一定浊度的复合物,浊度与TritonX-114的浓度成正比,通过测定A340计算TritonX-114残留量。
2 结 果
2.1 正交试验结果 加入不同TritonX-114的FHA纯化液蛋白回收率差异有统计学意义(P<0.05),其中,加入量为1%时蛋白回收率最高,因此选择1%为最佳TritonX-114加入量。随着4℃混匀时间、37℃分层时间、25℃16 743×g离心时间的变化,纯化液回收率差异均无统计学意义(P>0.05),当4℃混匀时间为30 min,37℃分层时间为60 min,25℃167 43×g离心时间为10 min时,蛋白回收率最高,见表3和表4。因此确定该条件为最佳检测条件。
2.2 内毒素去除效果20201101-01、20201101-02、20201101-03批无细胞百日咳疫苗FHA纯化液在最佳条件下去除内毒素后,内毒素含量均<0.25 EU/mL,去除率均>99%;TtitonX-114残留量均值为0.183%;蛋白回收率均值为91.04%。见表5。表明FHA生物活性在去除内毒素前后无变化。10%SDS-PAGE分析显示,去除内毒素前后FHA纯化液均可见相对分子质量约220 000的目的蛋白条带,大小与预期相符,纯度>95%,符合FHA纯化液的纯度要求,见图1。

表3 正交试验结果Tab.3 Result of orthogonal test
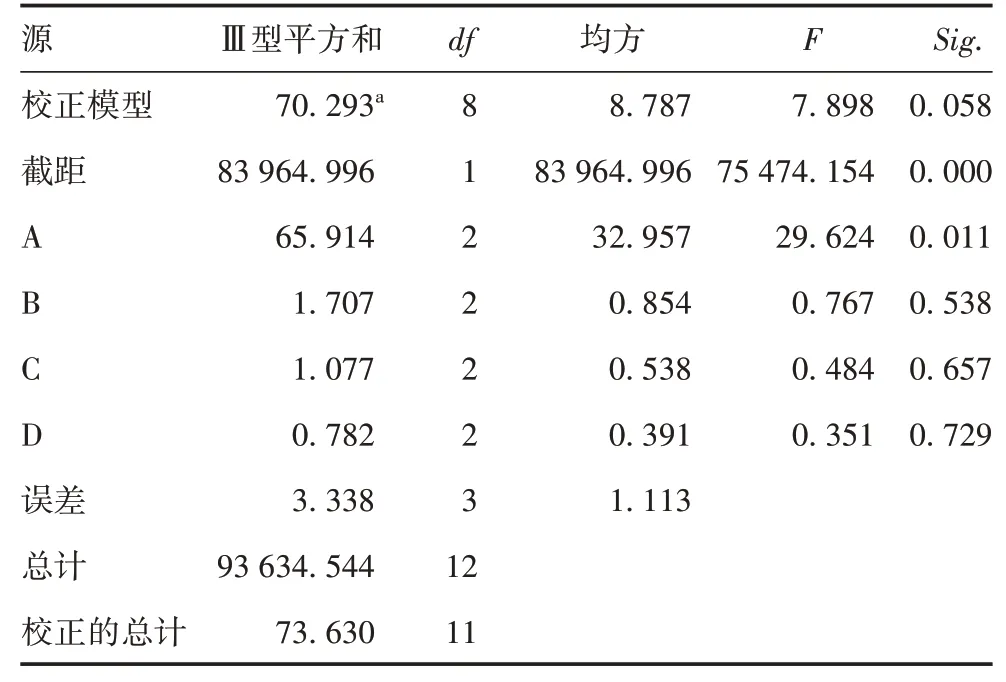
表4 正交设计的方差分析表Tab.4 Variance analysis of orthogonal design
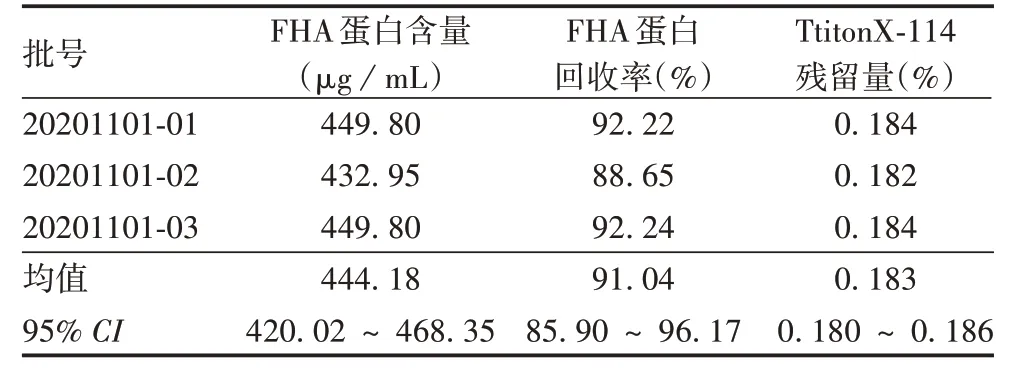
表5 去除内毒素后无细胞百日咳疫苗FHA纯化液的检测结果Tab.5 Test result of purified FHA of acellular pertussis vaccine after removal of endotoxin
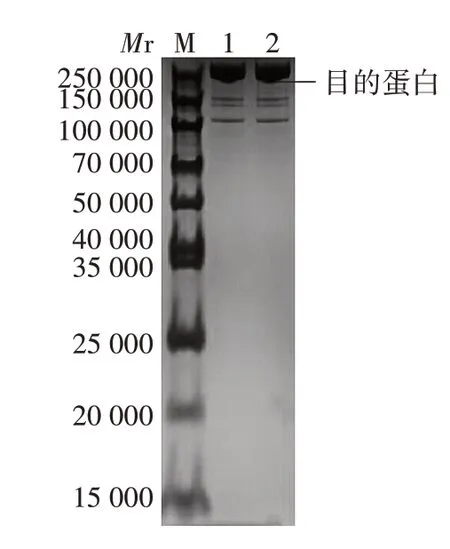
图1 FHA纯化液的SDS-PAGE分析Fig.1 SDS-PAGE profile of purified FHA
3 讨 论
本研究通过正交试验确定了TritonX-114去除百日咳疫苗FHA纯化液中内毒素的最佳条件为:TritonX-114加入量为1%,4℃混匀时间为30 min,37℃分层时间为60 min,25℃16 743×g离心时间为10 min。采用优化的最佳条件去除无细胞百日咳疫苗FHA纯化液中的内毒素后,内毒素含量<0.25 EU/mL,优于《欧洲药典》8.0版中对内毒素要求[1];蛋白回收率为91.04%,且SDS-PAGE纯度较高。
本课题组前期研究采用柱层析法去除FHA原液内毒素,结果表明,使用Capto adhere层析柱可将FHA纯化液中内毒素降至100 EU/mL以下,蛋白回收率<75%[14],且在该方法操作中需考虑抽提物的质量浓度、层析法的缓冲体系、pH条件、柱床比例、流速等诸多因素。与该结果比较,本研究采用TritonX-114液相分离法在内毒素去除及蛋白回收率上占有一定优势,且缩短了处理时间,简化了处理流程。同时TritonX-114液相分离法由于投入成本低,涉及物料简单,可较好地控制研发生产成本,减少环境污染。
《中国药典》三部(2015版)中未对TritonX-114残留量进行规定,参照重组乙型肝炎疫苗半成品对表面活性剂TritonX-100的含量要求(<15µg/mL),TritonX-114对FHA原液抽提后残留量<1 ng/mL,远低于该版《中国药典》中其他疫苗的要求[12]。有报道表明,以TritonX-114液相分离法提取的RNA对BALB/c小鼠无不良反应,对家兔也无发热作用[15],表明TritonX-114具有较好的安全性。
综上所述,采用TritonX-114液相分离法去除无细胞百日咳疫苗FHA纯化液内毒素,内毒素可降低至0.25 EU/mL,且TritonX-114残留量<1 ng/mL,该方法具有良好的应用前景。另外,TritonX-114是否适用于无细胞百日咳疫苗其他两组分PT及PRN内毒素的去除有待进一步深入研究。

