基于美国食品药物管理局不良事件报告系统的地舒单抗不良事件信号挖掘*
刘艳鑫,邹剑,董长江,陈力,何绪成,舒亚民,吴攀
(1.四川省彭州市人民医院,四川 成都 611930;2.四川大学华西第二医院,四川 成都 610041;3.出生缺陷与相关妇儿疾病教育部重点实验室,四川 成都 610041;4.四川省彭州市第二人民医院,四川 成都 611934;5.华中科技大学同济医学院附属同济医院,湖北 武汉 430030;6.四川省邛崃市妇幼保健计划生育服务中心,四川 成都 611530)
地舒单抗是特异性人类核因子-κB(NF-κB)受体活化因子配体(RANK-L)完全人源化单克隆免疫球蛋白G-2(IgG-2)的单克隆抗体,具有高度特异性,能与RANK-L特异性结合,使RANK-L不能和破骨细胞上的NF-κB受体活化因子结合,导致不能激活破骨细胞,进而骨吸收活性降低、骨密度增加、骨折风险也降低,是目前唯一上市的RANK-L抑制剂[1]。与传统的双膦酸盐类药物相比,地舒单抗具有可皮下注射给药,给药方便,给药间隔时间长,不受患者肾功能限制的优势[2]。随着地舒单抗的应用越来越广泛,其安全性也受到越来越多的关注,但目前地舒单抗的不良事件分析局限于文献报道和临床观察研究,缺少信号挖掘研究。美国食品药物管理局(FDA)不良事件报告系统(FAERS)是由消费者、医师、药师、律师等自发呈报药品不良事件(ADE)信息的数据库,其数据信息多样、数据量大且可自由获取,常被用于ADE信号挖掘研究[3]。本研究中基于FAERS挖掘地舒单抗的ADE并进行分析,为临床安全用药提供依据。现报道如下。
1 资料与方法
1.1 数据来源
地舒单抗ADE源数据收集:选取FAERS数据库2016年第1季度至2021年第2季度共22个季度的ADE数据,包括患者的行政信息和人口学、药物信息、报告国家、地舒单抗的ADE、患者结局等内容,导入MySQL 5.7数据库。22个季度的ADE数据在删除重复报告后,共获得首要怀疑药物为地舒单抗的ADE共99 698例。在MySQL 5.7数据库中以“drugname”字段进行模糊匹配,以“DENOSUMAB”“PROLIA”“XGEVA”匹配地舒单抗,筛选以地舒单抗为首要怀疑药物的报告。
ADE编码系统:采用由国际人用药品注册技术协调会(ICH)编撰的《ICH国际医学用语词典》(MedDRA)中首选语对FAERS中ADE进行编码[4]。
1.2 信号挖掘
选用报告比值比(ROR)法和英国药品和保健品管理局的综合标准(MHRA)法挖掘ADE数据,此方法基于比例失衡法四格表(表1),利用相对应的公式计算ROR值和比例报告比值比(PRR)值[5-7],再通过设定的阈值筛选出有信号的首选语(表2)。所有统计分析及计算均使用Microsoft Excel 2019软件完成。

表1 比例失衡法四格表Tab.1 Fourfold table of disproportionality measurement

表2 ROR法与MHRA法公式及阈值Tab.2 Formulas and thresholds of ROR method and MHRA method
1.3 统计学处理
采用MedDRA 23.1版软件对筛选后的数据进行标准化,合并中文含义相同的首选语并记录的总报告数,即四格表中的a值;再通过对应“所有药物产生的所有不良事件”计算出四格表中相对应的b,c,d值;通过相应的公式计算ROR值、PRR值、χ²值和95%CI下限。
2 结果
2.1 ADE报告基本信息
22个季度的ADE报告中,以地舒单抗为首要怀疑药物的ADE报告共182 887份,ADE种类共4 757种。上报的99 698例ADE报告中,女性占78.84%,远高于男性的10.89%;年龄主要集中在65岁及以上,占44.65%;上报者中,医师占比较高(50.63%),与大多数FAERS相关的研究上报者多为消费者有所不同,使研究结果的可信值更高,更值得参考;上报的国家中,美国的报告例数最多,占77.21%;上报年份中,2018年报告最多,占32.41%,后呈逐渐递减的趋势;适应证中,骨质疏松报告最多,占20.31%。详见表3。
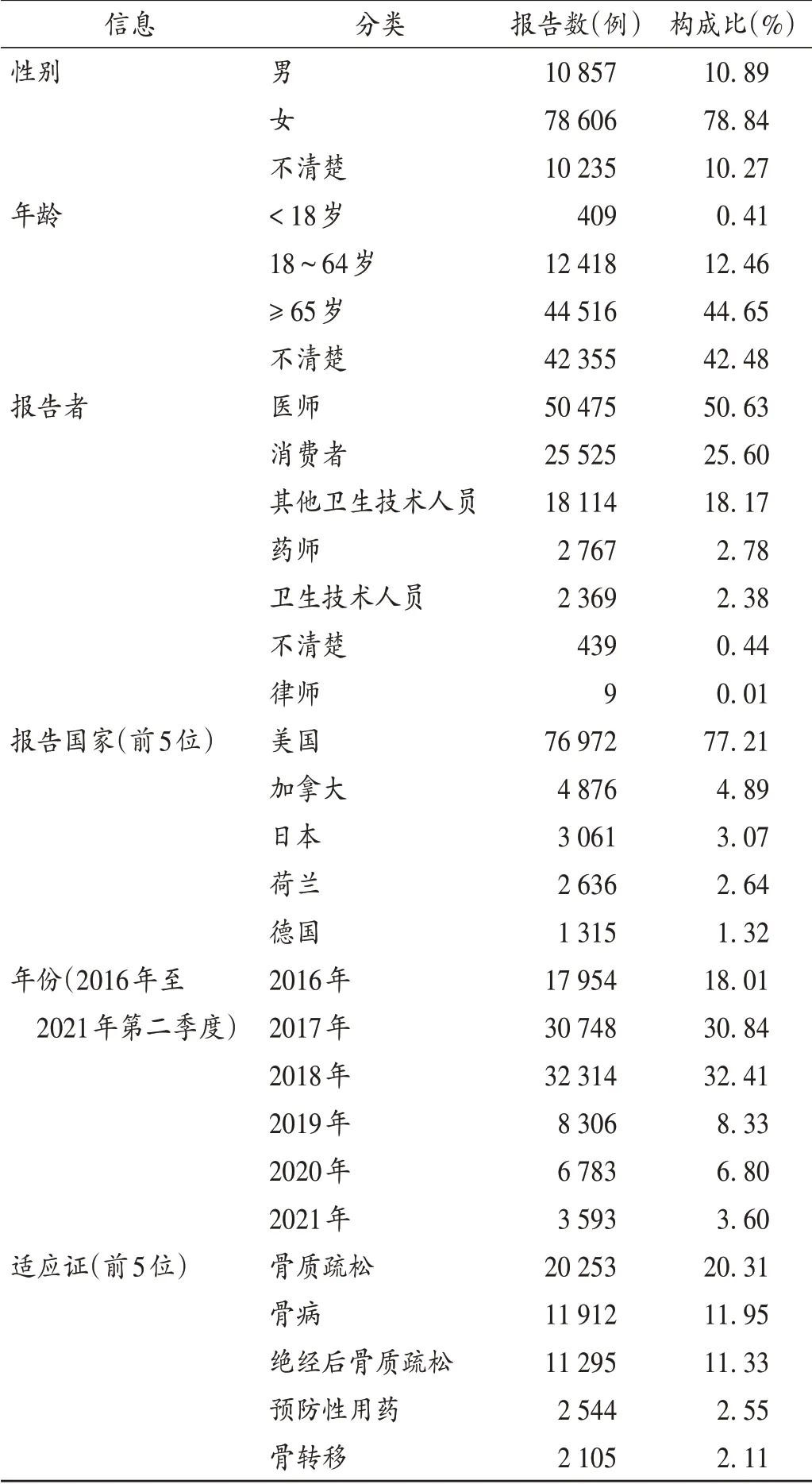
表3 地舒单抗相关ADE报告基本信息(n=99 698)Tab.3 Basic information of ADE reports of denosumab(n=99 698)
2.2 ADE信号分析结果
共获得以地舒单抗为首要怀疑药物的ADE信号875个,首选语报告总数为122 924个。取有信号的首选语前50位(按报告数和信号强度的大小降序排列,除去无关、无意义的,如药品不良反应等)。其中报告数较多的ADE信号有超药品说明书使用、死亡、颌骨骨坏死、关节痛等,信号强度较高的ADE有骨巨细胞瘤、颌骨外生性骨疣、颌骨骨坏死、牙齿护理等。详见表4。涉及13个事件未被药品说明书收录,包括步态障碍(PT数868,ROR=2.67,PRR=2.66),感觉减退(PT数470,ROR=2.05,PRR=2.04),骨髓炎(PT数374,ROR=12.21,PRR=12.17),龋齿(PT数310,ROR=22.02,PRR=21.95),乳腺癌(PT数310,ROR=2.51,PRR=2.51),高 钙 血 症 性 肾 病(PT数4,ROR=221.02,PRR=221.01),牙 吸 收(PT数36,ROR=209.46,PRR=209.38),动脉瘤样骨囊肿(PT数5,ROR=184.19,PRR=184.18),外 耳 道 骨 坏 死(PT数24,ROR=171.15,PRR=171.15),糖尿病性终末器官损伤(PT数3,ROR=132.61,PRR=132.61)、植入物周围炎(PT数11,ROR=127.97,PRR=127.95),低磷酸酯酶症(PT数6,ROR=69.80,PRR=69.79)、骨肉瘤(PT数3,ROR=66.31,PRR=66.30)。
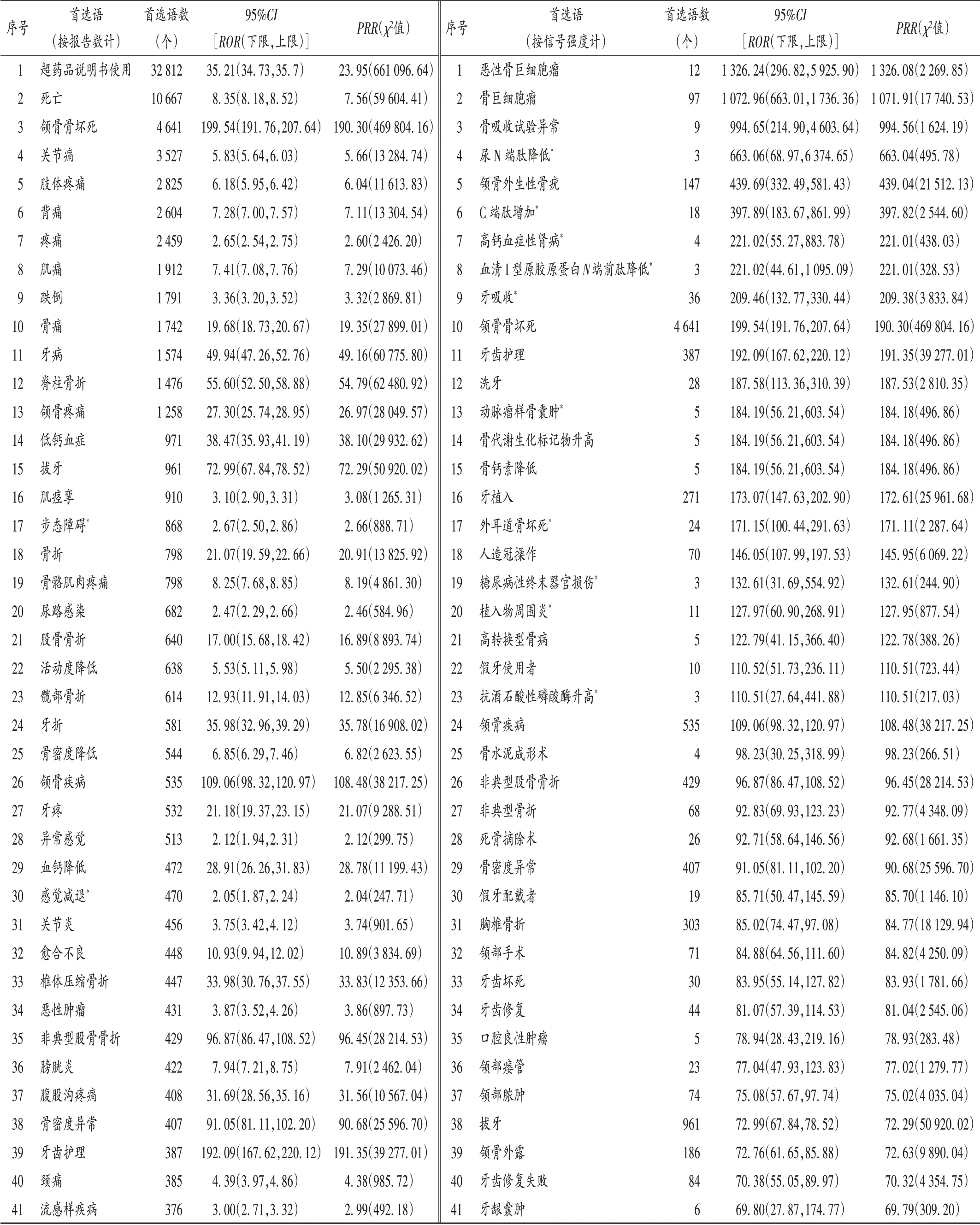
表4 地舒单抗报告数和信号强度排名前50的ADE信号Tab.4 Top 50 ADE signals of denosumab in the report number and signal intensity
2.3 各系统/器官分类(SOC)的ADE信号报告
在SOC项下,对有信号的首选语进行归类并按降序排列,发现26个有信号的SOC(MedDRA将SOC分为27个),本研究中仅未累及“妊娠期、产褥期及围产期状况”这一SOC。在122 924份报告中,各类损伤、中毒及操作并发症报告ADE最多,占36.67%,其中超药品说明书使用(32 812例)、跌倒(1 791例)、脊柱骨折(1 476例)、骨折(798例)、意外暴露于产品(762例)居前五位;各种肌肉骨骼及结缔组织疾病(颌骨骨坏死、关节痛、肢体疼痛等)、全身性疾病及给药部位各种反应(死亡、疼痛、步态障碍等)分别居第2位和第3位,分别占23.63%和15.61%。详见表5。由于地舒单抗引起感染的风险目前仍存在争议,选择感染及侵染类疾病SOC产生的首选语进行详细列举并分析。详见表6。
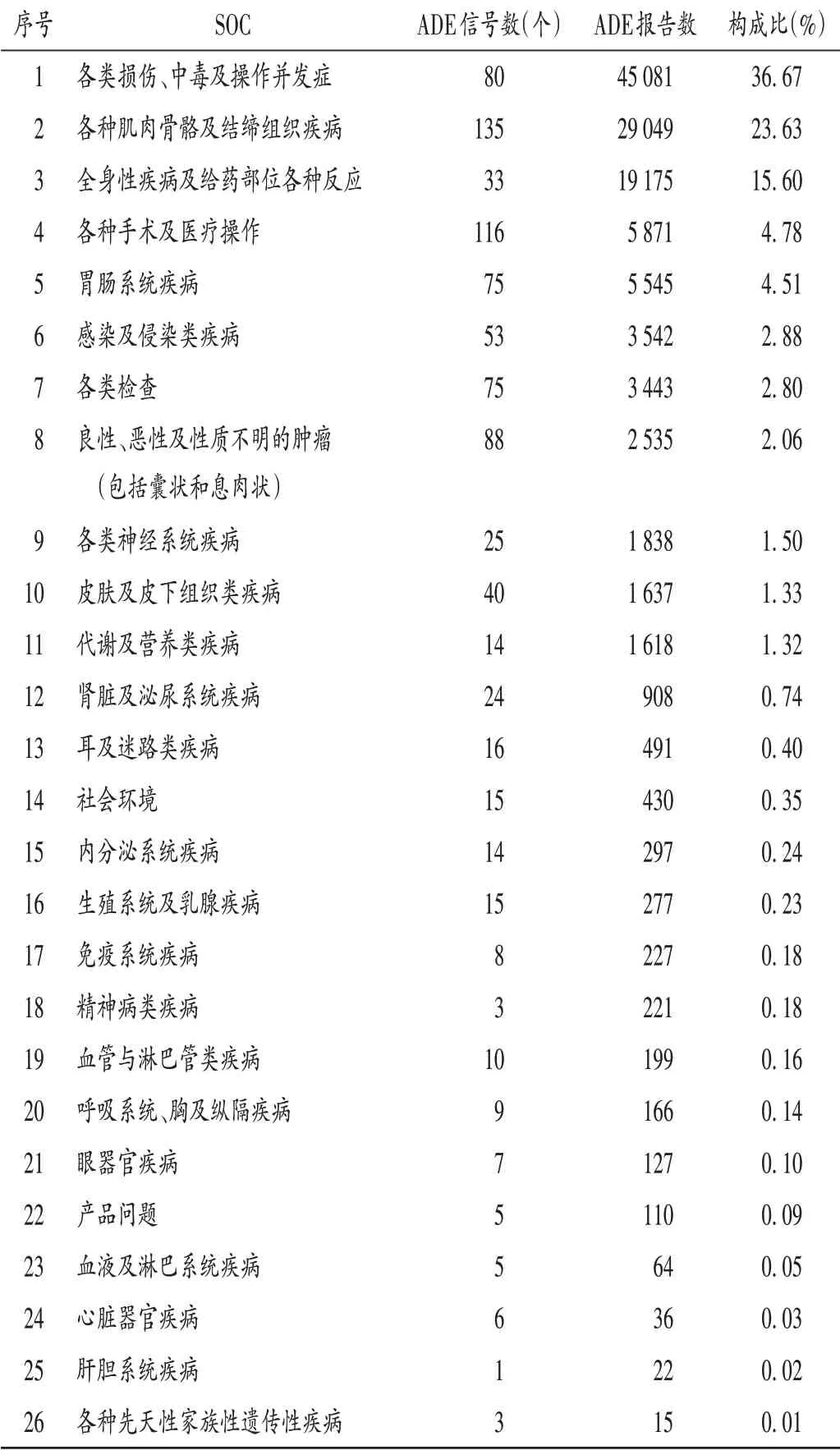
表5 SOC项下地舒单抗ADE信号报告(n=122 924)Tab.5 ADE signals of denosumab-involved systems and organs(n=122 924)

表6 感染及侵染类疾病SOC项下地舒单抗报告数排名前20的ADE信号Tab.6 Top 20 ADE signals of denosumab in the report number of infectious diseases by the SOC
3 讨论
3.1 地舒单抗ADE的人口学特征
本研究中从FAERS中提取地舒单抗的ADE报告共122 924个,涉及99 698例患者。其中,女性占比高于男性,这可能与地舒单抗主要适用于治疗骨折高风险的绝经后女性和男性骨质疏松症相关。女性在各个年龄段骨质疏松症发生率均比同年龄段的男性高,男性与女性的年龄每增加10岁骨质疏松的增长率分别为15%和20%[8-9]。因此,女性使用地舒单抗治疗的可能性更大,ADE发生也随之增长。在已知年龄的患者中,各个年龄段都有ADE发生,其中65岁及以上人群占比较大,可能与老年患者日常联合用药较多、身体机能下降及地舒单抗的主要适应证有关[10]。2016年至2018年,ADE报告数逐年递增,而2019年开始ADE报告数骤减,其主要原因可能与2017年被FDA批准用于预防多发性骨髓瘤和实体瘤骨转移患者的骨骼相关事件有关;也与2018年被批准用于治疗糖皮质激素诱导的骨质疏松症,使超药品说明书用药的ADE减少有关。2016年至2020年,超药品说明书ADE报告数分别为1 319例、14 150例、16 558例、317例、274例。
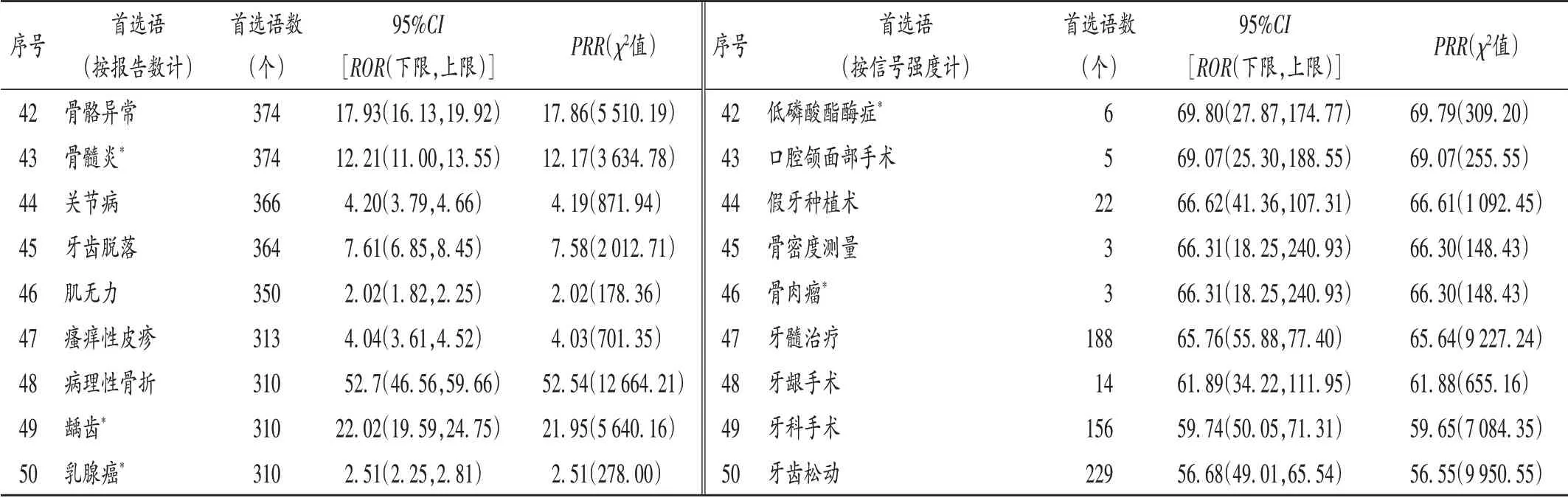
续表4地舒单抗报告数和信号强度排名前50的ADE信号Continued Tab.4 Top 50 ADE signals of denosumab in the report number and signal intensity
3.2 地舒单抗ADE累及系统特点
本研究中通过ROR法和MHRA法分析发现,与地舒单抗关联性较强的SOC信号是各类损伤、中毒及操作并发症,得到的首选语主要是跌倒、脊柱骨折、牙折、椎体压缩性骨折、非典型股骨骨折,说明各种类型的骨折是地舒单抗的严重ADE。有研究表明,既往接受过双膦酸盐类药物治疗可能是地舒单抗诱发非典型股骨骨折的危险因素[11]。临床试验结果显示,与地舒单抗相关性非典型股骨骨折患者中有超过1/2曾经接受过双膦酸盐类药物的治疗,但地舒单抗诱发骨折的作用机制还在进一步研究中[12]。由表4可知,地舒单抗与超药品说明书使用这一ADE信号关联性较强,报告数最多。目前,在中国上市的地舒单抗只有2种,但药品说明书载入的适应证却不相同,普罗力主要适用于骨折高风险的绝经后妇女的骨质疏松症,可显著降低椎体、非椎体和髋部骨折的风险;安加维主要用于实体肿瘤骨转移和多发性骨髓瘤的治疗。由表3可知,本研究中所纳入患者使用地舒单抗的适应证排名前5的分别为骨质疏松(20.31%)、骨 病(11.95%)、绝 经 后 骨 质 疏 松(11.33%)、预防用药(2.55%)、骨转移(2.11%),不存在超药品说明书使用的情况,故推测2种不同适应证的地舒单抗混用可能是导致地舒单抗超药品说明书使用的原因,建议临床在使用地舒单抗时严格遵照药品说明书指出的适应证,切勿2种地舒单抗混用。
由表4和表5可知,ADE信号较强的SOC还有各种肌肉、骨骼及结缔组织疾病,其中包括颌骨骨坏死、肢体疼痛、肌痉挛、关节炎等。颌骨坏死是地舒单抗最严重的不良反应,且在本研究中发生例数与关联性均较强。研究表明,地舒单抗引起颌骨坏死的发生机制可能是多因素的,包括局部的创伤或感染,服用双磷酸盐类药物史,骨转换减少等[13]。动物实验结果显示,在局部牙齿和牙周感染的动物中,颌骨坏死的发生率显著升高[14]。提示当患者存在创伤、感染及服用双磷酸盐类药物史时,应在用药过程中做好用药监护,嘱患者保持良好的口腔习惯,密切观察患者是否出现局限性的牙周或牙齿疾病,一旦出现,及时对症治疗,并评估能否继续用药,必要时可进行多学科的诊疗。
由表4可知,除骨相关疾病外,发生次数较多及关联性较强的首选语还有低钙血症。BODY等[15]研究提出了发生地舒单抗相关的低钙血症的预测因子,包括男性、前列腺癌、肺小细胞癌、肌酐清除率<60 mL/min、尿Ⅰ型胶原交联N端肽(uNTx)和骨特异性碱性磷酸酶(BSAP)基线值较高。此外,地舒单抗的药品说明书指出,严重肾功能损害、甲状腺功能减退、甲状腺手术史、吸收不良及小肠切除的患者,使用地舒单抗发生低钙血症的风险会增加。建议有以上病史的患者定期检测血钙,特别是在治疗开始的前2周。治疗前,临床药师要对患者进行充分的用药教育,使患者了解低钙血症的症状(包括肌肉抽搐、痉挛、刺痛、麻木、癫痫发作、心律失常),以及补充钙和维生素D的重要性。
虽然地舒单抗药品说明书中明确列举了感染相关的不良反应,主要包括泌尿道感染、皮肤感染、耳部感染、牙感染等,但多项随机对照试验对地舒单抗引起的感染风险仍是不明确的。考虑到临床前与临床试验间存在争议,本研究中将感染及侵染类疾病这一SOC进行列举并分析(表6),得到感染及侵染类疾病这一SOC项下共53个首选语,感染部位主要集中于口腔及牙感染、泌尿系感染等,其中95%CI ROR排名前3的分别为颌部脓肿(95%CI ROR75.08)、牙龈脓肿(95%CI ROR40.2)、牙周炎(95%CI ROR28.7),口腔及牙齿感染发生次数居多,且与地舒单抗关联性最强。有研究结果显示,在接受地舒单抗治疗的患者中严重感染不良事件(SAEI)的发生率较安慰剂组高21%,报道的SAEI主要是耳鼻喉(咽炎、鼻咽炎、鼻窦炎、中耳炎等)和胃肠道(胃肠炎、憩室炎、幽门螺杆菌胃炎等)[16]。与本研究结果基本一致,但地舒单抗引起的感染风险仍需进一步研究。
此外,在全部ADE信号报告中,死亡居第2名,但信号强度相较于其他ADE偏低,提示临床医师需密切关注地舒单抗可能引发的死亡风险,但也仍需考虑包括疾病进展等导致死亡的其他因素,虽然地舒单抗对实体肿瘤的骨转移和多发性骨髓瘤患者具有可靠的有效性,但仍无法完全逆转肿瘤患者死亡的结局。
3.3 新的ADE信号
本研究中通过FAERS得到的地舒单抗ADE信号与药品说明书及临床试验、文献[17-19]报道结果相似,验证了本研究结果的可靠性及方法的可行性。但本研究中还发现数个没有被地舒单抗药品说明书收录的ADE,包括低磷酸酯酶症、植入物周围炎、步态障碍、高钙血症性肾病、动脉瘤样骨囊肿、糖尿病性终末器官损伤、骨肉瘤、乳腺癌等。值得注意的是,本研究中发现了新的与地舒单抗相关的二次原发癌的ADE,是近年来地舒单抗研究的热点。有报道显示,接受地舒单抗治疗但未接受过放射治疗的骨巨细胞瘤患者发生骨肉瘤的不良反应[20]。有假说认为,地舒单抗相关的第二原发癌的可能机制为地舒单抗相关低钙血症引起的继发性甲状旁腺功能亢进[21],但目前仍需佐证上述假说。
3.4 研究的局限性
律师、卫生技术人员甚至消费者都可向FDA报告ADE,FAERS的信息均是基于自发呈报。不是所有接受药物治疗的患者产生的ADE都上报了,可能导致报告的偏差。此外,FAERS中某些重要信息可能被遗漏,如基础疾病,先前的治疗,甚至怀疑药物使用的开始和结束日期,或不良反应的发生日期[22]。虽然本研究中获得的ADE信号表示地舒单抗与该ADE在统计学上具有不同强度的关联性,但并不能表明地舒单抗与该ADE在生物学上存在因果关系,仍需进一步探索。由于ADE一般指因果关系尚未确定的反应,多见于国外的药品说明书;而药品不良反应一般指因果关系已确定的反应。本研究中基于FAERS得到的信号并不能完全推演致药品不良反应,仅是对潜在风险的警示,并不一定是真正的信号,还需结合药品说明书、专家意见做进一步解释与评价,判断药物与ADE之间是否存在因果关系,以及ADE是否与疾病本身有关,进一步确定是否是药品不良反应[23]。
3.5 结语
本研究中基于FAERS 2016年第一季度至2021年第二季度的ADE报告,利用ROR法和MHRA法挖掘地舒单抗的ADE信号,更完整、真实地挖掘出药品安全信息,发现了如低磷酸酯酶症、植物周围炎、步态障碍、高钙血症性肾病、动脉瘤样骨囊肿、糖尿病性终末器官损伤、骨肉瘤、乳腺癌等多个新的ADE。

