胃癌组织GLDC蛋白表达及其与根治术后复发的关系探讨
祝孟川,冯文婷,余强
(信阳市中心医院1.普外二科,2.急诊外科, 河南 信阳 464000)
胃癌是常见的恶性肿瘤之一,在国内发病率约为0.431‰,死亡率约为0.296‰[1]。目前,根治术仍是胃癌治疗的“金标准”[2],虽有较好的临床疗效,但术后复发风险极高。术后复发是胃癌患者术后死亡的主要因素,为改善患者术后生存率,筛选胃癌根治术后复发的危险因素非常必要。甘氨酸脱羧酶(GLDC)在甘氨酸裂解过程中发挥关键作用,Chen等[3-4]发现在肾细胞癌组织中GLDC可发挥一定抑癌作用,其表达水平与癌症的预后有一定的相关性。Min等[5]发现,GLDC在胃癌细胞系中也可发挥抑癌功效,但癌组织中GLDC蛋白水平是否与胃癌患者根治术后复发有关尚需深入探讨。鉴于此,本研究选取106例行根治术治疗的胃癌患者,探究其胃癌组织GLDC蛋白表达水平与术后复发的关系,以期为胃癌患者临床治疗提供参考。
1 资料与方法
1.1 一般资料
经伦理委员会批准后,选取2016年3月至2019年3月在本院行根治术治疗的胃癌患者106例,男75例,女31例;年龄29~81岁,中位年龄62岁;TNM分期Ⅰ期31例,Ⅱ期58例,Ⅲ期17例;肿瘤最大直径2.4~7.5(4.39±0.78)cm。纳入标准:(1) 均行组织病理学分析确诊为胃癌;(2) 均为原发胃癌,满足根治术指征并接受根治术;(3) 术前未行放化疗且无远处转移;(4) 均对本研究知情同意。排除标准:(1) 合并其他肿瘤;(2) 围术期内死亡;(3) 治疗前3个月内经历过其它手术或创伤;(4) 合并严重的肝、肾等脏器病变;(5) 合并传染病、血液疾病、免疫疾病。
1.2 方法
1.2.1 免疫组化法检测胃癌组织及切缘正常组织GLDC蛋白表达水平 将癌组织或切缘正常组织制成蜡块,依次进行切片、脱蜡、水化、抗原修复、孵育、显色、苏木素复染、脱水、封片、显微镜下观察。依据染色强度评分×阳性细胞百分比评分对蛋白表达行半定量分析,染色强度评分:无着色0分,淡黄色1分,棕黄色2分,棕褐色3分;阳性细胞百分比评分:阳性细胞占比≤5% 记0分,6%~25%记1分,26%~50%记2分,51%~75%记3分;>75%记4分;二者乘积<4分为低表达,≥4分为高表达[6]。
1.2.2 术后复发的判断 术后通过电话随访和门诊复诊观察复发情况,术后复诊前2年每3个月1次,随后每6个月1次,结合症状、体征和组织病理学综合诊断。
1.2.3 胃癌根治术后复发的影响因素分析 统计患者年龄、性别、肿瘤大小、病灶部位、lauren分型、T和N分期、分化程度、术后辅助化疗、癌组织GLDC蛋白表达水平等,将其记为自变量,将胃癌根治术后是否复发记为因变量,分析自变量与因变量之间的关系。
1.3 统计学处理
采用SPSS 25.0统计软件处理数据,计数资料以例表示,行χ2检验,若任一理论频数>1且<5需对检验校正;采用Cox回归分析术后复发影响因素;采用Kaplan-Meier生存曲线分析不同GLDC蛋白水平患者术后3年的复发率。P<0.05为差异有统计学意义。
2 结 果
2.1 胃癌组织与切缘正常组织GLDC蛋白表达水平比较
胃癌组织中GLDC蛋白低表达率(48.11%)高于切缘正常组织(3.77%)(P<0.05),见图1。

A.胃癌组织;B.切缘正常组织图1 胃癌组织与切缘正常组织GLDC蛋白表达(×400)Fig 1 GLDC protein expression in gastric cancer tissue and normal tissue at the incisal edge(×400)
2.2 不同临床特征患者胃癌组织GLDC蛋白表达水平比较
肿瘤直径≥5 cm、lauren分型为弥漫型、T3~T4分期 、N1~N3分期胃癌患者胃癌组织GLDC蛋白低表达占比均高于肿瘤直径<5 cm、lauren分型为肠型或混合型、T1~T2分期 、N0分期胃癌患者(P<0.05),见表1。
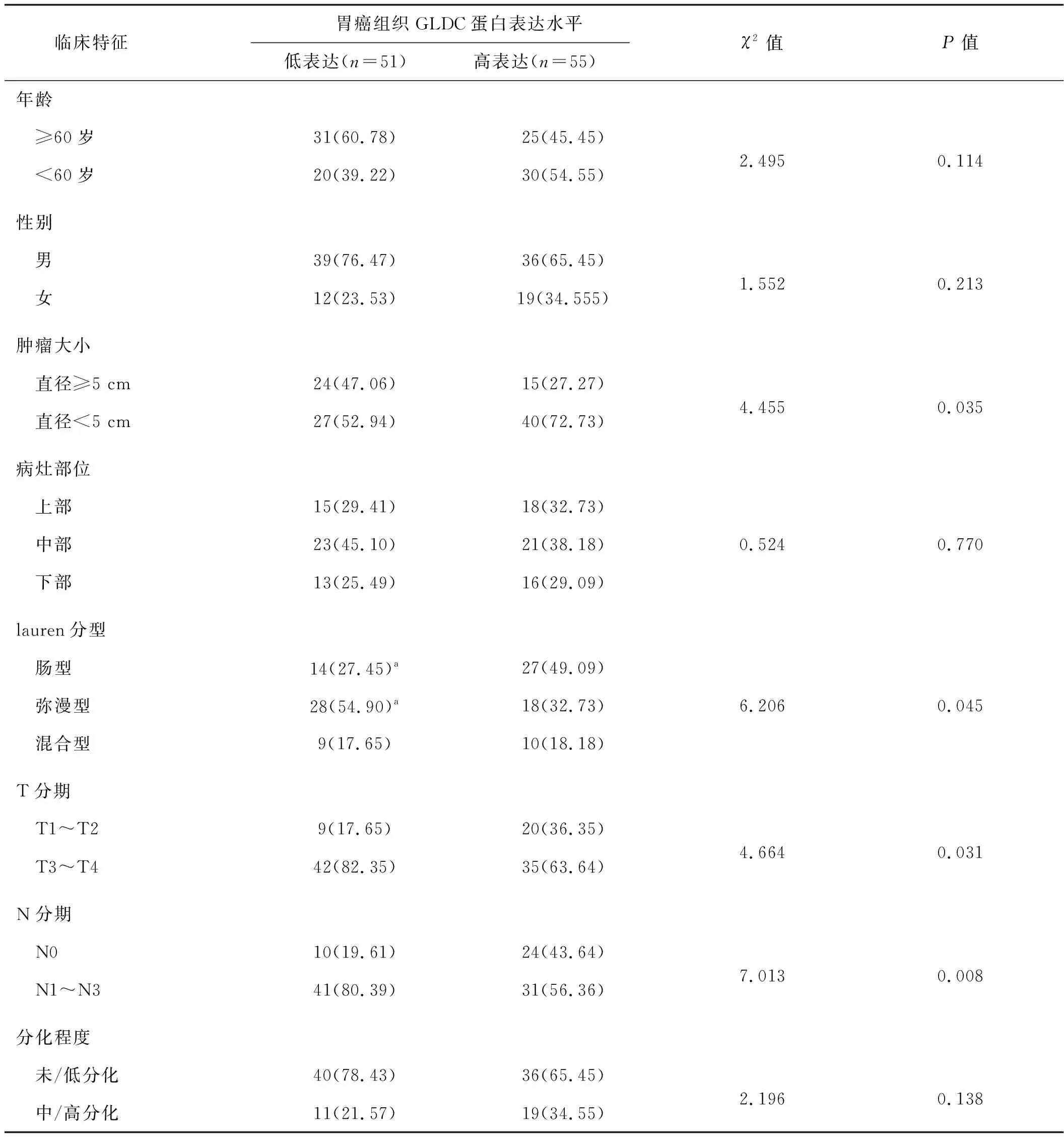
表1 不同临床特征患者胃癌组织GLDC蛋白表达水平比较 例Tab 1 Comparison of GLDC protein expression level in gastric cancer tissues of patients with different clinical characteristics cases
2.3 胃癌根治术后复发率及复发组与未复发组胃癌组织GLDC蛋白表达水平比较
106例胃癌患者根治术后随访3年,失访3例(GLDC低表达2例,高表达1例),余103例,复发67例(GLDC低表达39例),未复发36例(GLDC低表达10例),复发率为65.05%(67/103)。复发组胃癌组织GLDC蛋白低表达占比高于未复发组(χ2=8.695,P=0.003)。
2.4 胃癌患者根治术后复发的影响因素分析
复发组肿瘤直径≥5 cm、T3~T4分期、N1~N3分期占比均高于未复发组(P<0.05),行术后辅助化疗占比低于未复发组(P<0.05),见表2。
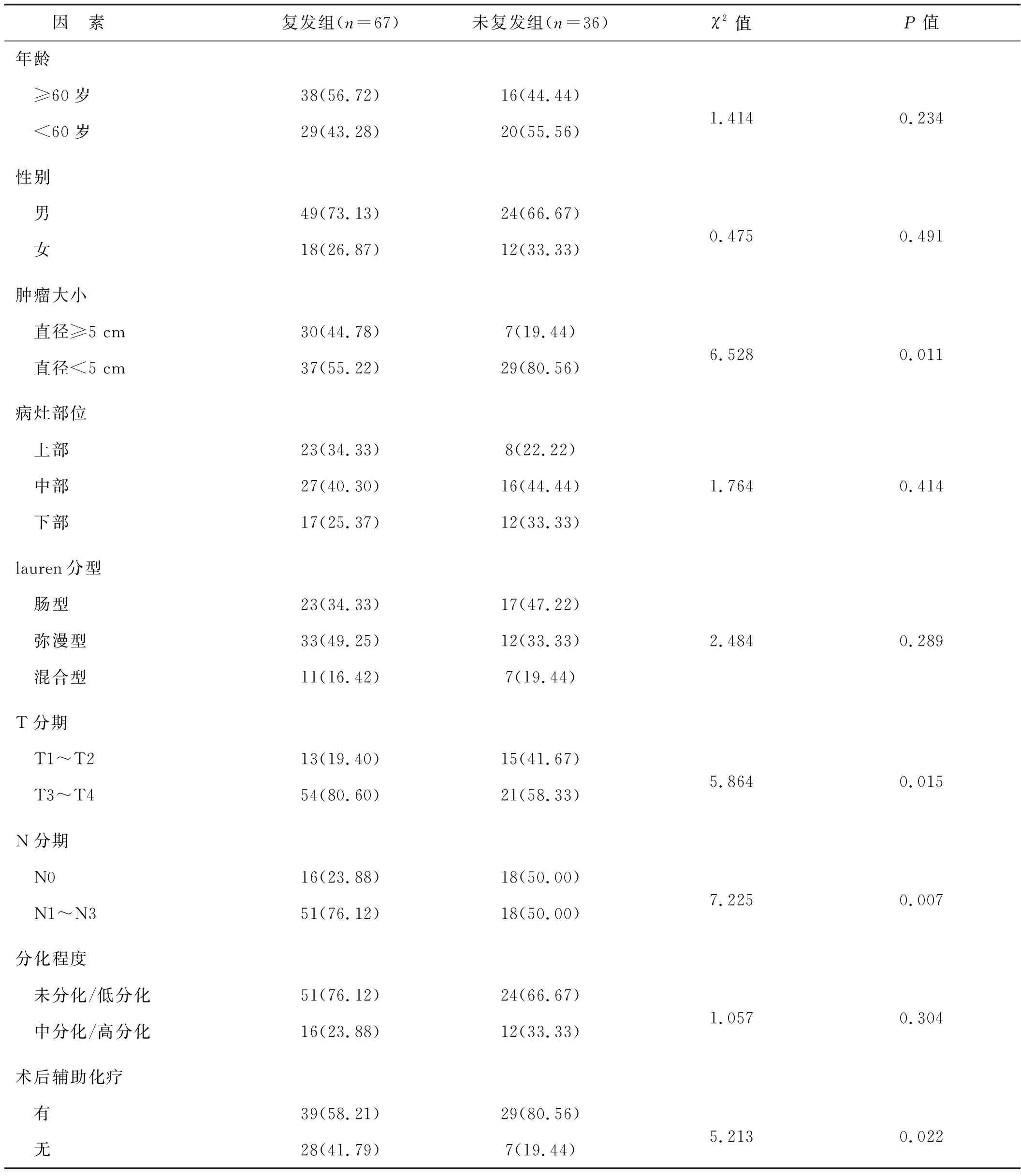
表2 胃癌患者根治术后复发与临床病理特征的关系 例Tab 2 Relationship between recurrence and clinicopathological characteristics of patients with gastric cancer after radical surgery cases
Cox分析结果显示,肿瘤大小、T分期、N分期是胃癌患者根治术后复发的危险因素(P<0.05),术后辅助化疗、胃癌组织GLDC蛋白高表达水平是其保护因素(P<0.05),见表3。
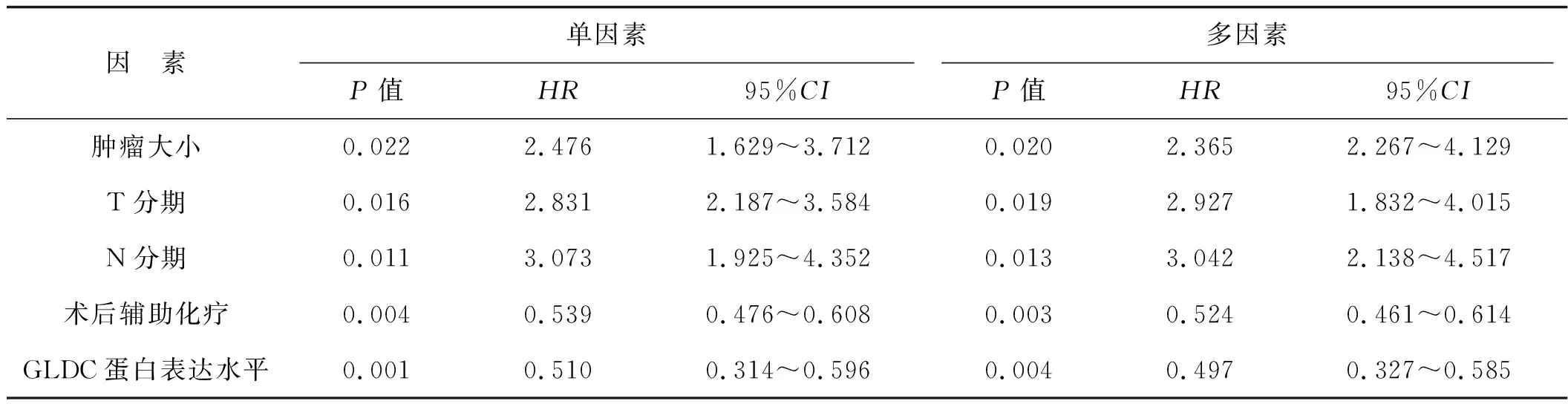
表3 Cox回归分析Tab 3 Cox regression analysis
2.5 胃癌组织GLDC蛋白不同表达患者根治后3年复发的Kaplan-Meier曲线
GLDC蛋白低表达的胃癌患者根治术后3年复发率明显高于GLDC蛋白高表达患者(Log-rank检验χ2=10.801,P=0.001),见图2。
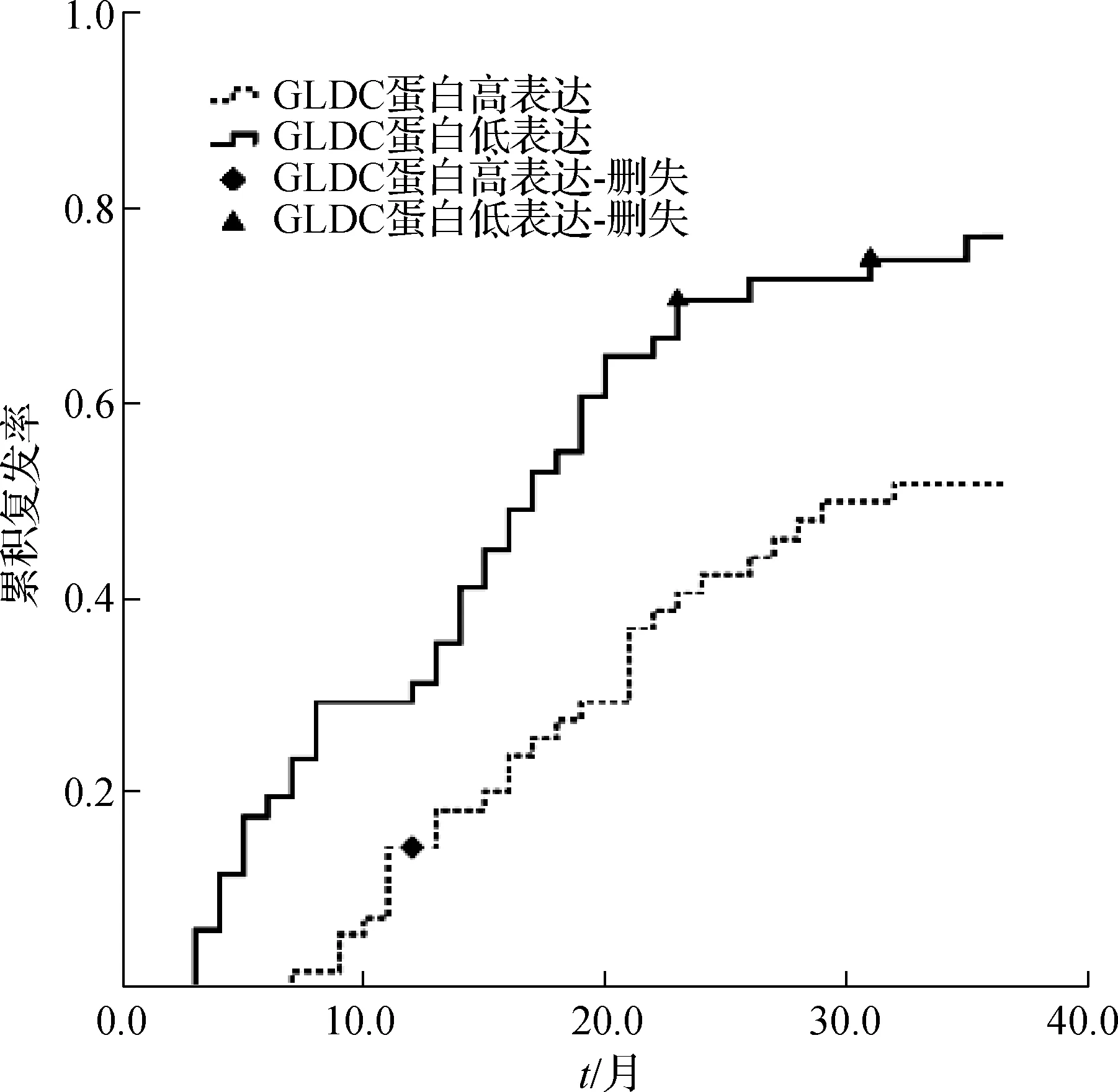
图2 GLDC蛋白高表达组与低表达组生存曲线Fig 2 Survival curve of GLDC protein high expression group and low expression group
3 讨 论
胃癌是消化系统常见的恶性肿瘤,手术是目前公认唯一能治愈胃癌的方法[7],但即使行根治术治疗,术后2年内复发率仍超过40%,而复发正是胃癌患者病死率高的重要原因[8],故分析胃癌根治术后复发的影响因素非常必要。
本研究表明,胃癌组织GLDC蛋白低表达率高于切缘正常组织,表明胃癌组织中GLDC会异常低表达。GLDC是一种甘氨酸代谢酶,其基因在胃癌发生、发展过程中突变,启动子脱氧核糖核酸发生了高度甲基化,抑制信使核糖核酸的转录,影响了基因表达与蛋白的合成,故胃癌组织中GLDC蛋白的表达水平下调,本研究结果与Min等[5]报道的一致,证实了胃癌组织中GLDC蛋白低表达。李哲丰等[9-10]发现在卵巢癌细胞、前列腺癌组织中,GLDC呈现高表达,发挥促癌功效,与在胃癌组织中的表达水平和作用相反,可能与GLDC在不同类型的癌症中的作用机制不同有关,有待深入探讨。
本研究显示,胃癌组织GLDC蛋白表达水平与肿瘤大小、lauren分型、T分期、N分期相关,且复发组癌组织GLDC蛋白低表达率高于未复发组,Cox分析显示GLDC蛋白高表达是胃癌患者根治术后复发的保护因素。GLDC基因在胃癌细胞中发挥抑癌基因功效,其GLDC基因组不仅参与细胞的增殖与分化、诱导细胞G1-S-G2分裂期阻滞,还可通过增强丝切蛋白的泛素化影响细胞骨架重塑,通过降低机体活性氧自由基的水平增强细胞的自噬能力发挥抑癌功效[11],且GLDC蛋白能抑制癌细胞的增殖、迁徙、浸润等行为,促进癌细胞的凋亡,削弱癌细胞的扩散、转移能力,进而抑制肿瘤进展,降低复发风险[12]。本研究Kaplan-Meier生存曲线分析结果显示,胃癌组织GLDC 蛋白低表达患者的复发率明显高于高表达患者,进一步证实了胃癌组织GDCL蛋白的表达水平与患者行根治术后复发的相关性。此外,Cox多因素分析结果显示,肿瘤大小、T分期、N分期均是胃癌患者根治术后复发的危险因素,术后辅助化疗是保护因素。肿瘤直径越大,浸润的范围越广,T分期级别越高,浸润的程度越深;N分期越高,淋巴结转移数目越多,侵犯程度越大,越容易导致术后复发;术后辅助化疗可更彻底清扫手术时可能残存的癌组织,提升根治切除率,与既往研究[13-15]结果一致。
综上所述,GDCL蛋白在胃癌患者癌组织中表达水平下调,在根治术后复发的胃癌患者癌组织中表达水平更低,GDCL蛋白表达水平、肿瘤大小、T分期、N分期、术后辅助化疗均是胃癌患者根治术后复发的影响因素。建议临床增加对胃癌组织GDCL蛋白低表达患者术后随访频率,结合肿瘤直径和T、N分期给予合理辅助化疗方案,以降低复发风险,改善患者预后。

