RP-HPLC法检测甜梦口服液(甜梦合剂)中淫羊藿苷、紫丁香苷和23-乙酰泽泻醇B的含量
师国袁,陈 璇
(1山西医科大学药学院,太原 030000;2山西医科大学药物分析教研室;*通讯作者,E-mail:wanfamoni_852@tom.com)
甜梦口服液(甜梦合剂),具有益气补肾、健脾和胃、养心安神等功能,临床主要用于治疗头晕耳鸣、视减听衰、失眠健忘、食欲不振、腰膝酸软、心慌气短、中风后遗症等病症的治疗,且其对脑功能减退、冠状血管疾患、脑血管栓塞及脱发也有一定作用[1-3]。甜梦口服液(甜梦合剂)系由刺五加、制马钱子、炙淫羊藿、泽泻、黄精等17味药材,采用煎煮、过滤、滤液浓缩、灭菌、灌封等工艺加工制成的口服中药制剂,药材组成中刺五加具有益气健脾、补肾安神等功效[4-6],淫羊藿具有促进人体造血功能、免疫功能、抗衰老、抗肿瘤等功效[7-9];泽泻具有利水渗湿、泄热、化浊降脂等功效[10-12]。目前,随着我国人口老龄化趋势的加重,越来越多的老年朋友患有失眠健忘、腰膝酸软等症状,因此甜梦口服液(甜梦合剂)在医院临床使用范围和使用量也日趋增多。甜梦口服液(甜梦合剂)现收载于2020年版《中国药典》一部中,其质量控制项目中的含量测定项,是以淫羊藿药材为检测对象,即通过控制淫羊藿苷成分的含量[13],实现对甜梦口服液(甜梦合剂)的含量质量控制。因甜梦口服液(甜梦合剂)药材组成较多,仅通过控制一种药材进行含量的质量控制,不能较全面地监测该药品的质量水平。因此,实验建立RP-HPLC法同时检测甜梦口服液中的淫羊藿苷、紫丁香苷和23-乙酰泽泻醇B成分含量的分析方法。现报道如下。
1 仪器与试药
1.1 仪器
岛津LC-30A型高效液相色谱仪,配置在线脱气机、DAD检测器等(日本Shimadzu科技有限公司);梅特勒-托利多AE200型电子天平(精度为万分之一,瑞士Mettler-Toled科技有限公司);Shimadzu CLC ODS C18液相色谱柱(日本Shimadzu科技有限公司);KQ-3200 ES型超声波清洗机(昆山超声设备公司)。
1.2 试药
紫丁香苷对照品(CAS号为118-34-3,批号为111574-202106,含量以94.3%计,规格为20 mg/支)、淫羊藿苷对照品(CAS号为489-32-7,批号为110737-202017,含量以98.1%计,规格为20 mg/支)、23-乙酰泽泻醇B对照品(CAS号为26575-95-1,批号为111846-202006,含量以98.3%计,规格为20 mg/支),均购买于中国食品药品检定研究院。甜梦口服液(甜梦合剂)供试品,为荣昌制药(淄博)有限公司生产的市售产品(规格:每支装10 ml,批号:20220112、20220232、20220302);乙腈、甲醇:HPLC级,购自德国赛尔策FLUKA试剂有限公司;实验用水:去离子水,自制;其他试剂:分析纯,购自国药集团。
2 方法与结果
2.1 色谱条件
色谱柱为Shimadzu CLC ODS C18(4.6 mm×250 mm,5 μm),色谱柱温:30 ℃。以0.3%磷酸溶液(流动相A)-乙腈(流动相B)为流动相,梯度洗脱(0~4 min,95%A;4~7 min,95%~78%A;7~10 min,78%~38%A;10~16 min,38%~26%A;16~23 min,26%~19%A;23~28min,19%A;28~28.5 min,95%A;流速:1.0 ml/min),测定波长:淫羊藿苷为271 nm、紫丁香苷为265 nm和23-乙酰泽泻醇B为207 nm,进样体积:10 μl。
2.2 溶液制备方法
2.2.1 单个对照品储备液 取淫羊藿苷对照品,精密称取适量,置10 ml量瓶中,制备每1 ml溶液中含淫羊藿苷196.2 μg的对照品储备液,同法分别制备每1 ml溶液中含754.4 μg紫丁香苷和196.6 μg 23-乙酰泽泻醇B的单个对照品储备液,分别加甲醇定容,摇匀。
2.2.2 对照品溶液 取2.2.1淫羊藿苷、紫丁香苷和23-乙酰泽泻醇B单个对照品储备溶液,分别准确吸取1.0 ml,置同一支10 ml棕色量瓶中,加甲醇定容,摇匀即得。
2.2.3 阴性供试品溶液 按甜梦口服液(甜梦合剂)制备方法和药材比例,分别制备缺淫羊藿、刺五加和泽泻药材的阴性供试品,阴性供试品按2.2.4供试品溶液制备方法,分别制备缺淫羊藿、刺五加和泽泻的阴性供试品溶液。
2.2.4 供试品溶液 取甜梦口服液(甜梦合剂)供试品,精密移取1.0 ml,置10 ml棕色量瓶中,加95%甲醇溶液溶解,超声提取15 min(超声功率250 W,频率50 Hz),取出放冷,加95%甲醇溶液定容,摇匀,0.45 μm滤膜滤过,取续滤液,即为供试品溶液。
2.3 方法学验证
2.3.1 专属性考察 取2.2.2对照品溶液、2.2.3阴性供试品溶液和2.2.4供试品溶液,按2.1色谱条件设置液相色谱仪,上述溶液分别注入10 μl,采集谱图峰面积。结果发现,在阴性供试品溶液谱图中,淫羊藿苷、紫丁香苷和23-乙酰泽泻醇B组分对应的位置无干扰,3种成分分离良好,理论塔板数均大于2 000(见图1)。
2.3.2 仪器精密度考察 取2.2.2对照品溶液,按2.1色谱条件设置液相色谱仪,上述溶液连续进样6次,每次注入10 μl,采集谱图峰面积。根据谱图记录的紫丁香苷、23-乙酰泽泻醇B和淫羊藿苷峰面积计算RSD(相对标准偏差)。结果显示,紫丁香苷、23-乙酰泽泻醇B和淫羊藿苷峰面积RSD分别为1.2%,1.0%和1.1%,表明仪器具有良好的精密度。
2.3.3 方法重复性考察 取甜梦口服液(甜梦合剂)供试品(规格:每支装10 ml,批号:20220112),精密移取1.0 ml,置10 ml棕色量瓶中,平行取样6份,后续按2.2.4供试品溶液制备方法进行处理,得6份供试品溶液,按2.1色谱条件设置液相色谱仪,上述溶液分别注入10 μl,采集谱图峰面积。以紫丁香苷、23-乙酰泽泻醇B和淫羊藿苷6次检测结果计算RSD。结果显示,紫丁香苷、23-乙酰泽泻醇B和淫羊藿苷检测结果RSD分别为1.5%,1.2%和1.4%,表明方法具有良好的重复性。
2.3.4 稳定性考察 取甜梦口服液(甜梦合剂)供试品(规格:每支装10 ml,批号:20220112),按2.2.4供试品溶液制备方法进行处理,得供试品溶液,常温放置,分别于0,4,8,12,16,24 h取样分析,按2.1色谱条件设置液相色谱仪,上述取样点分别注入10 μl,采集谱图峰面积。以紫丁香苷、23-乙酰泽泻醇B和淫羊藿苷峰面积计算RSD。结果发现,紫丁香苷、23-乙酰泽泻醇B和淫羊藿苷峰面积RSD分别为1.1%,1.4%和0.9%,表明溶液在24 h内稳定。
2.3.5 线性关系考察 取2.2.1紫丁香苷、23-乙酰泽泻醇B和淫羊藿苷单个对照品储备溶液,分别准确移取0.01,0.05,0.1,0.5,1 ml,置5个10 ml棕色量瓶中,加95%甲醇溶液定容,摇匀,按2.1色谱条件设置液相色谱仪,上述溶液分别注入10 μl,采集谱图峰面积。以峰面积(Y)为纵坐标、浓度(X)为横坐标进行线性回归,计算曲线方程。结果表明,紫丁香苷、23-乙酰泽泻醇B和淫羊藿苷分别在0.196 2~19.62 μg/ml,0.754 4~75.44 μg/ml和0.196 6~19.66 μg/ml浓度范围内有良好的线性关系,相关系数均在0.995以上(见表1)。

表1 三种组分曲线方程、线性系数及范围
2.3.6 加样回收考察 取已测定紫丁香苷、23-乙酰泽泻醇B和淫羊藿苷含量的甜梦口服液(甜梦合剂)供试品(规格:每支装10 ml,批号:20220112),精密移取1.0 ml,置10 ml棕色量瓶中,平行取样6份,分别加入2.2.1紫丁香苷、23-乙酰泽泻醇B和淫羊藿苷单个对照品储备溶液适量,再按2.2.4供试品溶液制备方法进行处理,得6份加标溶液;按2.1色谱条件设置液相色谱仪,上述溶液分别注入10 μl,采集谱图峰面积。计算回收考察结果。结果表明,紫丁香苷、23-乙酰泽泻醇B和淫羊藿苷平均加样回收率分别为99.47%,98.69%和100.26%(见表2),表明方法准确度良好。
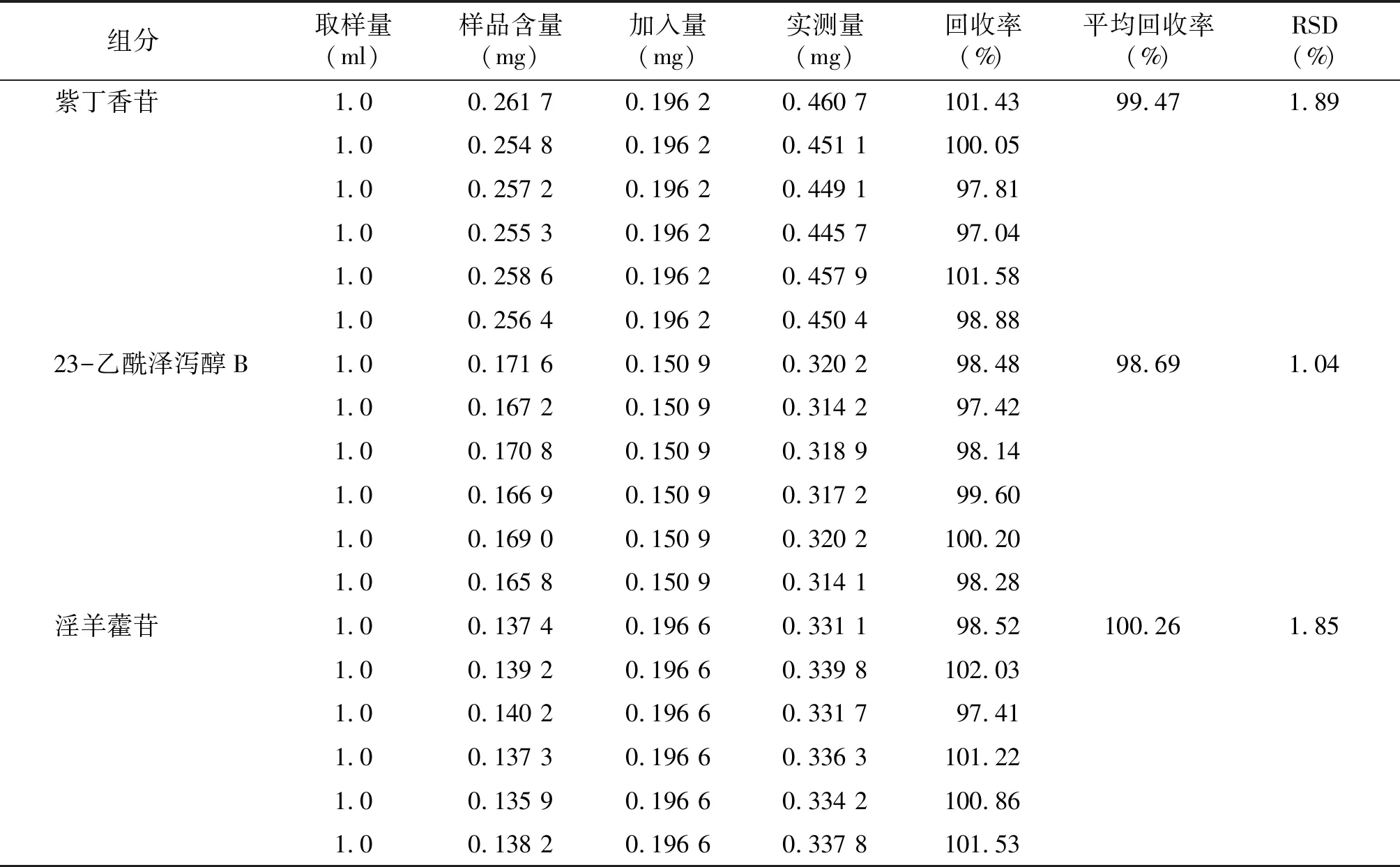
表2 甜梦口服液供试品加标回收考察结果
2.4 市售供试品检测
取甜梦口服液(甜梦合剂)供试品(荣昌制药(淄博)有限公司生产的市售产品,规格:每支装10 ml,批号:20220112、20220232、20220302),按2.2.4供试品溶液制备方法进行处理,每个供试品处理2份平行样;按2.1色谱条件设置液相色谱仪,上述溶液分别注入10 μl,采集谱图峰面积。根据峰面积计算3批供试品中紫丁香苷、23-乙酰泽泻醇B和淫羊藿苷的含量,结果见表3。
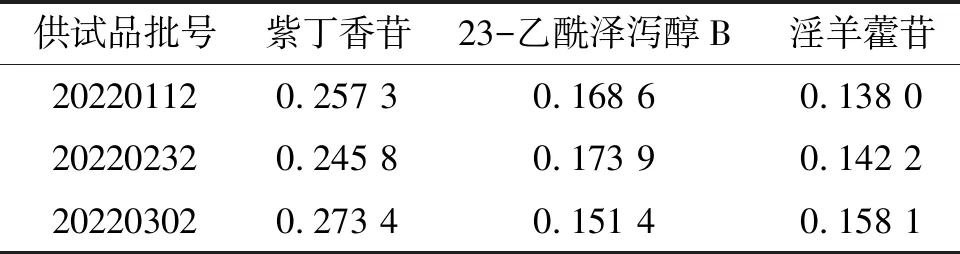
表3 甜梦口服液中紫丁香苷、23-乙酰泽泻醇B和淫羊藿苷含量检测结果 (mg/ml)
3 讨论
3.1 提取条件的优化
甜梦口服液(甜梦合剂)供试品基质较为复杂,由17味药材组成,因此选择合适的提取条件对提高检测灵敏度、降低基质干扰等具有关键的作用。实验分别考察选择85%,90%,95%甲醇溶液和无水甲醇[14-16]时,对甜梦口服液(甜梦合剂)供试品中紫丁香苷、23-乙酰泽泻醇B和淫羊藿苷的提取效果,结果选择95%甲醇溶液时提取效果最佳;确定提取溶剂后,分别考察超声功率和超声时间的影响,最终确定最佳的提取条件为:甲醇作为提取溶剂,超声功率控制250 W,时间控制15 min。
3.2 流动相体系的选择
液相色谱法常用的流动相有甲醇体系和乙腈体系[17-19],试验分别选择甲醇-水、乙腈-水、0.3%磷酸溶液-甲醇和0.3%磷酸溶液-乙腈作为流动相体系时,考察紫丁香苷、23-乙酰泽泻醇B和淫羊藿苷3种待测组分的出峰时间、分离效果等。结果发现,选择甲醇体系时,紫丁香苷、23-乙酰泽泻醇B和淫羊藿苷出峰时间较长,且因23-乙酰泽泻醇B最大吸收波长在207 nm附近,故23-乙酰泽泻醇B信号背景干扰较大,定量准确度偏低;选择乙腈-水体系时,淫羊藿苷色谱峰发生分叉,定量准确度偏低;选择0.3%磷酸溶液-乙腈时,3种待测组分分离良好,分析时间较短,且无基质干扰。故实验选择0.3%磷酸溶液-乙腈作为流动相体系。
3.3 检测波长的选择
实验选取甜梦口服液(甜梦合剂)药材组成中的淫羊藿、刺五加和泽泻3种药材,通过控制这3种药材的药效活性成分作为其质量控制的指标。取2.2.2紫丁香苷、23-乙酰泽泻醇B和淫羊藿苷对照品溶液,按2.1色谱条件设置液相色谱仪,设置波长扫描为200~400 nm[20-22],上述溶液注入10 μl,采集紫丁香苷、23-乙酰泽泻醇B和淫羊藿苷光谱图。结果显示,紫丁香苷、23-乙酰泽泻醇B和淫羊藿苷最大吸收波长分别在265 nm,207 nm和271 nm,差异较大。为提高检测效率,实验采用程序波长切换技术,实现了在同一色谱条件下,在3种成分最大吸收波长处测定其指标性成分的含量,即波长切换法定性、定量检测甜梦口服液(甜梦合剂)中紫丁香苷、23-乙酰泽泻醇B和淫羊藿苷组分的含量。
综上,实验建立以甜梦口服液(甜梦合剂)为研究对象,采用超声提取法将甜梦口服液(甜梦合剂)中的紫丁香苷、23-乙酰泽泻醇B和淫羊藿苷3种组分提取出来,RP-HPLC法定性、定量检测的分析方法。对方法的线性、溶液稳定性、重复性等进行了系统的考察,实验结果证明,此方法具有前处理简单、分析时间短、检测结果准确等优点,可以用于甜梦口服液(甜梦合剂)供试品的质量控制。

