金荞麦胶囊中间体制备工艺的优选及质量控制
李春霞 童晓东 陈银银

【摘 要】 目的:优选金荞麦胶囊中间体的制备工艺以及质量控制。方法:以表儿茶素为实验指标,通过正交实验,围绕提取时间、回流时间、回流次数考察选取最佳工艺。结果:当溶剂为药材的6倍量,乙醇浓度为50%,回流为1 h为最佳制备工艺。结论:所建立的方法操作容易,结果准确可靠重现,可显著提高表儿茶素的提取,可用于金荞麦胶囊中间体的制备。
【关键词】 金荞麦;表儿茶素;提取工艺;正交试验;高效液相
【中图分类号】R284.1 【文献标志码】 A 【文章编号】1007-8517(2024)03-0025-05
DOI:10.3969/j.issn.1007-8517.2024.03.zgmzmjyyzz202403006
Optimization and Quality Control of the Preparation Technology of Gold Buckwheat Capsule
LI Chunxia1 TONG Xiaodong2* CHEN Yinyin3
1.Nantong RichHospital(FourthClinicalMedical Collegeof Yangzhou University),Nantong 226010,China;
2.Nantong Hospital of Traditional Chinese Medicine(Nantong Hospital to Nanjing University of Chinese Medicine),
Nantong 226001,China;
3.Nanjing University of Chinese Medicine HanLin College, Taizhou 225300,China
Abstract:Objective The preparation technology and quality control of gold buckwheat capsule intermediate were optimized.Methods Taking epicatechin as the experimental index, through orthogonal experiment, the optimal process was selected around extraction time, reflux time and reflux times.Result The solvent was 6 times the amount of medicinal materials, the concentration of ethanol was 50%, and the best preparation process was reflux for 1 hour.Results The method is easy to operate, and the results are accurate and reproducible, The extraction of epicatechin can be significantly improved,and suitable forpreparation technology of Gold buckwheat capsule.
Keywords:Fagopyrum Dibotrys ; (-)-epicatechin; Extracting Technology; Orthogonal Test; HPLC
金蕎麦是蓼科Polygonaceae植物金荞麦 Fagopyrum dibotrys(D.Don) Hara 的干燥根茎,味道略微辛辣、苦涩、清凉刺激,归肺经,具有清肺排痰、清热解毒、祛风化湿、排脓消肿的功效[1]。金荞麦中含有各种成分,如表儿茶素、芦丁、槲皮素等有效活性成分,且这些成分具有显著的抑制癌症、遏制肿瘤细胞的侵袭和转移,以及消除炎症,抗菌等重要作用[2-3],市面上许多抵抗癌症药物和预防癌症的药物都是与金荞麦有关[4-5]。
金荞麦煎剂原本为南通地区民间药物,后南通市中医院的程云龙老专家在其基础上研究制成金荞麦药物制剂,其具有清热解毒、排脓祛瘀、祛痰止咳平喘的作用。临床常用于治疗急慢性气管炎、急性肺脓疡、支气管哮喘等疾病[6],但是具有不宜携带性,用量大等缺点,而胶囊却为更适用得多,便于大规模生产。现有金荞麦制剂直接以水煎提,工艺及质量不稳定,效率低,为有效控制金荞麦胶囊的质量,对荞麦胶囊中间体的制备工艺进行了优化,直接乙醇提取,不仅有效成分的提取率提高,而且节省工作时间,提高了工作效率,能够更准确、更全面、更有效地控制其质量,方法实用可靠,保证临床质量要求。
1 仪器与材料
1.1 主要仪器 MS105DU型十万分之一电子天平(Mettler Toledo贸易有限公司);UltiMate3000高效液相色谱仪(Thermo Fisher Scientific有限公司);HH.S11-4型数显恒温水浴锅(上海博迅医疗生物仪器股份有限公司);OSJ-UP-30超纯水机(济南欧莱博科学仪器有限公司);YM-080T型超声波清洗机(深圳市方奥微电子有限公司); RE-3000D旋转蒸发器(上海亚荣);TD4型离心机(湖南凯达科学仪器); C18分析色谱柱(Waters有限公司)。
1.2 药物和试剂 (-)表儿茶素对照品(批号878-200102):中国药品生物制品检定所;金荞麦中药饮片(批号20190607、20190924):南通三越中药饮片有限公司,(批号20191029):江苏建生源中药材有限公司;乙腈(分析纯):国药集团化学试剂有限公司;乙腈(色谱纯)、甲醇(色谱纯):德国默克公司;甲酸、磷酸、甲醇、乙酸乙酯、乙醇(分析纯):南京化学试剂股份有限公司;硅胶板(批号20180308):青岛海洋化工厂分厂。
2 方法与结果
2.1 药材的选取 为了控制胶囊中间体的质量,首先从药材的源头来选取了三批不同批次的金荞麦饮片,通过回流提取,以金荞麦中表儿茶素的含量作为指标来选取最佳的药材饮片。
2.2 药材薄层鉴别及含量测定
2.2.1 药材鉴别中对照品溶液的制备 称取表儿茶素标准品5 mg放置于5 mL容量瓶中,向其中加入甲醇适量定容至刻度线处,配置制成每1 mL含有1 mg的溶液。
2.2.2 药材鉴别中供试品溶液的制备 称取三种不同批次的金荞麦饮片各2.5 g,放置于圆底烧瓶中,再各自向其中加入20 mL甲醇,静置1 h,加热回流1 h,冷确至室温,过滤,在60 ℃下将滤液浓缩至5 mL,作为供试品溶液备用[7]。
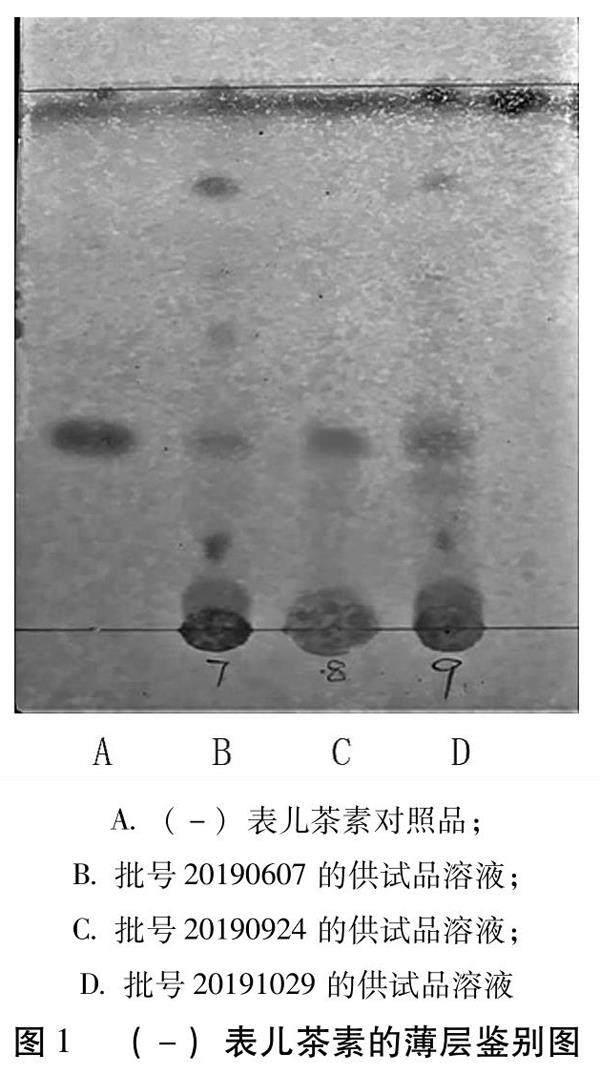
2.2.3 (-)表儿茶素的鉴别 按照薄层色谱法(通则0502)试验,用毛细管吸取供试品溶液和对照品溶液各5 μL,分别点于同一硅胶薄层板上,以甲苯-乙酸乙酯-甲醇-甲酸作为展开剂比例分别是1∶2∶0.2∶0.1,展开,取出薄层硅胶板,晾干,用25%磷钼酸乙醇溶液喷薄层板,用吹风机加热至斑点显色清晰,供试品在与对照品色谱相应的位置上,显相同颜色的斑点[7]。因只有单味药材,所以不做阴性对照。色谱图如图1所示。
2.2.4 药材含量测定对照品溶液的制备 精密称定表儿茶素标准品0.0041 g放置10 mL容量瓶中,加乙腈-水混合溶液两者比例为10∶90,定容至容量瓶刻度线。
2.2.5 药材含量测定供试品溶液的制备 将三种不同批次的金荞麦饮片(批号20190607、批号20190924、批号20191029)打成粗粉,每批次取2.0 g,精密称定,放入圆底烧瓶中,向其中加入50 mL稀乙醇,乙醇浓度为50%,用封口膜密封,然后精密称定,首先放置1 h,再通过水浴锅加热回流1 h,然后放冷至室温,再称定其重量,用稀乙醇補足失去的重量,充分摇匀,再过滤,精密量取续滤液25 mL,在60 ℃下加热浓缩至近干,残渣加比例为10∶90乙腈-水混合溶液分次洗涤,溶解液转移至10 mL量瓶中,再加乙腈-水混合溶液至刻度,振荡摇匀,用离心机离心5 min,转速为每分钟3000转,上清液精密量取5 mL,加于聚酰胺柱(湿法装柱,30~60目,柱长为15 cm,内径为1.0 cm)上,先用50 mL水洗脱,再用100 mL乙醇洗脱,收集乙醇洗脱液, 低温浓缩至近干,残渣用乙腈-水(10∶90)混合溶液溶解,转移至10 mL量瓶中,加乙腈-水混合溶液稀释至刻度,摇匀,即得[7]。
2.2.6 测定法 分别精密吸取对照品溶液与供试品溶液各10 μL,注入高效液相色谱仪,记录峰面积,通过标准曲线法算出相应含量即得,批号20190607、批号20190924、批号20191029的金荞麦饮片三者含量分别是670.19 μg/g、354.68 μg/g、512.28 μg/g,因此选取批号20190607的金荞麦饮片进行实验。
2.3 荞麦胶囊中间体含量测定
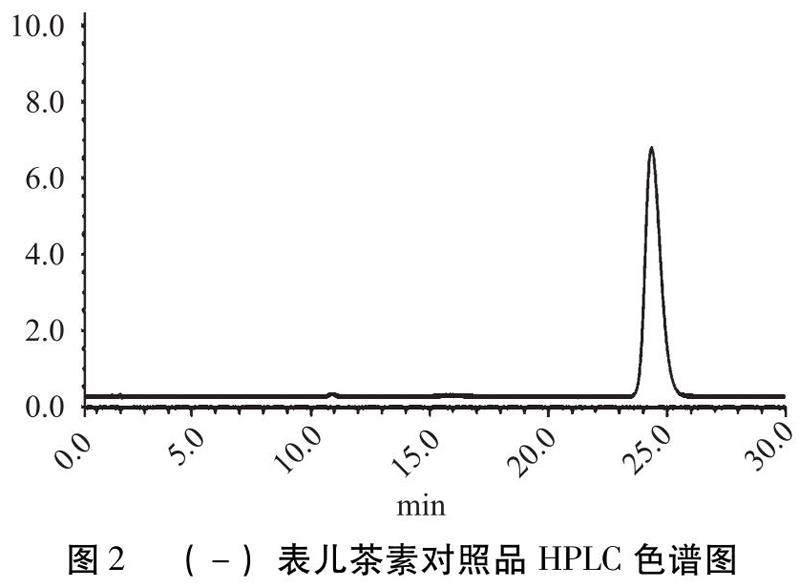
2.3.1 色谱条件与系统适用性条件 XBridgeC18(4.6 mm×150 mm,5 μm);以乙腈-0.004%磷酸溶液(7∶93)为流动相;流速:1.0 mL/min;进样量为10 μL。检测波长为280 nm;柱温30 ℃。色谱分离如图2、图3所示。
2.3.2 供试品溶液的制备 取金荞麦浸膏0.2 g,加入10 mL比例为10∶90乙腈-水混合溶液,超声直至溶解,量瓶中定容至10 mL,振荡摇匀,再用离心机(3000 r/min)离心5 min,上清液精密量取5 mL,加于聚酰胺柱(湿法装柱,30~60目,柱长为15 cm,内径为1.0 cm)上,先用50 mL水洗脱,再用100 mL乙醇洗脱,收集乙醇洗脱液,低温浓缩至近干,残渣用乙腈-水(10∶90)混合溶液溶解,转移至5 mL量瓶中,加乙腈-水混合溶液稀释至刻度,摇匀,即得[7]。
2.3.3 方法学考察
2.3.3.1 线性关系考察 精密称取表儿茶素对照若干,加乙腈-水混合溶液(两者比例为10∶90)稀释分别配成82 μg/mL、65.6 μg/mL、49.2 μg/mL、32.8 μg/mL、16.4 μg/mL的溶液,用使用0.45 μm微孔滤膜滤,分别进样,每个进样3针,每针进样10 μL,观察峰面积。以峰面积平均值对表儿茶素的浓度进行线性回归,得到回归方程为Y=0.0911X-1.1961,r=0.9992。表明表儿茶素在16.41~82 μg/mL内线性关系良好。
2.3.3.2 精密度试验 精密吸取标准溶液10 μL,连续进样5次,测定峰面积。测得的RSD为0.94%,表明仪器精密性良好。
2.3.3.3 稳定性试验 取供试品溶液,分别在放置0 h、2 h、4 h、6 h、8 h后进行测定,测得的RSD为0.61%。表明样品在8 h内稳定。
2.3.3.4 回收率试验 采用加样回收法,精密称取一份金荞麦浸膏0.2 g,依法按照“2.3.1供试品溶液的制备”制成供试品溶液,并在其中加入定量的表儿茶素标准品,连续进样5针,每针注入10 μL于高效液相色谱仪中,测量结果见表1,平均回收率为98.28%,RSD为1.56%。
2.4 制备工艺的优选
2.4.1 提取工艺的选择 溶剂量、回流时间、溶剂浓度是提取过程参考因素中是非常重要的,为了达到最佳的全面实验等效的结果以最少的次数,采用了三因素三水平正交试验。见表2。
2.4.2 正交试验 设计优选制备工艺按照 L9(34) 正交表安排试验,取9份粉碎成粗粉每份20 g的金荞麦药材,按正交表分别加入对应的乙醇,置于圆底烧瓶中进行回流提取,滤过,合并滤液,60℃浓缩成膏,干燥,即得样品,以表儿茶素的含量为指标筛选制备工艺。结果见表3正交试验设计及结果。
表儿茶素的含量=(测得表儿茶素的浓度×稀释体积×干膏)/(金荞麦的质量×干膏量)
2.4.3 实验结果的统计学分析 从表4可以分析出在三个因素中,回流时间的显著水平几乎无影响,不做考虑,溶剂浓度和溶剂量都具有显著差异,再结合实际生产选取回流时间为一h,通过图4的效应曲线图可知最佳溶剂浓度为50%、最佳溶剂量为6倍量的乙醇。所以乙醇浓度为50%,溶剂量为6倍量,回流1 h为最佳制备工艺。
2.4.4 验证性试验 根据正交试验结果,确定最佳的制备方法,取每份20 g金荞麦粗粉3份,加入6倍量50%的乙醇,回流两次,每次1 h,在60 ℃下浓缩至干膏。每份取0.2 g,用比例10∶90乙腈-水混合溶液溶解,按照2.3.2的方法制成供试品溶液,在测量其含量,测得表儿茶素的含量分别是190.1775 μg/g、195.0128 μg/g、193.2148 μg/g,计算RSD结果为1.27%,结果表明此最佳工艺稳定可行、可重复性好。
2.5 金荞麦胶囊中间体的质量控制 中药制剂较化学药来说更加复杂,因为其成分更多,更杂,而且中药制剂在制备过程和它的贮藏过程中都会产生一些变化,因此它的质量控制比化学药要复杂得多,而且不同批次的药材也会影响制成中药药物制剂质量的稳定性,因此中药制剂的质量控制是一项不可缺少的工作。对此我们可以从药材的质量控制、制法规范、卫生学3个方面来控制。
2.5.1 药材的质量控制的选择 中药制剂质量以药物的来源、药物的规格以及药材的品种为基本[8],在药物生产过程中占有巨大的影响,因此在制备中药制剂时必须以药材的来源、品种与规格作为选用的标准。而且但凡是药品标准收载的中药制剂,都应按照药品的标准规定的方法制备。
2.5.2 制法规范的选择 中药制剂制作方式与中药制剂的质量紧密相连,所以根据不同的需求选用不同的剂型,如临床的需要,药材的性质,药材的不同成分,待选定相应的剂型后,然后再研究药物制剂的生产过程,选择最佳的生产工艺,从而保证中药制剂的质量。因此但凡是在药品标准中收录的中药制剂,在生产制备过程中均应按照药品标准规定的标准进行生产。
2.5.3 卫生学标准的选择 为了保证临床用药的安全、有效,国家有关部门颁布了药品卫生标准,对中药制剂中的致病菌、活螨、细菌、真菌等做了規定。包括热原检查、细菌内毒素检查、无菌检查、微生物限度检查[9]。
2.5.4 鉴别与检查 目前最主要的鉴别方法是薄层色谱法,用来检查药材的正确性以及药物制剂中的主要有效成分。药物制剂主要的检查是药典中制剂通则所规定的项目,如相对密度、干燥失重、崩解时限、重金属等。
2.5.5 金荞麦胶囊中间体(-)表儿茶素的鉴别 取金荞麦胶囊中间体0.10 g,加入10 mL甲醇进行超声溶解,然后进行过滤,60 ℃下进行浓缩,依2.1.3(-)表儿茶素的鉴别法鉴别,具体操作如下:照薄层色谱法(通则0502)试验,用毛细管吸取供试品溶液和标准品溶液各5 μL,分别点于同一硅胶薄层板上,用甲苯-乙酸乙酯-甲醇-甲酸作为展开剂,展开,展开剂的比例分别是1∶2∶0.2∶0.1,待展开剂展开至前沿线,取出,晾干,用25%磷钼酸乙醇溶液喷薄层板,用吹风机加热至斑点显色清晰[7]。供试品与对照色谱在相同的位置上,显相同颜色的斑点因只有单味药材,所以不做阴性对照。
2.5.6 金荞麦胶囊中间体(-)表儿茶素的含量测定 按2.3荞麦胶囊中间体含量测定方法取金荞麦胶囊中间体配置供试品溶液,精密吸取标准品溶液与供试品溶液各10 μL,注入高效液相色谱仪,记录两者峰面积,通过标准曲线法算出相应含量即得。
3 讨论
3.1 指标成分的选择 临床研究表明,金荞麦中的表儿茶素的多羟基结构的分子结构特性导致其药理活性较多,具有抗氧化、降血脂、降血糖、抑制胰岛素、防止心血管疾病,此外还具有抗炎、抑菌、提高免疫力等生理活性[10],能够针对金荞麦药物的主治病症起到主要的治疗作用,因此最终选用表儿茶素作为检测对象。
3.2 流动相比例的选择 在药典基础上对乙腈-水的比例进行改变,分别为8∶92、7∶93、5∶95,结果表明在两者比例为7∶93和5∶95时分离都比较好,但5∶95时出峰时间远远大于7∶93时,考虑到操作的便捷性以及实验材料的损耗,选择流动相的比例为7∶93。
3.3 浓缩温度的选择 儿茶素类物质,在高温(100 ℃) 条件下儿茶素主要发生脱没食子酸和异构化反应[11],在碱性、过高温度等环境条件下也容易发生改变[12],温度设在60 ℃,此时通过薄层鉴别能够很好地观察到表儿茶素。
该实验以表儿茶素的含量为指标筛选制备工艺,对于荞麦胶囊中间体的提取具有方便操作,结果准确可靠重现,可显著提高表儿茶素的提取率,质量可控。可用于金荞麦胶囊中间体的制备。以表儿茶素和药材为对照品对金荞麦进行薄层鉴别可保证原料药的质量。
参考文献
[1]肖培根.新编中药志第一卷[M].北京:化学工业出版社,2002:607-610.
[2] 艾群,王斌,王国清. 金荞麦制剂的抑菌研究[J].黑龙江医学, 2002, 26(9):666.
[3] CHEN P K. 金荞麦体外抑制肿瘤细胞生长的研究[J].中西医结合学报, 2003,1(2):128-131.
[4] 张雯洁,李兴从,刘玉青,等. 威麦宁的酚性成分[J].南植物研究,1994, 16(4):354-356.
[5] 何显忠.金荞麦的药理作用和临床应用[J].珍国医国药, 2001, 12(4):316-317.
[6] 唐宇,贾洪锋,孙俊秀,等.金荞麦果实中有效成分的分析[J].中国野生植物资源,2013,32(1):52-55.
[7] 国家药典委员会.中国药典(一部)[S].北京:中国医药科技出版社,2010.
[8] 方亮.药剂学[M].8版.北京:人民卫生出版社,2016:387-388.
[9] 刘敏,刘志春.药品生产企业微生物实验室设计[J].医药工程设,2008(1):18-21.
[10]童观珍,付晓萍,杨艳,等.表儿茶素的分布及药理活性研究进展[J].云南农业大学学报(自然科学),2018,33(2):343-349.
[11] LI Z, XIAO T, GAO L P, et al.Effect of temperature on the color of green tea infusion[J]. Journal of Anhui Agricultural University, 2010,37(3) :465-470.
[12] LI N, TAYLOR L S,FERRUZZI M G, et al. Kinetic study of catechin stability: effects of pH, concentration, and temperature [J].Journal of Agricultural & Food ,2012, 60(51):12531-12539.
(收稿日期:2023-05-06 編辑:刘 斌)
作者简介:李春霞(1981—),女,汉族,本科,主管中药师,研究方向为中药学及中药制剂。E-mail: ntlicx@163.com

