紫杉醇磁性纳米脂质体的制备及其性质研究
肖 超,吴新荣,*
(1.华南理工大学轻工与食品学院,广东广州 510640; 2.广州军区广州总医院药学部,广东广州 510010)
紫杉醇磁性纳米脂质体的制备及其性质研究
肖 超1,2,吴新荣1,2,*
(1.华南理工大学轻工与食品学院,广东广州 510640; 2.广州军区广州总医院药学部,广东广州 510010)
采用超声薄膜分散法制备紫杉醇磁性纳米脂质体。通过正交设计优化制备工艺,以包封率和分布情况等为综合考察指标。结果表明,最佳处方和工艺条件为:卵磷脂∶胆固醇为 6∶1,紫杉醇∶(卵磷脂 +胆固醇)为 1∶30,超声时间40min,磁粉∶紫杉醇为2∶1,吐温-80∶紫杉醇为 4∶1,聚乙二醇-800∶磁粉为 8∶1。制备的紫杉醇磁性纳米脂质体包封率最高可达 84.4%±1.7%,平均粒径 150±20nm。该方法制备的紫杉醇磁性纳米脂质体包封率较高,分布均匀,符合靶向制剂的要求。
紫杉醇,磁性纳米脂质体,包封率,正交实验
1 材料与方法
1.1 材料与设备
紫杉醇原药 含量 99%以上,批号 CP-01-081201,福建南方生物技术股份有限公司;紫杉醇对照品 含量 99.5%,批号 1534-200202,中国药品生物制品检验所;大豆卵磷脂、吐温-80 广州威佳科技有限公司;胆固醇、色谱纯甲醇、聚乙二醇-800美国 Sigma公司;丙酮 天津市红岩试剂厂;四氧化三铁纳米磁粉 焦作伴侣纳米材料工程有限公司;氨水、油酸、无水乙醇 广州化学试剂厂,均为分析纯。
ZFQ-85A旋转蒸发器 上海医械专机厂;电热恒温水浴锅 上海锦萍仪器仪表有限公司; DL-720A超声波清洗仪 上海之信仪器有限公司; SHZ-D(III)型循环水式真空泵 巩义市予华仪器有限责任公司;ALc-210分析天平 美国ACCULAB公司;TP-320A电子天平 湘仪天平仪器设备有限公司;AXLC1805超纯水机 广州亿鑫生物科技有限公司;高效液相色谱仪 Waters2487系统,美国Waters公司;H-600型电子透射显微电镜 日本日立公司;截留分子量 3500透析袋 美国Viskase公司。
1.2 实验方法
1.2.1 紫杉醇磁性纳米脂质体的制备方法 称取处方量大豆卵磷脂和胆固醇,溶于适量无水乙醇中,搅拌至完全溶解,置于磨口圆底烧瓶中,55℃恒温水浴减压蒸去无水乙醇,使膜材在烧杯壁上形成均匀类脂薄膜,另将处方量的紫杉醇原料药溶于无水乙醇并溶解类脂膜,混匀振荡制得类脂溶液;然后加入一定量的油酸改性的纳米磁粉、溶有聚乙二醇 -800的 PBS (pH7.4)和吐温-80,超声分散,55℃(100r·min-1)条件下,再次减压蒸发约 2h除去有机溶剂,待达到胶态后,向烧瓶内吹氮气流 30min,使有机溶剂完全清除,继续旋转至溶液由乳白色变为浅黑色半透明状类脂即得[3-4]。
1.2.2 紫杉醇纳米脂质体制备实验设计
1.2.2.1 紫杉醇纳米脂质体制备单因素实验设计参考相关文献并结合实验室的制备方法,拟选取影响制备紫杉醇纳米脂质体性质的单因素为:磷脂和胆固醇的质量比 (A)、药物和脂类的质量比 (B)、超声时间 (C)、旋转蒸发的水浴温度 (D)[5],并取如下的水平 (以下比例均为质量比):
卵磷脂∶胆固醇为 9∶1、6∶1、3∶1、2∶1、1∶1、1∶2、1∶3、1∶6、1∶9;紫杉醇∶(卵磷脂 +胆固醇)为 1∶50、1∶40、1∶30、1∶20、1∶10、1∶5;超声时间为 10、20、30、40、50、60min;旋转蒸发的水浴温度为 30、40、45、50、55、60、70℃。
1.2.2.2 紫杉醇纳米脂质体制备正交实验设计 根据单因素和预实验结果,在影响紫杉醇磁性纳米脂质体的粒径大小及分布和包封率的因素中,磷脂和胆固醇的质量比 (A)、药物和脂类的质量比 (B)、超声时间(C)为主要因素,而旋转蒸发水浴温度为次要因素。因此设立A、B、C 3个考察因素,每个因素选择 3个水平,选用正交表 L9(34)考察制备紫杉醇纳米脂质体的最优工艺条件,因素水平如表 1。

表 1 紫杉醇纳米脂质体正交实验因素水平表
1.2.3 紫杉醇磁性纳米脂质体制备实验设计
1.2.3.1 紫杉醇磁性纳米脂质体制备单因素实验设计 按上述正交实验得到的最佳条件制备紫杉醇脂质体,并参考相关文献,对磁粉添加量、吐温-80添加量和聚乙二醇-800的添加量对添加磁粉后的紫杉醇磁性纳米脂质体的性质影响做单因素实验[6],选取如下水平:
磁粉∶紫杉醇为 6∶1、5∶1、4∶1、3∶1、2∶1、1∶1、1∶2、1∶3、1∶4、1∶5;吐温-80∶紫杉醇为 10∶1、8∶1、6∶1、4∶1、2∶1、1∶1、1∶2;聚乙二醇-800∶磁粉为 1∶1、3∶1、5∶1、8∶1、10∶1、12∶1、15∶1。
1.2.3.2 紫杉醇磁性纳米脂质体制备正交实验设计根据单因素和预实验结果,设立A(磁粉∶紫杉醇)、B(吐温-80∶紫杉醇)、C(聚乙二醇∶磁粉)3个考察因素,选用正交表 L9(34)进行考察,因素水平如表 2。

表 2 紫杉醇磁性纳米脂质体正交实验因素水平表
1.2.4 评价方法
1.2.4.1 RP-HPLC测定紫杉醇磁性纳米脂质体包封率和载药率 称取一定量冻存(4℃)产品,加入色谱纯甲醇溶解,充分振荡混匀,经高速离心后取上清液,向离心沉淀物中再加入色谱纯甲醇,充分摇匀再离心,将两次上清液合并,吸取约 1mL加入高效液相色谱仪进样管,振荡片刻,按顺序摆放,用反相高效液相色谱法分析[7]。
液相色谱的条件为:色谱柱:迪马 C18ODS色谱柱(4.6mm×250mm,5μm);流动相:甲醇-水 (7∶3);柱温:30℃;流速:1.0mL·min-1;进样量:20μL;紫外检测波长:228nm;进样时间:20min;紫杉醇标准品做对照。
包封率和载药量按以下公式计算:

1.2.4.2 显微形态观察 取少量紫杉醇磁性纳米脂质体混悬液滴至专用铜网上,37℃电热干燥箱内烘干 5min,使粒子在铜网上浓缩沉积,用透射电子显微镜进行观察粒径大小和分布情况,并摄制照片[8]。
1.2.4.3 体外释药实验 分别精密吸取紫杉醇磁性纳米脂质体、空白脂质体、同质量浓度的紫杉醇溶液5.00mL至V ISK ING透析袋中,放入 100mL介质 (乙腈-水 =47∶53的溶液)中,置于恒温 (37±1℃)水浴中。于 0.25、0.5、1、2、4、8、10、12、14、16、18、20、24、30、33、36、44、48h吸取介质 5.00mL,同时补充相同介质 5.00mL,分别以空白脂质体透析液和释放介质为参照,应用紫外分光光度法,于 228nm处测定不同时间点含药磁性脂质体和原料药物溶液透析出游离药物的紫外吸收,求算药物浓度和累积释放量,绘制含药脂质体和原料药累积释药曲线[9]。
2 结果与讨论
2.1 正交实验结果及制备方法的确定
2.1.1 紫杉醇脂质体制备的正交实验结果 如表 3所示。

表 3 紫杉醇纳米脂质体制备正交实验结果
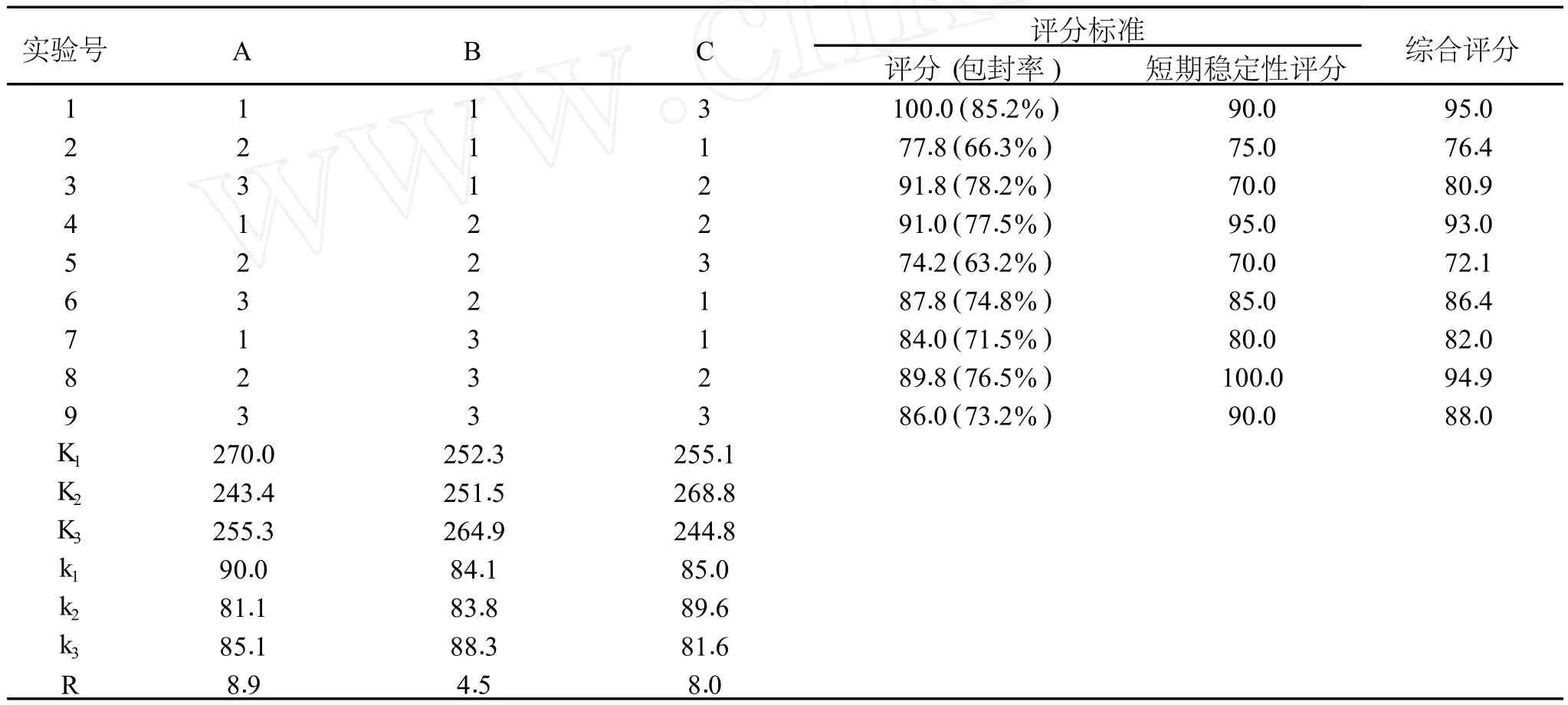
表 4 紫杉醇磁性纳米脂质体制备正交实验结果
由以上正交实验结果,结合实际需要,得到最佳制备紫杉醇脂质体的条件是:卵磷脂∶胆固醇 =6∶1,紫杉醇∶(卵磷脂 +胆固醇)=1∶30,超声时间 40min。
2.1.2 紫杉醇磁性纳米脂质体制备的正交实验结果如表4所示。
由以上正交实验结果得到最佳的制备紫杉醇磁性纳米脂质体的条件是:磁粉∶紫杉醇 =3∶1,吐温-80∶紫杉醇 =4∶1,聚乙二醇-800∶磁粉 =8∶1,考虑到对磁粉量的实际需求,采用磁粉∶紫杉醇 =2∶1。则最终的制备紫杉醇磁性纳米脂质体的最佳配方及相关条件是:卵磷脂∶胆固醇 =6∶1,紫杉醇∶(卵磷脂 +胆固醇)=1∶30,超声时间 40min,磁粉∶紫杉醇 =2∶1,吐温-80∶紫杉醇 =4∶1,聚乙二醇-800∶磁粉 =8∶1。
对于第一步的紫杉醇脂质体的制备,由正交分析得到三个因素中对于紫杉醇脂质体的包封率及其粒径分布贡献的大小依次是:卵磷脂∶胆固醇的比例>紫杉醇∶(卵磷脂 +胆固醇)的比例 >超声时间。表 3中的综合评分是包封率和颗粒分布的评分的平均值,其中颗粒分布感官评定的评分标准是:分散不均匀、分散相对均匀但有较多的聚集存在、分散相对均匀有较少的聚集存在、分散均匀,分别给分 80~100之间(约值)。单因素实验结果分别为:卵磷脂∶胆固醇 =4∶1,紫杉醇∶(卵磷脂 +胆固醇)=1∶30时药物的综合评分最高,超声时间达到 40min时综合评分已经很高,再延长时间基本没有增长。
对于第二步紫杉醇磁性纳米脂质体的制备,正交实验的结果可以看出,三个因素中对紫杉醇磁性纳米脂质体的包封率及其相对稳定性贡献的大小依次是:磁粉的添加量 >聚乙二醇-800的添加量 >吐温-80的添加量。表 4中的综合评分是包封率和短期稳定性的评分的平均值,其中短期稳定性的评分标准是:将制得的紫杉醇磁性纳米脂质体在常温下放置,每天观察三次,持续一个月,根据出现分层时间的长短来评分,出现分层时间越短分数越低,反之越高,并且以出现分层时间最长的为 100分,其他的按相对最好的比例给分(约值)。单因素的实验结果分别为:磁粉∶紫杉醇 =2∶1,吐温-80∶紫杉醇 =6∶1,聚乙二醇-800∶磁粉 =5∶1时药物的综合评分最高。
2.1.3 最佳条件制得的紫杉醇磁性纳米脂质体包封率及其显微观察 按照正交实验确定的实验条件制备紫杉醇磁性纳米脂质体,并依照上述药物包封率和载药量的测定方法测定,得到其最佳包封率约为87.1%,载药率约为 1.8%。显微形态可见外观圆整,粒度分布均匀,平均粒径在 150nm左右,多为球形或类球形具比较清晰的脂膜包裹结构,为小单室脂质体(图 1)。

图1 最佳条件制备的紫杉醇磁性磁性纳米脂质体(30000倍)
2.1.4 体外释药实验结果 实验结果(图 2)表明,紫杉醇原料药溶液的累积释药速率较快,在前 6h几乎呈直线增长速率,6h时药物累积释放百分率为71.1%,48h时可达到 92.7%;而相同时间内紫杉醇磁性纳米脂质体的累积释放量远低于原料药溶液,6h时仅为 20.2%,48h时仅为 36.1%,并且它的释药速率一直比较缓慢,说明紫杉醇磁性纳米脂质体相对原药具有明显的长效缓释的效果。

图2 紫杉醇原药和紫杉醇磁性纳米脂质体的体外释放曲线
2.2 讨论
制备紫杉醇磁性纳米脂质体,所需组分较多,影响的因素也较多,正交实验是选取了其中最重要的几个因素的优化实验,并且由于第一部分是紫杉醇脂质体的合成,第二部分是加进磁粉后的改性,两部分的评价标准也有不同之处,所以采用两步正交实验设计更合理一些。本实验发现超声对粒径大小有比较大的作用,超声时间合适,就能形成分布均匀、大小相近的囊泡,时间过短起不到好的分散效果,但是也不宜过长,因为过度超声还会引起脂质体膜结构破裂、药物渗漏,同时亦会使温度升高,影响含药脂质体的稳定性;聚乙二醇的加入对磁粉的稳定和均匀都能起到比较好的作用,并且它的存在除了对磁性紫杉醇体系的表面改性帮助脂质体分散外,还能增强脂质体在体内靶点部位的聚集,加强脂质体的渗透性和滞留效果;吐温-80的作用主要体现在辅助改性形成微乳体系。
体外释放实验表明,紫杉醇药物溶液在 8h内的累积释药量即达到了约 87.7%,而脂质体的释药速率明显减慢,8h内的累积释药量只有 24.7%,48h时仅为 36.1%,这也表明了透析膜对药物进入释放介质有一定阻碍,但并不是缓释的主要因素[10],而是由于紫杉醇脂溶性强,能够包封于脂质体的磷脂双分子层内,因此减慢了药物进入释放介质的速度,对阻碍药物释放起到了决定性的作用,从而证明了磁性脂质体的缓控释的效果。
磁性药物靶向治疗是近年来发展的一种新的肿瘤治疗方法,它可以降低药物用量,将药物最大量地集中在靶部位,同时借助磁性纳米粒的栓塞和磁场下的磁响应性可以进一步加强治疗作用。但要将其应用于临床,还要进行一系列的深入研究:优化磁靶向性脂质体纳米粒制备工艺,以期达到更好的控释效果,并使其稳定性能更适合临床用药和工业生产;寻找合适的脂质体干燥方法,以延长粒子保存期;配套的磁场产生装置的研制等。
3 结论
薄膜分散法可以较简便地制得紫杉醇磁性纳米脂质体,并且正交设计的优化使所得产品分布相对均匀,粒径大小合适,体外释放效果也不错。其药物包封率最高可达 87.1%,平均粒径为 150±20nm,释药速率明显减慢,8h内的累积释药量只有 24.7%, 48h时仅为 36.1%,基本满足靶向制剂的要求。
[1]张小静,张频 .紫杉醇新剂型的开发及临床研究进展[J].症进展杂志,2007,5(1):66-67.
[2]Maria RosaGasco.Lipid nanoparticles:perspectives and challenges[J].Advanced Drug Delivery Reviews,2007,59:377-378.
[3]辛胜昌,吴新荣,周丽珍 .紫杉醇磁性脂质体纳米粒的制备[J].药学学报,2006,41(10):933-938.
[4]黄红兵,刘韬,徐月红,等 .多西紫杉醇脂质体制备工艺及处方优化研究[J].中国药学杂志,2007,42(24):1872-1874.
[5]Fang Yang,Ling Li,Yixin Li,et al.Super paramagnetic nanoparticle-inclusion microbubbles for ultrasound contrast agents[J].Physics in Medicine and Biology,2008,53:6129 -6141.
[6]Tao Yang,Fu-De Cui,Min-Koo Choi,et al.Enhanced solubility and stability of PEGylated liposomal paclitaxel:In vitro and in vivo evaluation [J].International Journal of Phar maceutics,2007,338:317-326.
[7]Mi-Kyung Leea,Soo-Jeong L imc,Chong-Kook Kim.Preparation,characterization and in vitro cytotoxicity of paclitaxel loaded sterically stabilized solid lipid nanoparticles[J]. Biomaterials,2007,28:2137-2146.
[8]任文霞,李建科 .茶多酚脂质体的制备[J].食品工业科技, 2008(11):186-188.
[9]张洪记,丁盛,顾王文,等 .多西他赛脂质体冻干粉的制备及质量评价[J].中国医药工业杂志,2008,39(2):113-115.
[10]Zhu L,Wangl L,Nik Y,et al.Preparation of stable magne to liposomeswith high encapsula-tion efficiency ofmethotrexate[J]. Chinese Pharmaceutical Journal,2006,41(17):1324-1327.
Preparation and character evaluation of paclitaxelm agnetic nanoparticle liposom es
XI AO Chao1,2,W U Xin-rong1,2,*
(1.College ofLight Industry and Food Sciences,South China University of Technology,Guangzhou 510640,China; 2.Department of Phar macy,General Hospital of GuangzhouMilitary Command,Guangzhou 510010,China)
The ultrasound m em b rane d is integ ra tion m e thod was used to p rep a re the p ac litaxe l m agne tic nanop a rtic le lip osom e.Through the orthogona l des ign,the m e thod was op t im ized w ith encap sula tion ra tio and d is tribution cond itions as the m os t result technique p a ram e te rs.The results ind ica ted tha t the idea l com b ina tion of p rep a ra tion and form ula tion we re as follows:lec ithin∶choles te rol=6∶1,p ac litaxe l∶(lec ithin+choles te rol)=1∶30,the t im e of ultrasound was40m in,m agne tic p owde r∶p ac litaxe l=2∶1,tween-80∶p ac litaxe l=4∶1,p olye thylene-800∶m agne tic p owde r=8∶1.The ave rage encap sula tion effic iency of the op t im ized lip osom e was84.4% ±1.7%,the ave rage p a rtic le s ize was150±20nm.The thin fi lm ultrasonic m e thod and the op t im ized p rep a ra tion can be used to p rep a re p ac litaxe lm agne tic nanop a rtic le lip osom e successfully w ith high encap sula tion effic iency and good g ra in s ize.
p ac litaxe l;m agne tic nanop a rtic le lip osom e;enve lop e ra te;orthogona l des ign
TS201.2
A
1002-0306(2010)03-0162-05
紫杉醇是一种广谱有效的抗肿瘤药物,国际上目前已用于多种恶性肿瘤的一线治疗,并取得了较好的疗效[1]。但是因为紫杉醇水溶性很差,早前多用聚氧乙基代蓖麻油与无水乙醇的混合溶液作为溶酶来溶解它,这样临床用药前就必须预先给予患者大剂量的塞米松及 H2受体拮抗剂,以减轻由混合溶媒所引发的过敏反应及胃肠道反应,给病人带来不必要的痛苦的同时,也给临床用药带来不便。为了改进上述缺点,近年来开始尝试采用包埋的手段进行给药。本实验设计采用脂质体来包封药物[2],并加入四氧化三铁纳米磁粉制成磁性纳米脂质体,这样就可以结合外加磁场作用使药物定向输送到靶向病灶部位,降低药物在正常组织的分布,减轻其对正常组织的毒副作用,提高药物靶向治疗效果。
2009-05-25 *通讯联系人
肖超(1984-),男,硕士研究生,研究方向:糖类物质及其药物的制备与生物利用。
广州市科技计划项目(2005Z3-D2071)。

