中和法制备磷酸根吸附剂的研究
王 翔,周启立
(中海油天津化工研究设计院,天津 300131)
中和法制备磷酸根吸附剂的研究
王 翔,周启立
(中海油天津化工研究设计院,天津 300131)
采用氨水中和三氯化铁法制备无机水合氧化物的磷酸根吸附剂。该实验研究了吸附剂的制备、对磷酸根的吸附过程和再生实验,还讨论了影响吸附容量的各种因素:三氯化铁溶液浓度、熟化时间、中和时间、吸附时间、吸附剂粒径、吸附温度、pH、磷酸盐初始浓度、磷酸盐溶剂量等。实验结果表明:该吸附剂磷酸根的去除率最高达 93%以上,且再生条件简单,再生效果较好。
吸附剂;磷酸根;三氯化铁
磷的污染主要来源于生活污水中各种洗涤用水的大量排放和农业中磷肥的大量使用,以及工业上含磷废水的直接排放。因此,对含磷废水排放前的预处理才是抑制水体富营养化的根本途径。目前含磷废水的处理方法一般是采用化学法和生物法。前者除磷效率高,操作稳定但产生污泥多,运行费用高。后者虽可减少污泥的产生,但操作控制比较复杂,脱磷效率低。鉴于此,许多学者在复合吸附剂方面做了大量研究,例如:活性铝、氧化钛水合物、氧化锆系等,采用吸附法去除磷[1]。笔者采用氨水中和三氯化铁进行造粒制成无机水合氧化物对含磷废水进行处理。实验中对吸附剂的造粒、吸附和再生进行了研究。
1 实验部分
1.1 实验仪器
烘箱、恒温槽、振荡器、搅拌器、过滤装置、抽滤机、分析天平、光电分光光度计、酸度计等。
1.2 实验方法
1.2.1 吸附剂的制备
选用材料:固体三氯化铁颗粒、氨水溶液。
造粒方法:将三氯化铁粉末溶解在纯水中,制备质量浓度为 60 g/L的三氯化铁溶液,将浓氨水溶液稀释 3倍,然后将配制好的氨水溶液倒入三氯化铁溶液中,用玻璃棒搅拌至不再生成氢氧化铁沉淀,熟化 20 min后用纯水洗涤至无氯离子,用抽滤机进行抽滤,放入温度为 70℃左右的烘箱,烘干至恒重,碾成不同粒径的颗粒。
1.2.2 对磷酸根的吸附过程
配制磷酸二氢钾溶液,进行磷酸根吸附实验。首先配制出质量浓度为 50μg/mL的磷酸二氢钾溶液,将吸附剂放入一定量的磷酸二氢钾溶液中,放入振荡器中进行吸附实验,一定时间后取出,抽滤,取一定量滤液放入比色皿中,加钼酸铵、氯化亚锡显色,静止 20 min后进行测试。
1.2.3 再生实验
配制不同浓度的 NaOH溶液,加入失去活性的吸附剂,选择不同的再生时间进行再生,再生后选择最佳吸附条件进行吸附实验,分析不同再生条件对吸附剂的再生效果。
2 结果与讨论[2]
2.1 三氯化铁造粒条件的实验
2.1.1 三氯化铁溶液质量浓度对吸附容量的影响
不同三氯化铁溶液质量浓度 (30,40,50,60,70 g/L)配制的吸附剂 0.1 g,分别加入 10 mL质量浓度为 50μg/mL的磷酸二氢钾,放在振荡器上静态吸附 4 h,将它们取下来过滤得滤液,进行实验分析并计算吸附容量。其结果见图 1。从图 1可以看出:随着三氯化铁溶液浓度的不断增加,吸附容量也在不断增加,但在三氯化铁溶液质量浓度超过50 g/L的时候吸附容量的变化并不是很明显。因此三氯化铁溶液质量浓度为 50 g/L时效果最佳。
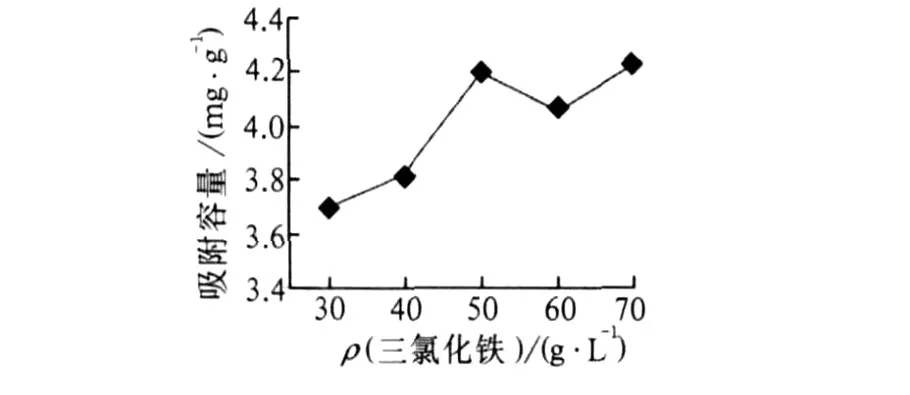
图 1 吸附容量与三氯化铁溶液质量浓度的关系
2.1.2 熟化时间对吸附容量的影响
分别称取熟化时间为 15,25,35,45,55 min的吸附剂 0.1 g放入 5个烧杯中,加入 10 mL,50μg/mL的磷酸二氢钾,进行振荡吸附 4 h,将它们过滤得滤液,进行实验分析。其结果见图 2。从图 2可以看出:随着熟化时间的变化,其吸附容量也在变化,当三氯化铁溶液熟化时间为 35 min时,其吸附效果最好。因此选择熟化时间为 35 min。
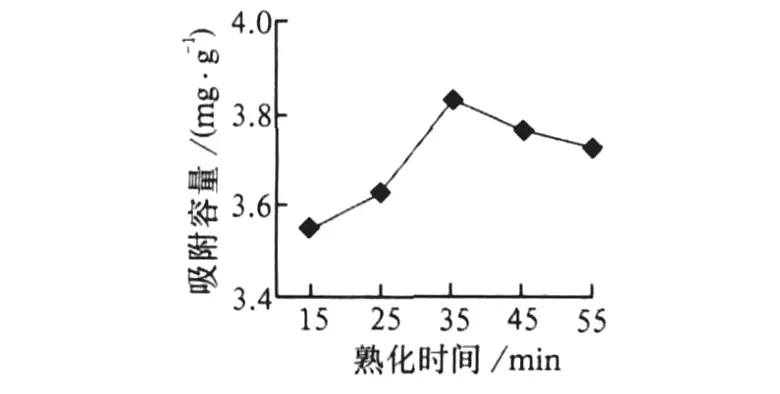
图 2 吸附容量与熟化时间的关系
2.1.3 中和时间对吸附容量的影响
分别称取中和时间为 0.5,1,1.5,2,2.5,3 h的吸附剂 0.1 g放入 5个烧杯中,加入 10 mL,50μg/mL的磷酸二氢钾,进行振荡吸附 4 h,将它们过滤得滤液,进行实验分析。其结果见图 3。从图 3可以看出:随着中和时间的不断延长,吸附效果明显提高,在中和时间为 2.5 h时,吸附容量已经达到饱和。之后,随着中和时间的延长其吸附容量变化不大。因此,选择中和时间为 2.5 h。
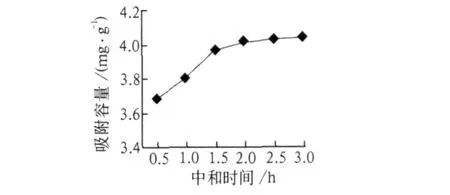
图 3 吸附容量与中和时间的关系
2.2 吸附剂对磷酸根吸附条件的实验[3]
2.2.1 不同吸附时间对吸附容量的影响
分别称取吸附剂 0.1 g放入 6个烧杯中,分别加入 10 mL,50μg/mL的磷酸二氢钾,放入振荡器中振荡,分别吸附 2,4,6,8,10,12 h后将它们取下来过滤得滤液,进行实验分析并计算吸附容量。其结果见图 4。从图 4可以看出:随着吸附时间的不断延长,吸附效果明显提高,当吸附剂吸附10 h时,吸附效果最佳。之后,随着吸附时间的延长其吸附容量变化不大。因此,选择吸附时间为10 h。
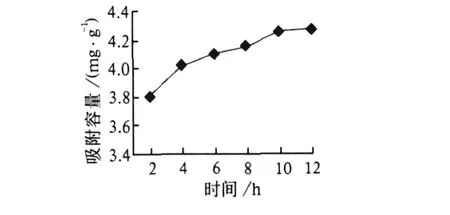
图 4 吸附容量和吸附时间的关系
2.2.2 不同粒径对吸附容量的影响
分别称取不同粒径的吸附剂 0.1 g(平均粒径分别为 180,200,300,550,850μm)放入 5个烧杯中,分别加入 10 mL,100μg/mL的磷酸二氢钾在振荡器上振荡 4 h后,将它们过滤得滤液,进行实验分析并计算吸附容量。其结果见图 5。从图 5可以看出:随着吸附剂粒径的不断变化,吸附容量也在变化。当吸附剂平均粒径为 550μm时,吸附效果最佳。因此,选择吸附剂平均粒径为550μm。
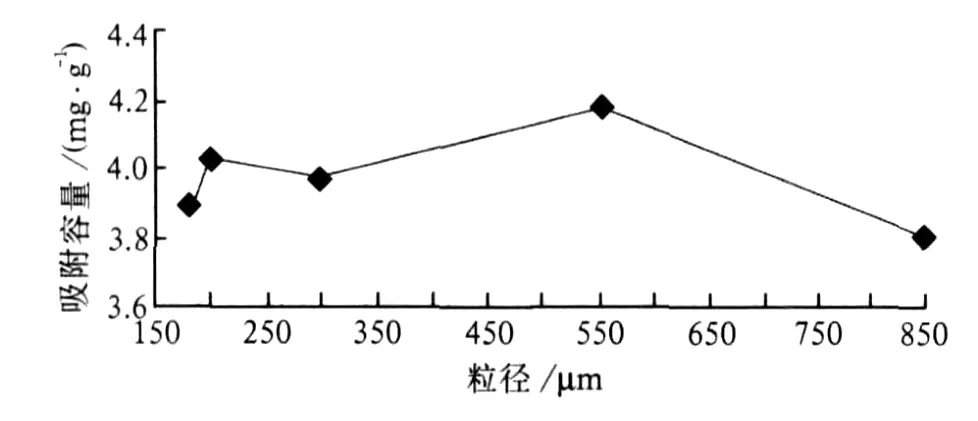
图 5 吸附容量和粒径的关系
2.2.3 不同吸附温度对吸附容量的影响
分别称取吸附剂 0.1 g放入 5个烧杯中,分别加入 10 mL,50μg/mL的磷酸二氢钾,分别在不同温度 (20,30,40,50,60℃)的恒温槽中吸附 4 h,每隔 30 min摇匀溶液。将它们取下来过滤得滤液,进行实验分析并计算吸附容量。其结果见图 6。从图6可以看出:随着吸附温度不断上升,吸附效果明显提高,当吸附剂在 50℃吸附时,吸附效果最佳。因此,选择吸附温度为 50℃。
2.2.4 不同介质 pH对吸附容量的影响
分别称取吸附剂 0.1 g放入 6个烧杯中,分别加入 10 mL,50μg/mL的磷酸二氢钾,放入振荡器中振荡 4 h,其介质的 pH分别是 2.5,4.5,5.5,7.5,9.5,11.5。分别取滤液进行实验分析并计算吸附容量。其结果见图 7。从图 7可以看出:随着 pH的升高吸附容量逐渐降低,当溶液的 pH为 2.5时吸附容量明显高出,之后降低且变化趋势稳定。因此,选择介质 pH为 2.5。
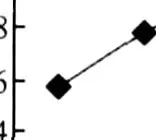
图 6 吸附容量和吸附温度的关系
2.2.5 磷酸盐的初始浓度对吸附容量的影响
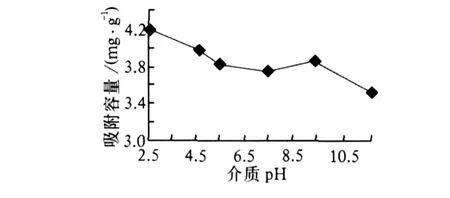
图 7 吸附容量和介质 pH的关系
分别称取吸附剂 0.1 g放入 5个烧杯中,各加入 10 mL不同浓度的磷酸二氢钾 (1.0,1.5,2.0,2.5,3.0 mmol/L),放在振荡器上振荡吸附 4 h。分别取滤液进行实验分析并计算吸附容量。其结果见图 8。从图 8可以看出:随着磷酸盐初始浓度的逐渐增加,吸附容量逐渐降低且变化较明显。因此,选择磷酸盐初始浓度为 1.0 mmol/L。
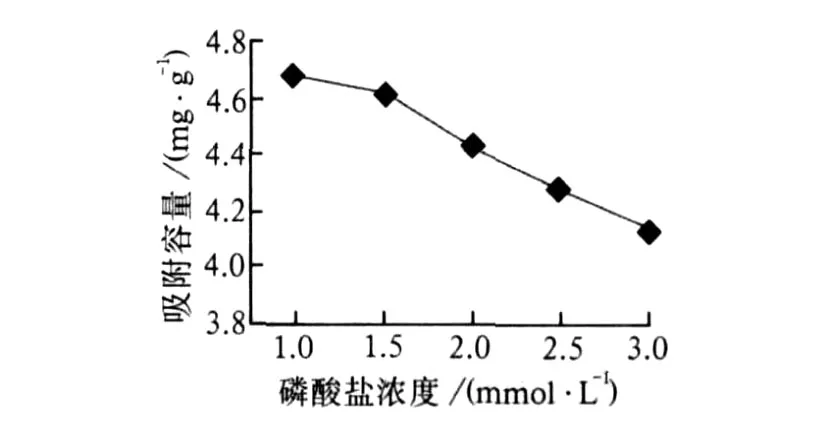
图 8 吸附容量和磷酸盐初始浓度的关系
2.2.6 不同溶剂量对吸附容量的影响
分别称取吸附剂 0.1 g放入 5个烧杯中,各加入 10,15,20,25,30 mL,50μg/mL的磷酸二氢钾,放入振荡器中振荡吸附 4 h。分别取滤液进行实验分析并计算吸附容量。其结果见图 9。从图 9可以看出:随着溶剂量的不断增加,其吸附容量在不断地增加,在溶剂量为 30 mL时吸附效果最佳。因此,选择溶剂量为 30 mL。
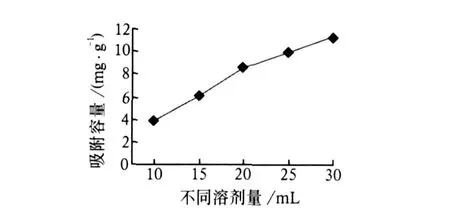
图 9 吸附容量和不同溶剂量的关系
2.3 再生条件实验[4]
2.3.1 再生时间对吸附容量的影响
将失去活性的吸附剂在室温下用 10 mL,1 mol/L的NaOH溶液再生。再生时间分别为 4,8,12,16,20 h。然后在最佳吸附条件下进行吸附实验。进行实验分析,并计算吸附容量。其结果见图10,从图10可以看出:再生时间为4 h效果最好。另外,在实验过程中,当再生时间少于 4 h的情况下,实验数据结果得到的是变化无常的曲线,无规律可言,只有再生时间在 4 h以上才稳定,有规律可循。因此,考察再生时间对吸附性的影响实验都在4 h以上。

图 10 吸附容量和再生时间的关系
2.3.2 NaOH溶液的浓度对吸附容量的影响
将失去活性的吸附剂在室温下用 10 mL浓度分别为 0.5,1.0,1.5,2.0 mol/L的 NaOH溶液再生,再生时间为 4 h。然后在最佳吸附条件下进行吸附实验。进行实验分析,并计算吸附容量。其结果见图 11。从图 11可看出:NaOH的浓度为 0.5 mol/L时,吸附容量最大。
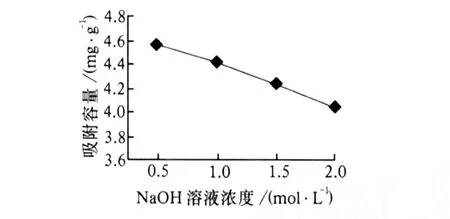
图 11 吸附容量和NaOH浓度的关系
3 结论
1)采用氨水中和三氯化铁造粒制成吸附剂,再吸附溶液中的磷酸根,实验过程分为造粒、吸附、再生 3部分。实验得出如下结论:造粒实验最佳条件:FeCl3溶液质量浓度为 50 g/L、熟化时间为 35 min、中和时间为 2.5 h;吸附实验最佳条件:吸附时间为10 h、吸附剂粒径为 550μm、吸附温度为 50℃、介质 pH为 2.5、磷酸盐初始浓度为 1 mmol/L、磷酸盐溶剂量为 30 mL;再生实验最佳条件:再生时间为4 h、NaOH溶液浓度为 0.5 mol/L。2)氨水中和三氯化铁进行造粒制成无机水合氧化物对含磷废水进行处理的方法可克服常见吸附剂价格高昂、货源较紧以及需要的设备和工艺过程的缺陷,因此具有很大的发展潜力和推广价值。
[1] 天津大学物理化学教研室.物理化学 (下册)[M].3版.北京:高等教育出版社,1992:196-200.
[2] 天津大学化工技术基础实验教研室.化工基础实验技术[M].天津:天津大学出版社,1989:39-59.
[3] 孙家寿,刘新星.天然沸石复合吸附剂处理含磷废水的研究[J].离子交换与吸附,1992,8(1):20-25.
[4] 魏复盛.水和废水监测分析方法[M].3版.北京:中国环境科学出版社,1997:297-321.
Research on preparation of phosphate radical absorbent with neutralization method
Wang Xiang,Zhou Qili
(CNOOC Tianjin Chem ical Research&Design Institute,Tianjin300131,China)
An absorbent forphosphate radicals has been preparedwith ferric trichloride and ammonia,which is an inorganic hydrous oxide.In exper iment,preparation of the absorbent,adsorption process to phosphate radicals,and regeneration were studied and discussed.Influencesof various factors,such as concentration of ferric trichloride solution,aging time,neutralization time,adsorption time,particle size of absorbent,adsorption temperature,pH,initial concentration of phosphate solution,and phosphate solvent dosage on adsorptive capacity,were discussed.Results indicated that the absorbent′smaximum removing rate of phosphate radicals reached above 93%.Furthermore,regeneration condition was simple and regeneration effectwas good.
adsorbent;phosphate radical;ferric trichloride
TQ126.35
A
1006-4990(2010)01-0037-04
2009-07-21
王翔 (1981— ),男,工学学士,助理工程师,从事环境咨询评价工作。
联系方式:seven811@126.com

