对比 思辨 提升
田长明
(苏州市吴中区教育局教研室江苏苏州215128)
对比 思辨 提升
田长明
(苏州市吴中区教育局教研室江苏苏州215128)
学习化学知识的过程中常常用到比较法,通过比较,弄清现象与本质、共性与个性之间的关系,引导学生通过比较、思辨,找到解决问题的不同方法,提高学生分析问题与解决问题的能力。
对比;现象;本质;共性;个性
比较是确定客观事物彼此之间差异点与共同点的思维方法。有比较才有鉴别,通过比较可以认定事物的本质,弄清事物的相互关系。所谓比较就是异中求同或同中求异的思维或实践过程。在学习化学知识的过程中也常常用到比较法。中学化学基础内容中有许多知识既有相同点,又有相异点,如果教师在教学中把这些既有联系又有区别的基础理论、基本概念、物质性质、实验、计算等进行分析归纳、纵横比较,引导学生找出各自特征和彼此间的联系,那么就能帮助学生加深理解,以获得牢固的基础知识。这里,笔者就谈谈在学习化学时常用的比较方法。
一、现象同、本质异
事物的本质是蕴含在事物的现象之中的,往往很难一眼看出,同时,其本质也有层次深浅或主次的区别,不易一下抓准。我们要用理性的睿智之光,对观察到的表象下一番“振叶以寻根,观澜而溯源”的功夫。注意运用比较的方法,对事物的现象进行概括,去伪存真,去粗存精,由此及彼,由表及里,进而上升、飞跃,形成对事物理性化的认识。我们绝不要被表面现象所迷惑,我们应该透过现象看本质。我们通过化学反应过程中的“褪色”这一现象来说明:
现象1:SO2和氯气通入品红溶液,品红溶液褪色。
分析:有机色素的褪色机理主要有2种。一种是色素结构被氧化破坏,具有不可逆性,如氯水、Na2O2、H2O2、O3等使酚酞、品红等溶液褪色;另一种是色素与某物质结合生成无色物质,色素主体结构未受破坏,是暂时的、可恢复的,如SO2使品红溶液褪色。
现象2:SO2通入溴水溶液,溴水溶液褪色。
分析:SO2气体通入某溶液中,溶液发生褪色,其原因也并非只表现出SO2的漂白性。因为SO2的漂白是指SO2和色素发生化合反应,使其褪色。SO2还具有还原性,能使溴水、酸性高锰酸钾等具有强氧化性的有色溶液褪色。
现象3:SO2通入石蕊试液,石蕊试液没有褪色,而是变红。
分析:中学实验室中的品红是一种偶氮化合物(偶氮染料),偶氮化合物颜色变化的一般规律是有机物分子中共轭体系增长而颜色加深。品红是由一种叫做碱性品红的发色母体(无色)加入盐酸后生成的,在品红溶液中存在着如下的平衡:
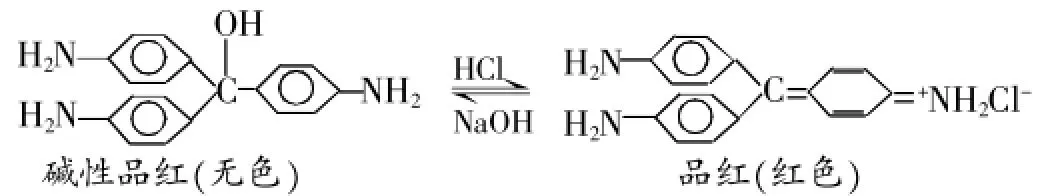
品红溶液中通入SO2后,发生如下反应:
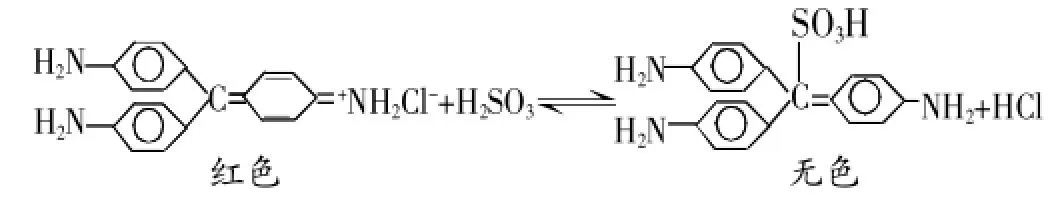
亚硫酸与品红发生了加成反应,破坏了品红结构中单双键交替的结构,所以品红褪色。加热褪色后的溶液,溶液又恢复到原来的颜色,颜色恢复是因为加热亚硫酸不稳定分解,平衡逆向移动,溶液恢复呈红色。[1]
石蕊(Litmus)是一种弱的有机酸,相对分子质量为3300,在酸碱溶液的不同作用下,发生共轭结构的改变而变色,如果用HIn代表石蕊分子,HIn在水中发生电离:HIn⇌H++In-。在酸性溶液中,由于c(H+)增大,根据平衡移动原理可知,平衡将向逆反应方向移动,使c(HIn)增大,因此主要呈现红色(酸色)。如果在碱性溶液中,由于c(OH-)增大,OH-与HIn电离生成的H+结合生成更难电离的水,使石蕊的电离平衡向正反应方向移动,于是c(In-)增大,因此主要呈现蓝色(碱色);在中性溶液里,红色的分子和蓝色的酸根离子共存,因而溶液呈紫色。通入SO2后,不能与石蕊发生加成反应,溶液因呈酸性而显红色。
二、本质同、现象异
在生活中有许多这样的例子:比如说滴水穿石和绳锯木断在表面形式上是不同,但表示了同样的思想,就是只要坚持不懈就会成功;披肝沥胆和开诚布公的形式不同但也是一个意思,为人处事非常忠诚。化学中也有类似的例子,如氢气在氯气中能安静的燃烧,而氢气和氯气混合在光照的条件下就会发生爆炸,本质都是氢气和氯气反应生成氯化氢等,现以铝与酸反应的现象为例:
现象4:pH值相等的稀盐酸和稀硫酸与少量铝粉反应,我们会发现铝粉与稀盐酸反应的速率比与稀硫酸反应的速率快。
分析:这两个反应的本质相同,都是2Al+6H+=2Fe3++ 3H2↑,现象为什么会产生差异?决定铝和酸反应的速率因素有4点:⑴是否生成配离子;⑵酸的浓度;⑶酸根离子的半径大小;⑷反应生成的铝盐是否可溶于水。现在c(H+)的浓度相同,生成的盐都能溶于水,其主要原因是c(Cl-)半径小,能穿透氧化铝薄膜取代氧化铝中的氧原子,从而使之溶解;另一方面Al3+能与Cl-络合生成[AlCl4]-,而硫酸没有配位效应,也没有穿透效应,因此造成了两者反应速率的差异。
三、共性存、个性异
唯物辩证法认为共性和个性是一切事物固有的本性,每一事物既有共性又有个性。共性决定事物的基本性质,个性揭示事物之间的差异性,个性体现并丰富着共性,共性是绝对的,个性是相对的、有条件的。我们研究化学问题也应该遵循这样的规律。
问题1:乙酸与乙醇发生酯化反应时为什么不加碎瓷片防暴沸?
分析:液体中的气泡在沸腾过程中起着汽化核的作用,当液体中缺少气泡时,即使温度达到并超过了沸点,也不会沸腾,形成了过热液体。过热液体是不稳定的,如果过热液体的外部环境温度突然急剧下降或侵入气泡,则会形成剧烈的沸腾,并伴有爆裂声,这种现象叫暴沸。如果加一点杂质后(本质是带入了微小气泡),沸腾滞后被打破,产生沸腾。在液体中加入碎瓷片的原理与加入杂质相同,主要是通过孔隙凝聚水蒸气,使成为气泡浮出,防止暴沸。所以很多有机反应以及蒸馏,都要加入碎瓷片以防暴沸。
乙酸与乙醇发生酯化反应时为什么不加碎瓷片防暴沸?实验表明,若在反应后在各试管中加入相应的试剂,实验开始在混合物中加入了碎瓷片,产生乙烯气体的速率显著加快,严重地影响了乙酸乙酯的生成,导致生产出酯的量明显减少,实验效果欠佳。通过查找有关资料得知:在乙醇、乙酸、浓硫酸的混合物中,硫酸既可与乙醇作用产生碳正离子,也可与乙酸作用使羧基上的碳原子带有更高的正电性,在这些“中间体”物质中,若有碎瓷片(Al2O3)存在,碎瓷片表面上的铝离子可促进由醇生成的盐迅速转化为乙烯,从而抑制了由乙酸与乙醇作用生成乙酸乙酯的过程。所以在做乙酸乙酯的制取实验中不能加入碎瓷片来防止爆沸,只能通过控制酒精灯的火焰大小来防溶液暴沸。[2]
四、问题同、方法异
有这样的一个故事,亚历山大曾经遇到了一个问题,有一个著名的死结,传说如果有人能够解开它,这个人就会成为王。亚历山大也想解开。但是他花了很长时间研究,用了很多办法之后,觉得真的难以解开,头绪太多,完全不知道从何下手。在这之前,很多人都被这个问题难住了,最后都不知道如何解开。最后,亚历山大拔出宝剑,说,既然我不能够用你的方法解开,那么我就用我自己的方法。说完之后,他挥剑斩断了这个死结,问题也迎刃而解。在许多情况下,我们将解决问题类似于亚历山大,并不是问题不能解决,或者问题太难,而是我们需要不同的方法。
问题2:用下图装置分别制取和收集两种干燥的气体。烧杯里NaOH溶液用来吸收尾气,防止污染空气。根据装置图填写下面的表格(填有关的化学式或化学方程式)。
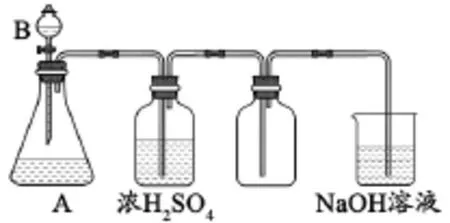
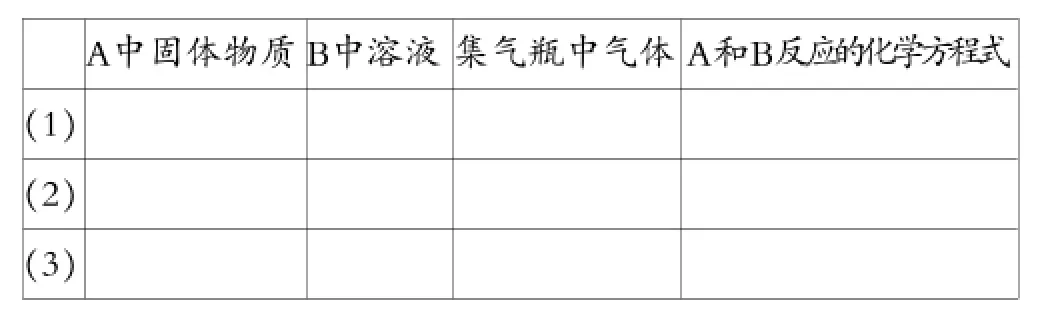
分析:⑴气体发生装置特点:①固体和液体反应;②反应不需要加热。可制备的常见气体有H2、O2、CO2、SO2、Cl2、H2S、NH3、C2H2、NO2等。⑵除杂装置中不能用浓硫酸干燥的常见气体有:H2S、NH3、HBr、HI、PH3等。⑶收集装置可用向上排空气法收集的气体有:O2、CO2、SO2、Cl2、H2S、NO2等。⑷尾气处理可用NaOH溶液吸收的气体的有:SO2、Cl2、H2S、NO2等。因此上述表格可填写如下:
1008-0546(2011)01-0008-02
G632.41
B
10.3969/j.issn.1008-0546.2011.01.004

