茶多酚对明胶的改性作用*
夏雨,焦志华,刘海英
(江南大学食品学院,江苏无锡,214122)
茶多酚对明胶的改性作用*
夏雨,焦志华,刘海英
(江南大学食品学院,江苏无锡,214122)
利用不同浓度茶多酚对明胶进行改性,研究明胶改性前后凝胶强度、流变学性质、分子结构以及蛋白质结晶度的变化,并探讨茶多酚作为明胶改性剂的最佳条件。结果表明,2 g/L的茶多酚对明胶凝胶的强度、熔点和凝固点提高最显著;傅里叶红外转换光谱和X-射线衍射的研究结果表明,2 g/L的茶多酚对明胶的交联作用最强。总之,浓度为2 g/L的茶多酚对明胶具有明显的改性作用。
明胶,茶多酚,改性
明胶具有很多优良的物理和化学性质,如它具有可逆性凝胶、高粘性和成胶性,同时它也是一种非常重要的高分子材料,广泛应用于食品、医学、化妆品、饲料、农业等领域。但是明胶自身也存在一些缺陷,如热稳定性差和机械强度差等,限制了它在某些领域的应用。现代食品化学的研究证明,改性可显著提高蛋白质的功能性质。明胶改性常用的方法有化学方法[1-2]和物理方法[3]。但这些方法多针对于照相明胶等应用材料,通过改性途径提高明胶在干性状态下的物理强度。而且许多应用于明胶改性的交联剂都具有生物毒性,不适合应用于食品和化妆品等领域。
明胶和多酚类物质容易结合,而且少数多酚类物质不像常用醛类改性剂具有生物毒性,使这部分多酚作为明胶的安全改性剂成为可能。目前本实验室已利用天然多酚单宁酸尝试制备了改性明胶[4]。结果表明,明胶凝胶性能和熔点均有所改善。但单宁酸并不安全,对人体存在毒性。
茶叶是人类可以摄入的最主要的三大安全的酚类物质膳食来源之一。茶多酚是茶叶中主要的多酚类物质,无毒,并具有抗氧化等多种生物活性[5-6]。茶多酚来源丰富,重量可以占到茶叶干重的22% ~30%,价格相对低廉。茶多酚中含有大量羟基,可与蛋白质和氨基酸结合,这是利用茶多酚改性鱼明胶生成水凝胶的理论前提。茶多酚易于制取和纯化,其粗提物的纯度即可达到30% ~40%,高纯度茶多酚已经进行工业化生产。由于茶多酚中主要成分含量高而易于精制,如将其作为鱼明胶改性的主研剂,不但成本较低,而且试验结果将比较稳定。
本研究的目的是利用不同浓度的茶多酚改性明胶,研究茶多酚对明胶的主要性质的影响。
1 实验方法和材料
1.1 实验材料
明胶,食品级,中国医药集团上海化学试剂公司;茶多酚,食品级,上海邦成化工有限公司;其他试剂均为分析纯。
1.2 实验仪器
TA-XT2质构测试仪,英国SMS公司;AR1000型流变仪,英国TA公司;D8 Advance型X-射线衍射仪,德国Bruker AXS公司;MlocroMoDuLYo-230型真空冷冻干燥机,Thermo Savant公司;傅立叶变换红外光谱仪NEXUS470,美国NICOLET公司;s-4800扫描电镜测试仪,日本日立有限公司。
1.3 实验方法
1.3.1 样品的制备
分别配制明胶与茶多酚的混合溶液,明胶的最终浓度为66.7 g/L,茶多酚的最终浓度分别为0.5 g/L、1 g/L、2 g/L、3 g/L、4 g/L,接着向各混合溶液样品中加入NaN3,使NaN3在各溶液中的最终浓度均为0.1 g/L。搅拌条件下,于50℃通氧气反应1 h,分别分装于冻力瓶中,于25℃恒温交联24 h,之后放到7℃环境保温16~18 h。
1.3.2 凝胶强度的测定
凝胶强度测定采用 Bloom法[7],采用质构仪测定。测定条件为:柱塞P0.5;下压 4 mm,压力5 g,压入后速度1 mm/s。测定步骤:将样品在质构仪圆台上放平,柱塞对准胶面中心后下压,记录最大力。
1.3.3 流变性的测定
按1.3.1方法制备改性明胶溶液,50℃通氧气反应1 h后,分别倒入平底培养皿,密封,冷却后成为厚度约为1 mm明胶凝胶薄片。明胶凝胶薄片于25℃恒温交联24 h,之后放到7℃环境保温16~18 h。
实验条件[8]:平板60 mm,磨具锥角为 2,夹缝为0.15 mm;扫描频率为1 Hz,蠕变应力为3.0 Pa。测定方式为温度扫描。将明胶样品于4℃保温,于流变仪上平衡至5℃,然后升温至40℃,升温速率为1℃/min;在40℃保温5 min后,降温至5℃,降温速率为1℃/min。在升温和降温过程中测量相角(δ)。
1.3.4 红外性质测定
样品的制备:将不同浓度茶多酚改性后的明胶真空冷冻干燥,之后研碎成粉末。红外测定的条件:采用KBr压片法制样;扫描范围为4 000~400 cm-1。
1.3.5 X-射线衍射分析
样品的制备:不同浓度茶多酚改性后的明胶真空冷冻干燥,之后研碎成粉末。测定条件:采用铜靶Cu Kα(λ=0.154 06 nm),功率为1 600 W(40 kV ×40 mA),采用NaI晶体闪烁计数器(Scintillation Counter)测量X-射线的强度,扫描范围为3°~90°,扫描速度4°/min,步长0.02°。发散狭缝DS、防散射狭缝SS和接受狭缝RS设置分别为1 mm、1 mm和0.1 mm。
1.3.6 表面状态观察
样品的制备:先按照1.3.3中的方法将空白明胶及用不同浓度茶多酚改性后明胶凝胶自然干燥成薄膜备用。测定方法:将明胶薄膜喷金处理后放在样品台上观察并拍照。
2 结果与讨论
2.1 改性后明胶的凝胶强度变化
不同浓度茶多酚与明胶混合后通氧气反应1 h,分别制备成浓度为0.5、1、2、3、4 g/L 的茶多酚改性明胶。通过磁力搅拌器充分混合均匀后,将其分别分装至冻力瓶中,各瓶颜色不同,深浅变化见图1,不同浓度茶多酚改性明胶的凝冻强度比较见图2。
空白明胶的颜色为淡黄色,与茶多酚反应后的明胶的颜色变为红褐色,且随着茶多酚浓度的增加,颜色逐渐加深。当茶多酚浓度继续增加时,过量的茶多酚与明胶呈白色沉淀析出。由图2可知,当茶多酚浓度继续增加时,凝胶强度也随着茶多酚浓度继续增加,当茶多酚浓度达到2 g/L后开始降低。其中主要原因为茶多酚具有多个酚羟基,而明胶肽链富含氨基和羧基。则酚羟基与明胶肽链间可形成氢键,拉近了明胶肽链间距离,增加了明胶肽链间作用力,其结果则是明胶凝胶的网状结构增强,使明胶的凝胶强度增大。
2.2 改性后明胶的相变温度变化
在动态流变特性的测量过程中,一般以tan(δ)=1作为胶凝和融化的转折点,其对应的温度即为胶凝温度和熔化温度。在动态黏弹性分析中,分别可以得出熔化温度和胶凝温度,如表1所示。

图1 不同浓度茶多酚与明胶反应后颜色变化

图2 不同浓度茶多酚改性明胶的凝冻强度比较

表1 不同浓度茶多酚改性明胶后熔化和胶凝温度变化
由于明胶的成熟时间延长和水分散失,故空白明胶的浓度升高,其熔化温度较高。相比较之下,添加茶多酚的明胶样品的熔化温度和凝胶温度均有所增加。其中,用2 g/L茶多酚改性的明胶,其熔化温度和凝胶温度上升幅度最大,上升幅度分别达到5.1℃和4.1℃。
明胶形成的是一种热可逆凝胶,通常稳定热可逆凝胶网络结构的主要作用力是氢键,氢键的形成和破坏依赖于温度。茶多酚增强了明胶肽链间的氢键作用力,使其结构更加稳定,从而使其熔化温度升高。同样,添加茶多酚明胶的凝胶形成会更加容易,即其凝胶温度也会升高。
2.3 改性后明胶的红外特征变化
蛋白质和多肽在红外区域表现为9个振动模式或基团频率,其中最常用于二级结构分析的是酰胺I带,位于1 600~1 700 cm-1范围,酰胺I带的振动频率取决于C=O和N—H之间的氢键性质,即特征振动频率反映了多肽或蛋白质的特定二级结构(α-螺旋、β-折叠、无规则卷曲等)[9-10]。
对空白明胶以及经过 0.5、1、2、3、4 g/L 茶多酚改性的明胶进行了红外光谱测定,结果见图3。图3中所标A为酰胺A带出峰位置,I为酰胺I带出峰位置,II为酰胺II带出峰位置,III为酰胺III带出峰位置。
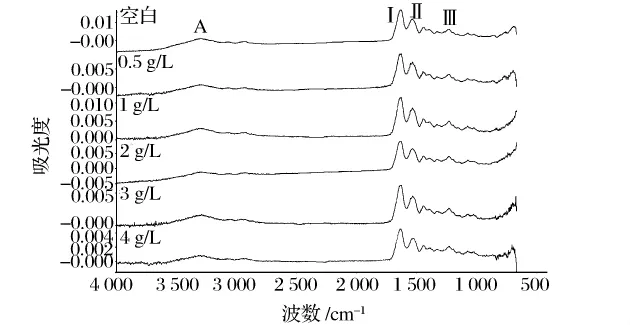
图3 各种明胶样品的红外光谱结果
不同明胶的酰胺A带、酰胺I带、酰胺II带、酰胺III带的出峰位置见表2。

表2 不同明胶红外光谱出峰处
酰胺A带峰出现在3 300 cm-1左右,为O—H和N—H的伸缩振动吸收峰,它反映氢键的存在以及变化情况。当氢键形成时,谱带将向低波数移动,通常氢键越强,降低越明显[11]。表2中可见样品在3 200~3 400 cm-1处的吸收峰分别为:3 308.72 cm-1、3 299.14 cm-1、3 292.76 cm-1、3 288.32 cm-1、3 295.91 cm-1和 3 304.00 cm-1,可见明胶在经过0.5 g/L茶多酚改性后谱带向低波数移动9.58 cm-1,经1 g/L茶多酚改性后谱带向低波数移动15.96 cm-1;经2 g/L茶多酚改性后谱带向低波数移动20.4 cm-1,经3 g/L茶多酚改性后谱带向低波数移动12.81 cm-1,经4 g/L茶多酚改性后谱带向低波数移动4.72 cm-1。由此可以说明随着茶多酚浓度的增加,明胶改性后形成氢键呈现先增多后减少的趋势,且2 g/L茶多酚改性使分子形成氢键最强,使分子链接触更为紧密,由此也证明了用浓度为2 g/L的茶多酚对明胶改性后的凝胶强度最好。酰胺I带、酰胺II带、酰胺III带分别表示C=O的伸缩振动、N—H的弯曲振动和C—H的伸缩振动,表2中各个浓度下茶多酚改性的明胶的酰胺I带、酰胺II带、酰胺III带出峰处相差不大。
2.4 改性后明胶的X射线衍射特征变化
图4~图9为空白明胶及不同浓度茶多酚改性明胶的X射线衍射图谱。

图4 空白明胶X-射线光谱

图5 0.5 g/L茶多酚改性明胶X-射线光谱

表3 多种明胶样品X-射线光谱出峰处及d值

图6 1 g/L茶多酚改性明胶X-射线光谱
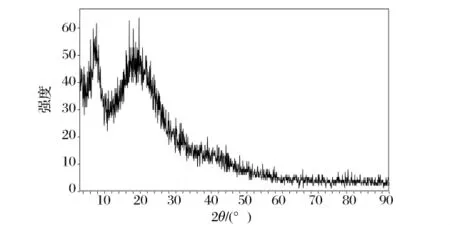
图7 2 g/L茶多酚改性明胶X-射线光谱

图8 3 g/L茶多酚改性明胶X-射线光谱

图9 4 g/L茶多酚改性明胶X-射线光谱
将上述X射线衍射图谱中出现的2个峰分别定义为峰A和峰B。峰B与漫散射有关,峰A代表肽链间的距离,用d值表示,d值越小代表蛋白质结晶面距离越小,明胶与茶多酚之间的交联作用越强。
表3为空白明胶及用不同浓度茶多酚交联后的明胶的光谱中的出峰处及d值,由表3可以看出,不同浓度茶多酚与明胶交联后蛋白质的结晶面距离均变小,且2 g/L茶多酚改性明胶的峰A的d值最小,因此2 g/L茶多酚与明胶交联后蛋白质结晶面的距离最短,即2 g/L茶多酚对明胶的交联作用最强。
3 结论
茶多酚分子具有多个酚羟基,因此1个茶多酚分子可以结合多个明胶肽链,从而拉近明胶肽链间距离,增强了明胶分子间作用力。对于改性后明胶凝胶而言,茶多酚增强了凝胶内的网状结构,从而增强的明胶凝胶的机械性能。但与此同时,茶多酚交联加深了明胶的颜色。
[1] .Kolodziejska I,Skierka E,Sadowska M,et al.Effect of extracting time and temperature on yield of gelatin from different fish offal[J].Food Chemistry,2008,107(2):700 -706.
[2] Gliko-Kabir I,Yagen B,Penhasi A,et al.Low swelling,crosslinked guar and its potential use as colon-specific drug carrier[J].Pharmaceutical Research,1998,15:1 019 -1 025.
[3] Yamashita M,Arai S,Imaizumi Y,et al.A one-step proeess for incorporation of L-methionine into soyprotein:by treatment with papain[J].Journal of Agricultural and Food Chemistry,1997,27(1):52-55.
[4] 陈颖佳,李文丽,刘海英.单宁改性的明胶性质变化研究[J].食品与发酵工业,2009,35(10):40-43.
[5] Cao N,Fu Y H,He J H.Mechanical properties of gelatin films cross-linked,respectively,by ferulic acid and tannin acid[J].Food Hydrocolloids,2007,21(4):575 -584.
[6] Wu Y,Chen Z X,Li X X,et al.Effect of tea polyphenols on the retrogradation of rice starch[J].Food Research International,2009,42(2):221 -225.
[7] 沃德A G,考茨A.明胶的科学与工艺学[M].北京:轻工业出版社,1982:537-547.
[8] Montero P,Fernández-Diaza M D,Gómez-Guilléna M C.Charaterization of gelatin gels induced by high pressure[J].Food Hydrocolloids,2002,16(3):197 -205.
[9] 刑木刚,梁宏.RT-IR在蛋白质二级结构研究中的应用发展[J].广西师范大学学报,1997,15(3):45-49.
[10] Krimm S,Bandekar J.Vibrational analysis of peptides,polypeptides and proteins.V.Normal vibrations of βturns[J].Bioplymers,1980,19(1):1 -29.
[11] 谢晶曦.红外光谱在有机化学和药物化学中的应用[M].北京:科学出版社,1987:299-302.
Study on the Properties of Gelatin Modified by Tea Polyphenols
Xia Yu,Jiao Zhi-hua,Liu Hai-ying
(School of Food Science and Technology,Jiangnan University,Wuxi 214122,China)
Gelatin was modified in this work by different concentrations of tea polyphenols.The gel strength,rheological properties,molecular structures and the protein crystallinity in the gelatin before and after modification were comparatively studied,and the optimum tea polyphenols concentration for gelatin modification was discussed.Results showed that 2 g/L of the tea polyphenols mostly benefited to the improvement of gel strength,melting point and freezing point.Results of the fourier transform infrared spectroscopy and the X-ray diffraction showed that 2 g/L of the tea polyphenols mostly improved the cross-linking of gelatin.All the results showed that 2 g/L of the tea polyphenols can improve the property of gelatin significantly.
gelatin,tea polyphenols,modification
博士,副教授(刘海英为通讯作者)。
* 江苏省基础研究计划(自然科学基金)(BK2009749、BK2008103);中央高校基本科研业务费专项资金(JUSRP21010)
2011-07-02,改回日期:2011-07-24

