右酮洛芬氨丁三醇注射液的人体药动学研究
宋颖,贾艳艳,丁莉坤,鹿成韬,冯智军,宋薇,文爱东(第四军医大学第一附属医院药剂科,西安710032)
右酮洛芬氨丁三醇(Dexketoprofen trometamol)是非甾体抗炎药酮洛芬右旋对映体的水溶性氨丁三醇盐。右酮洛芬氨丁三醇注射液在许多欧洲国家已广泛应用,其主要适应证为严重急性疼痛的对症治疗,包括术后疼痛和炎症性疼痛,如术后疼痛、骨骼-肌肉疼痛和肾绞痛。产品可单独用药,或者在控制术后疼痛必要的情况下,在阿片类治疗的基础上作为辅助用药。虽然国内、外已有关于右酮洛芬氨丁三醇人体药动学的研究报道,但是关于注射剂在中国人体内的药动学研究较少[1~3]。本研究用液-质联用(LC-MS)法分别测定单剂量和多剂量给药后健康受试者血浆中的右酮洛芬浓度,评价右酮洛芬氨丁三醇注射液在中国人群中的药动学特性,为在中国人群中开展随机、对照临床研究的给药方案提供依据。
1 材料
1.1 仪器
6410B型三级四极杆液质联用仪,配有自动进样器、液相色谱仪、柱温箱、电喷雾电离离子源(ESI)及Agilent MassHunterWorkstation Software数据处理系统(美国Agilent公司);AB135-S十万分之一天平(瑞士梅特勒公司);XW 80A涡旋混合器(上海沪西分析仪器厂);TGL16M型冷冻离心机(长沙英泰仪器有限公司)。
1.2 试药
右酮洛芬氨丁三醇注射液(德国Berlin-Chemie AG(Menarini Group),规格:50 mg∶2 mL,批号:02056);右酮洛芬氨丁三醇对照品(德国Berlin-Chemie AG(Menarini Group),含量:100.0%);内标:非布司他对照品(中国食品药品检定研究院,批号:100650-200301);甲醇为色谱纯,醋酸铵、乙酸为分析纯,试验用水为去离子水。
2 方法与结果
2.1 色谱及质谱条件
色谱条件:色谱柱:Diamonsil C18(2)(150 mm×2.1 mm,5 μm);流动相:甲醇-水(水中含5 mmol·L-1醋酸铵、0.05%乙酸,68∶32);流速:0.35 mL·min-1;柱温:35 ℃;进样量:8 μL。
质谱条件:采用电喷雾离子源(ESI),负离子选择性离子检测(SIM)模式;右酮洛芬:[M-H]-离子,m/z253.1;内标(非布司他):[M-H]-离子,m/z315.1;离子源参数:干燥气温度:350 ℃;干燥气流速:12 L·min-1;喷雾气压力:40 psi;毛细管电压:4 000 V。
2.2 标准溶液的制备
准确称取右酮洛芬氨丁三醇对照品,用甲醇配制成浓度为206.6、103.3、51.65、20.66、2.066、0.516 5 μg·mL-1的右酮洛芬标准溶液。另准确称取非布司他对照品,用甲醇溶解配成浓度为20.12 μg·mL-1的内标溶液。
2.3 血浆样品的处理
于1.5 mL离心管中精密加入血浆样品200 μL、内标(20.12 μg·mL-1非布司他)溶液25 μL,旋涡混匀。加入甲醇600 μL,涡旋混匀5 min,静置5 min,于15 600 r·min-1离心10 min。吸取上清液转移至自动进样器样品瓶,进行LC-MS分析。
2.4 方法学验证
2.4.1 标准曲线的制备:在空白血浆中分别加入右酮洛芬氨丁三醇标准溶液,配制成相当于血药浓度为0.010 33、0.051 65、0.206 6、0.826 4、2.066、5.165、10.33、20.66 μg·mL-1的含药血浆,按“2.3”项下方法操作,并进行LC-MS分析,记录色谱。计算右酮洛芬峰面积(As)和内标峰面积(Ai)的比值f(f=As/Ai)。以峰面积比值(f)对血药浓度(x)作权重回归计算,结果右酮洛芬的线性方程为f=-0.000 548 1x×0.206 2(r=0.997 8,权重系数w=1/c2)。结果表明,右酮洛芬血药浓度在0.010 33~20.66 μg·mL-1范围内线性关系良好,定量下限为0.010 33 μg·mL-1。
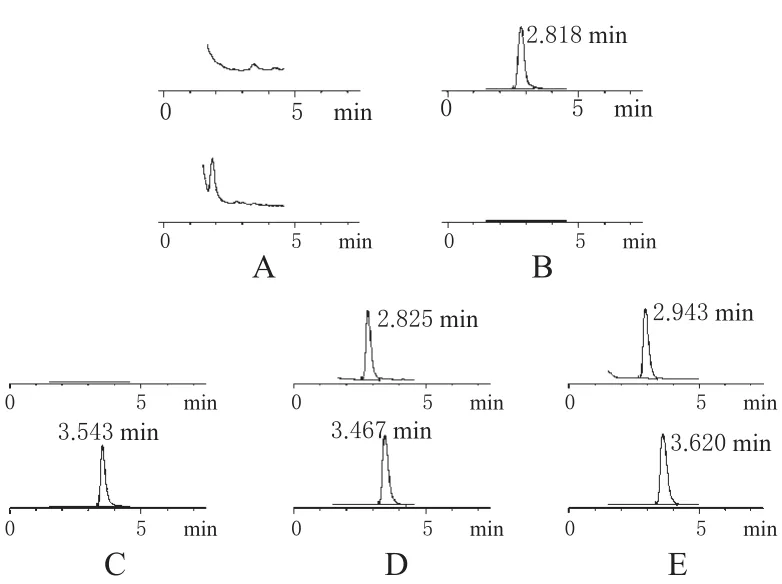
图1 LC-MS图谱A.空白血浆;B.右酮洛芬对照品;C.内标;D.空白血浆+右酮洛芬对照品+内标;E.0.17 h血浆样品Fig 1 LC-MS ChromatogramsA.blank plasma;B.dexketoprofen control;C.IS;D.blank plasma+dexketoprofen control+IS;E.plasma sample at 0.17 h
2.4.2 专属性:在选定的液-质条件下,各组分不受血浆中内源性物质的干扰。右酮洛芬的出峰时间在2.9 min左右,内标的出峰时间在3.6 min左右,LC-MS图谱见图1。
2.4.3 精密度和准确度:分别配制右酮洛芬低、中、高(0.025 83、1.033、16.53 g·mL-1)3种浓度的标准含药血浆,每个浓度平行配制5份,按“2.3”项下方法操作。依上述方法,连续3 d测定,每日随行一条标准曲线,记录色谱图。计算右酮洛芬面积As和内标峰面积Ai的比值f,代入随行标准曲线方程求得样品的实测浓度,考察日内和日间精密度。采用第1天的数据,将f代入随行标准曲线方程,计算所得浓度和加入浓度的比值即为准确度(相对回收率),结果详见表1。
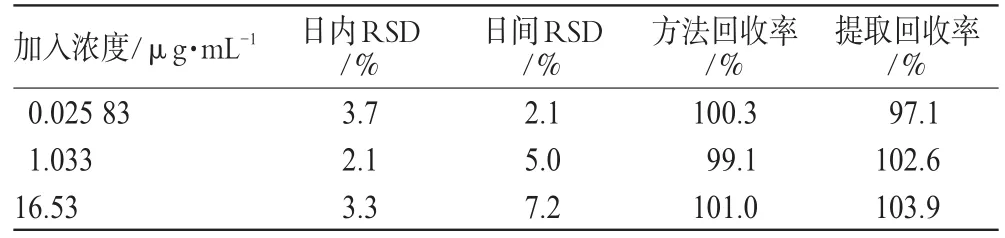
表1 精密度及回收率试验结果(n=5)Tab 1Results of precision and recovery tests(n=5)
2.4.4 提取回收率:分别取低、中、高3种浓度的右酮洛芬血浆样本各3份,以经过提取所得的色谱峰面积与标准溶液未经提取直接进样所得的色谱峰面积之比,来考察样品的提取回收率,结果详见表1。
2.4.5 样品稳定性:考察了右酮洛芬3种浓度(0.025 83、1.033、16.53 μg·mL-1)样品分别在即刻、4.5 h后、反复冻融3次和-40℃放置49 d,进样分析的稳定性、结果所有样品的RSD均<15%,即表明右酮洛芬血浆样品稳定性良好。
2.5 试验对象
12名健康受试者参加本项研究,男、女各半,年龄33~40岁,体重50~64.5 kg,无烟酒嗜好。试验前经病史询问、体格检查和实验室检查未发现异常。受试者无药物过敏史和药物依赖史,无精神病史以及其他慢性病史,2周内未服任何药物。受试期间禁烟、酒、茶及含咖啡因的饮料,统一清淡饮食。受试者试验前均签署知情同意书。本试验经本院医学伦理委员会审批通过。
2.6 给药和取样
12名健康受试者。第1天进行50 mg单剂量静脉滴注的人体药动学试验;经过7 d清洗期,第8~10天进行50 mg多剂量静脉滴注的人体药动学试验。分别于第8、9、10天给药前采集稳态谷浓度血样,第1、10天给药前抽取空白血样约4 mL,在静脉滴注开始后10、20、30、35、40、50 min及1、1.5、2、3、4、6、8、10、12 h时分别采集静脉血约4 mL。分离血浆,置-80℃冰箱保存待测。
2.7 数据处理
采用WinNonLin 6.2软件,根据本试验所测得的血药浓度绘制药-时曲线,选择非房室模型,计算各个体的药动学参数。
12名受试者静脉滴注右酮洛芬氨丁三醇注射液后,主要药动学参数见表2(注:AUC单剂量中代表AUC0~∞,多剂量中代表AUCss),其平均药-时曲线见图2。
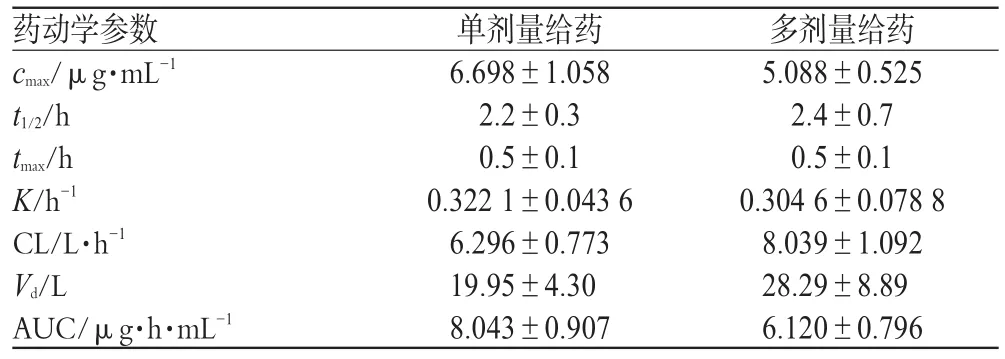
表2 12名健康受试者分别单剂量、多剂量给药后右酮洛芬的药动学参数Tab 2 Main pharmacokinetic parameters of dexketoprofen in 12 healthy volunteers after single and multiple doses administration
3 讨论
本试验建立的LC-MS法可检测血浆样品中右酮洛芬的浓度。本方法快速、灵敏、专属性强,可以满足低浓度药物测定及药动学研究的需要。
12名中国健康受试者静脉滴注右酮洛芬氨丁三醇注射液后,主要药动学参数在多剂量给药后4次可以达到稳态,稳态血药浓度波动度(DF)为6.5±0.8。与单剂量给药相比,多剂量给药后血浆中右酮洛芬的t1/2、tmax均无显著性差异。CL和Vd有显著性差异,表明多剂量给药后CL和Vd增加,致多剂量给药后cmax、AUC均比单剂量给药有所降低,此结论与国外报道相一致[2]。蓄积常数计算[4,5]结果表明在多剂量给药过程中,右酮洛芬在健康受试者体内无明显蓄积现象。
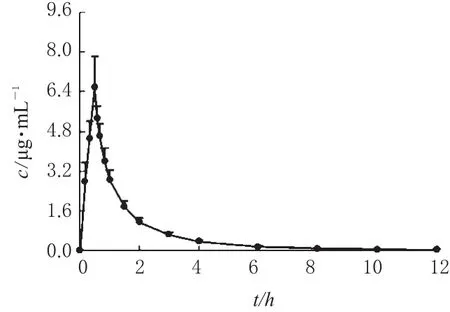
图2 12名受试者单剂量给药后血浆中右酮洛芬的平均药-时曲线Fig 2 Mean plasma concentration-time curves of dexketoprofen in 12 healthy volunteers after a single dose administration
[1]Valles J,Artigas R,Crea A,et al.Clinical pharmacokinetics of parenteral dexketoprofen trometamol in healthy subjects[J].Methods Find Exp Clin Pharmacol,2006,28(SupplA):7.
[2]黄 英,余 勤,梁茂植,等.高效液相色谱法测定人血浆中酮洛芬浓度[J].药物分析杂志,2000,20(1):99.
[3]Kaye CM,Sankey MG,Holt JE,et al.A high-pressure liquid chromatographic method for the assay of ketoprofen in plasma and urine,and its application to determining the urinary excretion of free and conjugated ketoprofen following oral adminastration of orudis to man[J].Br J Clin Pharmac,1981,11(4):395.
[4]Meineke I,Gleiter HG.Assessment of drug accumulation in the evaluation of pharmacokinetic data[J].The Journal of Clinical Pharmacology,1998,38(8):680.
[5]Colburn WA.Estimating the accumulation of drugs[J].Journal of Pharmaceutical Sciences,1983,72(7):833.

