丝胶对碳酸钙晶体生长的调控作用研究
丁 少,王海龙,须苏菊,孔祥东
(浙江理工大学 a. 材料与纺织学院;b. 生命科学学院,杭州 310018)
丝胶对碳酸钙晶体生长的调控作用研究
丁 少a,王海龙b,须苏菊b,孔祥东b
(浙江理工大学 a. 材料与纺织学院;b. 生命科学学院,杭州 310018)
以水溶性丝胶为有机模板调控碳酸钙晶体生长,探讨了丝胶质量浓度差异对晶体生长的影响作用。采用场发射扫描电镜(FESEM)、X射线衍射(XRD)、红外光谱(FTIR)对所制备的样品进行表征。结果表明:通过控制丝胶质量浓度可调控碳酸钙的晶体生长,引起晶体形貌与尺寸的显著变化,并抑制碳酸钙特定晶面的生长。制备了刺球状碳酸钙和片层结构组装而成的类正方体碳酸钙,并对其形成机理进行了初步探讨,结果表明丝胶与无机晶体之间存在复杂的相互作用,丝胶对碳酸钙晶体的生长具有调制作用。
碳酸钙;丝胶;生物矿化;调控
碳酸钙是一种重要的无机非金属材料,主要存在于天然矿藏及贝壳、珊瑚、珍珠等生物矿物中,在橡胶、塑料、造纸、涂料、食品等领域具有重要应用。近年来,由于碳酸钙具有优异的生物学特性,在药物缓释载体、生物传感器、骨修复材料等新兴领域逐渐得到利用。碳酸钙纳米材料及特殊结构、形貌具有特殊应用。碳酸钙含有3种无水晶型,分别是球霰石、文石和方解石,其稳定性依次递增[1]。球霰石、文石、方解石分别属于六方晶系、正交晶系、三方晶系,分别具有六角形结构、正交结构、菱形结构,通常分别组装成球形颗粒、针状颗粒、立方体颗粒[2]。目前,多种有机物质被用做调控碳酸钙等生物矿物合成的有机模板。这些有机物质按照相对分子质量和来源主要分为三类:人工合成高聚物,如聚氨基酸类[3]、PAA[4]等;低分子有机物,如 EDTA[5]、醇类[6]、氨基酸[7]等;生物大分子,如壳聚糖[8]、磷脂[9]、蛋白质[10-14]等。在自然界中,蛋白质是一种重要的生物矿化模板分子,因此人们对蛋白质调控碳酸钙合成进行了广泛的研究。
丝胶是一种可溶性蛋白,处于蚕丝的外层,对丝素起到保护作用[12]。丝胶由于具有很好的保水性、生物相容性和降解性等,因此在工业上被广泛应用于化妆品、生物材料领域[15-18]。
本研究利用丝胶作为有机模板来合成碳酸钙复合材料,分析丝胶质量浓度对碳酸钙晶型和形貌的影响,并探讨丝胶对碳酸钙晶体生长的影响作用。
1 材料和方法
1.1 试剂及仪器
试剂:无水氯化钙、碳酸钠、氢氧化钠、无水乙醇等(分析纯,杭州米克化学试剂有限公司),丝胶粉(相对分子质量为10~20 kDa,湖州奥特丝生物化工有限公司)。
仪器:恒温加热磁力搅拌器(上海梅颖浦仪器仪表制造有限公司),循环水式多用真空泵(河南省太康科教器材厂),恒流泵(上海嘉鹏科技有限公司),电热恒温鼓风干燥箱(上海一恒科技有限公司)。
1.2 碳酸钙合成
在20 ℃时,将10 mL的0.2 mol/L氯化钙溶液加入80 mL丝胶溶液(丝胶溶液质量浓度分别为0 g/L,0.5、1、1.5 g/L)中,然后轻微搅拌30 min,得到丝胶与氯化钙的混合溶液;氢氧化钠调节pH值至8后,用恒流泵将10 mL的0.2 mol/L碳酸钠溶液滴入上述混合溶液中,当碳酸钠全部滴加完成时,即反应时间为5 min,经过抽滤得到固体产物,用去离子水充分洗涤后,将固体产物在37 ℃下用烘箱干燥24 h。
1.3 碳酸钙表征
1.3.1 X射线衍射(XRD)测定
研究样品的晶型,使用X 射线粉末衍射仪(ARL XTRA, Thermo Electron)对粉末样品进行分析,采用Cu Kα射线(λ=1.540 56 Å),角度范围为2θ=20°~70°,扫描速度为4(°)/min。
1.3.2 红外吸收光谱(FTIR)分析
样品与溴化钾混合的质量比约为1∶100,用傅立叶变换红外光谱仪(Nicolet 5700, Thermo Electron)对样品的化学基团进行分析,分辨率为4 cm-1,扫描范围为4 000 cm-1~400 cm-1。
1.3.3 扫描电子显微镜(SEM)观察
观察样品的形态和微观结构,ULTRATM55场发射扫描电子显微镜(FESEM)的加速电压为2 kV。
2 结果与讨论
2.1 不同质量浓度丝胶溶液中合成的碳酸钙晶体的扫描电镜图
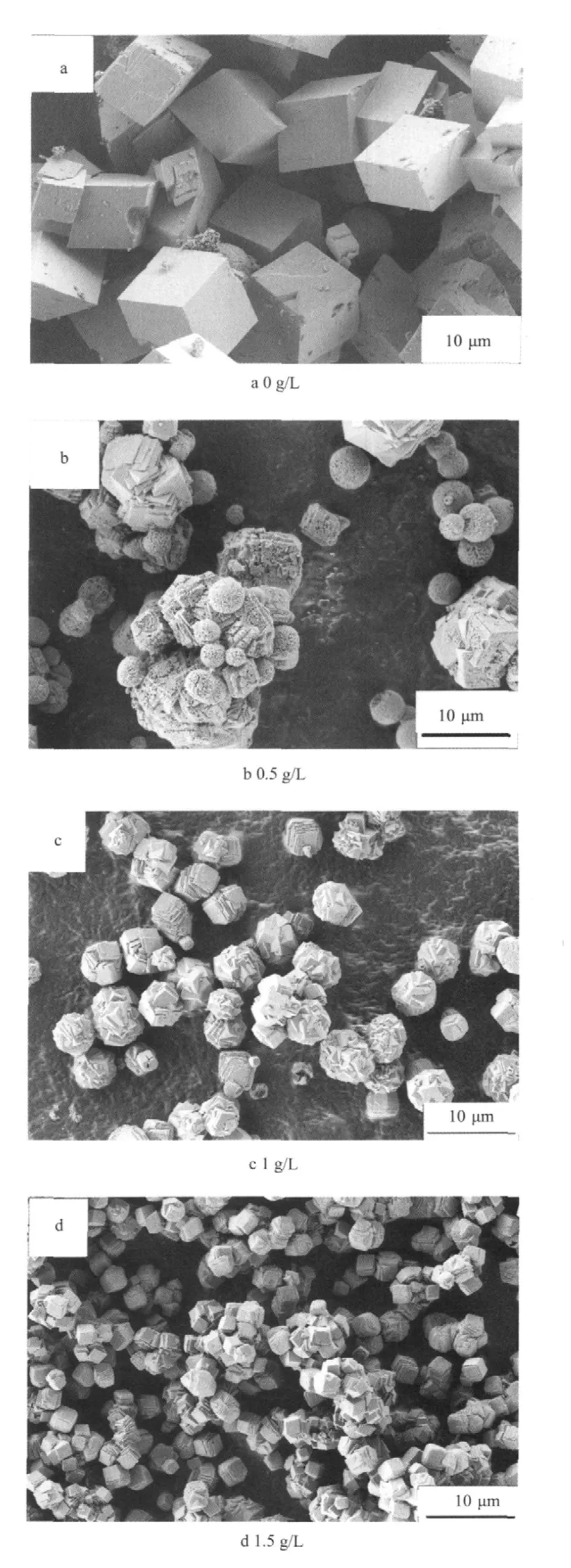
图1 不同质量浓度丝胶溶液中合成的碳酸钙FESEM图Fig.1 SEM images of the Calcium carbonate obtained at different sericin concentration
图1为在20 ℃、不同质量浓度丝胶溶液中制备得到中碳酸钙FESEM图。从图1可见,不同质量浓度丝胶溶液中制备的碳酸钙晶体形貌有明显的区别。从图1a可以看出,在纯水中得到碳酸钙晶体是规则的斜方六面体,晶体尺寸为8~10 μm;当丝胶质量浓度为0.5 g/L时,碳酸钙晶体呈现多种形貌,有球状、类正方体及无规则的碳酸钙;当丝胶质量浓度增加到1 g/L时,制备的碳酸钙晶体主要是由小的菱形晶体相互嵌合形成的刺球状颗粒(直径5~10 μm)、片层结构组装成的类正方体碳酸钙,尺寸约为5 μm;当丝胶质量浓度进一步增加到1.5 g/L时,碳酸钙晶体具有片层状结构组装成的类正方体,尺寸3~4 μm,且尺寸比较均一。
丝胶主要的氨基酸组成为丝氨酸(33.43 %)、天门冬氨酸(16.71 %)、甘氨酸(13.49 %),其分子侧链上含有大量羟基、羧基和氨基等极性基团[19],因此丝胶分子能够与碳酸钙之间形成复杂的相互作用,如氢键、螯合作用、静电作用等。随着丝胶蛋白质量浓度的增加,丝胶蛋白与碳酸钙之间相互作用方式存在较大差异,使得碳酸钙在丝胶分子特定区域里成核和生长时会受到强烈的影响。当丝胶质量浓度逐渐增大时,丝胶分子之间的相互作用增大,静电引力增大,氢键作用力大大降低了正电性基团的排斥,钙离子在溶液中的过饱和度增加,成核活化能降低,有利于碳酸钙晶体的成核结晶,因此,碳酸钙生长结晶趋向于更为有序的结构。此外,丝胶能够吸附在碳酸钙晶体的特定晶面上,而晶面上丝胶质量浓度高导致此晶面上的生长速率低,从而造成各个晶面生长速率不同,因此丝胶质量浓度增加,晶面上丝胶密度也在增加,晶体形貌与尺寸也随之发生变化[20]。
2.2 不同质量浓度丝胶溶液中合成的碳酸钙晶体的XRD图谱
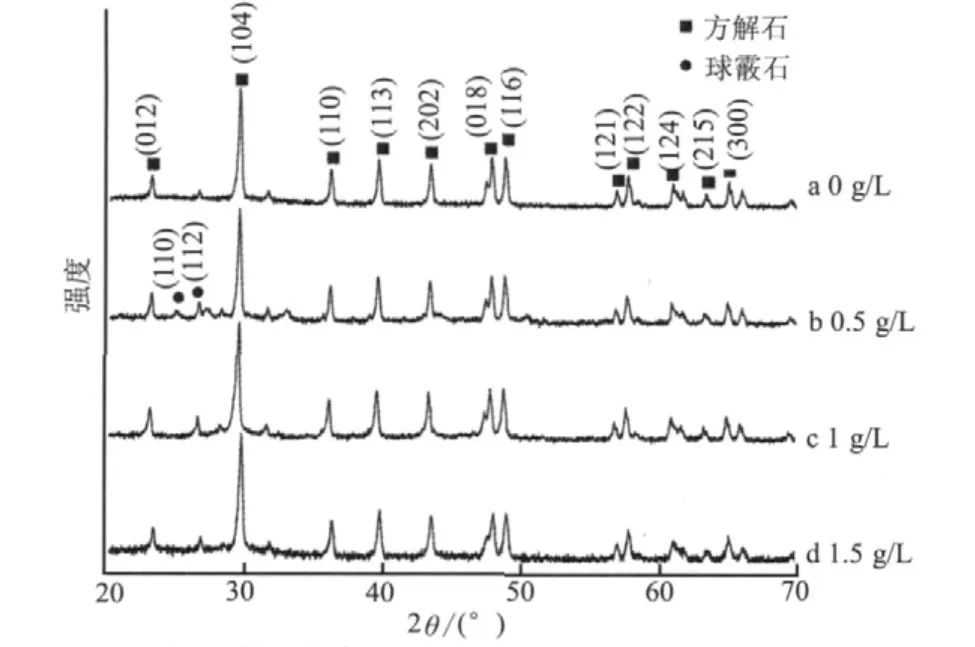
图2 不同质量浓度丝胶溶液中合成的碳酸钙XRD谱图Fig. 2 XRD spectra of the Calcium carbonate obtained at different sericin concentration
图2为不同丝胶质量浓度下得到的碳酸钙晶体的XRD图谱。从图2a可以看出,当溶液中不含丝胶时,生成的碳酸钙出现了(104)、(202)、(018)、(116)、(113)等特征衍射峰,与方解石的标准图谱(JCPDS 47-1743)完全一致;同时样品中还出现了球霰石(112)面衍射峰,表明所制备的碳酸钙主要为结晶良好的方解石晶体,并伴有极少量的球霰石晶体。当丝胶质量浓度为0.5 g/L时(图2b),得到的碳酸钙晶体主要是方解石,同时还出现了球霰石(JCPDS 33-0268)(110)、(112)面衍射峰,说明制备的碳酸钙中还含有少量球霰石;结合(图1b)SEM结果,样品中球霰石的数量显著高于未经丝胶蛋白调控的碳酸钙样品。图 2 c、d 中,随着丝胶质量浓度逐渐增加,所制备的碳酸钙的晶型与丝胶质量浓度为0.5 g/L时基本相同,均为球霰石和方解石混合晶型,但是球霰石的(110)面消失了,说明丝胶质量浓度增加后可抑制球霰石(110)面的生长。结合FESEM结果可知,丝胶对碳酸钙晶体的晶型仅有一定的影响作用,它对碳酸钙晶体生长的影响作用主要表现为对晶体生物矿化方式的控制,引起晶体尺寸和形貌的变化。
2.3 不同质量浓度丝胶溶液中合成的碳酸钙晶体的FTIR图谱
图3为在不同丝胶质量浓度下生成的碳酸钙晶体的红外光图谱。从图3a可知,所得的碳酸钙在712、875和1 420 cm-1处有强的吸收峰,它们分别是方解石晶体中CO32-基团的O―C―O面内弯曲振动峰,O―C―O面外弯曲振动峰和C―O反对称伸缩振动峰[21],在1 082 cm-1处出现了微弱的红外吸收峰,这是CO32-基团中C―O对称伸缩振动峰,说明碳酸钙晶体是有方解石和球霰石组成的混合晶体,而图3b、c、d中除了出现以上4个峰外,在1 654 cm-1处也出现了微弱的吸收峰,1 654 cm-1处是丝胶蛋白红外吸收光谱中酰胺Ⅰ键的酰胺基的CO伸缩振动特征峰[22],说明丝胶与碳酸钙之间存在一定的化学相互作用,这与XRD结果是一致的。

图3 在不同丝胶质量浓度下生成的碳酸钙晶体的FTIR谱图Fig.3 FTIR spectra of the Calcium carbonate obtained at different sericin protein concentration
3 结 语
本研究通过简单的共沉淀方法,在温和条件下以丝胶为模板调控合成了刺球状碳酸钙和片层结构的类正方体碳酸钙。结果表明,随着丝胶质量浓度的增加,丝胶可对生成的碳酸钙形貌和尺寸产生显著影响,并抑制碳酸钙特定晶面的生长。丝胶与无机晶体之间存在复杂的相互作用,丝胶对碳酸钙晶体的生长具有调制作用,本研究为仿生合成新型材料提供了一定的参考。
[1] KONTOYANNIS C G, VAGENAS N V. Calcium carbonate phase analysis using XRD and FT-Raman spectroscopy [J].The Analyst, 2000, 125(2): 251-255.
[2] FLATEN E M, SEIERSTEN M, ANDREASSEN J P.Induction time studies of calcium carbonate in ethylene glycol and water [J]. Chemical Engineering Research and Design, 2010, 88(12): 1659-1668.
[3] AJIKUMAR P K, LOW B J M, VALIYAVEETTIL S. Role of soluble polymers on the preparation of functional thin fi lms of calcium carbonate [J]. Surface and Coatings Technology,2005, 198: 227-230.
[4] CHENG B. Preparation of monodispersed cubic calcium carbonate particles via precipitation reaction [J]. Materials Letters, 2004, 58(10): 1565-1570.
[5] FENG B, YONG A K, AN H. Effect of various factors on the particle size of calcium carbonate formed in a precipitation process [J]. Materials Science and Engineering:A, 2007, 445-446: 170-179.
[6] FLATEN E M, SEIERSTEN M, ANDREASSEN J P. Polymorphism and morphology of calcium carbonate precipitated in mixed solvents of ethylene glycol and water[J]. Journal of Crystal Growth, 2009, 311(13): 3533-3538.
[7] TONG H, MA W T, Wang L L, et al. Control over the crystal phase, shape, size and aggregation of calcium carbonate via a l-aspartic acid inducing process [J]. Biomaterials, 2004,25(17): 3923-3929.
[8] LIANG P. The effect of carboxymethyl chitosan on the precipitation of calcium carbonate [J]. Journal of Crystal Growth, 2004, 261(4): 571-576.
[9] XIAO J W, WANG Z N, TANG Y C, et al. Biomimetic mineralization of CaCO3on a phospholipid monolayer:From an amorphous calcium carbonate precursor to calcite via vaterite [J]. Langmuir, 2010, 26(7): 4977-4983.
[10] YANG H Y, YAO W G, YANG L, et al. The self-assembly of CaCO3crystals in the presence of protein [J]. Journal of Crystal Growth, 2009, 311(9): 2682-2688.
[11] CHENG C, SHAO Z Z, VOLLRATH F. Silk fibroinregulated crystallization of calcium carbonate [J]. Advanced Functional Materials, 2008, 18: 2172-2179.
[12] 沈彤. 丝素蛋白调控磷酸钙生物矿化的研究进展[J]. 丝绸,2010,47(7):23-26.SHEN Tong. Development of current researches on biomineralization of calcium phosphate regulated by silk fi broin[J]. Journal of Silk, 2010, 47(7): 23-26.
[13] 薛辉,蔡玉荣,姚菊明. 微乳液法制备多孔中空羟基磷灰石微球的研究[J]. 浙江理工大学学报,2011,28(3):338-342.XUE Hui, CAI Yurong, YAO Juming. Study on porous hydroxyapatite microsphere with an internal cavity by emulsion method[J]. Journal of Zhejiang Sci-Tech University, 2011, 28(3): 338-342.
[14] CAO Z B, CHEN X, YAO J R, et al. The preparation of regenerated silk fi broin microspheres [J]. Soft Matter, 2007,3(7): 910-915.
[15] CAPAR G, AYGUN S, GECIT M. Treatment of silk production wastewaters by membrane processes for sericin recovery [J]. Journal of Membrane Science, 2008, 325(2):920-931.
[16] CHO K. Preparation of self-assembled silk sericin nanoparticles [J]. International Journal of Biological Macromolecules, 2003, 32(1-2): 36-42.
[17] ZHANG Y Q, MA Y, XIA Y Y, et al. Silk sericin-insulin bioconjugates: Synthesis, characterization and biological activity [J]. Journal of Controlled Release, 2006, 115(3):307-15.
[18] MANDAL B B, PRIYA A S, KUNDU S C. Novel silk sericin/gelatin 3-D scaffolds and 2-D fi lms: Fabrication and characterization for potential tissue engineering applications[J]. Acta Biomaterialia, 2009, 5(8): 3007-3020.
[19] DASH B C, MANDAL B B, KUNDU S C. Silk gland sericin protein membranes: Fabrication and characterization for potential biotechnological applications [J]. Journal of Biotechnology, 2009, 144: 321-329.
[20] SHEN F H, FENG Q L, WANG C M. The modulation of collagen on crystal morphology of calcium carbonate [J].Journal of Crystal Growth, 2002, 242(1-2): 239-244.
[21] ANDERSEN F. Infrared spectra of amorphous and crystalline calcium carbonate [J]. Acta Chemica Scandinavica, 1991, 45: 1018-1024.
[22] CAI Y R, JIN J, MEI D P, et al. Effect of silk sericin on assembly of hydroxyapatite nanocrystals into enamel prismlike structure [J]. Journal of Materials Chemistry, 2009,19(32): 5751-5751.
Study on the regulation and control of silk sericin on the crystal formation of Calcium Carbonate
DING Shaoa, WANG Hai-longb, XU Su-jub, KONG Xiang-dongb
(a.College of Materials and Textile; b.College of Life Sciences, Zhejiang Sci-Tech University, Hangzhou 310018, China)
This study uses silk sericin as organic template to regulate the crystal formation of calcium carbonate in the presence of protein, discusses the mass concentration of silk sericin on the crystal growth. The obtained samples are characterized by fi eld emission scanning electron microscopy (FESEM), X-ray diffraction (XRD), infrared spectroscopy(FTIR). The result shows that controlling the the mass concentration of silk sericin can regulate the crystal growth of calcium carbonate, significantly change the appearance and size of crystal and restrain the specific crystal growth of calcium carbonate. Cube-like calcium carbonate formed by thorn spherical calcium carbonate aggregates and lamellar structure was prepared, the formation mechanism of which is discussed preliminarily. The result shows that interaction between silk sericin and mineral crystal was very complex and silk sericin had a signi fi cant effect on the formation of calcium carbonate crystal.
Calcium carbonate; Silk sericin; Biomineralization; Crystal formation; Regulate and control
TS149
A
1001-7003(2012)06-0008-04
2011-09-07;
2012-05-20
国家自然科学基金资助项目(50942023、510021 39);浙江省教育厅科研计划重点项目(20070340)
丁少(1986- ),硕士研究生,研究方向为生物矿化与生物材料。通讯作者:孔祥东,副研究员,kongxiang dong@gmail.com。

