丙戊酸钠薄膜衣片的制备及稳定性研究
胡崇茂 陈佩英 胡晓晓 高 磊
(北京英茂药业有限公司,北京 101407)
丙戊酸钠薄膜衣片的制备及稳定性研究
胡崇茂 陈佩英 胡晓晓 高 磊
(北京英茂药业有限公司,北京 101407)
目的 研究丙戊酸钠薄膜衣片的制备方法。方法 分别用全水型和醇溶型薄膜包衣预混剂对该素片进行包衣,与该品种同规格糖衣片同时进行稳定性考察比较。结果 用全水型和醇溶型薄膜包衣预混剂对该产品素片进行包衣后,当增重达到(3.5±0.3)%时,本品6个月时的水分含量分别为6.3%、6.6%,糖衣片为8.9%,其他项目比糖衣片也显出一定的优势,且均符合规定。结论 按该工艺生产的丙戊酸钠薄膜衣片符合质量标准要求,工艺稳定可靠,适合大生产需要。
丙戊酸钠片;薄膜衣;制备;稳定性
为提高丙戊酸钠片的抗吸湿性能和掩盖其不良味道,同时考虑到其糖衣片的局限性和薄膜包衣的优势[2],我们在实验中将该片改成薄膜衣片。丙茂酸钠片是中国药典2010年二部中收载的化学药片剂[1],属于抗癲痫药类别,为糖衣片。规格为0.1g和0.2g。丙戊酸钠原料为白色结晶性粉末或颗粒;味微涩;有强吸湿性,在水中极易溶解,在甲醇或乙醇中易溶,在丙酮中几乎不溶。实验表明,将丙戊酸钠糖衣片改成薄膜衣片是可行的,适用于大生产操作,而且能达到防吸湿、掩味等效果。
试验中分别采用全水型薄膜包衣预混剂和醇溶型薄膜包衣预混剂,用量为素片重量的3%~4%(W/W)。分别用纯化水和80%乙醇(W/W)作溶剂配成固含量为13%(W/V)的包衣液。
1 仪器与试药
962型色差仪(美国爱色丽);JM-180型胶体磨(郑州玉祥机械设备有限公司);YD-1片剂硬度测试仪(天津市富兰斯电子科贸有限公司);CSD-1型脆碎度测试仪(天津市富兰斯电子科贸有限公司);BG-10型高效包衣机(南京天塔机械设备有限公司);BJ-ZN崩解时限仪(天津市富兰斯电子科贸有限公司);WD-A药物稳定性检查仪(天津市富兰斯电子科贸有限公司);SH10A型水分快速测定仪(上海精密科学仪器有限公司);101-3ASB电热恒温干燥箱(北京科伟永兴仪器有限公司);FA1104N电子天平(上海精密科学仪器有限公司)。
全水型薄膜包衣预混剂(北京英茂药业有限公司生产,批号121035);醇溶型薄膜包衣预混剂(北京英茂药业有限公司生产,批号121019);丙戊酸钠素片和其糖衣片(W药业有限公司按中国药典2010年版二部生产提供,批号为121015)。
2 方法与结果
2.1 素片的制备及其质量
取粉碎过100目的原料,加入预胶化淀粉、微晶纤维素等辅料,用沸腾制料法制粒,控制颗粒水分为3.5%~5.5%,整粒,加入硬脂酸镁、二氧化硅、滑石粉适量,混匀,检验,合格后压成1000片。
经检验:本批素片呈浅弧型,表面平整光洁,平均片重0.21g,硬度6.3kg,脆碎度0.10%,符合薄膜包衣操作对所包素片的基本要求。
2.2 薄膜包衣操作工艺方法
2.2.1 薄膜包衣液的制备
2.2.1.1 全水型包衣液的配制
各物料用量计算:按每锅投入素片量7kg、增重3.2%、固含量14%计算,需薄膜包衣预混剂干粉为0.224kg,纯化水1.376kg。
配制:称取计算量的纯化水,置于配料罐内,开启搅拌,将称好的薄膜包衣预混剂干粉缓缓加到溶剂旋涡上,并在3~5min内加完,搅拌45min后,在胶体磨中将包衣液进行匀化,再转移进配料罐内,继续慢速搅拌,待用。即得全水型包衣液。
2.2.1.2 醇溶型包衣液的配制
各物料用量计算:按每锅投入素片量7kg、增重3.8%、固含量16%计算,需薄膜包衣预混剂干粉为0.266kg,85%(W/W)浓度的乙醇溶液1.3965kg。
配制:称取95%(W/W)浓度的乙醇溶液1.2495kg,置配料罐内,再加入纯化水0.147kg,搅匀,配成85%(W/W)浓度的乙醇溶液,作为溶剂。开启搅拌桨,按上述操作即得。
2.2.2 包衣操作方法与过程
2.2.2.1 全水型包衣
将制备的符合薄膜包衣要求的素片7kg投入高效包衣机内,调节喷枪,使喷枪雾柱中心线垂直于片床,雾距为22~28cm,锅转速2~3r/ min,先对素片进行预热,待片床温度达到30~40℃时,开启喷雾,控制流量40g/min,出风温度55~60℃、锅转速7r/min、喷枪雾化压力0.40~0.60MPa,注意保持喷雾与干燥处于动态平衡状态,防止粘片、喷雾干燥现象发生,40min后包衣液喷完。
2.2.2.2 醇溶型包衣
将制备的符合薄膜包衣要求的素片7kg投入高效包衣机内,调节喷枪,使喷枪雾柱中心线垂直于片床,雾距为22~28cm,锅转速2~3r/ min,先对素片进行预热,待片床温度达到30~40℃时,开启喷雾,控制流量42g/min,出风温度55~60℃、锅转速6r/min、喷枪雾化压力0.40~0.60MPa,注意保持喷雾与干燥处于动态平衡状态,防止粘片、喷雾干燥现象发生,40min后包衣液喷完。
2.2.3 两种薄膜衣片的质量情况
对上述两种片子进行包衣增重检测和外观质量检查,结果:全水型包衣片增重为3.1%,醇溶型包衣片增重为3.6%;全水型薄膜包衣片的表面色泽均匀、光洁细腻,衣层牢固致密,无开裂、掉皮、杂色点等缺陷,硬度7.1kg;醇溶性薄膜包衣片的表面略显粗糙,其他均与前者相似。
2.3 两种薄膜衣片的稳定性试验
2.3.1 稳定性试验方法
参照中国药典2010年版二部中关于稳定性试验的相关内容[3],模拟市售包装,分别将两种薄膜衣片用铝塑泡罩包装成铝塑板,置药物稳定性检查仪内,按加速试验要求,在温度40℃±2℃,相对湿度75% ±5%条件下放置6个月。分别于0、1、2、3、6个月取样,按稳定性重点考察项目检验,水分测定方法见中国药典2010年版一部附录Ⅸ H第二法[4]。结果如下表所示。
2.3.2 实验结果
见表1~3。
表1 丙戊酸钠片(全水型包衣液)加速试验结果表[(),n=3]
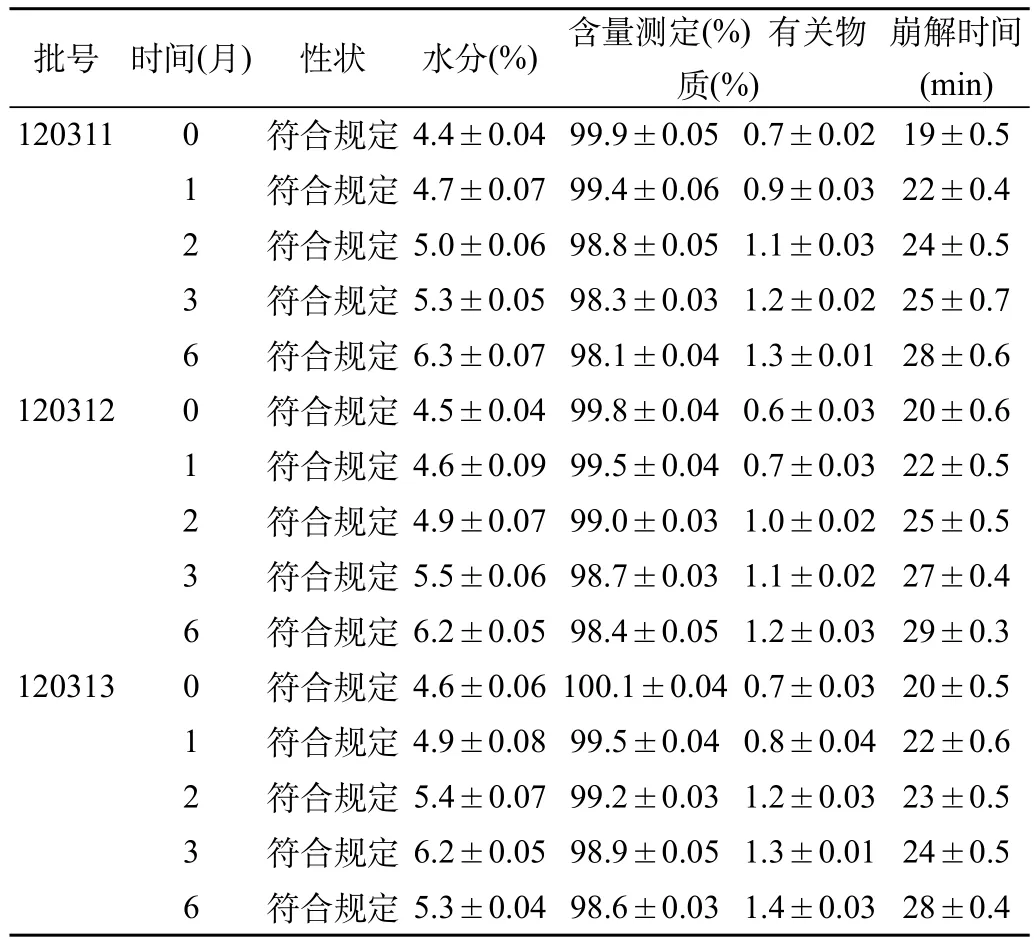
表1 丙戊酸钠片(全水型包衣液)加速试验结果表[(),n=3]
崩解时间(min) 1203110符合规定4.4±0.0499.9±0.050.7±0.0219±0.5 1符合规定4.7±0.0799.4±0.060.9±0.0322±0.4 2符合规定5.0±0.0698.8±0.051.1±0.0324±0.5 3符合规定5.3±0.0598.3±0.031.2±0.0225±0.7 6符合规定6.3±0.0798.1±0.041.3±0.0128±0.6 1203120符合规定4.5±0.0499.8±0.040.6±0.0320±0.6 1符合规定4.6±0.0999.5±0.040.7±0.0322±0.5 2符合规定4.9±0.0799.0±0.031.0±0.0225±0.5 3符合规定5.5±0.0698.7±0.031.1±0.0227±0.4 6符合规定6.2±0.0598.4±0.051.2±0.0329±0.3 1203130符合规定4.6±0.06100.1±0.040.7±0.0320±0.5 1符合规定4.9±0.0899.5±0.040.8±0.0422±0.6 2符合规定5.4±0.0799.2±0.031.2±0.0323±0.5 3符合规定6.2±0.0598.9±0.051.3±0.0124±0.5 6符合规定5.3±0.0498.6±0.031.4±0.0328±0.4批号时间(月)性状水分(%)含量测定(%) 有关物质(%)
表2 丙戊酸钠片(醇溶性包衣液)加速试验结果表[(),n=3]
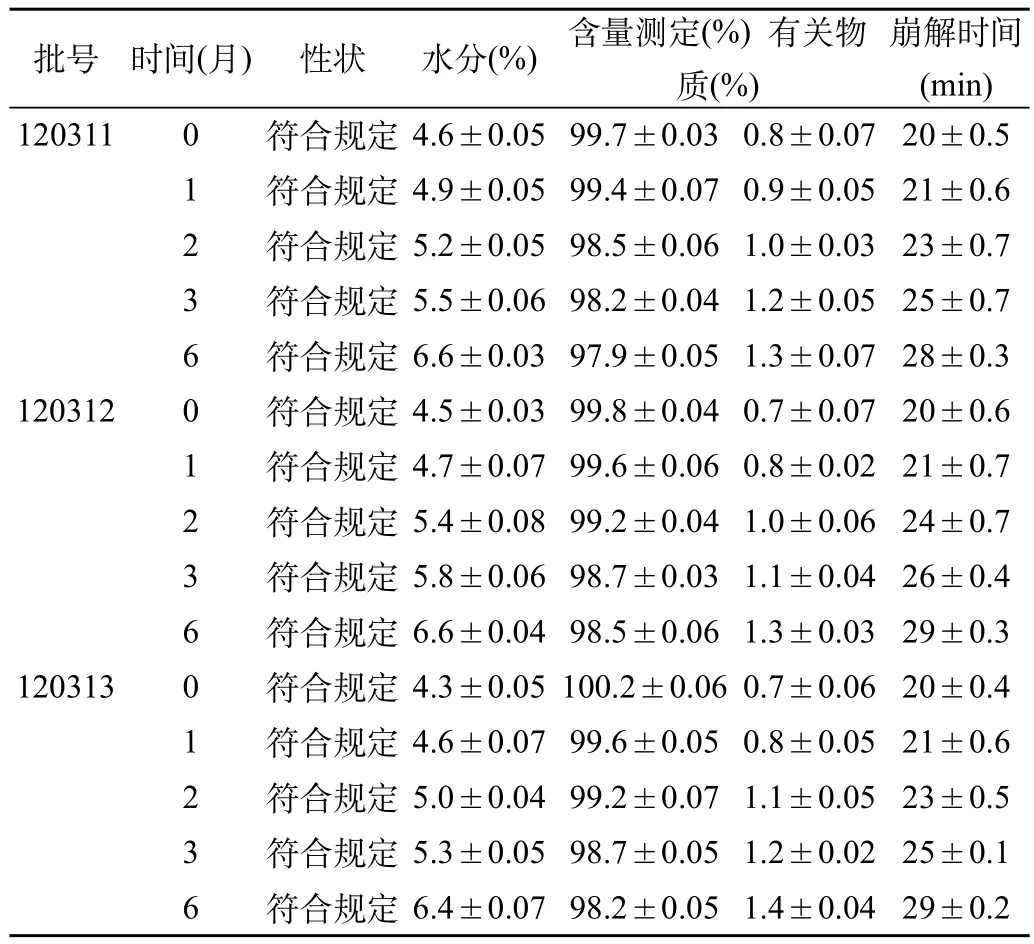
表2 丙戊酸钠片(醇溶性包衣液)加速试验结果表[(),n=3]
崩解时间(min) 1203110符合规定4.6±0.0599.7±0.030.8±0.0720±0.5 1符合规定4.9±0.0599.4±0.070.9±0.0521±0.6 2符合规定5.2±0.0598.5±0.061.0±0.0323±0.7 3符合规定5.5±0.0698.2±0.041.2±0.0525±0.7 6符合规定6.6±0.0397.9±0.051.3±0.0728±0.3 1203120符合规定4.5±0.0399.8±0.040.7±0.0720±0.6 1符合规定4.7±0.0799.6±0.060.8±0.0221±0.7 2符合规定5.4±0.0899.2±0.041.0±0.0624±0.7 3符合规定5.8±0.0698.7±0.031.1±0.0426±0.4 6符合规定6.6±0.0498.5±0.061.3±0.0329±0.3 1203130符合规定4.3±0.05100.2±0.060.7±0.0620±0.4 1符合规定4.6±0.0799.6±0.050.8±0.0521±0.6 2符合规定5.0±0.0499.2±0.071.1±0.0523±0.5 3符合规定5.3±0.0598.7±0.051.2±0.0225±0.1 6符合规定6.4±0.0798.2±0.051.4±0.0429±0.2批号时间(月)性状水分(%)含量测定(%) 有关物质(%)
表3 丙戊酸钠片(糖衣片)加速试验结果表[(),n=3]
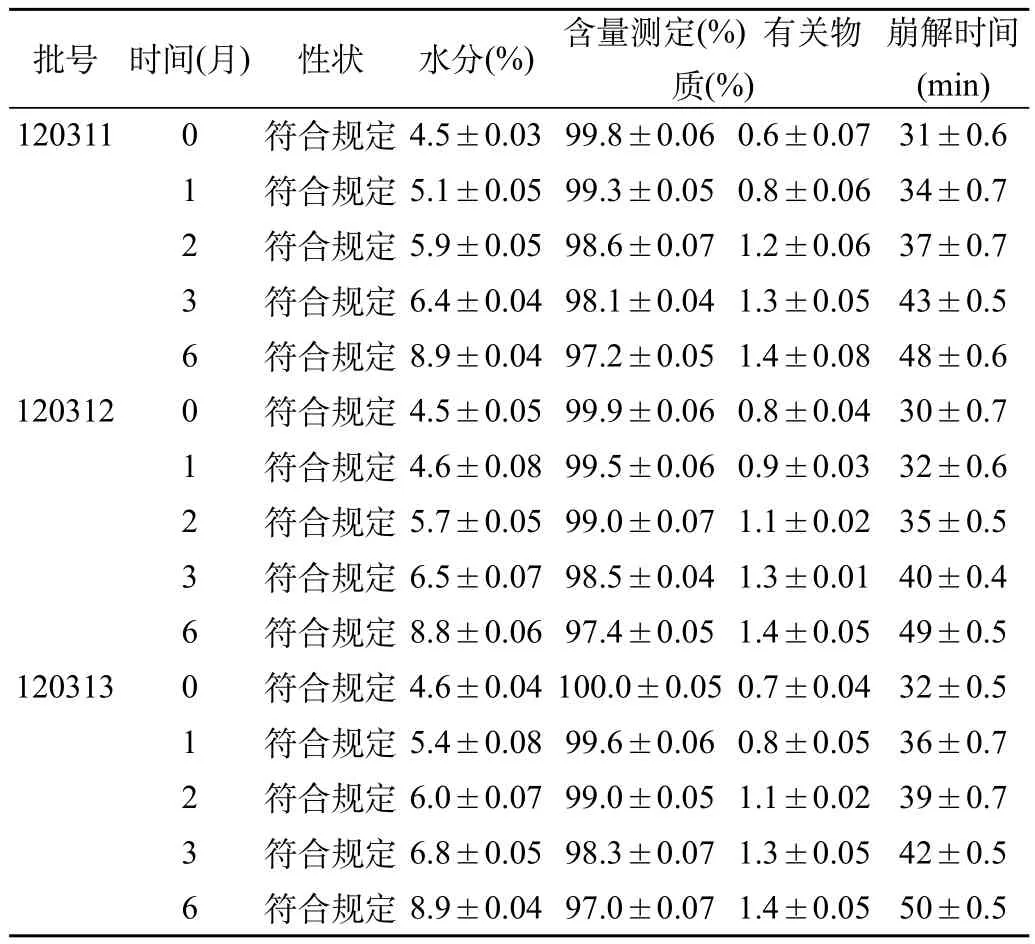
表3 丙戊酸钠片(糖衣片)加速试验结果表[(),n=3]
崩解时间(min) 1203110符合规定4.5±0.0399.8±0.060.6±0.0731±0.6 1符合规定5.1±0.0599.3±0.050.8±0.0634±0.7 2符合规定5.9±0.0598.6±0.071.2±0.0637±0.7 3符合规定6.4±0.0498.1±0.041.3±0.0543±0.5 6符合规定8.9±0.0497.2±0.051.4±0.0848±0.6 1203120符合规定4.5±0.0599.9±0.060.8±0.0430±0.7 1符合规定4.6±0.0899.5±0.060.9±0.0332±0.6 2符合规定5.7±0.0599.0±0.071.1±0.0235±0.5 3符合规定6.5±0.0798.5±0.041.3±0.0140±0.4 6符合规定8.8±0.0697.4±0.051.4±0.0549±0.5 1203130符合规定4.6±0.04100.0±0.050.7±0.0432±0.5 1符合规定5.4±0.0899.6±0.060.8±0.0536±0.7 2符合规定6.0±0.0799.0±0.051.1±0.0239±0.7 3符合规定6.8±0.0598.3±0.071.3±0.0542±0.5 6符合规定8.9±0.0497.0±0.071.4±0.0550±0.5批号时间(月)性状水分(%)含量测定(%) 有关物质(%)
3 讨 论
3.1 糖衣片加速6个月时,性状项虽然也符合规定,但片子表面与0d相比,明显发暗,并失去光泽,可能是因为吸湿等原因而引起。
3.2 通过对三种药片稳定性试验对比研究表明,北京英茂药业研制的全水型薄膜包衣预混剂和醇溶型薄膜包衣预混剂完全可以替代糖包衣,对丙戊酸钠片进行薄膜包衣显示出较多的优越性;全水型薄膜包衣预混剂以水为溶剂虽然价格便宜,操作安全,不需防爆,但本品吸湿性强,且主药成分易溶于水,包衣时要保证足够的干燥温度和空气量,采用较低的喷雾速度,水性系统中尽可能增大固体含量至12%(W/W)以上,以降低含水量[5]。
3.3 薄膜包衣对素片的质量要求:能否对某种素片进行薄膜包衣,以及包衣后片子的质量,在很大程度上依赖于素片质量。因此薄膜包衣预混剂的配方一般是按照素片特性和质量状况“量身定做”的。合适的外形是薄膜包衣所必需的,如浅弧型素片不存在容易脱落的锋利的边角,在包衣过程中不会磨损,翻滚均匀,能保持良好的包衣效果;此外,对化学药片剂来说,硬度一般宜在4~10kg/mm2、脆碎度宜不超过0.8%。
[1] 国家药典委员会.中华人民共和国药典(二部)[M].北京:化学工业出版社,2010:92.
[2] 庞凤华,郑捷,熊志玲.水性薄膜包衣技术在骨仙片生产的工艺研究[J].国际医药卫生导报,2005,11(4):86-88.
[3] 国家药典委员会.中华人民共和国药典(二部)[M].北京:化学工业出版社,2010:附录200.
[4] 国家药典委员会.中华人民共和国药典(一部)[M].北京:化学工业出版社,2010:附录52.
[5] 郑俊民.片剂包衣的工艺和原理[M].北京:中国医药科技出版社,2000:402.
Study on the Stability of Sodium Valproate and Film Preparation
HU Chong-mao, CHEN Pei-ying, HU Xiao-xiao, GAO Lei
(Beijing Yingmao Pharmaceutical Company Limited, Beijing 101407, China)
Objective Study on Preparation of sodium valproate film-coated tablets. Methods With full water and alcohol soluble film coating premix is coated on the core, and the varieties of the same specifications sugar-coated tablets and stability comparison. Results With the water and alcohol soluble film coating premix is coated on the tablet core, when the weight reached 3.5%±0.3%, the moisture content of the product at 6 months were 6.3%, 6.6%, sugar-coated tablets for 8.9%, other than sugar coated tablets also shows some advantages, which are in line with the provisions. Conclusions According to valproate film-coated tablets produced by this technology to meet the required quality standards, the technology is stable and reliable, and suitable for the industrial production needs.
Sodium valproate tablets; Thin film; Preparation; Stability
R94
B
1671-8194(2013)26-0065-03

