大剂量依托泊苷联合自体造血干细胞移植挽救性治疗进展期淋巴瘤的临床观察
上海交通大学附属第一人民医院血液科,上海 200080
大剂量依托泊苷联合自体造血干细胞移植挽救性治疗进展期淋巴瘤的临床观察
蔡宇 杨隽 姜杰玲 朱骏 王椿
上海交通大学附属第一人民医院血液科,上海 200080

王椿,主任医师,教授,博士研究生导师,上海交通大学附属第一人民医院血液科主任,加拿大安大略肿瘤研究所骨髓移植中心博士后。中华医学会血液学分会委员兼秘书长,上海市医学会血液专科分会第九届委员会主任委员,上海市血液学研究所副所长、上海市器官移植临床医学中心副主任,中国抗癌协会血液肿瘤分会常委,上海市医学会感染与化疗专业委员会委员,兼任《中国感染与化疗杂志》常务编委,《中华内科杂志》、《中华血液学杂志》、《临床血液学杂志》、《白血病·淋巴瘤》等杂志编委。主要研究方向为运用自体或异基因造血干细胞移植治疗各类血液肿瘤,并且在移植嵌合状态监测上处于全国领先水平。擅长血液肿瘤疑难病例诊断与治疗及造血干细胞移植。在血液肿瘤发病机制及治疗对策上有独到见解。承担10多项国家和上海市科研课题,牵头上海及全国多中心临床实验5项。在Blood、Leukemia、Oncology、Experimental Hematology、《中华血液学杂志》、《中国实验血液学杂志》等国内外学术期刊共发表论文160余篇,其中SCI论文15篇。曾获省级科技进步三等奖和上海医学科技奖三等奖各1项。
背景与目的:淋巴瘤复发是进展期淋巴瘤患者的主要死因,常规化疗疗效不佳。本研究旨在评估大剂量依托泊苷(VP16)联合自体造血干细胞移植治疗进展期淋巴瘤的疗效。方法:40例进展期淋巴瘤患者均接受大剂量VP16 10~15 mg/(kg·d)静脉滴注,持续2 d化疗,并在化疗后接受G-CSF 5~10 μg/kg皮下注射,至白细胞计数>4×109/L,采集患者干细胞并冻存于-80 ℃深低温冰箱中;40例患者均接受自体造血干细胞移植。结果:VP16治疗后中位随访时间39 d(17~172 d),40例患者中12(30%)例对大剂量VP16无反应,28(70%)例有反应。自体干细胞移植后,中位随访28个月(4~66 d)。40例患者中,16(40%)例达到完全缓解,其中对VP16有反应的28例患者,15(53.6%)例达到完全缓解,4(14.3%)例部分缓解,9(32.1%)例死于疾病进展,对VP16无反应的12例患者,仅1(8.3%)例达到完全缓解。1(8.3%)例部分缓解,10(83.4%)例死于疾病进展。对VP16有反应的患者1年的无事件生存率(event-free survival,EFS)为56.7%,总体生存率(overall survival,OS)为69.0%,2年EFS为52.0%,OS为63.0%。无反应的患者1年EFS为16.7%,OS为25.0%,2组数据相比,差异有统计学意义(P<0.01)。结论:大剂量VP16联合自体造血干细胞移植能使对大剂量VP16有反应的患者带来较高的EFS和OS,可作为难治性淋巴瘤患者挽救性治疗的选择之一。
大剂量VP16;进展期淋巴瘤;自体造血干细胞移植
进展期淋巴瘤虽然可以通过常规化疗来治疗,但疗效不佳[1],淋巴瘤复发仍是这部分患者主要死因。大剂量化疗(high dose therapy,HDT)联合自体造血干细胞移植(autologous hematopoietic stem cell transplantation,auto-SCT)能延长预后较差的淋巴瘤患者的无病生存期(disease free survival,DFS)[2-3]。但目前大多数研究报道除了包含原发难治的患者之外,还有许多复发的患者,后者可能对常规的挽救性化疗仍然敏感。那么,对于常规二、三线挽救方案不敏感,疾病评估仍为疾病进展(progressive disease,PD)的患者,预后极差,即使采用HDT加auto-SCT效果也不理想。目前临床试验很少单独入组疾病评估为PD的患者。本研究旨在评估应用大剂量依托泊苷(VP16)联合auto-SCT治疗进展期淋巴瘤的疗效。
1 资料和方法
1.1 研究对象
选择2004—2013年上海交通大学附属第一人民医院血液科收治的淋巴瘤患者40例,均经过常规化疗后疾病评估为PD的患者,其中男性28例(70%),女性12例(30%),中位年龄33(13~61)岁;其中霍奇金病(Hodgkin′s disease)8例(结节硬化型6例,经典型1例,混合细胞型1例),非霍奇金淋巴瘤(non-Hodgkin’s lymphoma) 32例(弥漫大B细胞25例,中大细胞型1例,灰区细胞型1例,NK/T细胞型1例,Burkitt细胞型1例,MALT 1例,间变大细胞2例);疾病分期:ⅠEA期1例,Ⅱ期2例,Ⅲ期6例,Ⅳ期31例,其中巨块型7例;所有患者入组之前均接受过多种常规化疗,包括IGEV、MINE和ESHARP等二线方案,中位方案数为4(2~7)个,中位疗程数为10(5~18)个疗程,10例接受过放疗。ECOG:0分4例,1分15例,2分17例,3分4例。
1.2 方法
1.2.1 化疗方案
动员方案:VP16 10~15 mg/(kg·d)静脉滴注,连续2 d。预处理方案:①BEAM方案,BCNU 300 mg/m2,第-6天,静脉滴注马法兰1 4 0 m g/m2,第-1天,静脉滴注VP16 150~200 mg/m2,第-5~-2天,静脉滴注阿糖胞苷200~400 mg/m2,第-5~-2天,静脉滴注。②CBV方案,BCNU 300 mg/m2,第-8~-6天,静脉滴注环磷酰胺1.2~1.8 g/m2,第-5~-2天联合VP16 250~800 mg/m2,第-8~-6天)。
1.2.2 评价标准
参照张之南《血液病诊断及疗效标准》第3版[4]进行疗效评价。
1.2.3 方法
40例患者均接受大剂量VP16的化疗,并在化疗后接受G-CSF 5~10 μg/kg皮下注射,至白细胞计数>4×109/L,采集患者干细胞并冻存于-80 ℃深低温冰箱中;40例患者均接受auto-SCT,BEAM方案5例(12.5%),BEAM联合西妥昔单抗14例(35%),CBV方案17例(42.5%),CBV联合利妥昔单抗4(10%)例。auto-SCT后部分患者接受了放疗及干扰素治疗。对于疾病仍处于PR或进展及复发的患者,再次予以姑息化疗。
1.3 统计学处理
采用Kaplan-Meier法进行生存分析,P<0.05为差异有统计学意义。
2 结 果
2.1 对VP16反应率
40例患者中,12例(30%)对VP16无反应,28例(70%)有反应。经干细胞动员后,40例患者均未达到CR,2例PR,26例患者肿块均有缩小,其中6例患者胸闷,腰背酸痛等症状缓解。
2.2 采集细胞数
从动员到采集时间中位14d(10~24 d),C D 3 4+细胞中位数6.3×1 06/L(0.8×1 06~22.3×106/L),有核细胞中位数7.1×108/L (1.3×108~18.6×108/L)。
2.3 移植后反应率
细胞采集到中位随访时间39d(17~172d),其中2例患者在VP16治疗有反应后继续行2~3个周期的常规化疗,以进步降低肿瘤负荷。40例患者中,16例(40%)患者达到完全缓解,其中对VP16有反应的28例患者中,15例(53.6%)达到CR,4例(14.3%)PR,9例(32.1%)PD。对VP16无反应的12例患者中,仅1例(8.3%)达到CR。1例(8.3%) PR,10例(83.4%)PD。
2.4 无事件生存率(event free survival,EFS)及总生存率(overall survival,OS)
中位随访28个月(4~66个月),40例患者中,15例(37.5%)患者获得长期无事件生存。28例对VP16有反应的患者,1年EFS为56.7%,OS为69.0%,2年的EFS为52.0%,OS为63.0%。无反应患者1年EFS为16.7%,OS为25.0%,2组数据差异有统计学意义(P<0.01,图1, 2)。
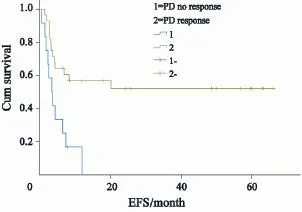
图1 VP16不同反应患者EFSFig. 1 EFS of patients with different VP16 response
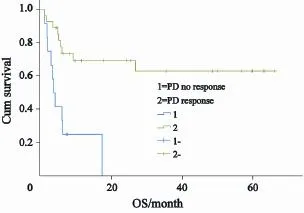
图2 VP16不同反应患者OSFig. 2 OS of patients with different VP16 response
3 讨 论
淋巴瘤是血液系统的恶性肿瘤,随着新的联合化疗方案(如ABVD)出现和单克隆抗体(如利妥昔单抗)靶向治疗,淋巴瘤的缓解率和治愈率明显提高。但仍然有一部分患者对常规的初始治疗不敏感,存在原发耐药,另一部分患者出现缓解后复发。因此,对于复发和难治的淋巴瘤患者需要进行挽救性治疗。对于B细胞非霍奇金淋巴瘤患者,CORAL临床试验的结果显示,在包含利妥昔单抗的一线治疗后仍评估为难治或早期复发的患者,3年EFS仅为23%[5]。对于难治或复发的霍奇金淋巴瘤,常规剂量化疗取得的PFS率和OS率分别为15%~32%和26%~36%[6]。很多纳入复发和难治性霍奇金淋巴瘤患者的单臂研究已经证明,HDCT/ASCT取得的PFS和OS率分别为40%~50%和50%~60%[7]。因此,HDT联合auto-SCT是复发和难治淋巴瘤患者挽救性治疗的最佳选择之一。
对常规剂量挽救性化疗不敏感的淋巴瘤患者,自体移植的疗效欠佳。HDT联合auto-SCT对于难治或复发的T细胞非霍奇金淋巴瘤有很高的复发率,长期生存很难被预计。而对于化疗敏感的复发的T细胞非霍奇金淋巴瘤患者,HDT联合auto-SCT是一个不错的选择[8-9]。针对复发侵袭性的B细胞非霍奇金淋巴瘤的PARMA显示,对于2个疗程DHAP敏感者给与auto-SCT治疗,患者EFS明显好于单用挽救性化疗的患者[10],HDT联合auto-SCT的8年EFS率为36%,而挽救性化疗的患者仅为11%。最近Schmitz等[11]报告了1项随机前瞻性临床试验结果,161例复发难治的HL患者接受DEXABEAM(地塞米松、卡氮芥、阿糖胞苷、马法兰)2个周期治疗,有反应的患者随机进入化疗和ASCT治疗组,随访3年,HDCT/ASCT复发率为34%。这些研究表明,HDCT/ASCT治疗比常规剂量的挽救性化疗对复发和难治性的HL有更好的疗效。但这些临床试验设计接受HDCT/ ASCT的患者的前提条件是,对常规诱导化疗仍然较敏感。
那么对常规剂量诱导化疗不敏感的患者是否一定不适合HDT?本研究的难治性淋巴瘤是指至少经过2种或2种以上常规剂量诱导化疗仍然进展的患者。本研究采用大剂量VP16挽救性治疗对常规化疗不敏感患者中筛选出一些对化疗敏感者,大剂量的VP16化疗能使70%的PD患者减少肿瘤负荷,接着行auto-SCT。对VP16有反应的28例患者中,2年EFS为52.0%,OS为63.0%;而无反应的患者1年EFS为16.2%,OS为25.0%,提示这部分患者对化疗不敏感,预后仍极差。对于这部分原发难治,化疗不敏感的患者可以考虑其他临床试验或异基因造血干细胞移植。因此,对大剂量VP16化疗有反应的患者仍然可以选择auto-SCT作为挽救性治疗。
淋巴瘤患者进行自体外周血造血干细胞移植时用于干细胞动员的化疗方案多为大剂量环磷酰胺。我们考虑到那些难治患者已经接受多个含有环磷酰胺的化疗,包括大剂量异环磷酰胺,因此,这些淋巴瘤细胞对环磷酰胺耐药的可能性较大。本研究采用VP16的剂量为20~30 mg/kg,是常规剂量的5~10倍,能够克服一部分耐药的淋巴瘤细胞,加上之后的auto-SCT,使40%难治性淋巴瘤达CR,37.5%患者获得长期无事件生存。同时,大剂量VP16化疗不影响干细胞动员所采集的干细胞的数量与质量,40例患者在auto-SCT中未发生植入失败。
综上所述,对于常规化疗不敏感的、疗效评估为PD的患者来说,目前没有较理想的挽救性方案,大剂量的VP16联合auto-SCT能使对大剂量VP16有反应的患者带来较长的DFS和OS。自体移植的结果与大剂量VP16的反应性相关。
[1] NADEMANEE A, MOLINA A, O’DONNELL M R, et al. Results of high-dose therapy and autologous bone marrow/ stem cell transplantation during remission in poor-risk intermediate- and high grade lymphoma: international index high and high intermediate risk group[J]. Blood, 1997, 90: 3844-3852.
[2] NADEMANEE A, MOLINA A, DAGIS A, et al. Autologous stem-cell transplantation for poor-risk and relapsed intermediate- and high-grade non-Hodgkin’s lymphoma[J]. Clin Lymphoma, 2000, 1: 46-54.
[3] MARTELLI M, GHELINZONI F, DE RENZO A, et al. Early autologous stem-cell transplantation versus conventional chemotherapy as front-line therapy in high-risk, aggressive non-Hodgkin’s lymphoma: an Italian multicenter randomizedtrial [J]. Clin Oncol, 2003, 7: 1255-1262.
[4] GISSELBRECHT C, GLASS B, MOUNIER N, et al. Salvage regimens with autologous transplantation for relapsed large B-cell lymphoma in the rituximab era [J]. Clin Oncol, 2010, 28(27): 4184-4190.
[5] 张之南, 沈悌. 血液病诊断及疗效标准 [M]. 第3版, 北京: 科学出版社, 2008, 219, 224-225.
[6] STIF P J, UNGER J M, FORMAN S J, et a1.The value of augmented preparative regimens combined with an autologous bone marrow transplant for the management of relapsed or refractory Hodgkin disease: A South-west Oneology Group phase Ⅱ trial [J]. Biol Blood Marrow Transplant, 2003, 9(8): 529.
[7] LINCH D C, WINFIELD D, GOLDSTONE A H, et a1.Dose intensification with autologous bone-marrow transplantation in relapsed and resistant Hodgkin disease: Results of a BNLI randomised trial [J]. Lancet, 1993, 341(8852): 1051.
[8] KYRIAKOU C, CANALS C, GOLDSTON A, et al. Highdose therapy and autologous stem-cell transplantation in angioimmunoblastic lymphoma: complete remission at transplantation is the major determinant of outcomelymphoma working party of the European group for blood and marrow transplantation [J]. Clin Oncol, 2008, 26(2): 218-224.
[9] NICKLELSEN M, CANALS Sr C, SCHMITZ N, et al. Patients with mature T-cell lymphoma show high relapse rates after high dose therapy and autologous stem cell transplantation[J]. Blood, 2008, 112(11): 774.
[10] PHILIP T, GUGLIELMI C, HAGENBEEK A, et al. Autologous bone marrow transplantation as compared with salvage chemotherapy in relapses of chemotherapy-sensitive non-Hodgkin’s lymphoma[N]. Engl J Med, 1995, 333(23): 1540-1545.
[11] SCHMITZ N, PFISTNER B, SEXTRO M, et a1.Aggressive conventional chemotherapy compared with high——dose chemotherapy with autologous haemopoietic stem-cell transplantation for relapsed chemosensitive Hodgkin’s disease: A randomised trial [J]. Lancet, 2002, 359(9323): 2065.
第一届朝阳国际医学大会将于北京召开
第一届“朝阳国际医学大会”将于2014年12月20~21日在北京隆重召开。本次会议由首都医科大学附属北京朝阳医院、北美中华医学会主办,首都医科大学、北京大学医学部、北京市医院管理局联合主办,主题为“加强合作,推动创新,促进医学发展”。大会将以科学合理、灵活多样的形式全方位地展现中美医学研究的最新成果和未来全球医学发展面临的机遇与挑战,可谓是一次融国际、地区和国内学术活动于一体的医学盛宴。届时,美国二十余位呼吸、心血管、神经、急诊与危重症、转化医学、泌尿系统疾病及新药开发、肿瘤和免疫等领域的顶级专家以及国内数位颇具影响力的工程院院士将亲临论坛,为全体参会者做精彩纷呈的报告和演讲。我们还将精心组织六个紧贴临床、紧扣热点、紧跟国际的专题分论坛,邀请北京朝阳医院知名医学专家以及美国同道对所在领域的重点和难点问题进行深入探讨,并同与会者进行面对面的交流。
报到时间:2014年12月19日
会议时间:2014年12月20-21日
会议地点:北京国际会议中心(北京市朝阳区北辰东路8号)
注册费用:人民币 1000 元/人(含会议资料、会议期间的午餐及茶歇)
组委会联系方式
联系人:钟老师 在线注册:www.cicm-bj.org
电 话:010-5710 8106 短信报名:188 1024 2122
传 真:010-6591 9906 E-ma i l:cicm2014@126.com
High-dose etoposide in mobilization for 40 patients with refractory lymphoma
CAI Yu, YANG Juan, JIANG Jie-ling, ZHU Jun, WANG Chun
(Department of Hematology, Shanghai Jiao Tong University Af fi liated First People’s Hospital, Shanghai 201620)
WANG Chun E-mail: wangchun2@medmail.com.cn
High-dose etoposide; Refractory lymphoma; Autologous stem cell transplantation
10.3969/j.issn.1007-3969.2014.10.006
R733
A
1007-3639(2014)10-0750-05
2014-07-03)
王椿 E-mail:wangchun2@medmail.com.cn
[Abstract]Background and purpose: The patients with aggressive lymphoma who have a poor prognosis and unlikely to be cured with conventional chemotherapy. This study was aimed to evaluate the effect of high-dose etoposide in mobilization followed auto-SCT in treating refractory lymphoma. Methods: 40 patients [median age 33 (13-61) years] with refractory non-Hodgkin’s lymphoma (NHL, n=32) or Hodgkin’s lymphoma (HD, n=8) received high-dose etoposide [VP16 10-15 mg/(kg·d)×2 d] in mobilization in our center. Remission status prior to mobilization was PD (n=40). The use of such granulocyte colony-stimulating factor [G-CSF, 5-10 μg/(kg·d)] mobilized peripheral blood stem cells (PBSC) after high-dose etoposide until the end of leukapheresis. Peripheral blood stem cell was collected and frozen in -80℃ refrigerator. All these patients received auto peripheral blood stem cell transplantation (auto-PBSCT). Conditioning regimen was BEAM (n=19, 47.5%) or CBV (n=21, 52.5%). Results: Twenty-eight patients (70%) were assessable for response after high-dose etoposide at a median pretreatment time of 39 days (range 17-172 days), 12 patients (30%) had no response. Median follow-up of 28 (4-66) months, 16 patients (40%) reached CR after auto-PBSCT. Fifteen of the 28 patients (53.6%) who had response to high-dose etoposide reached CR, 4 patients (14.3%) reached PR, 9 patients (32.1%) succumb to progression of disease. One of the 12 patients (8.3%) who had no response to high-dose etoposide reached CR, 1 patients (8.3%) reached PR, 10 patients (83.4%) succumb to progression of disease. The estimated 1-year OS and EFS were 69% and 56.7% respectively, 2-years OS and EFS were 63% and 52% respectively. The prognosis of the patients who had no response to etoposide was poor. The estimated 1-year OS and EFS were 25% and 16.7% respectively. Two group of comparison differences have statistics signi fi cance (P<0.01). Conclusion: High-dose etoposide could be used in refractory lymphoma as rescue therapy in mobilization. It can increase the EFS and OS of patients who had response. The hematopoietic stem cells collection and hematopoietic reconstitution are not affected by etoposide.

