组合支架精确覆盖技术与单一覆膜支架技术的前瞻性随机对照研究
王昌明,李选,傅军,吕献军,栾景源,李天润,赵军,董国祥
组合支架精确覆盖技术与单一覆膜支架技术的前瞻性随机对照研究
王昌明,李选,傅军,吕献军,栾景源,李天润,赵军,董国祥
目的对照研究经颈静脉门体分流术(TIPS)组合支架精确覆盖技术与单一覆膜支架技术的临床应用效果。方法2011年4月—2012年12月收治30例门脉高压症所致上消化道出血患者,行TIPS术。按事先产生的随机分组表将患者分为组合支架组17例和对照组(单一覆膜支架组)13例。比较两组手术成功率、门静脉分支通畅率、门腔静脉压力梯度(PSG)质量控制、支架通畅率以及肝性脑病发生率和生存率等。结果两组手术成功率均为100%。分流后,两组PSG下降较术前差异均有统计学意义(P<0.000);由质量控制图可见组合支架组在PSG调控方面有优越性。术后5 d与术后次日相比,组合支架组血氨下降显著(P=0.029),对照组无显著差异(P=0.065)。术后6 d组合支架组死亡1例;中位随访时间181 d(32~563 d)。随访中,两组各死亡3例,组间生存率差异无统计学意义(P=0.906)。组合支架组2例、对照组1例肝性脑病经药物治疗缓解。两组支架通畅率为100%,再出血率为0%。门静脉分支通畅率组合支架组高于对照组,差异有统计学意义(P=0.039)。结论与传统单一覆膜支架技术相比,组合支架技术更有利于实现支架准确定位释放,且在门静脉分支通畅率及PSG控制方面显示出一定优越性;但在分流道通畅率、肝性脑病发生率、再出血率、生存率等方面与单一覆膜支架技术效果相似。
高血压;食管和胃静脉曲张;放射学,介入性;支架
胃食管曲张静脉出血是门脉高压的严重并发症,是肝硬化患者死亡的主要原因之一。血管活性药物联合内镜技术是治疗急性曲张静脉出血的推荐方法[1],但失败率可达10%~15%[2-3]。在此情形下,经颈静脉门体分流术(transjugular intrahepatic portosystemic shunt,TIPS)是控制出血的有效措施,最近也有建议对急性出血者直接行TIPS[4]。TIPS术后死亡率仍较高,可能与分流术后肝功能进一步恶化有关[5-6]。
在技术层面,提高分流道通畅率、保证止血效果和合理调节分流量、减少因门静脉血供障碍导致的肝功能衰竭发生率是提高整体治疗效果的关键。
本研究提出以“裸支架联合相应长度覆膜支架”形式对肝实质分流道精确覆盖,保证门静脉分支血供,提高分流道通畅率;通过不同口径球囊、支架组合,实现分流量主动调控,保护肝功能。对其实际临床应用效果,通过前瞻性随机对照研究与经典TIPS手术(单一覆膜支架,Fluency®)进行比较,现报道如下。
1 材料与方法
1.1 病例资料
2011年4月—2012年12月我科收治30例门脉高压症所致上消化道出血患者,行TIPS手术。手术适应证均为药物及内镜治疗后复发出血或因急性上消化道出血,胃镜治疗无效。30例中,男性23例,女性7例,年龄41~77岁,中位年龄59岁;乙型肝炎15例,自身免疫性肝炎6例,酒精性肝硬化4例,丙型肝炎1例,布-加综合征1例,药物性肝炎1例,病因不明2例。其中3例合并原发性肝癌。术前Child-Pugh分级A级12例,B级13例,C级5例。1.2研究设计及随机分组方法
本临床研究方案经我院伦理委员会批准后施行。以事先设计的病例报告表记录整个研究过程。手术前征得患者及家属知情同意并签字确认。
1.2.1 随机分组方法借SPSS20.0软件产生随机分组表,密封保存,术前拆封,决定患者进入组合支架组(裸支架联合覆膜支架)或对照组(覆膜支架)。1.2.2样本含量估计TIPS术后1年,分流道功能障碍发生率一般为10%~15%[2],我们希望组合支架组门静脉分支通畅率能达到这个水平;而对照组因支架覆膜部分对相应门静脉分支血流的几乎完全阻断,门静脉分支血栓形成率在1年时可能会大于60%,据此,设定α=0.05,1-β=0.80,两组率之差设为45%,按查表法[两样本率比较时所需样本含量(双侧)表],估算样本含量为17例,考虑失访等因素,我们设定30例的观察例数。
1.3 围手术期处理
术前行肝脏增强CT明确门静脉系统情况,确定有无血栓并明确门静脉分支与肝静脉相对位置;明确有无肝脏占位。择期手术者,纠正低蛋白血症,使血清白蛋白达到30 g/L左右。术前2 d低蛋白饮食,防止血氨增高诱发或加重肝性脑病。纠正贫血、低血小板等情况,调整凝血功能,改善肝功能。急诊患者采用三腔管或药物止血治疗,纠正休克,血红蛋白调整至60~70 g/L,生命体征相对平稳,意识清楚,即行手术。术中予全身肝素化(普通肝素80 u/ kg),术后以普通肝素抗凝24 h,同时予保肝、降氨等治疗。
1.4 手术过程
肠系膜上动脉造影及间接门静脉造影,了解门静脉解剖及血流方向。选择性肝动脉造影,了解肝动脉解剖,注意有无原发性肝癌。将肝动脉导管选择性送至左肝动脉,间接标示门静脉脐部。右颈内静脉穿刺,成功后将导丝送入下腔静脉,引入静脉长鞘。经右肝静脉穿刺门静脉,选择右肝静脉开口处为穿刺点,在“直视”下将穿刺针向前下穿刺门静脉脐部(以左肝动脉内留置导管为参照);将导丝引入门静脉主干,侧孔造影导管行直接门脉造影及压力测定。扩张分流道:交换导丝留置肠系膜上静脉,导入球囊导管行肝内分流道扩张(通常选用直径7 mm×60mm球囊导管)。组合支架组门腔分流道建立:裸金属支架直接短路门静脉与下腔静脉(常用直径10mm,自膨式支架)。裸支架释放后,其通过肝实质部分(最窄段)获清晰显示,测量其长度。门静脉测压,下腔静脉测压,计算门腔静脉压力梯度(PSG),确认降压程度。若PSG大于设定值,可以更大直径(8~10mm)球囊再扩张分流道。根据裸支架经过肝实质段长度及球囊直径选择相应规格Fluency®覆膜支架覆盖分流道肝实质段;若PSG低于设定值,则选择较小直径Fluency®覆膜支架,以减少分流量(图1)。
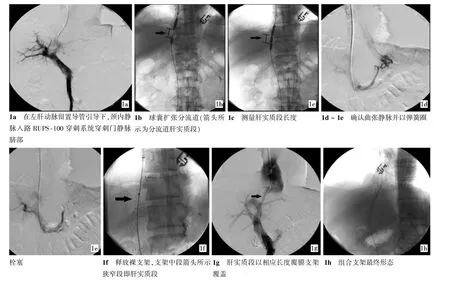
图1 组合支架组手术过程
对照组一般选择直径8 mm×8 cm Fluency®支架直接在门、腔静脉间建立分流道。
1.5 手术成功标准
①在肝静脉和门静脉分支之间成功建立分流通道。②血流动力学标准:PSG较术前降低50%。③组合支架组:覆膜支架准确覆盖肝实质段,门静脉分支血流通畅。
1.6 随访
1.6.1 术后近期(12个月)随访术后3、6、12个月定期行血常规、肝功能、凝血功能、血氨检查;腹部彩色多普勒超声、肝脏增强CT或需要时血管造影检查,了解支架通畅情况。
1.6.2 12个月后随访每6个月进行门诊随访,获取中远期生存情况,支架通畅情况,并发症发生情况。
1.7 统计学分析
采用SPSS20.0软件进行统计学分析。计量资料以K-S拟合优度检验判断是否为正态分布,符合正态分布的计量资料采用均数±标准差(±s)表示,并用t检验(其中配对资料,使用配对t检验);不符合正态分布的计量资料采用最小值~最大值(中位数)表示。计数资料采用卡方检验。生存率分析采用Kaplan-Meier法。P<0.05为差异有统计学意义。
2 结果
2.1 分组情况
组合支架组17例,对照组13例,年龄分别为(56.82±9.70)岁和(60.69±11.73)岁,组间比较差异无统计学意义(P=0.331);两组Child-Pugh评分分别为(7.76±1.86)分和(6.46±1.81)分,组间比较差异无统计学意义(P=0.064)。
2.2 手术结果
两组手术成功率均为100%。分流道经肝实质段平均长度(前后位测量)为(25.2±8.6)mm。组合支架组实际使用支架情况见表1。一般选择10mm直径裸支架与8 mm直径相应长度(一般不超过4 cm)覆膜支架进行组合。通过不同口径扩张球囊与支架组合控制分流量。

表1 组合支架组支架实际组合使用情况
2.3 PSG测量结果
组合支架组分流前和分流后的PSG分别为(28.57±7.26)mmHg和(12.52±3.12)mmHg,差异有统计学意义(P<0.000),分流后PSG平均降为分流前的43.99%±5.25%;对照组分别为(25.81± 6.62)mmHg和(11.71±4.86)mmHg,差异有统计学意义(P<0.000),分流后PSG平均为分流前的46.06%±11.69%。
为考察两组对PSG降低幅度的调控稳定性,以两组PSG比值(术后/术前)作质量控制图(图2),可见组合支架组在控制PSG方面较对照组有更稳定的结果。
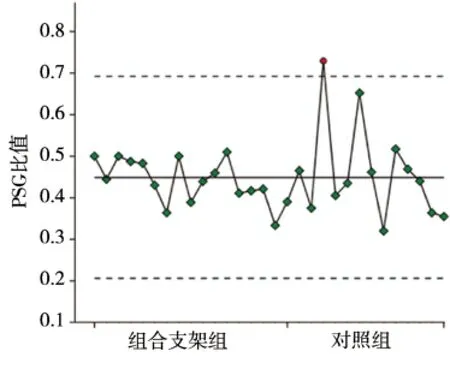
图2 组合支架组与对照组PSG比值(术后/术前)质量控制图
2.4 术后近期结果
组合支架组因肝肾功能衰竭死亡1例(术后6 d)。术后次日,组合支架组平均血氨为(92.5± 45.6)μmol/L(参考上限为47μmol/L),对照组为(76.2±35.8)μmol/L,组间差异无统计学意义(P= 0.298)。术后5 d,血氨明显下降,组合支架组平均为(65.5±21.2)μmol/L,对照组为(58.1±17.7)μmol/ L。术后次日与第5天血氨水平比较,组合支架组血氨下降差异有统计学意义(P=0.029),对照组差异无统计学意义(P=0.065)。
2.5 远期结果
除术后近期死亡1例外,余29例均获随访,随访中位数时间为168 d(61~563 d)。
2.5.1 生存情况随访中,组合支架组死亡3例,死亡原因分别为败血症(术后61 d),肝性脑病(术后75 d),原发性肝癌远处转移,肝功能衰竭(术后106 d);对照组死亡3例,死亡原因分别为肝肺综合症(术后69 d),肝肾功能衰竭(术后84 d),原发性肝癌肝内播散,肝功能衰竭(术后106 d)。Kaplan-Meier生存函数(图3)显示,两组生存率差异无统计学意义(χ2=0.014,P=0.906)。
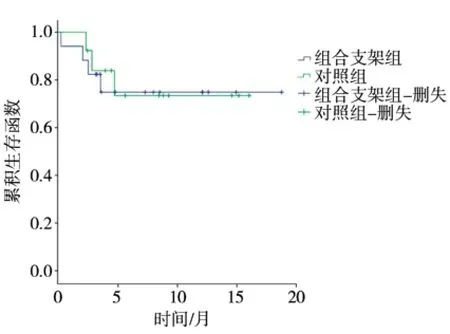
图3 组合支架组与对照组Kaplan-Meier生存函数
2.5.2 门静脉分支通畅率组合支架组门静脉左右支通畅11例,血栓形成2例;对照组门静脉左右支通畅4例,门静脉左支血栓形成6例,组间差异有统计学意义(χ2=4.960,P=0.039)。
2.5.3 分流道通畅情况23例长期存活者,至随访结束分流道支架均通畅,未再发生消化道出血。
2.5.4 其他情况3例发生肝性脑病(组合支架组2例,对照组1例),门诊经药物治疗后缓解。23例长期存活者,Child-Pugh评分术前平均为(7.1± 2.0)分,随访结束时为(7.0±1.9)分,差异无统计学意义(P=0.700)。随访结束时,组合支架组Child-Pugh评分为(7.5±1.8)分,对照组为(6.3±1.8)分,组间差异无统计学意义(P=0.138)。
3 讨论
在临床应用中,一直在力求改进TIPS术的疗效,表现在提高分流通道(支架)通畅率、合理调控分流量以及减少肝性脑病及肝功能衰竭发生。近年来,已经证明覆膜支架在提高支架通畅率方面较裸金属支架优越[7-8];更有了已商业化的TIPS专用支架(Viatorr®)。Viatorr®支架分为裸区和覆膜区,在释放时需要特殊的定位技术,操作上有一定难度,有时因为定位不精确,需要另外放置支架修正[5]。覆膜支架(如Fluency®)或专用支架(Viatorr®)的覆膜区,主要是通过覆盖肝静脉-门静脉间通道的肝实质部分,减少胆汁等对支架的影响提高通畅率;但超范围的覆盖会影响门静脉分支血供,形成血栓,影响肝功能,我们在以前的病例随访中已发现此现象[9]。精确定位是覆膜支架,特别是Viatorr®支架成功释放的基本技术要求。
为实现覆膜支架精确覆盖肝实质段,我们设计了组合支架。以组合支架建立门腔静脉分流道的设计受文献中对TIPS术后肝性脑病患者治疗的启发,即在原分流道支架内通过再置入裸支架组合[10]或置入球扩覆膜支架联合裸支架组合实现分流量的调控[11]。我们设想以祼支架联合覆膜支架的形式建立分流道,通过球囊扩张及第1枚祼支架的释放(图1),分流道肝实质段得到清晰显示及准确测量,减少覆膜支架精确释放的难度,提高定位准确性。这一优势见于Viatorr®支架的释放过程。实际使用中,可见较多采用组合使用情况,如Viatorr®联合祼支架,Viatorr®联合Fluency®等[12],大多是因为支架释放过程中,定位准确性难以保证而采取的补救措施。
经实际测量,分流道肝实质段长度一般在2~4 cm(表1),远小于TIPS手术中常用支架的长度(8 cm),从保留门静脉分支血供的角度,门腔静脉间全程以覆膜支架建立分流道不利。而组合支架,以较短长度覆膜支架准确覆盖肝实质段,将能保证门静脉相应分支血供,减少血栓形成。实际应用中,组合支架释放的技术成功率达100%,通过精确定位,门静脉分支血供全部得以保留。而对照组,应用全程覆膜支架将不可避免在释放后阻隔穿刺侧门静脉分支(左或右支)血流,结果局部门静脉血栓形成,相应侧肝脏门脉血供永久丧失。至随访结束,组合支架组11/13例门静脉分支通畅,而对照组4/10例门静脉分支通畅,组间差异有统计学意义。门脉血是肝脏的主要营养血供,对于处于功能代偿期的硬化肝脏,任何1支门脉分支血供的中断,理论上都将会加快相应侧肝脏功能衰竭的速度,因此,尽量维持左右门静脉分支供血,对于肝功能的稳定有重要意义。
TIPS术中,PSG的合理控制是保证术后长期疗效的另一关键环节。实现主动调控有利于在保证门静脉降压的同时,减少因过度分流引起肝功能衰竭。组合支架组通过不同口径支架、球囊的组合应用,以及多次门静脉测压,逐步操作,为实现PSG质量控制提供了可能。
TIPS术后次日,所有患者血氨水平皆明显升高,平均达到正常上限值2倍以上,术后5 d,即迅速降至正常上限1.5倍以下,所有病例均无明显临床症状。血氨在术后近期的下降,得益于术后常规的降氨措施及人体的生理代偿。
至随访结束,组合支架组与对照组在支架通畅率、再出血率、肝性脑病发生率、肝功能Child-Pugh评分、生存率方面差异均无统计学意义,在有限随访期内,两组整体治疗效果等同。
总之,通过随机对照研究,与传统单一覆膜支架技术相比,组合支架技术在支架准确定位、保证门静脉分支通畅率、稳定血氨及PSG控制方面显示出一定优越性;在术后近期,支架通畅率、肝性脑病发生率、再出血率、生存率等方面与单一覆膜支架技术效果相似,其长期临床效果仍有不确定性,有待长时间随访观察。
[1]Bosch J,Abraldes JG,Groszmann R.Current management of portal hypertension[J].JHepatol,2003,38:S54-S68.
[2]Boyer T,Haskal Z.AASLD practice guidelines:the role of transjugular intrahepatic portosystemic shunt(TIPS)in the managementof portalhypertension[J].Hepatology,2010,51:1-16.
[3]Vignali C,Bargellini I,Grosso M,et al.TIPS with expanded polytetrafluoroethylene-covered stent:results of an Italian multicenter study[J].Am JRoentgenol,2005,185:472-480.
[4]Maleux G,Nevens F,Wilmer A,et al.Early and long-term clinical and radiological follow-up results of expandedpolytetrafluoroethylene-covered stent-grafts for transjugular intrahepatic portosystemic shunt procedures[J].Eur Radiol,2004,14:1842-1850.
[5]Hausegger KA,Karnel F,Georgieva B,et al.Transjugular intrahepatic portosystemic shunt creation with the Viatorr expanded polytetrafluoroethylene-covered stent-graft[J].JVasc Interv Radiol,2004,15:239-248.
[6]童玉云,王家平,朱清亮,等.肝硬化门脉高压患者经颈静脉肝内门腔分流术后肝功能随访及疗效评估[J].介入放射学杂志,2013,22:540-544.
[7]Jung HS,Kalva SP,Greenfield AJ,et al.TIPS:comparison of shunt patency and clinical outcomes between bare stents and expanded polytetrafluoroethylene stent-grafts[J].JVasc Interv Radiol,2009,20:180-185.
[8]Rossi P,Salvatori FM,Fanelli F,et al.Polytetrafluoroethylenecovered nitinol stent-graft for transjugular intrahepatic portosystemic shunt creation:3-year experience[J].Radiology,2004,231:820-830.
[9]滕磊磊,吕献军,李选,等.经颈静脉门体分流术治疗门脉高压症所致曲张静脉出血及腹水疗效观察[J].传染病信息,2012,25:208-212.
[10]Jacquier A,Vidal V,Monnet O,et al.A modified procedure for transjugular intrahepatic portosystemic shunt flow reduction[J].JVasc Interv Radiol,2006,17:1359-1363.
[11]Weintraub JL,Mobley DG,Weiss ME,et al.A novel endovascular adjustable polytetrafluoroethylene-covered stent for the management of hepatic encephalopathy after transjugular intrahepatic portosystemic shunt[J].JVasc Interv Radiol,2007,18:563-566.
[12]Saad WE,Darwish WM,Davies MG,et al.Transjugular intrahepatic portosystemic shunts in liver transplant recipients for management of refractory ascites:clinical outcome[J].J Vasc Interv Radiol,2010,21:218-223.
Combined-stent covered technique and single covered stent technique for transjugular intrahepatic porto-system ic shunt:a prospective random ized controlled study
WANG Chang-ming,LIXuan,FU Jun,LV Xian-jun,LUAN Jing-yuan,LI Tian-run,ZHAO Jun,DONG Guo-xiang.Department of Interventional Vascular Surgery,Third Hospital of Peking University,Beijing 100191,China
LIXuan,E-mail:lixuanbysy@163.com
ObjectiveTo compare the technique of combined stentswith thatof single stent-graft for the construction of transjugular intrahepatic porto-systemic shunt(TIPS)and to discuss their clinical outcomes.MethodsDuring the period from April 2011 to Dec.2012,a total of 30 patients with upper gastrointestinal bleeding due to portal hypertension were admitted to the hospital.TIPS procedure was carried out in all the 30 patients.The patients were random ly allocated into either combined-stent group(n=17)or stent-graft group(control group,n=13)on the basis of a computer-generated randomization sequence.The PSG quality control,the patency rate of portal vein branches and the shunts,the incidence of encephalopathy and the survival rate of the two groups were documented and analyzed.ResultsTechnical success rate was 100%.After the treatment,in both groups the PSG became significantly lower than the PSG determined before the treatment(P<0.000).According to quality control chart,the of combined stentswas superior to stent-graft technique in effectively controlling PSG.Five days after TIPS,the ammonia level in the combinedstent group was significantly decreased(P=0.029),while in the control group the ammonia level showed no significant changes(P=0.065).One patient died shortly after TIPS.The median followup time was 181 days.During the follow-up period death occurred in 3 cases in each group.The difference in the survival rate between the two groups was no significant(P=0.906).Of the three patientswho developed encephalopathy,two were in the combined-stent group and one was in the control group.A fter medication the symptoms of encephalopathy were relieved.The patency rate of the shuntswas 100%and the re-bleeding rate was 0%for both groups.The patency rate of portal vein branches was significantly higher in the combined-stent group than that in the control group(P=0.039). Conclusion For the construction of TIPS,the technique of combined-stent is superior to single stent-graft technique.The advantages of combined-stent technique are as follows:the accurate position of stents,the patency rate of portal branches,the stabilization of ammonia,themodification of PSG,etc.Nevertheless,the rate of shunt patency,the incidence of re-bleeding as well as encephalopathy,and the survival rate of the two groups are similar.(JIntervent Radiol,2014,23:18-23)
portal hypertension;esophageal and gastric varices;radiology,interventional;stent
R575.2
A
1008-794X(2014)-01-0018-06
2013-08-05)
(本文编辑:侯虹鲁)
10.3969/j.issn.1008-794X.2014.01.006
100191北京大学第三医院介入血管外科(李选、王昌明、傅军、栾景源、李天润、赵军、董国祥);南京明基医院放射科(吕献军)
李选E-mail:lixuanbysy@163.com