评价HPPH对细胞色素P450酶体外代谢活性的影响
刘晓强 ,袁淋文 ,臧 敏 ,曹 云 ,王 丹 ,杨 劲 *,孔 毅 *
1中国药科大学生命科学与技术学院,南京 210009;2中国药科大学药学院,南京210009
肝脏是机体最重要的药物代谢器官之一,细胞色素P450酶系(CYP450)是药物在肝脏内氧化代谢最主要和最重要的酶,是临床前药物代谢研究的重要 对 象 。 其 中 CYP1A2、CYP2C9、CYP2C19、CYP2D6、CYP2E1和CYP3A4是其中最主要的6种亚型,其含量约占肝脏内CYP450酶总量的80%以上,且90%以上的上市药物由这6种亚型代谢的,在已经发现的药物相互作用中,CY P450酶系引起的药物相互作用约占全部相互作用的70%。肝微粒体孵育试验可以在亚细胞水平上确定药物代谢稳定性、药物对细胞色素酶各亚型的调控等重要特性[1]。在新药研发过程中常通过评估新药对CY P450酶特异性探针底物在体外孵育体系(如人肝微粒体和大鼠肝微粒体的CY P450酶)中代谢的影响程度,判断该药物对CY P450酶的抑制作用[2],从而预测它在体内可能引起的药物相互作用,为进一步的临床药物相互作用试验提供有价值的信息。
HPPH属于我国药品注册管理办法化学药品注册分类1.1类新药,尚未在国内外上市销售,为第二代抗肿瘤光敏剂,分子式为C39H48N4O4,相对分子量为636.37,属于结构单一、长激发波长、暗毒性[3-5]小的二氢卟酚类,具体结构见图1。HPPH具有很好的光动力活性,理想的作用光谱以及很好的靶向性,对肿瘤组织的穿透率高,临床用于肺癌、食管癌、头面颈癌、膀胱癌、胃癌等多种实体肿瘤的治疗;较第一代相比,其光毒性明显降低,基本不需要避光,用量小,使用方便,是一种极富市场潜力的光动力疗法[6-8]、治疗癌症用的光敏剂。
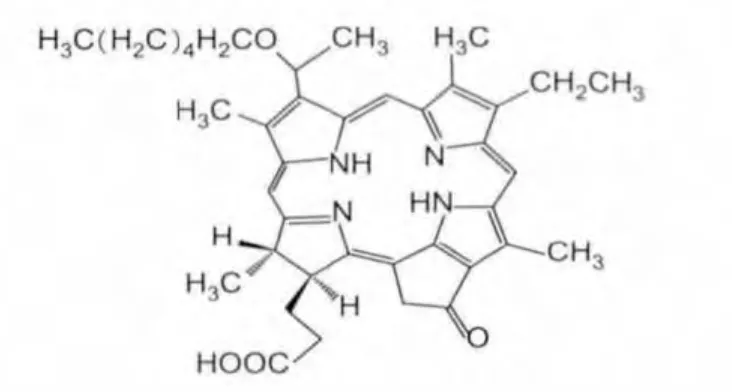
图1 HPPH结构
Cocktail探针底物法是指同时给予多种相对低剂量的探针药物,测定生物样本中每个探针药物的代谢率或其他代谢分型指标,以获取多个代谢酶的表型信息。本实验采用体外cocktail法研究注射用HPPH对细胞色素P450酶的6种主要亚型 (包括CYP1A2、CYP2C9、CYP2C19、CYP2D6、CYP2E1、CYP3A4)是否存在抑制作用,为是否进行临床人体内药物相互作用研究提供线索。
1 材 料
1.1 药品与试剂
注射用HPPH(浙江海正药业股份有限公司提供);α-萘黄酮、非那西汀、奎宁丁、甲苯磺丁脲、磺胺苯吡唑、4-甲基吡唑、酮康唑、氯唑沙宗、(S)-美芬妥因、盐酸噻氯匹定、O-去甲基右美沙芬酒石酸盐、6-羟基氯唑沙宗、羟基甲苯磺丁脲均购于百灵威科技有限公司;1-羟基咪达唑仑、4-羟基美芬妥因、对乙酰氨基酚、右美沙芬均购于瑞德肝脏疾病研究(上海)有限公司;马来酸咪达唑仑购于中国药品生物制品检定所;甲醇(色谱纯,Merck Co.Ltd.);乙酸乙酯(色谱纯,Roe Scientific INC);其余试剂均为市售分析纯;水为自制超纯水。
1.2 仪器
API3000液相串联质谱联用仪,含:自动进样器、在线脱气系统、柱温箱、二元梯度泵、电喷雾离子化接口、三重四极杆质谱检测器、色谱工作站(Analyst 1.4.2);BT25X型分析天平(北京赛多利斯仪器系统有限公司);3K15高速冷冻离心机(Sigma公司,美国);优普超纯水制造系统;H-101型多功能漩涡混合器(上海医科大学仪器厂);单道移液器(Thermo Electron 公司,美国)。
1.3 动物
Sprague Dawley(SD)大鼠 12 只,6~8 月龄,SPF级,雄性,体重200~230 g,由上海西普尔-必凯试验动物有限公司中心提供,许可证号SCXK(沪)2008-0016。
1.4 肝微粒体来源[10]
按文献[10]的方法制备大鼠肝微粒体,用考马斯亮蓝染料结合比色法测定所制备的大鼠肝微粒体的蛋白含量;混合人肝微粒体由瑞德肝脏疾病研究(上海)有限公司提供。
2 方 法
2.1 色谱条件
色谱柱 Phenomenex C18柱(150 mm×2.00 mm,4 micron.);流动相:1‰甲酸水溶液-甲醇;柱温:35℃;进样量:5 μL;内标:格列吡嗪。
2.2 质谱条件
见表1。
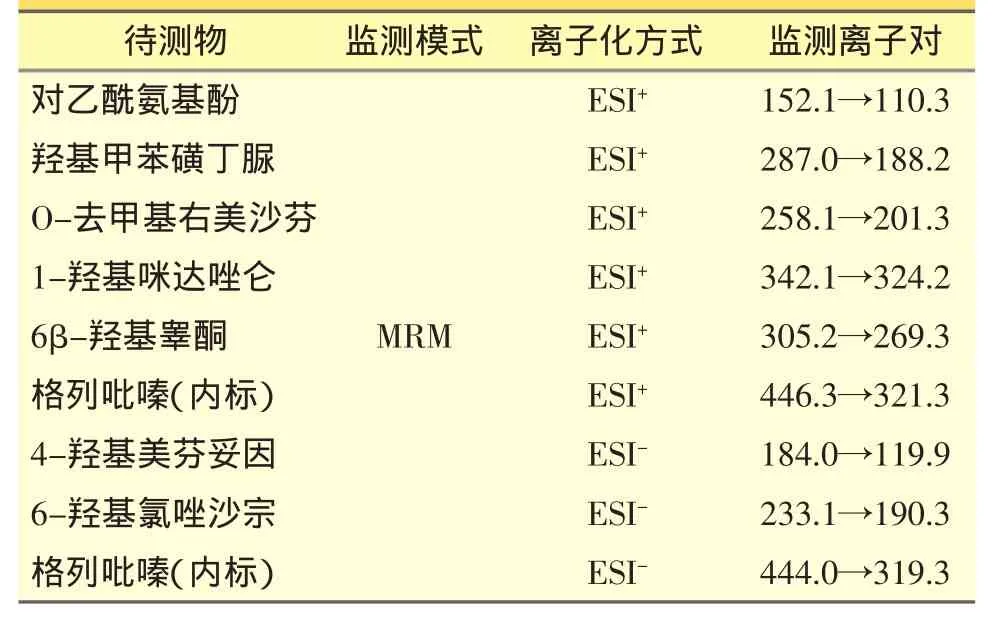
表1 质谱条件
3 孵育实验
3.1 酶活性指标
各亚酶所选择的探针底物、其代谢产物(见表2)以及特异性抑制剂(见表3)[11-15],以各底物代谢产物生成量的多寡来评价对应酶的活性。
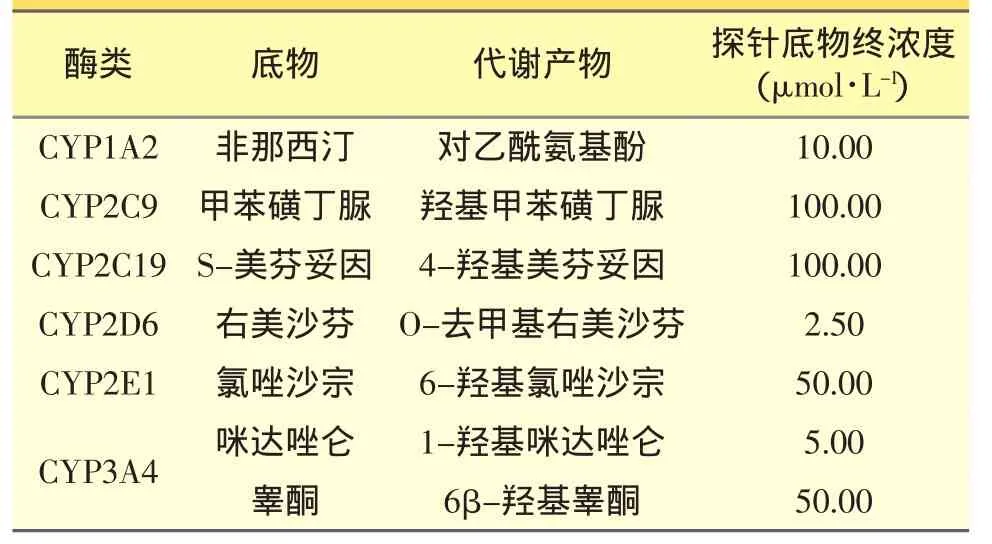
表2 各亚酶的探针底物、其代谢产物及探针底物终浓度

表3 各亚型抑制剂的选择以及抑制剂的终浓度
3.2 微粒体体外孵育体系
每个孵育体系总体积200 μL,反应体系中包含NADPH(1 mmol·L-1)、微粒体蛋白(0.5 mg·mL-1)、PBS缓冲液(pH 7.4)、底物、HPPH及各种已确认的抑制剂,反应体系中甲醇终体积分数小于1%。反应在37℃水浴中进行,预孵5 min,加入NADPH启动反应,30 min后,加冰乙酸乙酯1 mL终止反应。
3.3 实验设计
本实验采用cocktail法和单一温孵结合的方法进行实验,各分为9组,共18组,每组平行制备3份。其中9组以混合底物[非那西汀(CYP1A2)、甲苯磺丁脲(CYP2C9)、S-美芬妥因(CYP2C19)、右美沙芬 (CYP2D6)、 氯唑沙宗 (CYP2E1)、 咪达唑仑(CYP3A4)]进行实验;9组单独以CYP3A4酶的特异性底物睾酮进行实验。各自分别设为纯阴性对照组A(不含NADPH)、阴性对照组B、低浓度阳性对照组C、高浓度阳性对照组D、低浓度HPPH实验组E、次低浓度HPPH实验组F、中浓度HPPH实验组G、次高浓度HPPH实验组H、以及高浓度HPPH实验组I。分组方案见表4。

表4 温孵实验分组方案
根据初步的药效学和安全性试验结果设计给药剂量,以大鼠中剂量组血药浓度范围来设计大鼠肝微粒体HPPH浓度,鼠微粒体温孵实验HPPH浓度 从 低 到 高 依 次 为 1.00、5.00、10.00、25.00、50.00 μmol·L-1。HPPH浓度一次为以比格犬中剂量组血药浓度范围来设计人鼠肝微粒体HPPH浓度,人微粒体温孵实验中HPPH浓度从低到高依次为0.50、1.00、2.00、5.00、10.00 μmol·L-1。
3.4 微粒体温孵样品处理方法
温孵结束后,加入置于-18℃冰箱冷藏的乙酸乙酯 1000 μL,内标 10 μL,涡旋混匀 3 min,15000 r·min-1离心5 min,取上清液至干净玻璃离心管中,置于氮吹仪下40℃吹干,取200 μL流动相复溶,涡旋混匀 1 min,吸取上清液 50 μL 至进样瓶中,5 μL 进样。
4 结果与数据统计
4.1 大鼠肝微粒体孵育实验结果
经大鼠肝微粒体孵育后,各底物的代谢产物生成量变化情况见表5。
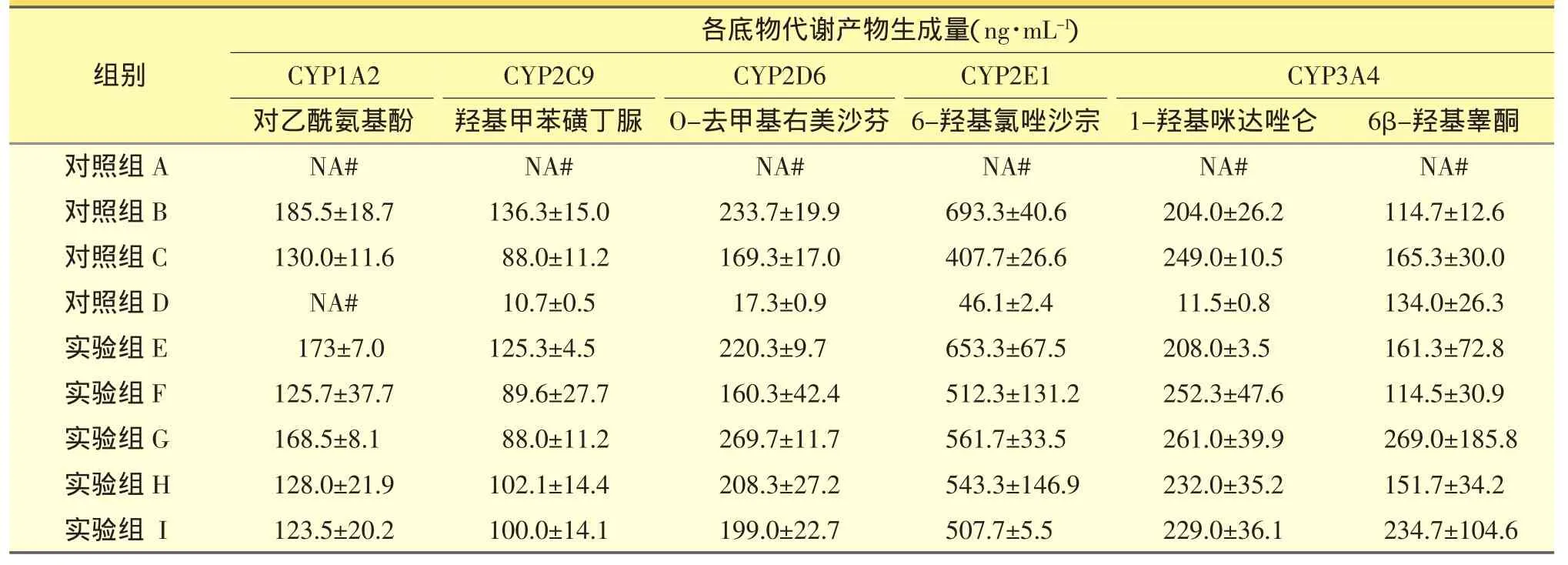
表5 大鼠肝微粒体孵育后代谢产物生成量细表(n=3)
在特异性抑制剂的作用下各亚酶底物代谢物生成量均明显减少,表明上述亚酶活性良好。用SPSS 11.5(IBM SPSS)单因素方差分析得出,上述5种CYP450酶在特异性抑制剂的作用下,其探针底物代谢产物生成量均未明显减少(P>0.05),差异不具有统计学意义。因而当HPPH浓度为1.00~50.00 μmol·L-1时 , 大 鼠 CYP1A2、CYP2C9、CYP2D6、CYP2E1和CYP3A4的各探针底物代谢产物生成量与对照组对比差异均无统计学意义(P>0.05)。从上述结果看出,在本实验条件下未发现注射用HPPH对 大 鼠 的 CYP1A2、CYP2C9、CYP2D6、CYP2E1、CYP3A4产生抑制作用。
4.2 混合人肝微粒体孵育实验结果
经混合人肝微粒体孵育后,各底物的代谢产物生成量变化情况见表6。
用SPSS 11.5(IBM SPSS)进行单因素方差分析得出,HPPH 在 0.50~10.00 μmol·L-1时,人 CYP1A2的探针药物代谢产物生成量与对照组对比差异均无统计学意义(P>0.05);因而在本实验条件下,未发现HPPH对人CYP1A2存在抑制作用。人CYP2C9、CYP2C19、CYP2D6、CYP2E1 各探针药物代谢产物生成量与对照组对比差异有统计学意义 (P<0.05);说明在本实验条件下HPPH对人CYP2C9、CYP2C19、CYP2D6、CYP2E1 存在抑制作用; 利用SPSS 11.5软件求得HPPH对人CYP2C9、CYP2C19、CYP2D6、CYP2E1 的 IC50值分别为:5.28 μmol·L-1、10.00 μmol·L-1、2.28 μmol·L-1、5.64 μmol·L-1。 而 HPPH 在 0.50~10.00 μmol·L-1时 , 对 人CYP3A4,底物咪达唑仑代谢产物生成量与对照组比较差异有统计学意义(P<0.05),对底物咪达唑仑存在抑制作用,经SPSS 11.5软件分析得IC50值为5.17 μmol·L-1;底物睾酮代谢产物生成量与对照组对比差异均无统计学意义(P>0.05),因而在本实验条件下未发现HPPH对底物睾酮产生抑制作用。
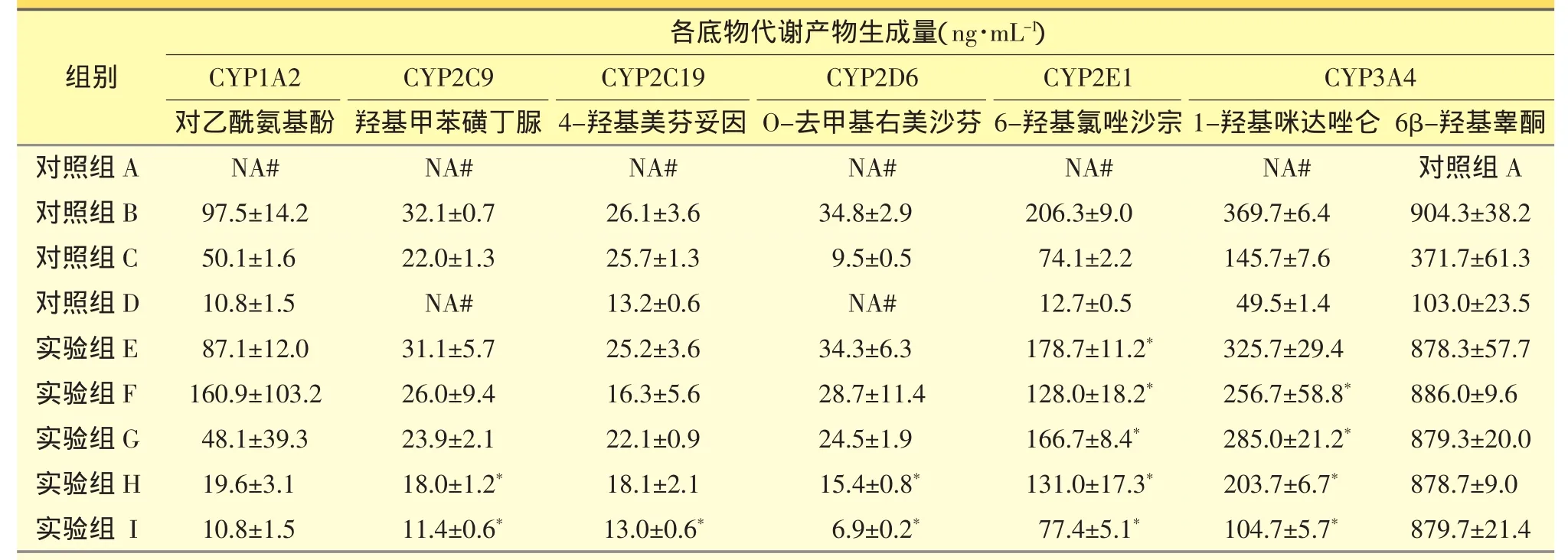
表6 混合人肝微粒体孵育后代谢产物生成量变化情况(n=3)
5 讨 论
经验证,建立的方法为:对乙酰氨基酚、羟基甲苯磺丁脲、O-去甲基右美沙芬、1-羟基咪达唑仑的正离子LC-MS/MS检测方法;4-羟基美芬妥因、6-羟基氯唑沙宗的负离子LC-MS/MS检测方法以及6β-羟基睾酮的LC-MS/MS测定方法。肝微粒体温孵液中的杂质不干扰样品的测定,对乙酰氨基酚、羟基甲苯磺丁脲、4-羟基美芬妥因、6-羟基氯唑沙宗以及的6β-羟基睾酮标准曲线线性范围为10~1000 ng·mL-1,O-去甲基右美沙芬、1-羟基咪达唑仑的标准曲线线性范围为5~500 ng·mL-1,且线性关系良好;高、中、低3种浓度的批内、批间精密度RSD均小于15%;准确度均在85%~115%;样品的提取回收率为80%左右,样品无明显介质效应,符合生物样品分析要求。
本实验中采用的大鼠肝微粒体为普通大鼠肝微粒体,其体内CYP2C19表达很弱,故而未鉴定其探针底物的代谢产物。由于仪器响应、温孵操作等原因导致某些物质响应可能不稳定,因而致使某些数据异常,但是总体趋势是对的,在本实验条件下未发现抑制作用的酶其底物代谢产物的生成量呈平缓趋势,在本实验条件下发现抑制作用的酶其底物代谢产物的生成量呈下降趋势。大鼠肝微粒温孵结果与混合人肝微粒体温孵结果的差异提示HPPH对CYP450的抑制作用可能存在种属差异。
根据大鼠药代、大鼠组织分布以及比格犬药代结果,且假设大鼠与人的血浆组织抽提比相同,人体肝组织的最高浓度仅为0.3 μmol·L-1左右,远远低于上述计算得到的IC50值。同时注射用HPPH采用的单次给药的方式,因而其在机体内不会产生蓄积作用。结合上述两点,推测HPPH在人体内对所研究的各CYP450亚型不存在抑制作用或者仅存在较弱的抑制作用。
[1]侯丛颂,杨志宏,孙晓波.“cocktail”探针药物法及其在研究中药对细胞色素P450影响中的应用进展[J].中国药理学与毒理学杂志,2013,27(3):445-50.
[2]Zientek M,Miller H,Smith D,et al.Development of an in vitro drug-drug interaction assay to simultaneously monitor five cytochrome P450 isoforms and performance assessment using drug library compounds[J].J Pharmacol Toxicol Methods,2008,58(3):206-214.
[3]李忠明.光动力学治疗原理与影响因素(英文)[J].咸宁学院学报,2004,24(6):62-8.
[4]Wang Zhenya.Research progress on photodynamic diagnosis and photodynamic therapy of tumors[J].Photoelectric Technique and Information,1998,11(6):1-9+28.
[5]陈靖京.卟啉类光敏抗肿瘤化合物评价 [D].北京协和医学院,2011:35.
[6]Juzeniene A,Nielsen KP,Moan J,Biophysical aspects of photodynamic therapy[J].J Environ Pathol Toxicol Oncol,2006,25(1):7-28.
[7]Niedre M,Patterson MS,Wilson BC.Direct near-infrared luminescence detectionof singlet oxygen generated by photodynamic therapy in cells in vitro and tissues in vivo[J].Photochem Photobiol,2002,75(4):382-91.
[8]Wright A,Bubb WA,Hawkins CL,et al.Singlet oxygen-mediated protein oxidation:evidence for the formation ofreactive side chain peroxides on tyrosine residues[J].Photochem Photobiol,2002,76(1):35-46.
[9]呼自顺,王 琤,张 弋,等.Cocktail探针药物法评价黄芩对大鼠CYP450活性的影响 [J].中国医院药学杂志,2010,30(2):108-10.
[10]郭海方,邹晓丽,许 卉,等.丹参酚酸A对大鼠肝微粒体细胞色素P450酶系的影响 [J].中国中药杂志,2010,35(3):348-51.
[11]孙鲁宁,丁 黎,严拯宇,等.LC-MS/MS法研究苯环喹溴铵对大鼠肝微粒体CYP450酶的抑制作用 [J].中国药科大学学报,2013,44(2):134-40.
[12]熊海伟,文红梅,徐智勇,等.探针药物评价藤黄酸对肝细胞色素P450酶亚型的影响 [J].中药新药与临床药理,2010,21(1):40-3.
[13]He F,Bi H,Xie Z,et al.Rapid determination of six metabolites from multiple cytochrome P450 probe substratesin human livermicrosome by liquid chromatography/massspectrometry:application to highthroughput inhibition screening of terpenoids[J].Rapid Commun Mass Spectrom,2007,21(5):635-643.
[14]郑 姣,周宏灏.黄酮类化合物对细胞色素P450 CYP1,2E1,3A4 和 19 的影响 [J]. 药学学报,2007,42(1):8-12.
[15]Youdim KA,Lyons R,Payne L,et al.An automated,high-throughput,384 well Cytochrome P450 cocktail IC50assay using a rapid resolution LC-MS/MS endpoint[J].J Pharm Biomed Anal,2008,48(1):92-9.

