羊毛角蛋白溶液的离子液体法制备
孙艳丽, 姚金波, 李 博, 贾书刚
(1. 天津工业大学 纺织学院, 天津 300160; 2. 武汉纺织大学 化学与化工学院,湖北 武汉 430073)
羊毛角蛋白溶液的离子液体法制备
孙艳丽1, 姚金波2, 李 博1, 贾书刚1
(1. 天津工业大学 纺织学院, 天津 300160; 2. 武汉纺织大学 化学与化工学院,湖北 武汉 430073)
以离子液体1-烯丙基-3-甲基咪唑氯盐([AMIM]Cl)为主溶剂,以巯基乙醇为辅助试剂,研究了羊毛纤维在该溶剂体系中的溶解行为。正交试验结果表明,在m(羊毛)∶m( [AMIM]Cl)∶m(巯基乙醇)=1∶8.5∶1、温度为120 ℃、时间为7.5 h的条件下,羊毛纤维可全部溶解。分析可知,离子液体[AMIM]Cl的强极性作用利于打开纤维内部的氢键,巯基乙醇可有效拆开二硫键,再辅以机械搅拌的剪切作用,可使纤维解体直至溶解。
离子液体; 溶解; 羊毛纤维; 角蛋白
羊毛具有许多优良的特性,如弹性好,手感丰满,吸湿能力强,保暖性好,不易沾污,光泽柔和,独特的缩绒性等[1],然而,羊毛纤维在经历使用周期后将成为废弃物。在现有的羊毛资源中,除品质优良的羊毛已得到充分的利用外,还有大量品质较差的粗短毛以及纺织加工过程中形成的短绒等,它们因无纺织利用价值而成为废弃物。上述废弃物不仅带来了环境压力,而且也是对优质角蛋白资源的浪费。因此,如何充分利用这些资源已经引起了各行各业的关注,尤其希望将其溶解进而制取再生角蛋白。
离子液体是近年来新生的环保型溶剂,具有不挥发、溶解强、可调节、易回收等特性[2]。离子液体是由有机阳离子和无机/有机阴离子构成,在室温呈液体状态的盐类[3]。目前,离子液体多用于溶解纤维素[4-5],但由于离子液体能够有效拆开氢键,近年来人们开始关注离子液体法溶解羊毛的研究[6-7]。
为获得高制得率、高分子质量的角蛋白溶液,本文在选用离子液体的基础上,加入适量的巯基乙醇以有效打开角蛋白分子间—S—S—,进而提高溶剂体系的溶解能力。
1 试验部分
1.1 试验材料、试剂与设备
材料:羊毛毛条66支。试剂:巯基乙醇,分析纯,天津市科密欧化学试剂有限公司;1-烯丙基-3-甲基咪唑氯盐([AMIM]Cl),上海成捷化学有限公司;亚硫酸氢钠(NaHSO3),分析纯,天津市化学试剂研究所;碳酸钠(Na2CO3),分析纯,天津市化学试剂研究所;无水乙醇,分析纯,天津市风船化学试剂科技有限公司;二氯异氰尿酸(DCCA),天津市化学试剂研究所。设备:数显磁力搅拌器,巩义市英峪仪器厂;DYY-6C型电泳仪,北京市六一仪器厂; BA2000电子显微镜,天津市二十八中仪器厂。
1.2 羊毛去鳞片处理
羊毛去鳞片工艺为:DCCA 6%(o.w.f)、浴比1∶25、pH值4.5、温度25 ℃的条件下处理90 min;40 ℃、NaHSO33%(o.w.f)、浴比1∶25条件下处理15 min后,加入Na2CO3将pH值调节至8~9处理15 min,取出水洗,自然晾干。
1.3 离子液体与巯基乙醇对羊毛的溶解
将1 g去鳞片的羊毛纤维分别置于不同配比的溶剂体系中,观察不同温度下的溶解效果,以溶解时间和SDS-PAGE凝胶电泳作为考察指标,正交试验设计如表1、2所示。
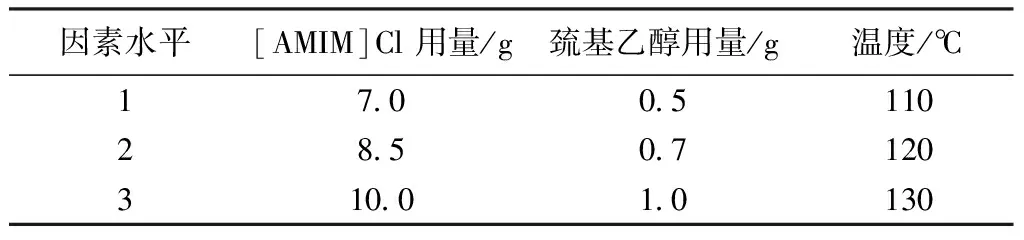
表1 羊毛溶解的正交试验因素水平表Tab.1 Orthogonal factor level of dissolving of wool
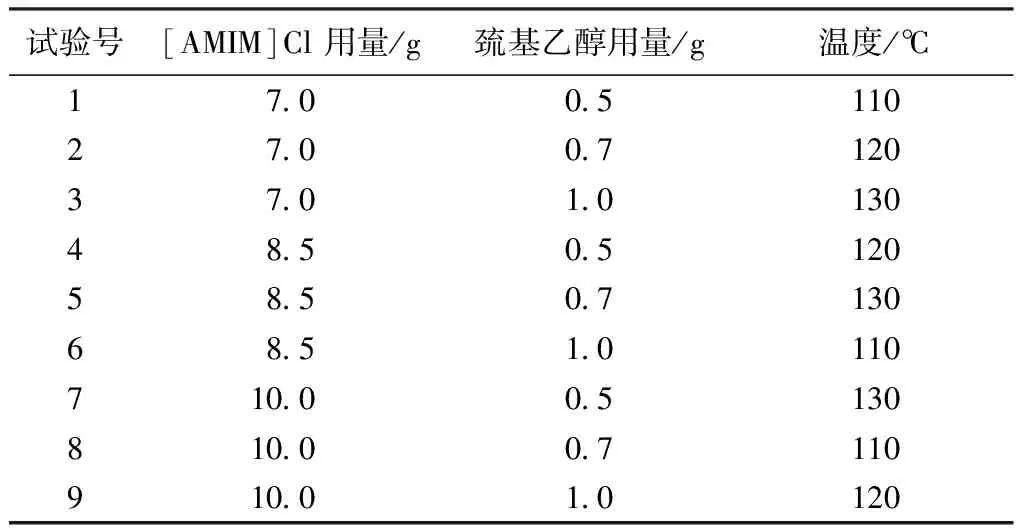
表2 羊毛溶解的正交试验Tab.2 Orthogonal experiment of dissolving of wool
1.4 羊毛鳞片对溶解的影响
去鳞片的羊毛纤维和未去鳞片的羊毛纤维各1 g,分别置于8.5 g[AMIM]Cl、1 g巯基乙醇组成的溶剂体系中,于120 ℃、机械搅拌(700 r/min)的条件下进行溶解。用显微镜观察溶解效果,溶解时间和SDS-PAGE凝胶电泳作为考察指标。
1.5 巯基乙醇对溶解的影响
分别取2份1 g去鳞片处理的羊毛按表3的试验方案进行溶解,具体试验安排如表3。用显微镜观察溶解效果,溶解时间和SDS-PAGE凝胶电泳作为考察指标。

表3 溶解工艺对比Tab.3 Comparison dissolving process
1.6 测试方法
1.6.1 显微镜观察
在试样的溶解过程中,使用显微镜在放大100倍条件下拍摄记录羊毛溶解状态。为了方便观察,用弱酸性红染料进行着色。
1.6.2 凝胶电泳(SDS-PAGE)
采用SDS-聚丙烯酰胺(SDS-PAGE)凝胶电泳法。分离胶15%、浓缩胶5%,垂直平板电泳,加样量5 μL,电极缓冲液Tris-HCl(pH=8.3)系统,电压80 V。标准蛋白Marker(14.4、22、31、43、66.2、97.4 ku)。
2 结果与讨论
2.1 羊毛鳞片对溶解的影响分析
按1.4的方法进行试验,羊毛去鳞片溶解时间为7.5 h,羊毛未去鳞片溶解时间为9 h,具体溶解状态及分子质量分布结果见图1、2。

图1 溶解效果对比(×100)Fig.1 Comparison of dissolving effect(×100). (a) Dissolving effect of removing scales; (b) Dissolving effect of keeping scales; (c) Dissolving effect without mercaptoethanol
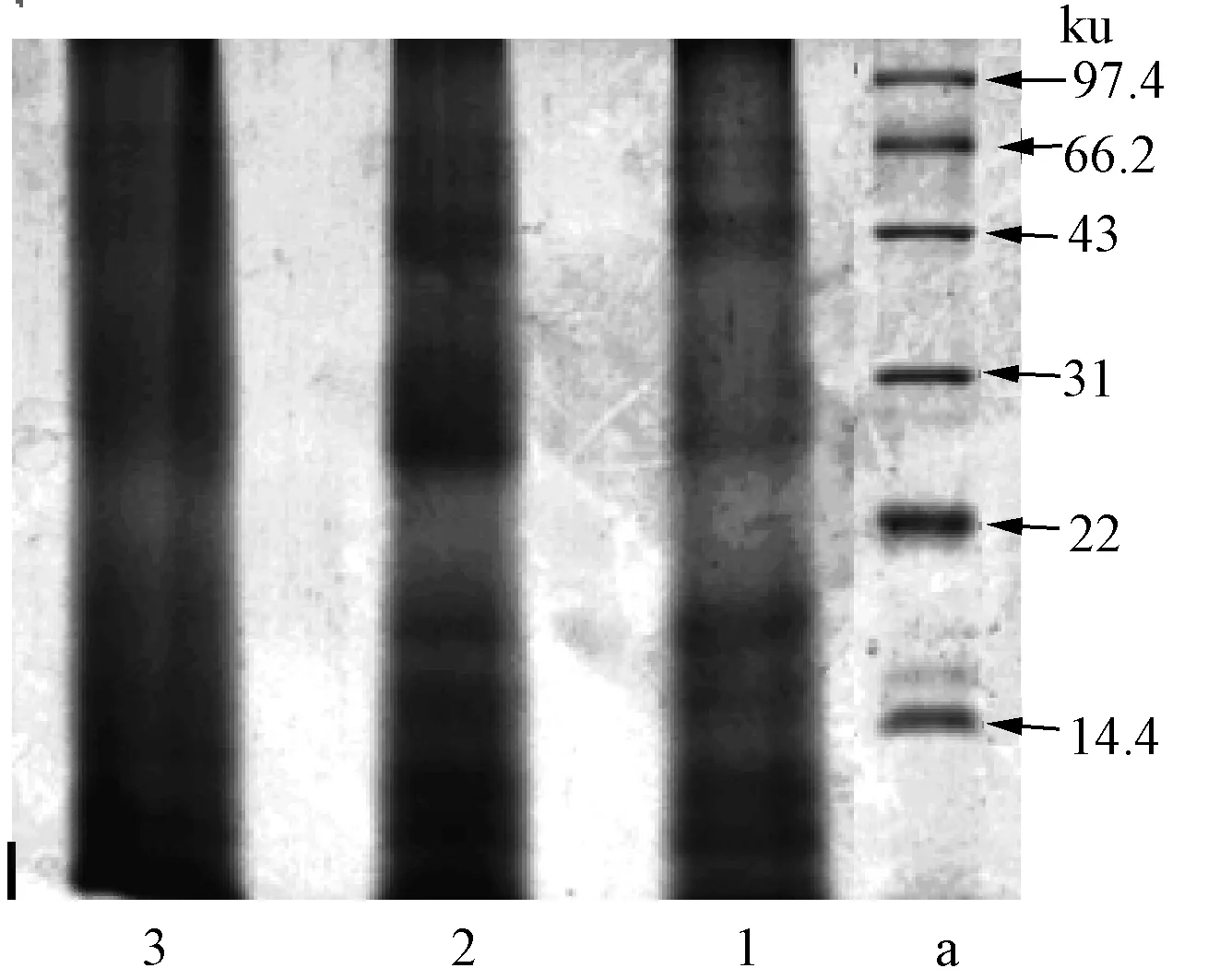
图2 SDS-PAGE凝胶电泳羊毛角蛋白分子质量Fig.2 SDS-PAGE gel electrophoretogram
比较溶解时间可知,未去鳞片的羊毛需要的溶解时间较长。比较图1(a)、(b),未去鳞片的羊毛溶解得到的角蛋白不均匀且溶解不彻底,存在较多未彻底溶解的片段。去鳞片羊毛不仅溶解时间短,而且溶解的效果较未去鳞片的彻底,只存在少许未溶解的片段,得到角蛋白溶液更均匀。综合分析可知,羊毛鳞片层对其溶解过程具有一定的消极影响,有研究结果表明鳞片表层和外层由于胱氨酸含量很高而极难溶解[8-9],图1(b)中较多的片段有可能是鳞片表层和外层。鳞片层中存在大量的二硫键,虽然巯基乙醇可以打开二硫键,离子液体对鳞片层也有一定的作用[10],但受鳞片中网状结构交联的影响,导致溶解过程中溶剂对其溶胀作用减弱。同时在羊毛去鳞片处理中,虽然DCCA反应主要发生在羊毛的鳞片层部位,但对羊毛内部结构也有一定影响,也导致其易于溶解。
图2中a为Mark电泳谱带,1、2分别为去鳞片羊毛及未去鳞片羊毛溶解得到角蛋白的分子质量电泳谱带。分析可知,1、2号样品分子质量分布相同,角蛋白分子质量分布较宽,主要分布在31、43、66.2 ku和14.4~22 ku,还有少量分布在14.4 ku以下。综合分析可知,去鳞片与处理过程不但不会影响制得的角蛋白的分子质量,而且有利于羊毛溶解的均匀性。
2.2 巯基乙醇对溶解的影响分析
按照1.5小节工艺进行试验,加巯基乙醇所需的溶解时间为7.5 h,不加巯基乙醇所需的溶解时间为13.5 h,比较溶解时间可知,不加巯基乙醇溶解羊毛需要的时间更长,观察图1(c)可见羊毛溶解得到的角蛋白均匀性较好,但仍存在少量未溶解的片段。显然,巯基乙醇对—S—S—的反应能力有利于离子液体对纤维的溶胀乃至溶解作用。
在图2中3为不加巯基乙醇溶解羊毛得到角蛋白的分子质量电泳谱带。对比1、3可知,加与不加巯基乙醇得到的角蛋白分子质量具有大体相同的分布。但由不加巯基乙醇溶解羊毛工艺得到角蛋白分子质量在31~66.2 ku的分布明显比加巯基乙醇溶解工艺宽一些,说明巯基乙醇的加入使羊毛彻底溶解。综合分析可知,巯基乙醇的加入不仅缩短溶解的时间,而且有利于打开二硫键使纤维彻底溶解。
2.3 溶解工艺优化
按1.3小节工艺将羊毛溶解,以溶解时间及分子质量作为考察指标进行工艺优化。溶解时间的具体结果如表4、5所示。
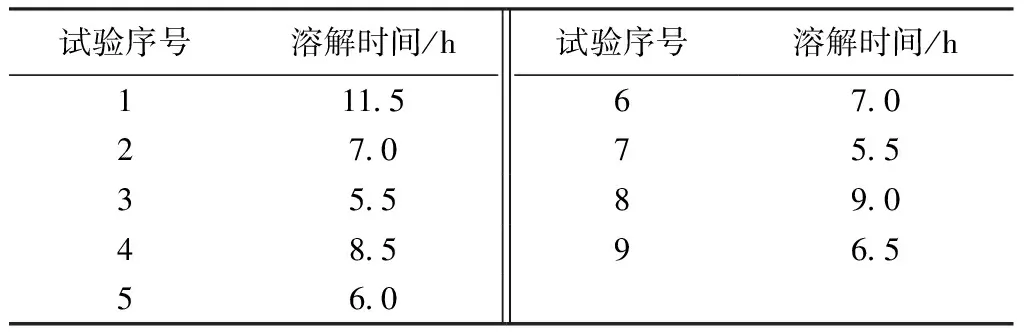
表4 溶解时间Tab.4 Dissolution time
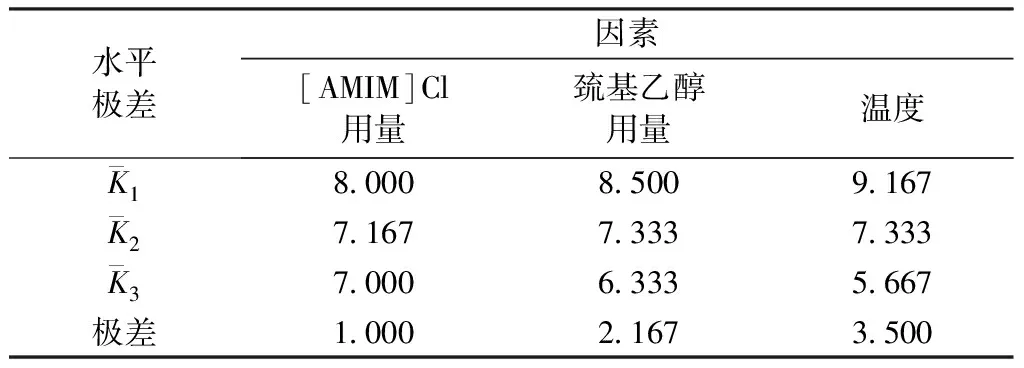
表5 溶解时间的主次因素分析Tab.5 Analysis of primary and secondary factors of dissolution time
由表4、5可知,影响溶解时间的主次因素次序为:温度>巯基乙醇的用量>[AMIM]Cl的用量。可以看出,随着温度的升高、巯基乙醇和[AMIM]Cl用量的增加,溶解时间不断缩短。
制得的羊毛角蛋白分子质量分布如图3所示。图中a为Mark电泳谱带,1~9为1~9号样品电泳谱带。分析可知,1~9号样品分子质量分布大致相同,角蛋白分子量分布较宽,分子质量集中在31、43、66.2 ku和14.4~22 ku,在14.4 ku以下的分布随工艺不同而存在差异。3、5、7号样品的分子质量同其他样品相比,因为使用的温度最高,22 ku以下的分布较宽,高分子质量的条带明显减少,说明此时羊毛角蛋白发生不同程度的降解。

图3 正交试验SDS-PAGE凝胶电泳羊毛角蛋白分子质量结果Fig.3 SDS-PAGE gel electrophoretogram of orthogonal experiments
综合分析可知,影响羊毛溶解的最关键因素是温度,尽管高温有利于羊毛的溶解,但对分子质量也会产生一定的影响,羊毛角蛋白易发生降解。为减少角蛋白的降解,并保证羊毛在较短时间内溶解,则将温度选取为120 ℃。[AMIM]Cl的用量对溶解时间产生的影响最小,说明当其用量达到一定值时,溶解时间的变化并不大,但从成本、操作性和溶解效率的角度出发,[AMIM]Cl的用量以8.5 g(以1 g羊毛计量)为最好。巯基乙醇用量对溶解时间的影响较大,增加用量可明显缩短溶解时间,且对分子质量影响较小,以 1 g/g羊毛为宜。
离子液体[Amim]Cl、巯基乙醇溶解体系溶解羊毛的最佳工艺为:m(羊毛)∶m([AMIM]Cl)∶m(巯基乙醇)=1∶8.5∶1,温度120 ℃,机械搅拌(700 r/min)。
3 结 论
1)巯基乙醇与离子液体[AMIM]Cl配合使用可以高效溶解羊毛,最终获得透明淡黄色角蛋白溶液,通过正交试验优化的溶解工艺为:m(羊毛)∶m([AMIM]Cl)∶m(巯基乙醇)=1∶8.5∶1,温度120 ℃,机械搅拌(700 r/min)。
2)去除羊毛鳞片可以有效提高溶解效率,角蛋白质溶液的分子质量分布主要集中在31、43、66.2 ku和14.4~22 ku,也有少量分布在14.4 ku以下。
FZXB
[1] 蔡再生.纤维化学与物理[M].北京:中国纺织出版社,2004. CAI Zaisheng. Chemistry and Physics of Fiber[M]. Beijing: The Textile Industry Publishing,2004.
[2] 赵玲,汤尧旭,赵瑞芳.羽毛在离子液体中的溶解及再生研究[J].毛纺科技,2010,38(8):1-5. ZHAO Ling, TANG Yaoxu, ZHAO Ruifang. Dissolution and regeneration of feather keratins in ionic liquids[J]. Wool Textile Journal, 2010, 38(8):1-5.
[3] SEDDON K R. Ionic liquids for clean technology[J].Chem Biotechnol, 1997(2):351-356.
[4] 卢芸,孙庆丰,于海鹏.离子液体中的纤维素溶解、再生材料制备研究进展[J].有机化学,2010,30(10):1593-1602. LU Yun, SUN Qingfeng, YU Haipeng, et al. Dissolution and regeneration of cellulose and development in processing cellulose-based materials with ionic liquids[J]. Chinese Journal of Organic Chemistry, 2010, 30(10): 1593-1602.
[5] ROY M. Broughton investigation of organic liquids for fiber extrusion[J].National Textile Center Annual Report,2006(9): 1-8.
[6] XIE Haibo. Ionic liquids as novel solvents for the dissolution and blending of wool keratin fibers[J].Green Chem,2005(7): 606-608.
[7] 王明,汪青,王怀芳,等.用离子液体溶解羊毛纤维的研究[J].中原工学院学报,21(6):52-54. WANG Ming, WANG Qing, WANG Huaifang, et al. Dissolved wool fiber with ionic liquids[J]. Journal of Zhongyuan Universit of Technology, 21(6):52-54.
[8] 王江波,刘建勇,王洁.基于新型还原剂羊毛角蛋白的高效溶解[J].材料导报:研究篇B,2012,26(3):7-9. WANG Jiangbo, LIU Jianyong, WANG Jie, et al. The efficient dissolution of wool based on new reductant[J]. Mater Rev:Res B,2012,26(3):7-9.
[9] DANIEL J CLINE, SARAH E Redding, STEPHEN G Bronhawn. New water-soluble phosphines as reductants of peptide and protein disulfide bonds:Reactivity and membrane permeability[J].Biochemistry,2004,43(48):15195-15203.
[10] 袁久刚,范雪荣,王强.离子液体对羊毛纤维的改性作用[J].纺织学报,2008,29(8):60-62. YUAN Jiugang, FAN Xuerong, WANG Qiang. Modification of wool fibers using ionic liquid[J]. Journal of Textile Research,2008,29(8):60-62.
Preparation of wool keratin solution with ionic liquid
SUN Yanli1, YAO Jinbo2, LI Bo1, JIA Shugang1
(1.SchoolofTextile,TianjinPolytechnicUniversity,Tianjin300160,China; 2.SchoolofChemicalEngineering,WuhanTextileUniversity,Wuhan,Hubei430073,China)
The dissolution of wool fiber was studied in the solvent system with 1-allyl-3-methyl imidazole chloride (AMIM [Cl]) as main solvent and mercaptoethanol as auxiliary reagent. The orthogonal experiments result indicates that the optimal dissolving process of wool fabric was thatm(wool):m(AMIM[Cl]):m(mercaptoethanol)=1∶8.5∶1, temperature at 120 ℃ and time for 7.5 h. Under these treatment conditions, wool fibers can be completely dissolved. The polarity of AMIM[Cl] and mercaptoethanol can open the hydrogen bonds and disulfide bonds, in combination with the shearing of mechanical mixing, wool fiber can be dissolved.
ionic liquid; dissolve; wool fiber; keratin
2014-03-31
2014-08-11
国家科技支撑计划项目(2014BAE01B02)
孙艳丽(1989—),女,硕士生。研究方向为纤维结构与性能。姚金波,通信作者,E-mail:yao_yaojinbo@tjpu.edu.cn。
10.13475/j.fzxb.20140307304
TS 195.5
A

