小型化电晕放电—原子发射光谱仪检测痕量汞
罗虹 侯贤灯 龙舟

摘 要 采用电晕放电激发源和手持式电荷耦合检测器组装了小型化原子发射光谱仪,将其用于检测痕量汞。以光化学蒸气发生技术作为进样手段,在甲酸辅助下用紫外光照射样品溶液产生汞蒸气,并由氩气带入电晕放电光源中,激发后产生汞原子发射光谱信号,用电荷耦合检测器在253.7 nm处检测。经优化得到的最佳实验条件为甲酸浓度4%,电晕放电电压90 V,载气流速200 mL/min;检测信号稳定,相对标准偏差为2.5%;标准曲线线性范围为0.5~1000 μg/L,线性相关系数大于0.99,汞的检出限可以低至0.03 μg/L。同时,对两种含汞的标准样品进行了分析, t检验表明,检测结果与样品标准值在95%的置信水平上无显著性差异;另外,对成都市府南河水和四川大学校园荷花池水的汞含量进行了测定,加标回收率在93.8%~103%范围之内。该小型化原子发射光谱测汞仪具有组装简单、低能耗、高灵敏度、便携式适用于现场分析等优点。
关键词 电晕放电; 汞; 光化学蒸气发生; 原子发射光谱法
1 引 言
汞是一种毒性元素,通常通过人为源和自然源两个途径释放到环境中。汞会通过食物链累积,转化成毒性更大的形态,危害生态系统和影响人类健康[1]。目前,汞污染已成为世界性的环境问题。很多学者致力于新颖有效的汞分析方法的研究。
痕量汞的分析方法很多,冷蒸气发生原子吸收光谱法(AAS)和原子荧光光谱法(AFS)因其测量灵敏度高,成为环境样品、生物样品中汞测定最常用的方法[1~4]。但是,传统原子吸收光谱仪和原子荧光光谱仪体积大,不能满足监督监控、应急监测和现场分析的要求。紧凑的便携式仪器设备具有体积小、成本低、能耗低、易操作的优点,能满足上述需求,因而更适用于应急监测和现场分析。最近,许多研究工作都集中在原子光谱系统的小型化发展。数十年前已经开始改进放电技术产生和维持低温等离子体,包括介质阻挡放电[5~7]、辉光放电[8,9]、电容耦合等离子体[10,11]和微等离子体装置等[12]。电晕放电(Corona discharge, CD)是一种常见的气体放电现象。在丝状或针尖电极附近,气体发生电离和激发,出现电晕放电。电晕放电技术的应用可追溯到第一台静电除尘器[13]。CD目前已经广泛用于复杂生物样品的分析[14]、污水处理和空气净化[15,16], 更被用作质谱分析[17]和离子迁移光谱[18,19]分析的离子源。由于电晕放电是一种大气压下的低能耗放电,也可用于挥发性物质的原子化甚至进一步激发产生原子发射光谱。
汞冷蒸气发生作为传统的进样方式通常需要使用SnCl2 或 NaBH4等还原性化学试剂,伴随产生的氢气带来背景干扰,蒸气发生效率较低,这些不足都限制了这一还原体系的广泛应用[20]。另一些蒸气发生进样技术则不需要使用化学试剂。如:电化学蒸气发生[21]、超声辅助化学蒸气发生[22,23]以及光化学蒸气发生[24~26]。其中,光化学蒸气发生体系采用无毒性还原性试剂,是一种很有吸引力的绿色进样技术。在紫外光照射下,有机酸分解产生还原自由基,将汞转化成汞蒸气。
本研究组研制了一种小型化的原子发射光谱分析系统,以电晕放电等离子体为激发光源,采用光化学蒸气发生进样,电荷耦合器件(CCD)作检测器对汞进行测定。本装置结构紧凑、能耗低、操作方便、灵敏度高。与传统的冷原子荧光测汞仪相比,本装置采用电晕放电作为激发源,放电稳定,激发能力较强。甲酸辅助的紫外光化学蒸气发生进样,效率高,所用化学试剂少,是一种相当绿色的分析方法。
2 实验部分
2.1 仪器装置
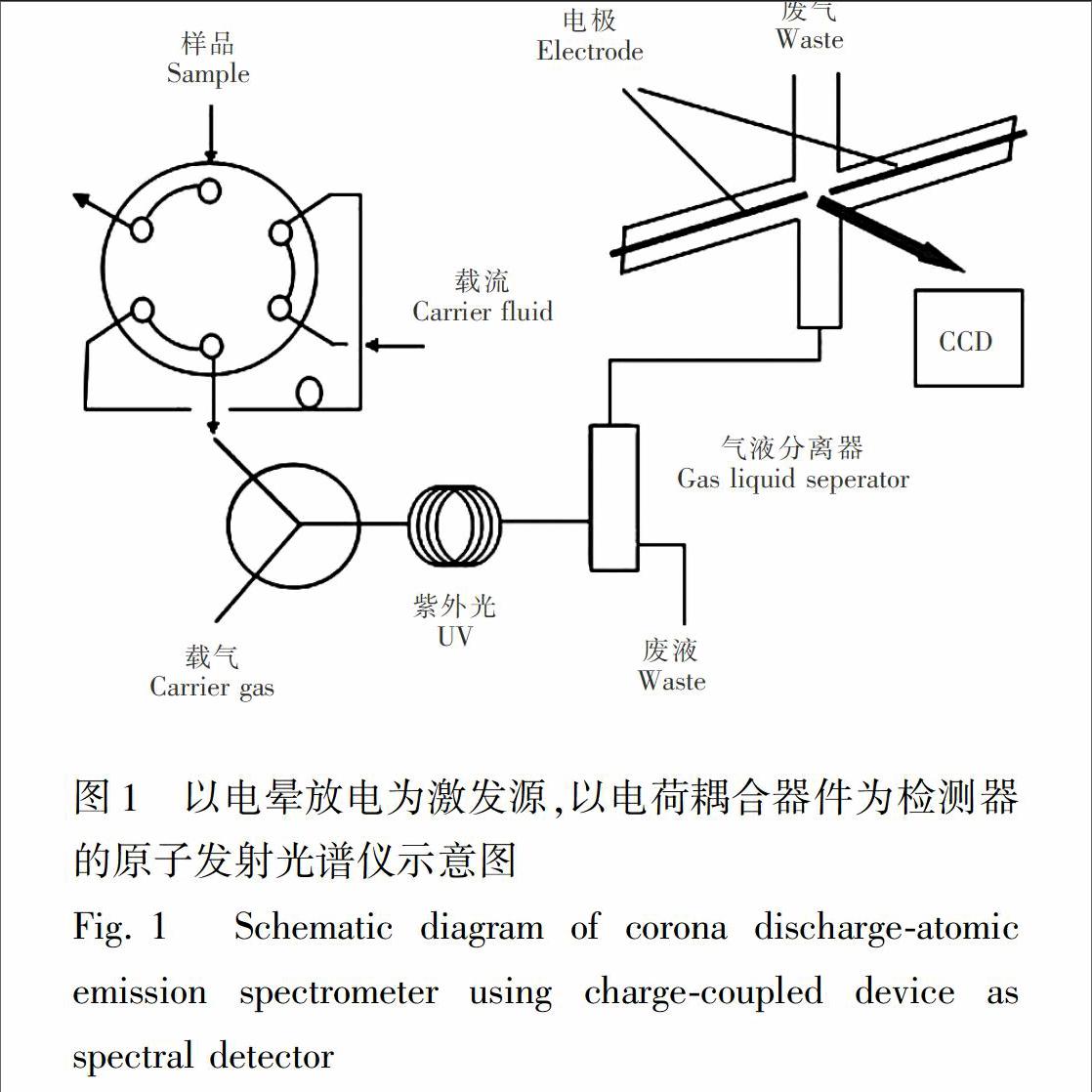
小型化的CD-AES检测系统(图1)由4部分组成:六通阀、实验室自制的电晕放电装置、紫外灯和USB2000电荷耦合器件(美国海洋光学仪器公司)。六通阀连接了一个3 mL的定量环。六通阀手柄在装载(Load)位置时,样品进入定量环,将手柄转动至进样(Flow)位置时,甲酸溶液推动样品进入反应管,在紫外光照射下,生成挥发性的汞蒸气,并通过氩气引入电晕放电区域,以氩气作为放电气体,在曲率半径很小的尖端电极附近,由于局部电场强度超过氩气的电离场强,使氩气发生电离和激励,产生电晕放电。放电过程中氩气流速恒定,放电管的气压保持恒定,使电晕放电均匀、稳定,放电产生的能量使汞受到激发并产生相应的原子发射光谱信号,由CCD检测,采用峰面积进行定量分析。实验室自制的电晕放电装置由十字形石英管(50 mm×5.0 mm i.d., 7.0 mm o.d.)和两个铂铱丝电极(直径0.5 mm)构成。电极安装在石英管中轴线上,电极间距离为1.5 mm,能产生稳定的CD微等离子体。臭氧发生器(YG. BP101P,广州救捞局电子设备厂)以及转换器(TDGC2-1,浙江正泰电器股份有限公司)为CD稳定放电提供能量。
2.2 试剂与材料
氩气(99.99%)用作载气和放电气体,购于成都乔源气体有限公司。汞标准溶液由高浓度标准储备液稀释,介质为4%甲酸。其它化学试剂均为分析纯,购于成都科龙化学试剂公司。超纯水由成都超纯科技有限公司纯水系统制得。
2.3 样品分解
准确称取0.5 g样品于25 mL离心管中,加入5 mL 50%(V/V)HCl。在室温下超声30 min,离心分离。吸取上清液转入容量瓶,用去离子水稀释到25 mL, 待测。
3 结果与讨论
3.1 条件优化
3.1.1 载气流速的优化 如图2a所示,氩气作为载气和放电气体,考察了氩气流速对汞原子发射强度的影响。在100~200 mL/min范围,汞原子发射强度随着流速的增大而增强;当载气流量大于250 mL/min后,其发射光谱信号显著下降。因此选用200 mL/min的载气流速。
3.1.2 放电电压优化 臭氧发生器以及转换器为CD稳定放电提供能量。考察了放电电压在80~100 V之间的汞原子发射光谱信号(图2b)。较高电压能提供较高的能量,产生较多的自由基,还原能力增强,汞原子发射光谱强度也随之增大。当电压大于95 V,信号会变得不稳定,信噪比也逐渐减低。综合考虑,放电电压选择90 V。
图2 载气流速(a)和放电电压(b)的优化
Fig.2 Effect of flow rate of carrier gas (a) and discharge voltage (b)
进样体积:3 mL (汞浓度为4 ng/mL); a, 放电电压: 90 V; b, 载气流速: 200 mL/min。
Injection volume: 3 mL of 4 ng/mL mercury; a, discharge voltage: 90 V; b, gas flow rate: 200 mL/min.
3.1.3 甲酸浓度优化 在紫外光照射下,甲酸能产生还原性自由基,将汞元素还原成汞原子蒸气[24,27]。甲酸浓度为1%~8%的影响如图3a所示,当甲酸浓度大于2%时,汞发射光谱信号的强度趋于稳定,因此选择4%的甲酸作为介质。
3.1.4 光照时间优化 光化学蒸气发生效率与光照时间有关。足够的紫外光照射时间能保证产生足够的还原自由基,将汞元素还原成汞原子蒸气。但是,过长时间的紫外光照射可能会导致样品的分解,减弱汞原子发射光谱强度,如图3b所示,因此选择50 s作为最佳的光照时间。
3.1.5 放电稳定性的考察 为了考察电晕放电系统的稳定性,在两个电极间加上高频电流,每60 s采集一次光发射信号。汞在253.7 nm的特征发射强度稳定,1 h内的相对标准偏差为2.5%。
3.2 分析性能和样品分析
在优化的实验条件下,考察CD-AES系统的分析性能。校正曲线线性范围为0.5~1000 μg/L,相关系数大于0.99。空白溶液11次重复测定,检出限(LOD,3σ)低至0.03 μg/L。为验证方法的准确性,将本方法应用于两个固体标准参考样品中汞的分析(DORM-2 和 DORM-3, 加拿大国家研究委员会),如表1所示。经t检验,在置信度95%时,样品测定结果与样品标准值之间无显著性差异。
另外,将本方法用于府南河水和四川大学荷花池水的检测,结果见表2,加标回收率在93.8%~103%范围内。结果表明,所建立的痕量汞检测方法应用于实际样品的分析是可行的。
4 结 论
研制了一种基于电晕放电微等离子体激发光源、手持式电荷耦合器件检测器、光化学蒸气发生进样方式的小型原子发射光谱系统。与传统的原子发射光谱仪相比,本系统具有体积小、结构紧凑、响应快速、灵敏度高、成本低、能耗低、操作方便等优点,为现场样品中痕量汞的测定提供了一种新的选择。
References
1 Gao Y, Shi Z M, Long Z, Wu P, Zheng C B, Hou X D. Microchem. J., 2012, 103: 1-14
2 YANG Meng, XUE Jiao, LI Ming, LI Jia, HUANG Xiu, XING Zhi. Chinese J. Anal. Chem., 2012, 40(8): 1164-1168
杨 萌, 薛 蛟, 李 铭, 李 佳, 黄 秀, 邢 志. 分析化学, 2012, 40(8): 1164-1168
3 WU Ying-Juan, CHEN Yong-Heng. Spectroscopy and Spectral Analysis, 2008, 28(9): 2189-2191
吴颖娟, 陈永亨. 光谱学与光谱分析, 2008, 28(9): 2189-2191
4 YIN Xue-Feng, ZHANG Jian-Jun, WANG Xiao-Fang. Chinese J. Anal. Chem., 2004, 32(10): 1365-1367
殷学锋, 张建君, 王小芳. 分析化学, 2004, 32(10): 1365-1367
5 Li W, Jiang X M, Xu K L, Hou X D, Zheng C B. Microchem. J., 2011, 99(1): 114-117
6 KuermaitiBiekesailike, WANG Juan, HAN Guo-Jun, XING Zhi. Chinese J. Anal. Chem., 2010, 38(3): 357-361
别克赛力克·库尔买提, 王 娟, 韩国军, 邢 志. 分析化学, 2010, 38(3): 357-361
7 Han B J, Jiang X M, Hou X D, Zheng C B. Anal. Chem., 2014, 86(13): 6214-6219
8 Ogino H, Seki T. Anal. Chem., 1997, 69(17): 3636-3640
9 Zhu Z L, Chan G C Y, Ray S J, Zhang X R, Hieftje G M. Anal. Chem., 2008, 80(18): 7043-7050
10 Frentiu T, Mihaltan A I, Ponta M, Darvasi E, Frentiu M, Cordos E. J. Hazard. Mater., 2011, 193: 65-69
11 Frentiu T, Mihaltan A I, Senila M, Darvasi E, Ponta M, Frentiu M, Pintican B P. Microchem. J., 2013, 110: 545-552
12 Weagant S, Karanassios V. Anal. Bioanal. Chem., 2009, 395(3): 577-589
13 Lodge-Cottrell Ltd.U. S. Patent, 4569685, 1986
14 Ebeling D D, Westphall M S, Scalf M, Smith L M. Anal. Chem., 2000, 72(21): 5158-5161
15 Huang L, Nakajyo K, Hari T, Ozawa S. Ind. Eng. Chem. Res., 2001, 40(23): 5481-5486
16 Sano N, Kawashima T, Fujikawa J, Fujimoto T, Kitai T, Kanki T. Ind. Eng. Chem. Res., 2002, 41(24): 5906-5911
17 LIANG Hua-Zheng, ZHANG Xie, CHEN Shuang-Xi, SHAO Zhao. Chinese J. Anal. Chem., 2008, 36(8): 1152-1156
梁华正, 张 燮, 陈双喜, 邵 昭. 分析化学, 2008, 36(8): 1152-1156
18 Jafari M T, Saraji M, Sherafatmand, H. Anal. Chem., 2012, 84(22): 10077-10084
19 Jazan E, Mirzaei H. J. Pharmaceut. Biomed., 2014, 88: 315-320
20 Wu P, He L, Zheng C B, Hou X D, Sturgeon R E. J. Anal. At. Spectrom., 2010, 25(8): 1217-1246
21 Li X, Wang Z H. Anal. Chim. Acta, 2007, 588(2): 179-183
22 Capelo J L, Maduro C, Mota A M. Ultrason. Sonochem., 2006, 13(1): 98-106
23 Gil S, Lavilla I, Bendicho C. Anal. Chem., 2006, 78(17): 6260-6264
24 Zheng C B, Li Y, He Y H, Ma Q, Hou X D. J. Anal. At. Spectrom., 2005, 20(8): 746-750
25 Li Y, Zheng C B, Ma Q, Wu L, Hu C W, Hou X D. J. Anal. At. Spectrom., 2006, 21(1): 82-85
26 Guo X M, Sturgeon R E, Mester Z, Gardner G J. Anal. Chem., 2003, 75(9): 2092-2099
27 Guo X M, Sturgeon R E, Mester Z, Gardner G J. Environ. Sci. Technol., 2003, 37(24): 5645-5650

