超高效液相色谱-高分辨率质谱法筛查化妆品中12种糖皮质激素
李 强,张晓光,马俊美,李润岩,范素芳,张 岩*
(1.河北省食品检验研究院,河北 石家庄 050091;2.河北省食品安全重点实验室,河北 石家庄 050091)
超高效液相色谱-高分辨率质谱法筛查化妆品中12种糖皮质激素
李强1,2,张晓光1,2,马俊美1,2,李润岩1,2,范素芳1,2,张岩1,2*
(1.河北省食品检验研究院,河北石家庄050091;2.河北省食品安全重点实验室,河北石家庄050091)
摘要:建立了超高效液相色谱-四极杆-静电场轨道阱质谱快速筛查和确证化妆品中可能添加的12种糖皮质激素的分析方法。样品经乙腈提取,用Acquity UPLC BEH C18柱(100 mm×2.1 mm,1.7 μm)分离,以0.1%甲酸甲醇和0.1%甲酸水溶液为流动相进行梯度洗脱。以正离子全扫描模式得到糖皮质激素的精确质量数,与理论精确质量数对比,精确度偏差小于2×10-6。建立了筛查列表,并将12种糖皮质激素物质的二级质谱数据库加入确证条件中,实现了对12种糖皮质激素类物质的快速筛查。检出限为1~2 μg/kg,定量下限为3~5 μg/kg;加标水平为10,20,40 μg/kg时,回收率为78.3%~112.5%,相对标准偏差(RSD)为1.0%~11.2%。该方法可作为化妆品中非法添加糖皮质激素成分的高通量筛选和确认检测方法。
关键词:超高效液相色谱;四极杆-静电场轨道阱高分辨质谱;糖皮质激素;化妆品
随着人们生活水平的提高,化妆品成为不可缺少的消费类产品。化妆品是指以涂擦、喷洒或其他类似的方法,散布于人体表面任何部位(皮肤、毛发、指甲、口唇等),以达到清洁、消除不良气味、护肤、美容和修饰目的的日用化学工业产品[1]。据统计,中国已成为全球最大的化妆品市场之一,化妆品年销售额达2 000多亿元,约占全球化妆品市场的8.8%,仅次于美国[2]。伴随着化妆品市场的高增长和高需求,化妆品质量问题日益突出,含毒化妆品严重危害人们的身体健康。
糖皮质激素是皮肤科最常见的外用药物,可抑制纤维细胞再生,对皮肤具有一定的美白功效,但长期使用会产生激素依赖症及其他副作用,甚至引发癌症,对人体造成严重伤害。我国《化妆品卫生规范》2007版明确规定,糖皮质激素属于禁用物质[3]。但是,由于其具有明显的美白、祛痘等效果,不少厂家仍然非法向化妆品中添加糖皮质激素类物质。近期曝光的含有糖皮质激素的“毒面膜”事件,使得化妆品安全问题又被推到了舆论的风口浪尖。由此可见,研究糖皮质激素类物质的检测,建立简单高效的筛查方法对于行业监管和保障消费者权益具有十分重要的意义。
目前,糖皮质激素的检测方法主要有液相色谱法[4]、液相色谱-三重四极杆质谱联用法[5-9]以及毛细管电泳法[10-12]。但以上方法均存在分辨率低、检测种类有限、易造成假阳性等问题。近年来,以飞行时间质谱和静电场轨道阱质谱为代表的液相色谱-高分辨质谱联用法逐渐成为研究热点。静电场轨道阱的原理是利用不同物质在阱中运动轨迹不同而实现精确定量,可得到一级精确质量数以及多级结构碎片,且可以自建数据库。静电场轨道阱为目标分析物提供精准而全面的数据,大大降低了筛查和确证的误差,在食品保健品非法添加检测[13-14]、农药残留检测[15-16]、化妆品禁用物质筛查[17-18]等领域得到了一定应用,但将其用于检测化妆品中激素的研究较少。本文利用超高效液相色谱-静电场轨道阱质谱联用仪建立了化妆品中12种糖皮质激素的快速筛查和确证方法,为政府部门对化妆品市场监管提供了有效的补充方案。
1实验部分
1.1仪器、材料和试剂
Ultimate 3 000超高效液相色谱仪(美国ThermoFisher公司);Q-Exactive超高效液相色谱-四极杆-静电场轨道阱组合式高分辨质谱仪(美国ThermoFisher公司);高速冷冻离心机(美国Sigma公司);IKA Vortex Genius 3旋涡混合器(德国IKA公司);KQ-250DV型超声波仪(昆山市超声仪器有限公司)。
甲酸(色谱纯,美国Sigma公司);甲醇、乙腈(色谱纯,美国Fisher公司);实验用水为自制的二级水,符合GB/T6682规定;12种糖皮质激素标准品均购自中国食品药品检定研究院,纯度≥95%,标准储备液用甲醇配制,系列标准工作液用乙腈-水溶液(体积比3∶7)配制;化妆品购于当地超市。
1.2样品前处理
称取1.00 g(精确至0.001 g)样品,置于50 mL离心管中,加入5 mL水,涡旋3 min,再加入5 g NaCl、10 mL乙腈,涡旋1 min,超声15 min,于4 ℃下以10 000 r/min离心3 min,移取上层清液,加入10 mL正己烷,剧烈振荡1 min后弃去正己烷层,剩余乙腈层再加入10 mL正己烷,剧烈振荡1 min后弃去正己烷层,剩余乙腈层过0.22 μm滤膜,上机测定。
1.3仪器条件
1.3.1色谱条件色谱柱:Waters ACQUITY UPLC BEH C18柱(100 mm×2.1 mm,1.7 μm;美国Waters公司)。流动相A为水(含0.1%甲酸),B为甲醇(含0.1%甲酸)。梯度洗脱程序:0~2 min,B相保持30%;2~6 min,B相从30%线性升至95%;6~8 min,B相保持95%;8~9 min,B相从95%线性降至30%;9~10 min,B相保持30%。
1.3.2质谱条件质量分析器:四极杆-静电场轨道阱;电喷雾离子源;鞘气流量:35 Arb;辅助气流量10 Arb;喷雾电压:3.8 kV;离子源温度:350 ℃;毛细管温度:320 ℃。
一级精确质量数获取采用正离子全扫描模式,质量扫描范围:m/z150~8 000。二级碎片图谱获取采用目标离子监测模式,分辨率17 500,碰撞能量为35%。
样品检测采用正离子全扫描+基于数据依赖的二级质谱碰撞解离(Full MS+ddMS2)扫描模式;全扫描分辨率:70 000;基于数据依赖的二级质谱碰撞解离分辨率:17 500;碰撞能量为35%。
2结果与讨论
2.1样品的提取
由于化妆品基质较为复杂,因此需要选择合适的提取溶剂。本实验选取了3种不同的提取溶剂(甲醇、乙腈、乙酸乙酯)和不同的超声时间(5,10,15,20,25 min),按照“1.2”方法进行样品前处理,考察了12种糖皮质激素的回收率(样品空白基质加标浓度10 μg/kg)。结果表明,在相同的超声时间下,以甲醇为提取溶剂时,甲醇和水无法分层,溶液较为浑浊,造成过滤膜困难;以乙腈和乙酸乙酯为提取溶剂时,在加入盐的情况下,乙腈和乙酸乙酯均能和水分层,12种糖皮质激素的回收率分别为78.3%~111.1%和57.1%~119.8%,由于乙酸乙酯和正己烷互溶,因此无法实现加入正己烷以进一步除去杂质的目的。而在乙腈中加入正己烷后,对12种糖皮质激素的回收率几乎无影响。因此选取乙腈为提取溶剂,在该条件下,考察了超声时间对回收率的影响,发现随着超声时间的增加,提取效果增加,当超过15 min后,提取回收率增加不明显,因此选择超声时间为15 min。
2.2色谱-质谱条件的优化
考察了4种不同的流动相体系(水-甲醇、水-乙腈、 0.1%甲酸水溶液-0.1%甲酸甲醇、0.1%甲酸水溶液-0.1%甲酸乙腈)对色谱峰形和出峰强度的影响。结果表明,使用水-甲醇以及0.1%甲酸水溶液-0.1%甲酸甲醇2种流动相体系得到的色谱峰形较优;当使用乙腈为流动相时,泼尼松和地夫可特的出峰出现分叉,而使用甲醇为流动相时,所有目标分析物的峰形良好,但使用0.1%甲酸水溶液-0.1%甲酸甲醇流动相所得的峰面积大于水-甲醇流动相所得的峰面积,这可能是由于加入甲酸,对正离子模式电离起到了增强作用。
分别采用正离子模式和负离子模式对12种糖皮质激素的质谱条件进行优化,结果表明,12种糖皮质激素均可产生[M+H]+以及[M-H]-分子离子峰,但在负离子模式下,产生的[M-H]-分子离子峰强度较小,约为正离子模式下[M+H]+峰强度的1/10,且产生的二级碎片信息较少,不利于定性筛查。
综上所述,本实验确定以0.1%甲酸水溶液-0.1%甲酸甲醇作为流动相,正离子模式进行全扫描,提取[M+H]+分子离子峰。12种糖皮质激素的提取离子色谱图见图1。
2.3基质效应的评价
由于化妆品基质较为复杂,提取液中的非目标组分可能对目标分析物产生影响。虽然静电场轨道阱质谱比三重四极杆质谱具有更强的抗干扰能力,但仍然存在基质效应,因此,需要对基质效应进行评价。本实验将12种糖皮质激素标准品混标分别用乙腈和空白基质提取液配制成一系列浓度标准曲线(2,10,50,100,200,500 ng/mL),以相同物质在不同基质中标准曲线的斜率大小来判断基质效应情况(见表1)。结果表明,12种糖皮质激素在空白基质中均为基质抑制效应,其中哈西奈德的抑制效应最为明显。
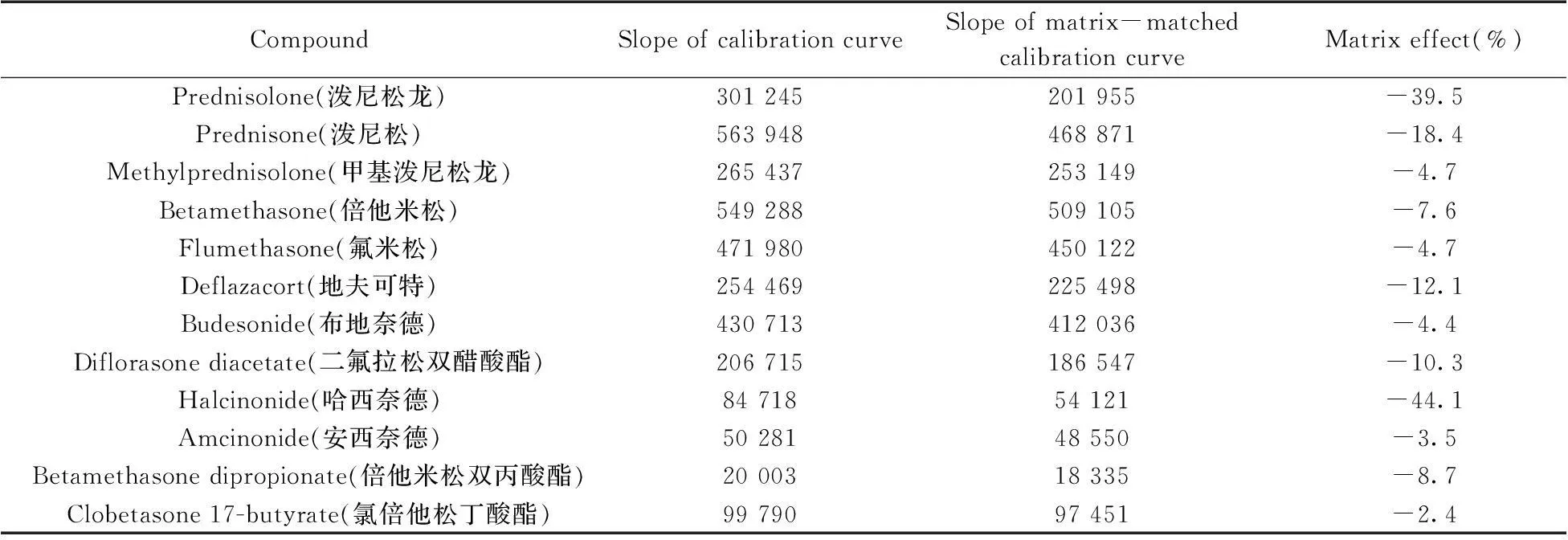
表1 12种糖皮质激素的基质效应比较
2.4理论精确质量数的验证
本方法以正离子模式全扫描方式运行,12种糖皮质激素得到较好的分离效果,且提取的精确质量数与理论精确质量数相差较小,精确度误差均小于2×10-6(5 ppm),具体质量精度见表2。
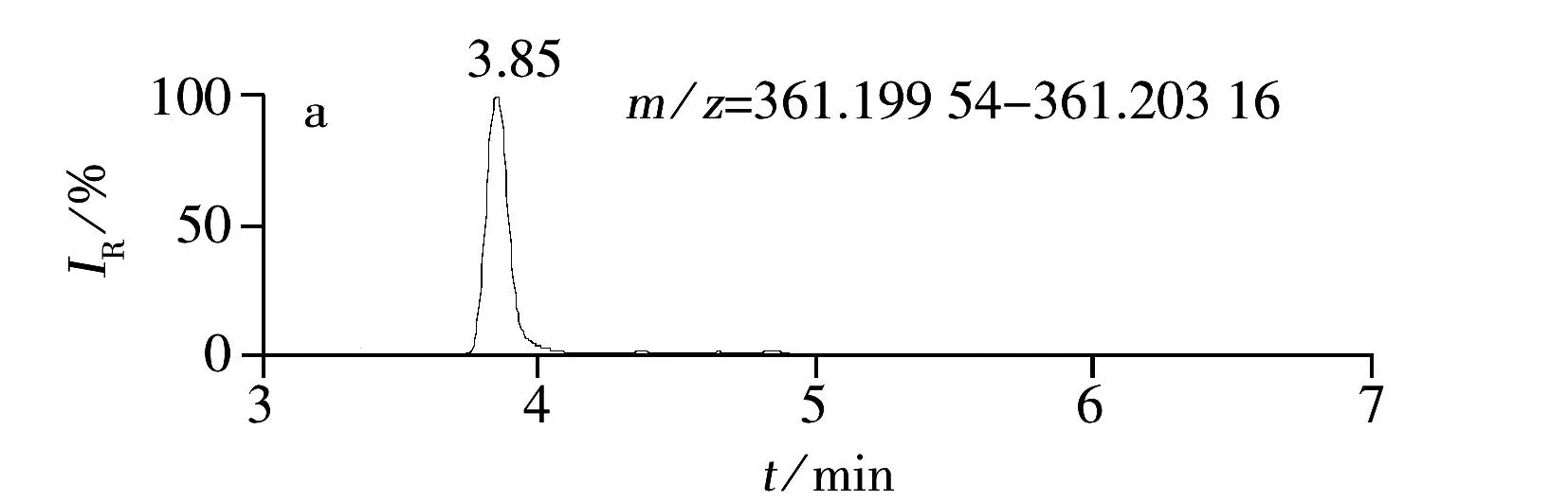
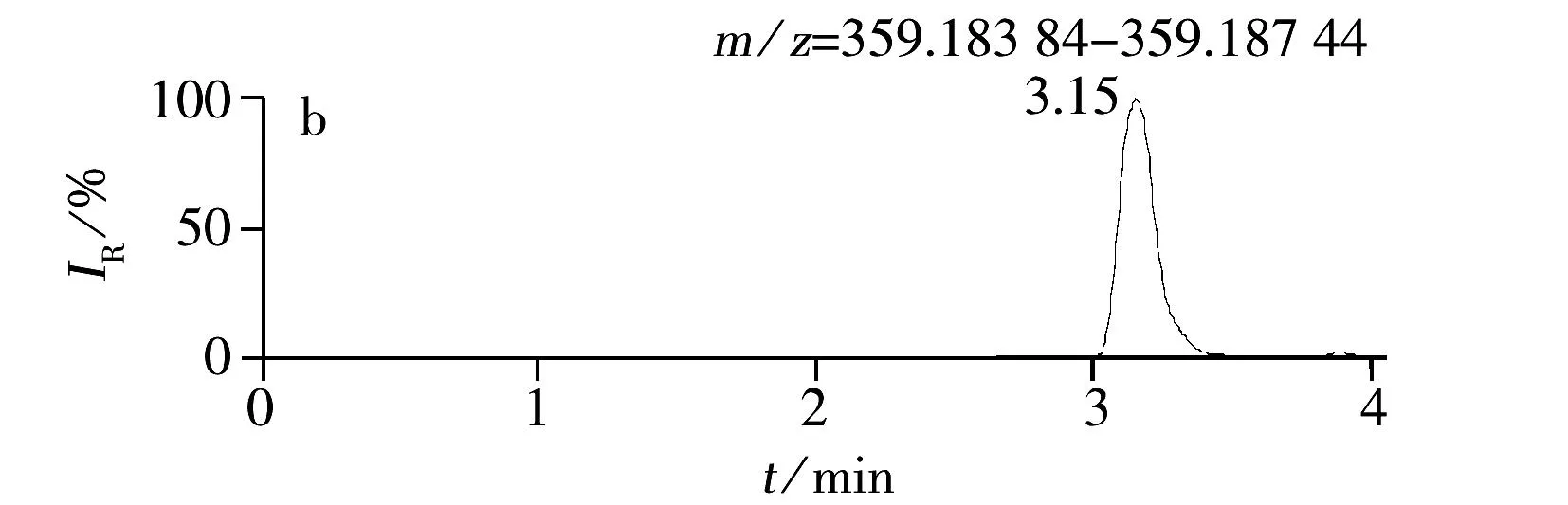
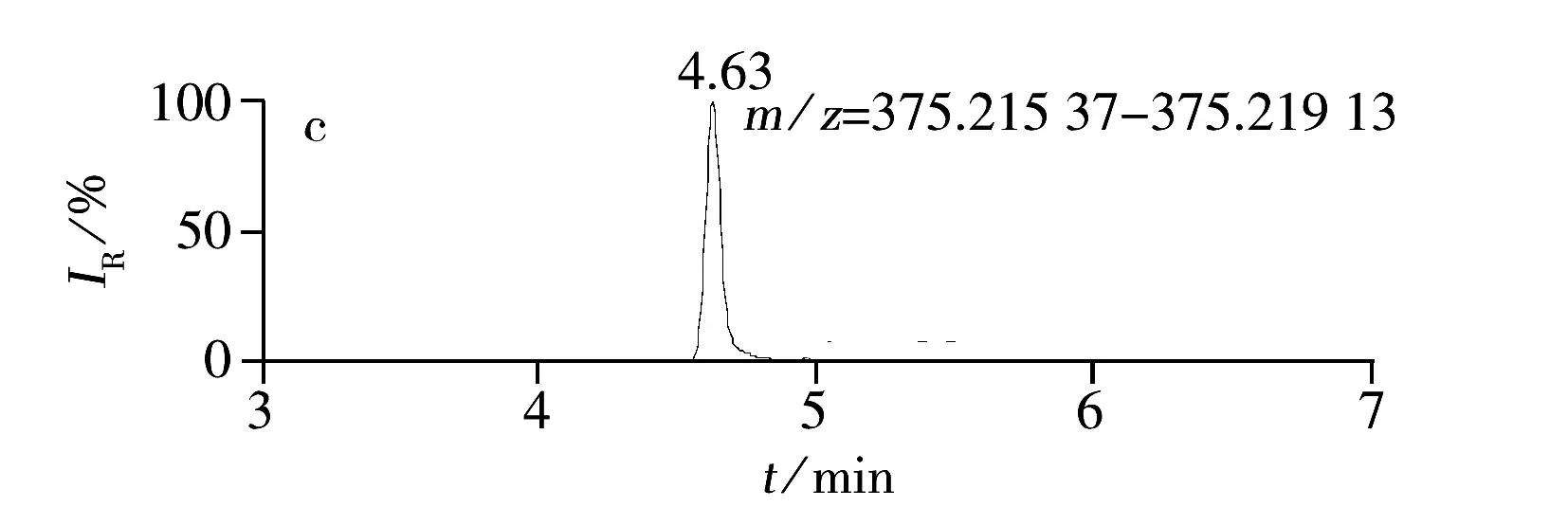
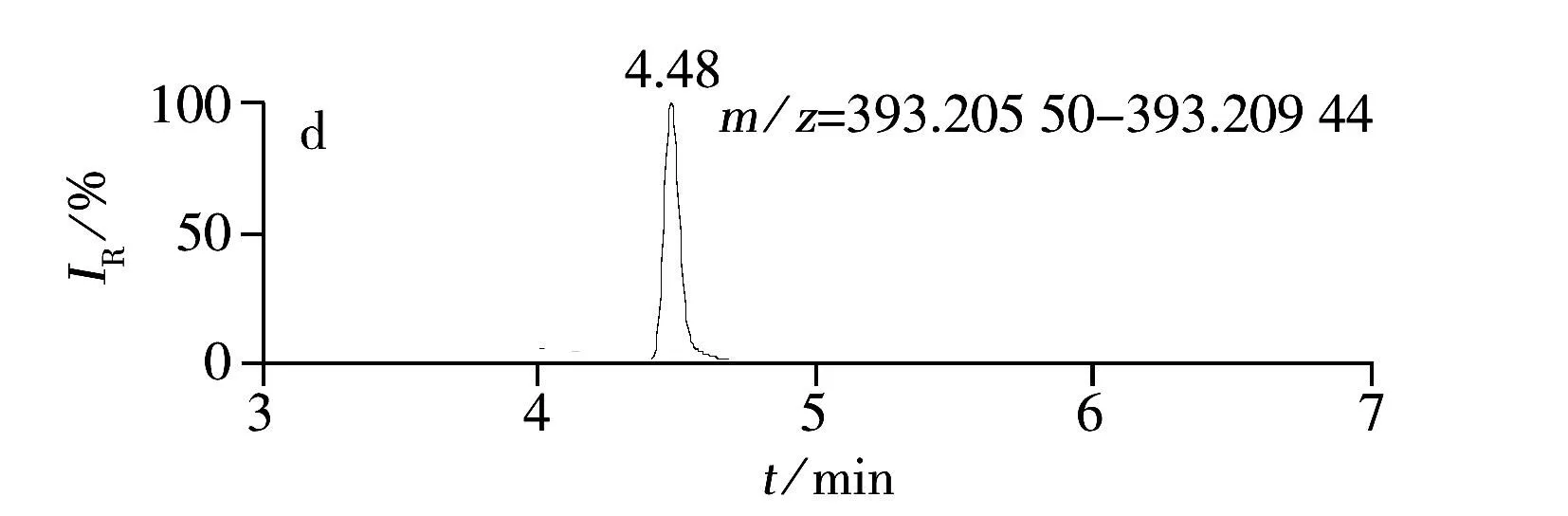
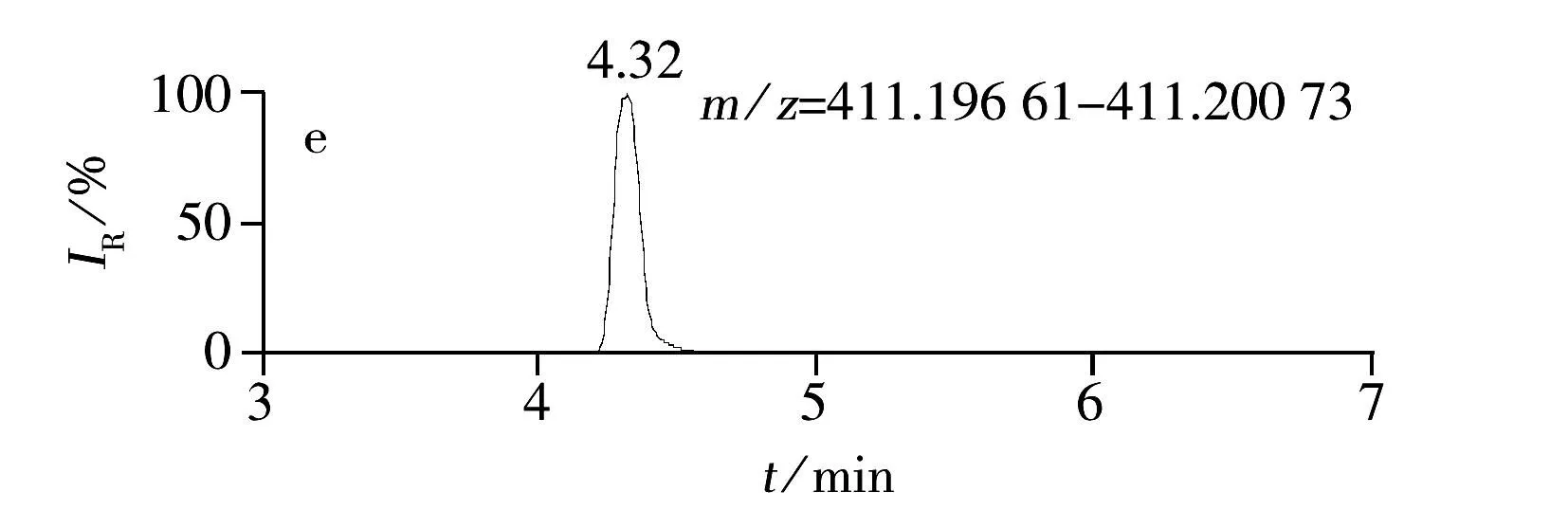
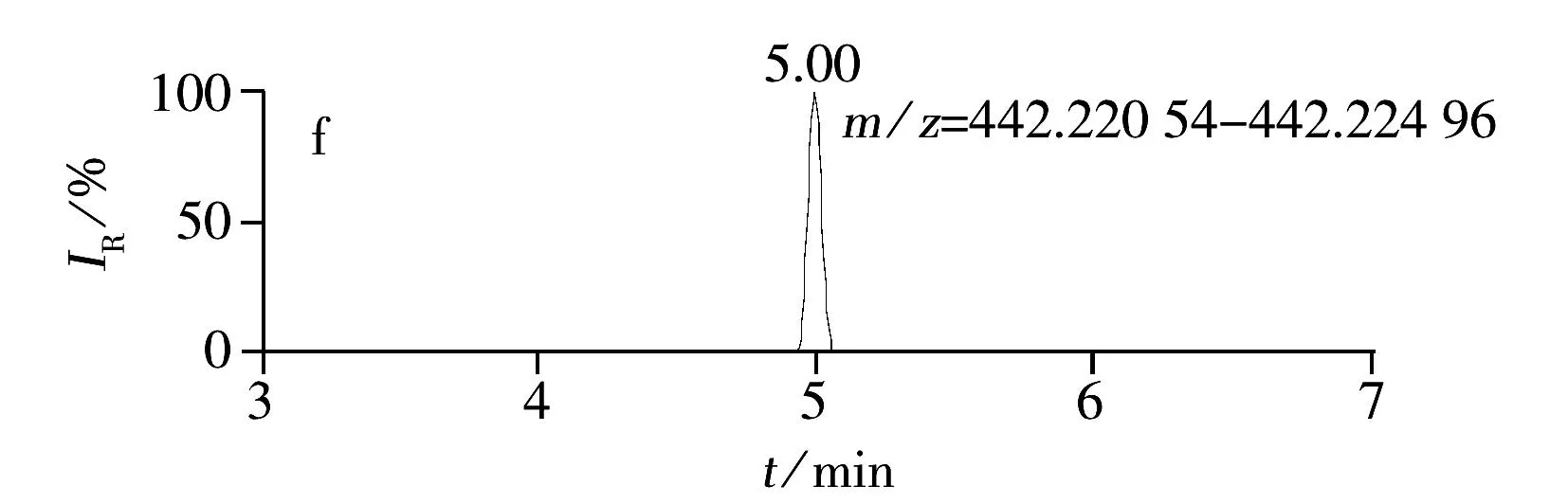
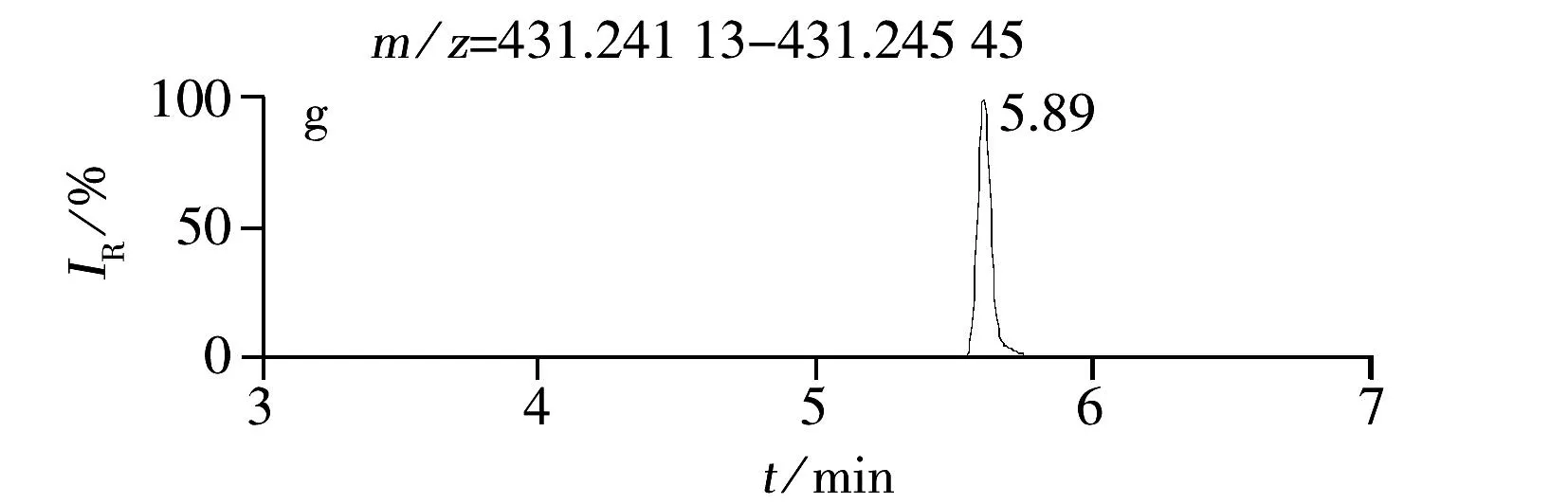
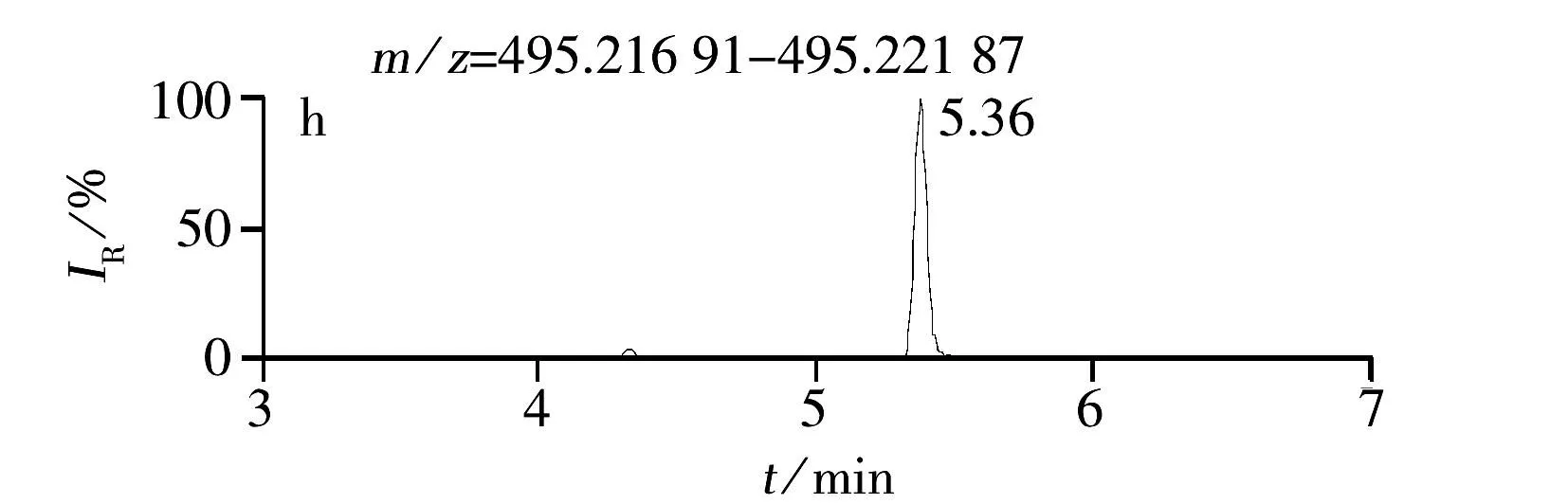
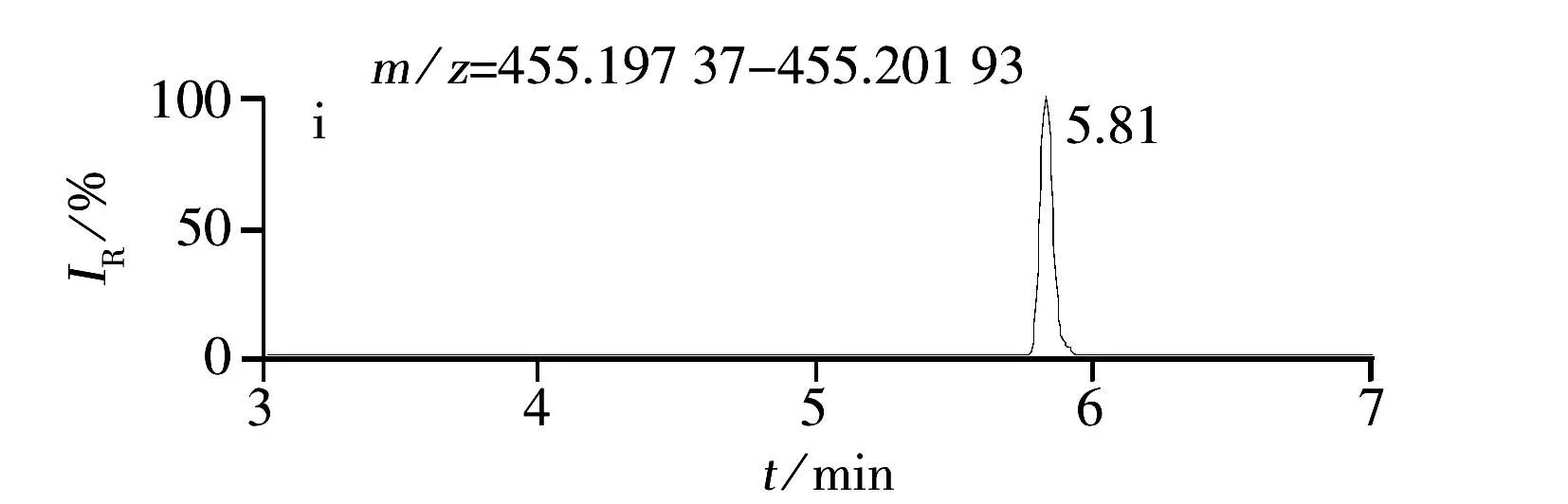
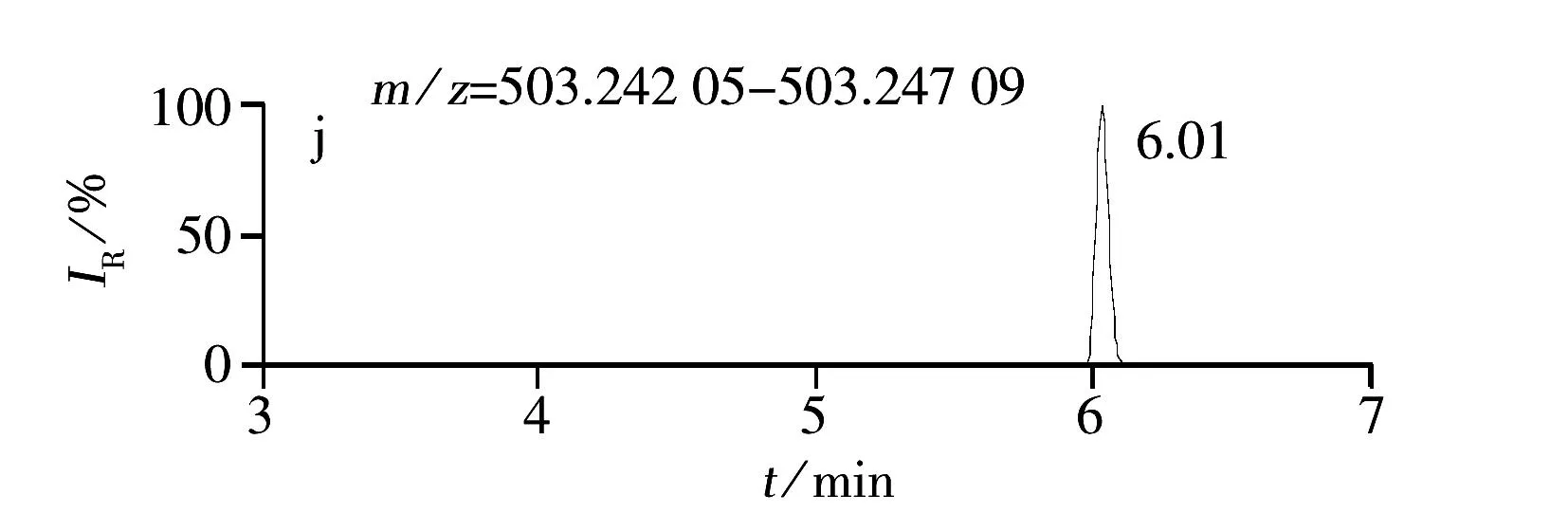


图1 12种激素化合物的提取离子色谱图
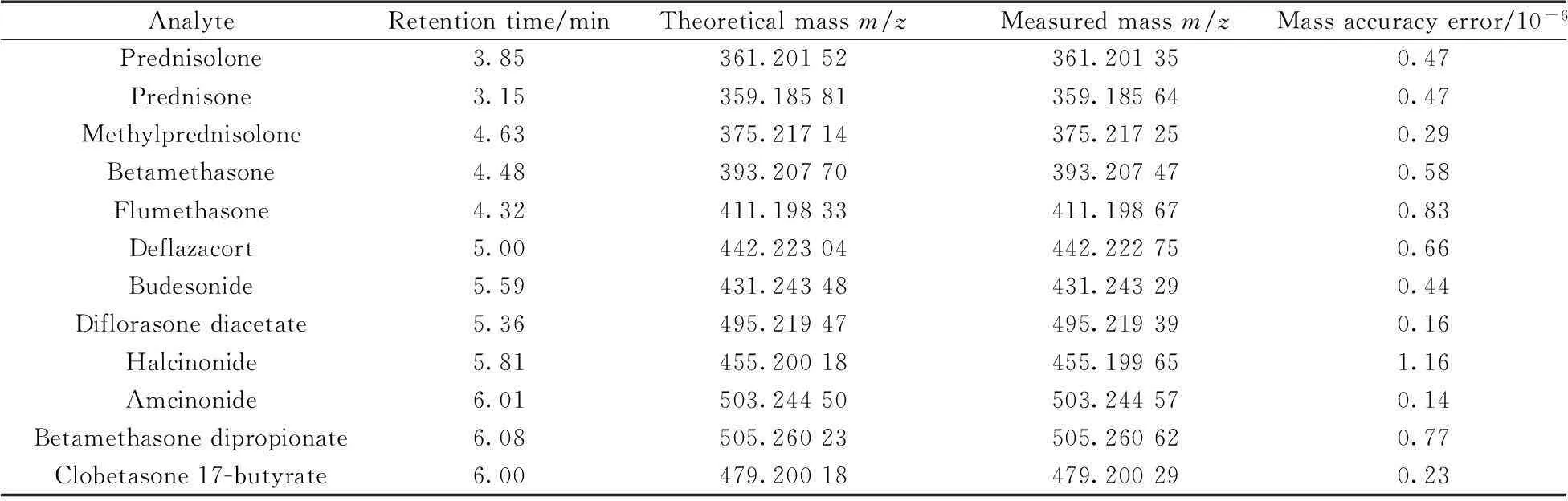
AnalyteRetentiontime/minTheoreticalmassm/zMeasuredmassm/zMassaccuracyerror/10-6Prednisolone3.85361.20152361.201350.47Prednisone3.15359.18581359.185640.47Methylprednisolone4.63375.21714375.217250.29Betamethasone4.48393.20770393.207470.58Flumethasone4.32411.19833411.198670.83Deflazacort5.00442.22304442.222750.66Budesonide5.59431.24348431.243290.44Diflorasonediacetate5.36495.21947495.219390.16Halcinonide5.81455.20018455.199651.16Amcinonide6.01503.24450503.244570.14Betamethasonedipropionate6.08505.26023505.260620.77Clobetasone17-butyrate6.00479.20018479.200290.23
2.5基于二级质谱图库筛查方法的建立
利用Extract Finder软件建立筛查方法,首先采用目标离子监测(Target MS2)方法,对12种糖皮质激素的二级质谱数据进行采集,将采集的二级特征图谱添加入二级质谱数据库。其次,建立12种糖皮质激素的筛查列表,将理论分子式、保留时间、特征碎片离子、同位素理论分布、二级质谱数据等加入筛查列表,并设置各指标的偏差范围,对于未知样品,采用正离子全扫描+基于数据依赖的二级质谱碰撞解离(Full MS+ddMS2)模式运行,将采集的原始数据导入筛查列表,系统通过对各个参数进行计算,最终得到确证结果。
2.6方法学验证
用空白基质配制一系列的标准工作液,以12种糖皮质激素的一级质量数提取离子峰面积(y)为纵坐标,相应的质量浓度(x,ng/mL)为横坐标,进行线性回归计算,得到线性方程、线性范围、相关系数。采用空白基质配制标准溶液,以3倍信噪比和10倍信噪比对应的质量浓度分别作为方法的检出限(LOD)和定量下限(LOQ),结果见表3。在空白基质中添加12种糖皮质激素,添加水平分别为10,20,40 μg/kg,每个添加水平平行测定6 次,回收率与相对标准偏差(RSD)结果见表4。12种化合物在2~500 ng/mL范围内呈良好的线性关系,检出限为1~2 μg/kg,定量下限为3~5 μg/kg,回收率为78.3%~112.5%,RSD为1.0%~11.2%。该方法完全能够满足实际样品的筛查和确证需要。
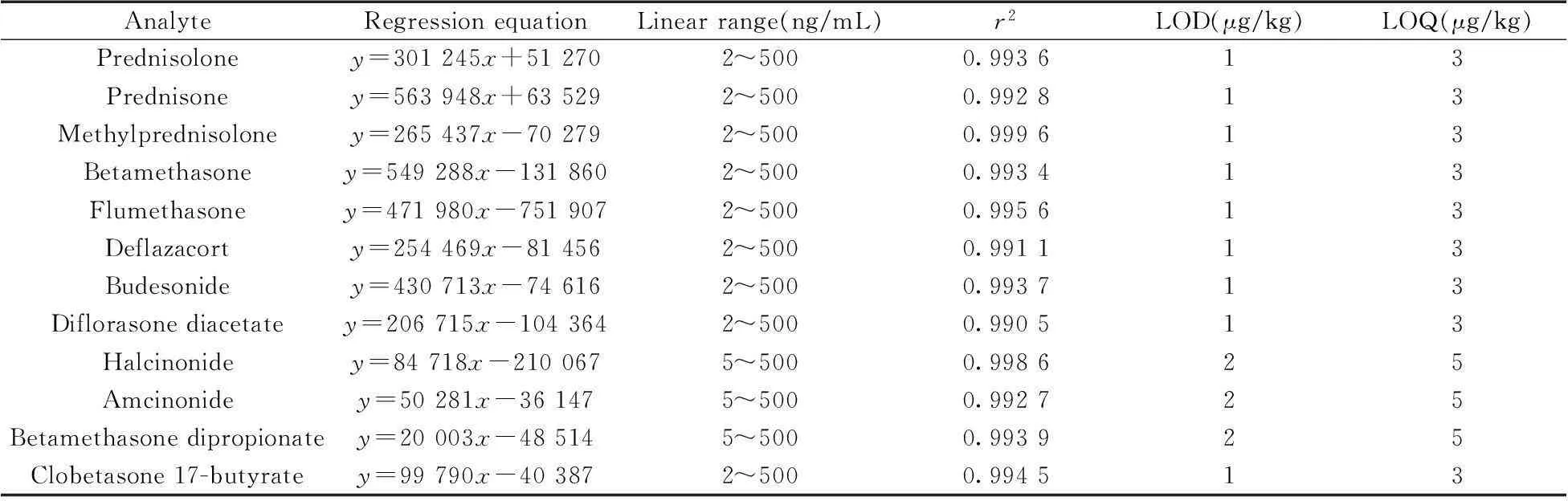
表3 12种化合物的线性关系、线性范围、检出限与定量下限

表4 12种糖皮质激素的回收率与相对标准偏差
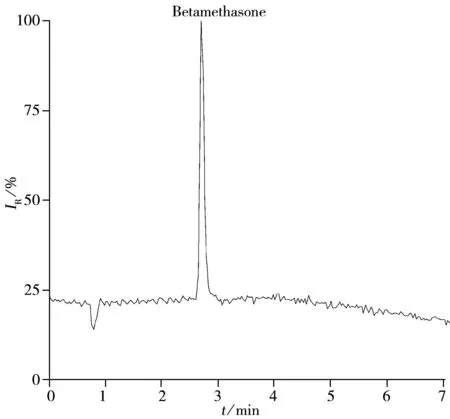
图2 某化妆品样品中倍他米松的提取离子色谱图Fig.2 Extracted ion chromatogram of betamethasone in a real sample
2.7实际样品的检测
利用本方法对购自超市的20份化妆品进行筛查分析,在某品牌化妆品中检出倍他米松(见图2),含量为280 μg/kg。将原始数据导入建立的筛查列表进行筛查,结果显示,该化妆品中含有倍他米松,其在保留时间、一级母离子、二级碎片离子、同位素理论分布等方面与倍他米松标准物质高度一致(提取的母离子、主要子离子误差小于5 ppm)。根据欧盟2002/657/EC的规定,利用高分辨率质谱对禁用药物确认至少需要4个识别点,而利用本方法,获得了大于9个识别点(母离子505.260 62,碎片离子149.023 51,71.086 33,279.174 20)的定性分数。利用国标GB/T24800.2-2009《化妆品中四十一种糖皮质激素的测定 液相色谱/串联质谱法和薄层层析法》对该样品进行测定,得到倍他米松的含量为302 μg/kg,与本方法测定的含量相差较小。由此可见,利用本方法对化妆品中糖皮质激素进行筛查和确认是可行的。
3结论
本实验利用超高效液相色谱-四极杆-静电场轨道阱串联质谱对化妆品中的12种糖皮质激素物质进行筛查。在10 min内完成了对12种糖皮质激素较好的分离,建立了筛查列表以及二级质谱图数据库,筛查确证结果可信度较高,该方法前处理简便、抗干扰性强,可实现在无标物情况下对样品的筛查,且自建数据库可扩充,是对现有国家标准检测化妆品中糖皮质激素物质的有力补充。
参考文献:
[1]Lu Y,Qiu Y H,Chen P P,Liu J J,Wang T J,Li J.Chin.J.Pharm.Anal.(鲁艺,邱颖姮,陈平平,刘吉金,王铁杰,李军.药物分析杂志),2010,30(10):1913-1914.
[2]China Information.ChinaHasBecometheLargestCosmeticsConsumerMarketwithAnnualConsumptionof200Billion.(中国报告大厅.我国成全球最大化妆品市场之一年销售额达2000亿),[2015-01-19].http://www.chinabgao.com/stat/stats/40148.html.
[3]Hygienic Standard for Cosmetics.Ministry of Health of the People’s Republic of China(化妆品卫生规范.中华人民共和国卫生部).[2007-01].
[4]Zhao X Y,Lin Y F,Hu X Z,Fu X F,Li J,Wang P.Chin.J.Anal.Lab.(赵晓亚,林雁飞,胡小钟,付晓芳,李晶,王鹏.分析试验室),2009,28(2):111-115.
[5]Wang W P,Zhang M Y,Lin J,Yakufu P.Chin.J.Pharm.Anal.(王伟萍,张明玥,蔺娟,帕孜来提·亚库甫.药物分析杂志),2013,33(5):837-843.
[6]Xu J Z,Zhang X Y,Ding T,Wu B,Shen C Y,Jiang Y,Liu F.Chin.J.Anal.Chem.(徐锦忠,张晓燕,丁涛,吴斌,沈崇钰,蒋原,刘飞.分析化学),2009,37(3):341-346.
[7]Tan L C,Ge F,Shan Z J,Wang Y.Chin.J.Anal.Chem.(谭丽超,葛峰,单正军,王懿.分析化学),2012,40(4):545-550.
[8]Zhang Y J,Li X D.J.Instrum.Anal.(张雅军,李晓东.分析测试学报),2007,26(Suppl):67-68.
[9]Xia R,Che B Q,Zhang Z.Chin.J.Chromatogr.(夏瑞,车宝泉,张喆.色谱),2007,25(6):926-929.
[10]Sun X T,Shang S M,Chen X Y,Wang Y,Li J.Chin.J.Anal.Chem.(孙雪婷,商少明,陈秀英,汪云,李娟.分析化学),2014,42(1):36-40.
[11]Chen X,Tian Z Z,Liu Y,Huang Y,Cao Y H.J.Instrum.Anal.(陈新,田志壮,刘瑛,黄尧,曹玉华.分析测试学报),2011,30(2):203-206.
[12]Li B X,Zheng M M,Lu L X,Wu X P.Chin.J.Chromatogr.(李博祥,郑敏敏,卢兰香,吴晓苹.色谱),2011,29(8):798-804.
[13]Chen D W,Lü B,Zou J H,Yang X,Miao H,Zhao Y F.J.Instrum.Anal.(陈达炜,吕冰,邹建宏,杨欣,苗虹,赵云峰.分析测试学报),2014,33(12):1327-1333.
[14]Ding T,Lü C,Liu H,Guo L,Wu B,Chen G S,Shen C Y,Zhang R,Fei X Q,Zhang X Y,Yu J L.J.Instrum.Anal.(丁涛,吕辰,柳菡,郭玲,吴斌,陈国松,沈崇钰,张睿,费晓庆,张晓燕,庾金良.分析测试学报),2014,33(1):27-32.
[15]Wu B,Ding T,Liu H,Chen H L,Zhao Z Y,Zhang R,Shen C Y.Chin.J.Chromatogr.(吴斌,丁涛,柳菡,陈惠兰,赵增运,张睿,沈崇钰.色谱),2012,30(12):1246-1252.
[16]Sun Y A,Wang K,Li Z X,Yu W H,Wang G Q.J.HenanNormalUniv.:Nat.Sci.Ed.(孙雨安,王珂,李振兴,于文浩,王国庆.河南师范大学学报:自然科学版),2015,43(3):69-73.
[17]Li Z Y,Wang F M,Niu Z Y,Luo X,Chen J H,Wang X R.J.Anal.Sci.(李兆永,王凤美,牛增元,罗忻,陈军辉,王小如.分析科学学报),2015,31(2):171-177.
[18]Li Z Y,Wang F M,Niu Z Y,Luo X,Zhang G,Chen J H.Chin.J.Chromatogr.(李兆永,王凤美,牛增元,罗忻,张罡,陈军辉.色谱),2014,32(5):477-484.
Screening of 12 Glucocorticoids in Cosmetics by High Performance Liquid Chromatography-High Resolution Mass Spectrometry
LI Qiang1,2,ZHANG Xiao-guang1,2,MA Jun-mei1,2,LI Run-yan1,2,FAN Su-fang1,2,ZHANG Yan1,2*
(1.Hebei Food Inspection and Research Institute,Shijiazhuang050091,China;2.Key Laboratory of Food Safety of Heibei Province,Shijiazhuang050091,China)
Abstract:A method was developed for screening of 12 kinds of glucocorticoids in cosmetics by high performance liquid chromatography-quadrupole/orbitrap high-resolution mass spectrometry(Orbitrap MS) .The samples were extracted with acetonitrile,and separated with an Acquity UPLC BEH C18(100 mm×2.1 mm,1.7 μm) using a binary solvent system composed of 0.1% formic acid methanol solution and 0.1% formic acid water solution by gradient elution.Accurate mass number of target compound were got in full scan mode.Compared to accurate mass number in theory,the mass accuracy error was below 2×10-6.The screening list was built,and the database of secondory characteristic fragment ions for the glucocorticoids were added in screening option.Qualitative screen was achieved.The limits of detection(LOD) of the method ranged from 1 μg/kg to 2 μg/kg,and the limits of quantitation(LOQ) ranged from 3 μg/kg to 5 μg/kg.Satisfactory recoveries from 78.3% to 115.2% were obtained at spiked concentration levels of 10,20,40 μg/kg,and the relative standard deviations(RSDs) were in the range of 1.0%-11.2%.The method could be used for the determination of glucocorticoid in cosmetics as a high-throughput and confirmatory method.
Key words:ultra high performance liquid chromatography;orbitrap mass spectrometry(Orbitrap MS);glucocorticoid;cosmetic
中图分类号:O657.63;O629.8
文献标识码:A
文章编号:1004-4957(2016)02-0179-06
doi:10.3969/j.issn.1004-4957.2016.02.008
*通讯作者:张岩,博士,高级工程师,研究方向:化学生态学,Tel:0311-67568335,E-mail:snowwinglv@126.com
收稿日期:2015-08-19;修回日期:2015-09-16

