化妆品中有害物质分析检测方法研究进展
朱 俐,刘 洋,曾三平,王伟娇,陈亚飞,尹利辉*
(1.中国食品药品检定研究院,北京 100050;2.湖南省食品药品检验研究院,湖南 长沙 410001)
化妆品中有害物质分析检测方法研究进展
朱俐1,刘洋1,曾三平2,王伟娇2,陈亚飞1,尹利辉1*
(1.中国食品药品检定研究院,北京100050;2.湖南省食品药品检验研究院,湖南长沙410001)
摘要:功能性化妆品常被非法添加禁限用物质,不仅侵害消费者利益和身体健康,也扰乱了市场秩序。该文按检测的有害物质分类,重点讨论了近些年非法添加的药用物质(激素、抗生素)、防腐剂、防晒剂和其他有毒有害物质的较新颖的前处理技术和检测方法,并对化妆品检测方法的发展前景进行了展望,引用文献86篇。
关键词:化妆品;有害物质;分析方法;综述
化妆品的质量安全一直是人们关注的热点,目前化妆品种类繁多,各种不同成分、不同功效的化妆品层出不穷,我国《化妆品卫生规范》(2007年版)规定了1 286种(类)禁用物质、73种(类)限用物质、56种限用防腐剂、28种限用防晒剂[1],虽然这些禁限用物质对人体有一定的毒副作用,但部分企业在经济利益的驱使下,为了片面追求某种效果,例如美白、祛痘等功效,在化妆品配方中非法添加禁用物质或者超量使用限用物质。长期使用这类化妆品将造成人体的多种急性或慢性损伤。因此,化妆品中有毒有害物质检测方法的研究,不仅有助于提高政府的监管能力,而且有利于保障消费者利益和身体健康。目前化妆品的分析方法主要有高效液相色谱法、液相色谱-质谱联用法、固相萃取/液相色谱法和毛细管电泳法等。本文按检测的物质分类,综述了近些年较新的样品预处理技术和检测方法,以期对化妆品的检测研究提供参考。
1非法添加药用物质
功能化妆品常非法添加激素和抗生素药用物质,影响了化妆品的使用安全。在化妆品中检出的非法添加药物大部分为激素和抗生素[1]。
1.1激素类
在化妆品中添加激素可以快速嫩肤、美白、祛斑、祛痘、抗敏,但长期使用会造成内分泌失调、激素依赖性皮炎等多种疾病的发生。化妆品中添加的激素主要有糖皮质激素和性激素这两类甾体类固醇激素,糖皮质激素主要起抗炎、免疫抑制等作用,性激素主要有促进毛发生长、丰乳、美白、除皱等功效。已报道的检测方法大部分是高效液相色谱法(HPLC)[2]和超高效液相色谱[3],前处理一般采用萃取的方法,文献中根据萃取对象做了不同程度的改进和优化,李晶瑞等[3]采用超高效液相色谱-串联质谱法同时测定祛痘化妆品中的15种禁用雄激素,方法针对不同类型的化妆品样品,以甲醇为提取溶剂进行超声提取,样品提取液经离心处理后,上清液以 Oasis HLB 固相萃取柱净化,经ACQUITY UPLC BEH C18(2.1 mm×50 mm,1.7 μg)色谱柱分离,目标化合物在正离子模式下电离,采用多反应监测模式进行定性定量分析。结果表明,15种禁用雄激素的定量下限为1.0~20.0 μg/kg,在低、中、高3个加标水平下的平均回收率为76.5%~92.1%,相对标准偏差(RSD)为1.3%~9.6%。该方法准确、快速、灵敏,能够为祛痘化妆品检验和生产质量控制提供科学依据及技术支持。De Orsi等[4]采用超声萃取与HPLC联用技术建立了美甲产品中7种邻苯二甲酸酯的检测方法,采用乙醇-水(90∶10)超声萃取,C18柱为色谱柱,梯度洗脱,检测波长为254 nm。7种邻苯二甲酸酯的线性范围为5~200 μg/mL,检出限约为0.5 μg/mL。采用超声萃取和液相色谱联用检测化妆品中的激素灵敏度较低,聚合物整体柱是一种新型固相微萃取分离介质,这种材料具有取材广泛、萃取体积小等优点。文毅等[5]利用聚合物整体柱微萃取与高效液相色谱联用技术,建立了同时检测水性化妆品中睾酮、甲基睾酮和孕酮含量的分析方法。样品经过磷酸盐溶液稀释和过滤后可直接进行萃取分析。睾酮、甲基睾酮和孕酮在10~1 000 μg/L浓度范围内具有良好的线性关系,检出限分别为2.3,2.8,4.6 μg/L,应用于实际样品的检测,3种激素的加标回收率为83%~119%。Lei等[6]采用磁力搅拌液液微萃取法提取化妆品中的8种激素,并采用高效液相色谱法进行检测,检出限为0.91~1.01 ng/mL。Vias等[7]用乙腈超声辅助萃取后,再用分散液液微萃取方法提取化妆品中的邻苯二甲酸酯,采用液相色谱-二极管阵列检测器(HPLC-DAD)和电喷雾离子阱串联质谱(ESI-IT-MS /MS)在多反应监测模式(MRM)下进行检测,检出限在0.04~0.45 ng/mL之间,回收率为84%~124%,RSD低于10%,分析检测了33个实际样品,发现邻苯二甲酸二乙酯的检出率最高。气相色谱法的相关文献较少,Llompart等[8]采用基质固相分散和气相色谱-质谱联用,建立了化妆品中18种邻苯二甲酸酯类的检测方法,检出限为1.4~17 ng/g。实际样品检测最常见的化合物为邻苯二甲酸二乙酯,检出含量为0.7~3.57 μg/g。
毛细管电泳法由于具有快速、高效、超低样品量、低溶剂用量等优点,也是近年来化妆品中激素类检测应用较为广泛的一种方法。陈新等[9]建立了以离子液体为添加剂的反向微乳毛细管电泳(MEEKC)法,分离测定化妆品中氢化可的松、泼尼松和醋酸氧化可的松3种糖皮质激素,其检出限为5~800 mg/L,方法快速、灵敏、有效,已成功用于实际样品中糖皮质激素的检测。由于β-环糊精具有独特的中空筒状疏水性空腔,可以作为第二固定相运用于毛细管电泳中,提高了复杂组分的分离度,可分离更多结构相似的激素。李萌等[10]建立了以离子液体和β-环糊精为添加剂的反向微乳毛细管电泳(MEEKC)法分离测定化妆品中丙酸氟替卡松、曲安奈德、醋酸可的松、地塞米松、氢化可的松和泼尼松6种激素。在优化实验条件下,6种物质于12 min内达到基线分离,检出限最低可达0.66 mg/L。为了提高检测灵敏度,孙雪婷等[11]采用场放大堆积反向微乳毛细管电色谱电动进样,建立了在线富集检测化妆品中6种糖皮质激素的分析方法。在优化条件下,6种激素的富集倍数可达100~186倍,与常规毛细管电泳法相比,方法灵敏度提高了2个数量级。除了反相微乳毛细管电泳,还有采用毛细管电动色谱分离分析化妆品中激素类物质的文献报道,如Xu等[12]采用两亲聚合物胶束(甲基丙烯酸甲酯和甲基丙烯酸)作为毛细管电动色谱(EKC)的准固定相,分析检测化妆品中8种激素类物质(氢化可的松、泼尼松龙、醋酸氢化可的松、泼尼松、醋酸可的松、醋酸泼尼松龙、地塞米松和曲安奈德),在优化条件下,8种激素类物质可在16.5 min分离检测,该方法精度高、可重复、预处理简单,适用于化妆品的质量控制。
就目前来看,文献报道的前处理方法以固相萃取为主,但这类方法溶剂消耗大且灵敏度较低,为了提高检测灵敏度,也有不少研究采用较新颖的样品预处理技术如整体柱微萃取[5]、磁力搅拌多级液液微萃取[6]和分散液液微萃取[7]。微萃取技术不仅减少了有机试剂的用量而且提高了富集因子,结合液相色谱法[4]、液质联用技术[7]和毛细管电泳[11]等检测技术,大大降低了检出限。由于化妆品基质成分复杂且激素类化合物为化妆品中的禁用物质,因此建立准确、灵敏度高的检测方法,严格控制该类化妆品质量尤为重要。
1.2抗生素类
抗生素因具有杀菌、抑菌的功效,常被非法添加在祛痘化妆品中,长期使用会导致耐药性,后续治疗更加困难。我国《化妆品卫生规范》(2007年版)规定此类物质为禁用成分,因此,研究化妆品中抗生素的检测方法,对政府更好地实施卫生监督、保障消费者身体健康具有重要意义。目前,化妆品中抗生素的检测方法为液相色谱法[13]、超高效液相色谱-串联质谱法[14]和高效液相色谱-串联质谱法[15]等,前处理仍以萃取方法为主。Jin等[16]建立了抗痘类化妆品中抗生素的快速LC-DAD检测方法,样品采用0.1 mol/L磷酸缓冲液(pH 2.5)和石油醚提取,色谱柱为SB RP18(50 mm× 4.6 mm,1.8 μm),流动相为0.1 mol/L磷酸二氢钾(pH 2.5)和乙腈,梯度洗脱,该方法可在7 min内检测9种抗生素,检出限为0.02~0.2 μg/mL。Wu等[17]建立了化妆品5种盘尼西林抗生素的超高效液相色谱检测方法,样品经液液萃取后用UPLC-DAD分析检测,采用C18(100 mm× 2.1 mm,1.7 μm)色谱柱,流动相为乙腈和磷酸二氢钾缓冲溶液(pH 5.5),梯度洗脱,待测物的检出限可达0.2 μg/mL。Liu等[18]用中性解析电离-萃取电离质谱联用建立了化妆品中磺胺类抗生素的检测方法,检出限为0.001~1 ng/g,检测时间小于1 min,适用于粘性化妆品样品的检测。
关于化妆品中抗生素检测的文献相对较少,分析原因可能是因为抗生素的检测方法研究较早,一般采用液相色谱法,方法已较为成熟。根据近期报道,液质联用及UPLC已经逐渐应用于化妆品中抗生素的检测。由于抗生素在化妆品中属于禁用物质,因此亟需建立高灵敏、快速、环保并能够同时分析多种组分的方法,用于质量监督。
2防腐剂类
化妆品中的防腐剂主要用于杀灭和抑制化妆品中的微生物,是长时间维持化妆品品质的保护剂。防腐剂种类繁多且均有一定的毒性,化妆品中常用的防腐剂按化学结构可分为甲醛供体和醛类衍生物防腐剂(如咪唑烷基脲、季铵盐等),苯甲酸及其衍生物防腐剂(如苯甲酸、对羟基苯甲酸酯类),醇类防腐剂(如苯氧乙醇、苯甲醇等)和其他有机化合物防腐剂(如布罗波尔、异噻唑啉酮类等)。
HPLC广泛应用于化妆品中防腐剂的检测[19-20],前处理常用甲醇超声提取,过滤后直接检测。 Gao等[19]建立了一种快速、灵敏的HPLC方法用于检测膏状化妆品中的氢醌、苯酚和6种防腐剂,采用甲醇-水(60∶40)提取,C18色谱柱(100 mm×2.1 mm)分离,甲醇和0.05 mol/L甲酸铵(pH 3.0)梯度洗脱,结果表明,8种待测物在10 min内完全分离,检出限为0.05~1.0 μg/mL。
武婷等[21]比较了甲醇、乙醇、四氢呋喃和流动相等4种溶剂对不同种类化妆品(膏霜类、水类)的提取效率,发现甲醇对各物质的提取率均较高,提取效果最佳,采用反相HPLC建立了24种防腐剂的检测方法。由于化妆品中油脂成分含量较高,单纯采用有机溶剂萃取不仅效率低而且用量较大,因此研究人员在前处理技术方面进行了改进。 Msagati等[22]采用中空纤维液体膜(HFSLM)萃取化妆品中的对羟基苯甲酸酯,以2-n-己基醚作为有机试剂固定中空纤维膜,HPLC-UV进行分析检测,该萃取方法简单、便宜,且降低了有机试剂的使用量。由于防腐剂的挥发性弱,采用浸入式固相微萃取方法富集时,对萃取材料的耐溶剂性能有很高的要求。费婷等[23]使用丙烯酸-3-三氯硅烷基异丙酯(TPM)对玻璃纤维表面进行预处理,然后通过紫外光引发双丙烯酸封端的聚乙二醇(PEG-DA)在纤维表面聚合制备了高分子材料涂层,使萃取纤维获得了良好的抗溶剂性能,考察了涂层制备中不同平均分子质量PEG-DA的使用对萃取结果的影响,并优化了萃取条件。同一纤维对样品检测结果的重复性及不同纤维间样品检测结果的重现性均良好。萃取纤维的饱和吸附容量约为540 μg,结合高效液相色谱技术,成功实现了化妆品中对羟基苯甲酸酯类防腐剂的快速检测,方法检出限(S/N=3)可达0.12~0.15 μg/mL。
气相色谱法也是目前化妆品中防腐剂的主要检测方法,前处理大多使用甲醇、乙醇或丙酮超声提取。王改香等[24]采用气相色谱-质谱法(GC-MS)同时测定化妆品中的10种防腐剂含量,样品经甲醇超声提取,无水硫酸钠脱水后过滤进样检测。侯雪丽等[25]采用硫酸催化甲酯化气相色谱法检测了化妆品中的十一烯酸及其锌盐,方法适用于膏霜、乳液、化妆水和洗手液中十一烯酸的检测。Tsai等[26]联用固相微萃取和GC-MS建立了化妆品中防腐剂的检测方法,实验发现在石英纤维上涂聚丙烯酸酯可获得最高的提取效率,检出限为0.4~8.5 ng/mL。Saraji等[27]采用单液滴微萃取(SDME)后注射器内衍生,用GC-MS对化妆品中的对羟基苯甲酸酯类防腐剂进行测定,检出限为0.001~0.015 μg/L,富集倍数为23~150倍,RSD为8.1%~13%。
目前,有部分文献报道采用毛细管电泳技术检测化妆品中的防腐剂。韩康等[28]采用毛细管电泳法对化妆品中氢醌、苯酚、山梨酸和苯甲酸进行分离研究,考察了缓冲溶液种类和pH值对分离的影响。以15 mmol/L 硼砂(pH 9.2)为电泳缓冲液,采用压力进样方式,在20 kV恒压下进行分离,并在波长240 nm处检测,各组分可达到基线分离。4种标样在0.5~100.0 mg/L范围内呈良好的线性关系,加标回收率为93.2%~110.1%,方法的检出限为0.1~0.5 mg/L。 Ye等[29]采用石墨烯作为固相萃取(SPE)吸附剂萃取化妆品中的防腐剂,并用毛细管电泳法进行检测,优化了SPE萃取参数,用25 mmol/L硼酸盐溶液(pH 10.0)作为缓冲液,结果显示4种对羟基苯甲酸酯可在10 min内达到分离,检出限最低可达0.1 mg/L。由于传统毛细管电泳方法的检测灵敏度较低,有时不能满足质量监控要求,因此,近年来在线富集技术成为毛细管电泳分析领域的研究热点,仅通过对缓冲液组成和进样程序进行调控即可显著提高检测灵敏度。Han等[30]通过自制分流接口实现了毛细管电泳和流动注射分析的联用,并成功应用于化妆品中对羟基苯甲酸酯类防腐剂的在线分析检测。对MEKC分离条件和固相萃取条件进行优化,实验发现,通过在线C8固相萃取前处理过程,增大了样品的富集倍数,减少了化妆品复杂基体对分离测定的干扰,大大提高了方法的分析速度、分析的选择性和灵敏度。胶束毛细管电泳(MECC)[31-32]拓宽了毛细管电泳的应用范围,Wang 等[31]采用胶束电动毛细管电泳电化学检测(MECC-ED)建立了同时检测化妆品中8种酚类防腐剂的方法,以9 mmol/L十二烷基硫酸钠(SDS)-60 mmol/L硼酸盐缓冲液(pH 8.0)为缓冲液,8种分析物在26 min内实现良好分离,检出限为1.1×10-7~1.2×10-6g/mL,实际样品分析结果满意。 Huang等[32]采用胶束毛细管电泳紫外检测器建立了化妆品中7种防腐剂的检测方法,检出限为0.31~1.52 μg/mL。Huang等[33]比较了胶束毛细管电泳(MEKC)和微乳毛细管电泳(MEEKC)对化妆品中苯甲酸、山梨酸、对羟基苯甲酸乙酯及丙酯和脱氢乙酸等防腐剂的分析测定。研究了温度、缓冲溶液pH值以及表面活性剂浓度对分离的影响。通过改变温度可以提高分离度,高浓度SDS可以保证微乳滴的稳定性。比较结果发现,MEEKC方法比MEKC方法需要更长的分离时间和更高的pH值。表1总结了近年来报道的化妆品中防腐剂的检测方法。
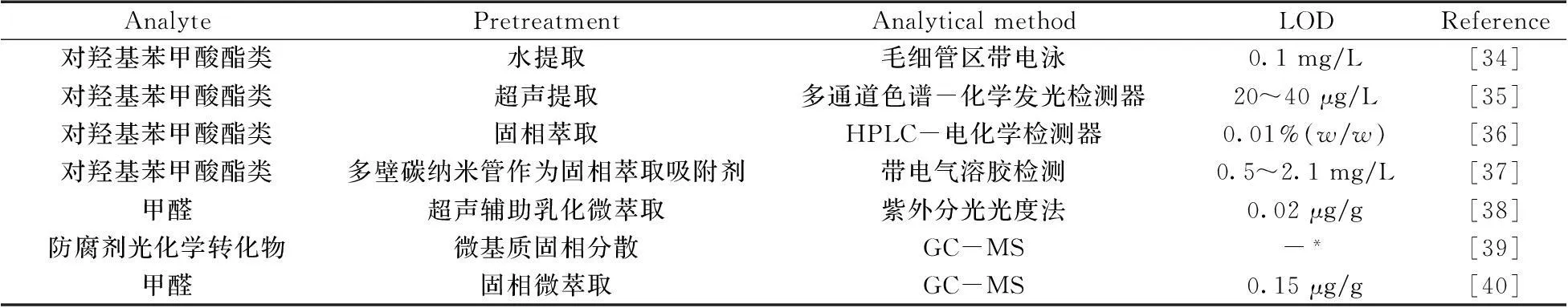
表1 近期报道的化妆品中防腐剂的检测方法
*no data
近期关于化妆品中防腐剂的检测文献报道,检测对象大部分是对羟基苯甲酸酯类,早期的检测方法多为HPLC-UV法,近期有研究开始采用毛细管电泳法[34]、HPLC-化学发光检测器[35]、HPLC-电化学检测器[36]及光谱法检测化妆品中的防腐剂。光谱法相比较于HPLC灵敏度较低,易受基体干扰,因此常采用化学计量学的方法进行数据处理,同样能得到较好的检测结果,Esteki等[41]采用分光光度法和连续投影算法同时研究了化妆品中对羟基苯甲酸甲酯和对苯二酚的检测方法,回收率可达84%~112%,方法无需萃取过程,简单、快速、经济、环保。方凤等[42]采用紫外多波长光谱,构建本底光谱库和标准光谱库,采用向量扣减方法分析了化妆品中的对羟基苯甲酸酯,方法线性范围为0.25~10 mg/L,线性系数r>0.999 2,测量相对误差小于1.2%,其结果与液相色谱法结果接近。
3防晒剂类
防晒剂是使化妆品具有防晒功能的活性物质,能有效防止有害波长的紫外线直接侵害皮肤。防晒剂最初仅用于防晒护肤品,现已广泛应用于保湿日霜、护发产品、须后水、口红及彩妆等产品。防晒剂可分为物理阻挡剂(如二氧化钛、氧化锌等)和紫外吸收剂(如甲氧基肉桂酸乙基己酯和丁基甲氧基二苯酰基甲烷等)。通常认为防晒剂在化妆品中的浓度低于规定标准,则会使该产品达不到宣称的SPF值,而浓度太高,又会对皮肤产生毒副作用。根据《化妆品卫生规范》(2007版),我国目前允许使用的紫外吸收剂共有28种,并规定了其最高允许使用浓度。因此,控制化妆品中紫外吸收剂的含量不仅事关产品质量,而且事关消费者的身体健康。化妆品中紫外吸收剂的检测最常用的是液相色谱法[43-44],Chisvert等[44]在流动相中加入羟丙基-β-环糊精,使得7种防晒剂在20 min内分离,检出限为1.5~2.3 mg/L。该课题组[45]又研究了一种环境友好的反相液相色谱方法检测化妆品中的18种防晒剂,可应用于霜、乳液、唇膏等化妆品。气相色谱法最早在1972年应用于化妆品中防晒剂的检测,Paulus[46]检测了防晒霜中的肉桂酸酯和水杨酸酯。由于气相色谱法要求被检测的物质具有挥发性和热稳定性,而大多数紫外吸收剂都具有较高的沸点,因此限制了GC在这方面的应用,文献较少,且集中在早期。Li等[47]、Masse等[48]建立了化妆品中防晒剂的气相色谱-质谱联用检测方法。还有部分文献用毛细管电泳技术分析检测化妆品中的防晒剂,如Wang等[49]以甲醇和乙酸作萃取溶剂,超临界流体萃取(SFE)法提取化妆品中的对氨基苯甲酸酯和肉桂酸酯,采用胶束电动毛细管电泳测定,回收率为98.43%~101.83%,检出限为157~828 ng/mL,所建立的方法在灵敏度和重现性上稍逊于HPLC,但更快速、经济。Klampfl等[50]建立了胶束毛细管电泳方法用十二烷基硫酸钠(SDS)和十二烷基聚乙二醇醚(Brij 35)检测9种防晒剂,并用于商业防晒化妆品的分析检测[51]。Júnior等[52]用电化学方法检测了化妆品中的防晒剂奥克立林(OCR)。表2为近期报道的化妆品中防晒剂的检测方法 。

表2 近期报道的化妆品中防晒剂的检测方法
*no data
已报道的化妆品中防晒剂的检测研究大部分集中在紫外吸收剂方面,方法大多使用液相色谱法,近年来也有部分文献采用气相色谱法[47-48,57]、毛细管电泳法[49,51,55]、电化学方法[52]、分子光谱法[53]及激光诱导击穿光谱法[56]等对化妆品中的防晒剂进行检测。
4其他有毒有害物质的检测
除上述激素、抗生素、防腐剂和防晒剂之外,化妆品中还有很多禁限用的有毒有害物质,如美白抗氧化作用的氢醌[58-61]、泛醇[62-63]、磷酸酯类[64]、尿素[65]、过敏类[66]、松香酸[67]、重金属[68-76]、杀菌剂[77-78]、着色剂[79-80]、杜鹃醇[81]、香豆素类[82]、阿魏酸[83]、多环芳烃[84]等,且大部分采用色谱以及毛细管电泳法进行分析。还有一些较新颖的方法,如Wang 等[72]建立了化妆品中Hg2+的间接竞争性酶联免疫吸附(ELISA)测定方法,线性范围为0.1~100 ng/mL,检出限为0.08 ng/mL;该方法与冷原子吸收光谱的线性关系为0.98,方法灵敏、快速、准确。尹利辉[74-76]课题组采用X射线荧光元素分析技术建立了化妆品中重金属的无损检测方法,经济环保,可实际应用。关于化妆品中其他有毒有害物质检测的近期文献总结如表3所示。

表3 近期报道的化妆品中其他有毒有害物质的检测方法
(续表3)

AnalytePretreatmentAnalyticalmethodLODReference熊果苷、氢醌超声萃取HPLC-DAD0.0085~0.0119μg/mL[61]泛醇SPESFC0.5μg/mL[62]泛醇加碱水解后茚三酮处理荧光光谱法0.005μg/mL[63]5种磷酸三酯类化合物(OPEs)膏霜乳液类和蜡基类化妆品经溶剂提取后,采用,固相萃取柱净化;粉剂类和水剂类化妆品经溶剂提取、浓缩后直接检测GC-MS1.0~30μg/kg[64]尿素,尿囊素、焦谷氨酸和赖氨酸乙腈提取后,残渣60℃干燥,然后水提取亲水作用液相色谱0.7~13.5μg/mL[65]挥发性可致过敏原直接接触吸收带萃取(DC-STE)GC-MS15~200ng/mL[66]松香酸(AA)和脱氢枞酸(DHAA)密闭注射器内超声提取衍生HPLC-FLD-MS/MSAA:8.2~10.8ng/mL;DHAA:19.4~24.3ng/mL[67]吡硫锌超声提取HPLC,HPLC-MS/MS0.015%(HPLC),0.003%(HPLC-MS/MS)[68]Ge,As,Cd,Sb,Hg,Bi流动注射蒸汽发生ICP-MS0.025~0.2ng/g[69]Hg2+-荧光相关光谱(FCS)和寡核苷酸的识别0.14nmol/L[70]Al,Si,P,S,K,Ca,Ti,Mn,Fe,Ni,Cu,Zn,As,Br,Rb,Sr,Ba,Cd,Ce,Nd,Pb,Μo,Th,La无需预处理能量色散偏振X射线荧光光谱法(ED-PXRF)-[71]Hg2+30%HNO3提取酶联免疫法(ELISA)0.08ng/mL[72]Hg甲酸溶解同位素稀释电感耦合等离子体质谱0.6pg/mL[73]铅、砷无需预处理X射线荧光元素分析5mg/kg[74]铅、汞、砷、锑无需预处理X射线荧光元素分析2mg/kg[75]汞无需预处理X射线荧光元素分析5mg/kg[76]百菌清、腈菌唑、敌菌丹等5种禁用杀菌剂氯化钠破乳,甲醇提取,无水硫酸钠脱水,分散固相萃取净化气质联用0.1,0.2,0.01mg/kg[77]甲硝唑,奥硝唑,洛硝唑和塞克硝唑4种硝基咪唑类化合物碳酸钠溶液溶解后,乙酸乙酯提取气质联用0.05~0.1mg/kg[78]酸性紫49,颜料红57,颜料红53∶1,酸性黄36,结晶紫,罗丹明B分散黄3,颜料橙5,苏丹红Ⅰ,苏丹红Ⅱ,苏丹红Ⅳ,和溶剂蓝35,12种合成着色剂四氢呋喃(THF),二甲基亚砜(DMSO)和甲醇分步超声波辅助萃取,HLB固相萃取柱净化超高效液相色谱串联质谱法1.4~2000μg/kg(LOQ)[79]吖啶黄,溶剂蓝35,溶剂红49,酸性紫49,氯化四甲基副玫瑰苯胺,颜料橙5,颜料红53,氯化五甲基副玫瑰苯胺,苏丹红Ⅱ,氯化六甲基副玫瑰苯胺,苏丹红Ⅳ,罗丹明B,分散黄3,苏丹红Ⅰ,14种禁用着色剂四氢呋喃分散,并对目标物进行提取后,用含有醋酸铵的甲醇)水混合溶液将基质析出高校液相色谱法3~10μg/g(LOQ)[80]杜鹃醇5%三氯乙酸-乙腈混合溶液(70∶30)超声提取15min超高校液相色谱2.5mg/kg(LOQ)[81]香豆素经超声提取后,以OasisHLB固相萃取柱净化超高效液相色谱-四极杆-飞行时间质谱10~60μg/kg(LOQ)[82]阿魏酸-纸基比色装置-TLC7ppm[83]
(续表3)

AnalytePretreatmentAnalyticalmethodLODReference荧蒽,苯并[a]蒽,苯并[b]荧蒽,苯并[a]芘,二苯并[a,h]蒽,苯并[g,h,i]芘6种多环芳烃超声萃取-在线富集反相微乳毛细管电泳8.8~84mg/L[84]
*no data
5结论及展望
目前,化妆品中有害物质的分析检测方法以液相色谱法为主,多采用UV、DAD检测器,化学发光检测器和电化学检测器也有一些应用;毛细管电泳及相关技术正逐渐发展,且报道日益增多。原子光谱技术,如火焰原子吸收光谱、电感耦合等离子体和X射线荧光光谱已用于化妆品中金属的检测,该类方法具有良好的特性,均可应用于化妆品中有毒有害物质的分析检测。然而由于化妆品基质复杂,大多数检测方法均要预处理,需消耗一定的有毒试剂,对人员的身体健康和环境产生一定的危害。值得一提的是已有采用分子光谱[41,53,85]进行化妆品检测的文献报道,方法采用化学计量学进行数据处理,克服了分子光谱灵敏度低的问题。虽然化妆品基质复杂限制了分子光谱技术在这方面的应用,但该方法不需要使用有毒试剂进行复杂的前处理,快速、经济、环保,且结果与HPLC法非常接近,为化妆品的现场分析提供了可行方案。
“绿色”分析化学已成为目前化妆品检测的发展方向,可通过仪器小型化(如便携式仪器)、新材料(如纳米材料)、无毒试剂(如乙醇)等方法建立绿色分析化学方法。Mohamed[86]阐述了绿色分析化学检测化妆品的设计、开发和验证,目前科研工作者在化妆品检测方法开发时不仅要考虑到方法精确性,同时也要考虑其安全实用性和对环境的影响。目前,建立一种简单、准确、快速、环保并且灵敏的检测方法,对于化妆品的质量监控具有重要意义。
参考文献:
[1]Gao R Y.CosmeticsQualityInspection.Beijing:Chemical Industry Press(高瑞英.化妆品质量检验技术.北京:化学工业出版社),2011.
[2]Xiong X T,Tang J H,Li H Y,Zhao T T,Zhao Q W,Jia F,Wang J C,Xi S F,Wu Y L.J.Instrum.Anal.(熊小婷,谭建华,李慧勇,赵田甜,招启文,贾芳,王继才,席绍峰,吴玉銮.分析测试学报),2013,32(4):448-453.
[3]Li J R,Ma Q,Meng X S,Chen Y X,Ma H J,Zhang Q,Bai H.J.Instrum.Anal.(李晶蕊,马强,孟宪双,陈云霞,马会娟,张庆,白桦.分析测试学报),2015,34(1):43-49.
[4]De Orsi D,Gagliardi L,Porra R.Anal.Chim.Acta,2006,555(2):238-241.
[5]Wen Y,Wang Y,Zhou B S,Xu Y,Feng Y Z.Chin.J.Anal.Chem.(文毅,汪颖,周炳升,徐盈,冯钰铸.分析化学),2007,35(5):681-684.
[6]Lei L,Kang M Q,Li N.Anal.Methods,2014,6(11):3674-3681.
[8]Llompart M,Celeiro M,Lamas J P.J.Chromatogr.A,2013,1293:10-19.
[9]Chen X,Tian Z Z,Liu Y,Huang R,Cao Y H.J.Instrum.Anal.(陈新,田志壮,刘瑛,黄尧,曹玉华.分析测试学报),2011,30(2):203-206.
[10]Li M,Jin M M,Li J,Chen X,Shang S M,Liu Y,Mao M X.Chin.J.Anal.Lab.(李萌,金勉勉,李娟,陈新,商少明,刘瑛,毛明星.分析试验室),2012,31(2):75-78.
[11]Sun X T,Shang S M,Chen X Y,Wang Y,Li J.Chin.J.Anal.Chem.(孙雪婷,商少明,陈秀英,汪云,李娟.分析化学),2014,41(1):36-40.
[12]Xu X,Ni X,Cao Y,Zhuo X,Yang X,Cao G.Electrophoresis,2014,35(6):827-835.
[13]Lei Y,He J W,Huang Y T,Huang W J.J.Instrum.Anal.(雷毅,何嘉雯,黄艳婷,黄文静.分析测试学报),2013,32(3):326-330.
[14]Chen J,Zheng R,Ji S,Wang K.Chin.J.Anal.Chem.(陈静,郑荣,季申,王柯.分析化学),2013,41(6):931-935.
[15]Zhao X Y,Li J,Lin Y F,Hu X Z,Wang P,Fu X F,Li J.J.Instrum.Anal.(赵晓亚,李娟,林雁飞,胡小钟,王鹏,付晓芳,李晶.分析测试学报),2009,28(10):1138-1142.
[16]Jin W,Yang Y J,Wang W Y.Chromatographia,2009,69(11/12):1221-1226.
[17]Wu Z J,Peng Y.Adv.Mater.Res.,2011,233:87-90.
[18]Liu Y,Zhang X,Ouyang Y Z,Hu Z,Ma L,Zhang J H,Lin J M,Chen H W.J.MassSpectrom.,2011,46(8):794-803.
[19]Gao W,Legido-Quigley C.J.Chromatogr.A,2011,1218(28):4307-4311.
[20]Aoyama A,Doi T,Tagami T,Kajimura K.J.Chromatogr.Sci.2014,52(9):1010-1015.
[21]Wu T,Wang C,Wang X,Ma Q,Zhang F,Liu L.Chin.J.Anal.Chem.(武婷,王超,王星,马强,张帆,刘柳.分析化学),2007,35(10):1439-1443.
[22]Msagati T,Barri T,Larsson N,Jönsson J.Int.J.CosmeticSci.,2008,30(4):297-307.
[23]Fei T,Li H,Ding M,Ito M,Lin J M.J.Sep.Sci.,2011,34(13):1599-1606.
[24]Wang G X,Zhang L,Tang X J,Zhang S H,Zhao X,Hu G S.Phys.Test.Chem.Anal.:Chem.Anal.(王改香,张磊,唐晓军,张锁慧,赵鑫,胡国胜.理化检验:化学分册),2015,51(1):35-38.
[25]Hou L X,Li Q,Wu X J,Cui J J.J.Instrum.Anal.(侯雪丽,李琼,武晓剑,崔俭杰.分析测试学报),2012,31(1):113-116.
[26]Tsai T F,Lee M R.Chromatographia,2008,67(5):425-431.
[27]Saraji M,Mirmahdieh S.J.Sep.Sci.,2009,32(7):988-995.
[28]Han K,Zhai X L.Chin.J.Anal.Lab.(韩康,翟学良.分析试验室),2011,30(11):107-109.
[29]Ye N,Shi P,Li J.Anal.Lett.,2013,46(13):1991-2000.
[30]Han F,He Y Z,Yu C Z.Talanta,2008,74(5):1371-1377.
[31]Wang J,Zhang D,Chu Q.Chin.J.Chem.,2010,28(2):313-319.
[32]Huang J Q,Hu C C,Chiu T C.Int.J.CosmeticSci.,2013,35(4):346-353.
[33]Huang H Y,Chiu C W,Chen Y C.Electrophoresis,2005,26(4/5):895-902.
[34]Dolzan M D,Spudeit D A,Azevedo M S.Anal.Methods,2013,5(21):6023-6029.
[35]Rodas M,Portugal L A,Avivar J.Talanta,2015,143(1):254-262.
[36]Martins I,Carreira F C,Canaes L S.Talanta,2011,85(1):1-7.
[37]Márquez-Sillero I,Aguilera-Herrador E,Cárdenas S.J.Chromatogr.A,2010,1217(1):1-6.
[38]Lavilla I,Cabaleiro N,Pena F.Anal.Chim.Acta,2010,674(1):59-63.
[39]Alvarez-Rivera G,Llompart M,Garcia-Jares C,Lores M.J.Chromatogr.A,2015,1390:1-12.
[40]Feher I,Schmutzer G,Voica C.ProcessesInIsotopesAndMolecules,2013,1565(1):294-297.
[41]Esteki M,Nouroozi S,Shahsavari Z.Int.J.CosmeticSci.,2015.DOI:10.1111/ics.12241.
[42]Fang F,Su H,Yao Z X,Chen C,Liang X M,Huang L M.J.Instrum.Anal.( 方凤,粟晖,姚志湘,陈成,梁晓梅,黄丽梅.分析测试学报),2013,32(6):732-736.
[43]Sarveiya V,Risk S,Benson H A.J.Chromatogr.B,2004,803(2):225-231.
[44]Chisvert A,Pascual-Marti M C,Salvador A.J.Chromatogr.A,2001,921(2):207-215.
[45]Salvador A,Chisvert A.Anal.Chim.Acta,2005,537(1):15-24.
[46]Paulus G L.J.Assoc.Off.Anal.Chem.,1972,55(1):47-50.
[47]Li Y,Wang C Y,Liu L,Zhang W Y,Yang Z J.Chin.J.Anal.Lab.(李英,王成云,刘丽,张伟亚,杨左军.分析试验室),2003,22(5):77-80.
[48]Masse M O,Delporte C,Bervelt E.Int.J.CosmeticSci.,2001,23(5):259-279.
[49]Wang S P,Chen W J.Anal.Chim.Acta,2000,416(2):157-167.
[50]Klampfl C W,Leitner T,Hilder E F.Electrophoresis,2002,23(15):2424-2429.
[51]Klampfl C W,Leitner T.J.Sep.Sci.,2003,26(14):1259-1262.
[52]Júnior J B G,Araujo T A,Trindade M A,Ferreira V S G.Int.J.CosmeticSci.,2012,34(1):91-96.
[53]Abdolmohammad-Zadeh H,Falaghi S,Rahimpour E.Int.J.CosmeticSci.,2014,36(2):140-147.
[54]Chang N I,Yoo M Y,Lee S H.Int.J.CosmeticSci.,2015,37(2):175-180.
[55]Hsiao W Y,Jiang S J,Feng C H,Wang S W,Chen Y L.J.Chromatogr.A,2015,1383 (27):175-181.
[56]Menneveux J,Wang F,Lu S.Spectrochim.ActaB,2015,109:9-15.
[57]Vila M,Lamas J P,Garcia-Jares C.J.Chromatogr.A,2015,1405:12-22.
[58]Uysal U D,Güray T.J.Anal.Chem.,2008,63(10):982-986.
[59]Lin C H,Sheu J Y,Wu H L.J.Pharm.Biomed.Anal.,2005,38(3):414-419.
[60]Zhao K X,Su Y,Chen X Y.J.Instrum.Anal.(赵孔祥,苏毅,陈旭艳.分析测试学报),2011,30(6):701-704.
[61]Jeon J S,Kim B H,Lee S H.Int.J.CosmeticSci.,2015.37(6):567-573.
[62]Khater S,West C.J.Pharm.Biomed.Anal.,2015,102:321-325.
[63]Shehata M,Tawakkol S,Abdel Fattah L.J.Pharm.Biomed.Anal.,2002,27(5):729-735.
[64]Han W Q,Luo H Y,Chen L W,Wu Y L,Xian Y P,Wang B.Chin.J.Anal.Chem.(韩婉清,罗海英,陈立伟,吴玉銮,冼燕萍,王斌.分析化学),2014,42(10):1441-1446.
[65]Dallet P,Labat L,Kummer E,Dubost J P.J.Chromatogr.B,2000,742(2):447-452.
[66]Sgorbini B,Ruosi M R,Cordero C,Liberto E,Rubiolo P,Bicchi C.J.Chromatogr.A,2010,1217(16):2599-2605.
[67]Liu J,Liu M,Li X,Lu X,Chen G,Sun Z,Li G,Zhao X,Zhang S,Song C,Wang H,Suo Y,You J.J.Chromatogr.A,2014,1371:20-29.
[68]Gu Y X,Wang Q H,Zhou Z L,Lv Q,Mai C H.J.CosmeticSci.,2013,65(5):265-276.
[69]Chen W N,Jiang S J,Chen Y L,Sahayam A C.Anal.Chim.Acta,2015,860:8-14.
[70]Xu Z,Lan T,Huang X,Dong C,Ren J.Luminescence,2015,30(5):605-610.
[71]Roselli C,Desideri D,Cantaluppi C,Mattioli M,Fasson A,Meli M A.J.Toxicol.Environ.HealthA,2015,78(5):316-324.
[72]Wang Y,Yang H,Pschenitza M,Niessner R,Li Y,Knopp D,Deng A.Anal.Bioanal.Chem.,2012,403(9):2519-2528.
[73]Gao Y,Shi Z,Zong Q,Wu P,Su J,Liu R.Anal.Chim.Acta,2014,812:6-11.
[74]Li J Q,Yin L H,Wang J.Chin.JPharm.Anal.(李俊卿,尹利辉,王瑾.药物分析杂志),2012,32(7):1129-1132.
[75]Zhu L,Liu M L,Yin L H.Chin.JPharm.Anal.(朱俐,刘明理,尹利辉.药物分析杂志),2014,34(10):140-144.
[76]Li Y,Zhu L,Wang J,Sun X C,Yin L H.Chin.JPharm.Anal.(李野,朱俐,王瑾,孙晓翠,尹利辉.药物分析杂志),2014,34(8):1470-1474.
[77]Ma Q,Bai H,Wang C,Li W T,Ma H J,Li J R,Meng X S,Chen Y X.J.Instrum.Anal.(马强,白桦,王超,李文涛,马会娟,李晶瑞,孟宪双,陈云霞.分析测试学报),2014,33(3):248-255.
[78]Meng X S,Li J R,Ma Q,Bai H,Zhang Q,Lü Q,Guo X Y.J.Instrum.Anal.(孟宪双,李晶瑞,马强,白桦,张庆,吕庆,郭项雨.分析测试学报),2015,34(8):944-948.
[79]Mao X Q,Ren G J,Li C L.J.Instrum.Anal.(毛希琴,任国杰,李春玲.分析测试学报),2014,33(9):1083-1088.
[80]Qian X Y,Liu H S,Zhu X Y,Chen X M,Mo W M.J.Instrum.Anal.(钱晓燕,刘海山,朱晓雨,陈笑梅,莫卫民.分析测试学报),2014,33(5):527-532.
[81]Xu Z D,Shi J H,Gu J H,Zhai W J,Yu W J,Pan K,Chen J,Zhu Z H,Li J J.J.Instrum.Anal.(徐振东,石建华,顾娟红,翟纹静,余雯静,潘葵,陈军,朱振华,李建军.分析测试学报),2014,33(7):792-797.
[82]He D,Li X Y,Xian Y P,Fang J,Guo X D.J.Instrum.Anal.(何东,李秀英,冼燕萍,方军,郭新东.分析测试学报),2015,34(8):911-916.
[83]Tee-ngam P,Nunant N,Rattanarat P,Siangproh W,Chailapakul O.Sensors,2013,13(10):13039-13053.
[84]Chen X,Ni X J,Zhang J,Liu Y,Cao Y H.Chin.J.Anal.Chem.(陈新,倪鑫炯,张佳,刘瑛,曹玉华.分析化学),2015,43(1):81-86.
[85]Fang F,Su H,Yao Z X,Chen C,Liang X M,Huang L M.J.Instrum.Anal.( 方凤,粟晖,姚志湘,陈成,梁晓梅,黄丽梅.分析测试学报),2013,32(6):732-736.
[86]Mohamed H M.TrendsAnal.Chem.,2015,66:176-192.
Progress on Determination of Harmful Substances in Cosmetics
ZHU Li1,LIU Yang1,ZENG San-ping2,WANG Wei-jiao2,CHEN Ya-fei2,YIN Li-hui1*
(1.National Institutes for Food and Drug Control,Beijing100050,China;2.Hunan Institutes for Food and Drug Control,Changsha410001,China)
Abstract:Prohibited or restricted ingredients are often added into functional cosmetics.This kind of cosmetics not only cause damage to the interests and health of consumers,but also disrupt the market order.In this paper,analytical methods and pretreatment techniques for pharmaceutical substances(hormones,antibiotics),preservatives,sunscreens and other hazardous substances in cosmetics,which could be found in the literature,are reviewed.The applications of the analytical methods,techniques and sample preparation are discussed,and the prospects for the development of cosmetic detection methods are outlooked.
Key words:cosmetic;harmful substances;analytical method;review
中图分类号:O657.7;TQ658
文献标识码:A
文章编号:1004-4957(2016)02-0185-09
doi:10.3969/j.issn.1004-4957.2016.02.009
*通讯作者:尹利辉,硕士,主任药师,研究方向:药物分析,Tel:010-67095316,E-mail:yinlihui@nicpbp.org.cn
收稿日期:2015-08-20;修回日期:2015-11-06

