CT引导下经皮椎体成形术治疗骨质疏松椎体压缩骨折的疗效评价
徐玉生 朱海洋 钟斌 崔浩 汪鑫 理阳
(郑州大学第一附属医院 骨科六病区 河南 郑州 450002)
CT引导下经皮椎体成形术治疗骨质疏松椎体压缩骨折的疗效评价
徐玉生朱海洋钟斌崔浩汪鑫理阳
(郑州大学第一附属医院 骨科六病区河南 郑州450002)
【摘要】目的评估CT精确引导下经皮椎体成形术(PVP)治疗骨质疏松性椎体压缩骨折的疗效及其并发症的预防。方法87例脊柱病变患者(共98个伤椎)行CT精确引导下经皮椎体成形术,记录术前、术后患者视觉模拟疼痛评分(visual analogue scale,VAS)、Oswestry功能障碍指数(oswestry disability index,ODI)以及远期疗效评估,并对结果进行统计学分析。结果术中应用优化的CT引导经皮椎体穿刺成功率100.00%,注入骨水泥2~9 ml,平均(4.17±1.34)ml。VAS评分术前(7.96±0.48)分,术后6月(1.89±0.47)分;术前ODI平均(72.85±6.84)分、术后6个月(9.24±8.30)分;两指标术后与术前比较,差异具有统计学意义(P<0.05)。远期疗效WHO评估:总有效率为97.70%。术后即刻CT证实,共4例患者发生无症状性骨水泥渗漏,其中1例出现暂时性神经根性痛。结论术中CT精确引导可优化椎体成形术的手术操作,有效控制椎体骨折引起的疼痛,提高患者的生活质量,是一种微创、安全、高效的治疗方法。
【关键词】CT;椎体成形术;压缩骨折
经皮椎体成形术(percutaneous vertebroplasty,PVP)具有创伤小、可迅速缓解疼痛等优点,是治疗骨质疏松性椎体压缩骨折(osteoporotic vertebral compression fractures,OVCF)的主要手段[1-5]。较常见的PVP是在X线C臂机监视下操作,但X线C臂机监视下手术操作复杂,对较高位胸椎骨折定位困难,重度骨质疏松患者术中C臂机透视图像往往较为模糊,手术困难。所以椎体穿刺的风险和术中骨水泥渗漏等并发症仍是目前影响手术效果的重要原因。术中CT精确引导下经皮椎体成形术可对任一椎体直观定位、准确穿刺。本研究应用视觉模拟疼痛评分、Oswestry功能障碍指数以及远期疗效评估对2013年7月至2015年6月郑州大学第一附属医院PVP治疗87例疼痛性OVCF患者进行评价,旨在探明术中CT精确引导下PVP的疗效,并探讨其并发症的预防,现报告如下。
1资料与方法
1.1研究对象入选标准:①患者发病前日常生活能完全自理,发病后神志清晰,可独立表达自己意愿,有正常沟通能力;②经CT、MRI检查证实为骨质疏松性椎体压缩骨折;③ MRI显示骨折椎体T1WI呈低信号,T2WI及脂肪抑制像呈高信号,且CT显示椎体骨折裂隙判断为疼痛椎体;④血常规、生化等常规实验室检查正常。排除标准:①椎体原发肿瘤、血管瘤、结核、转移瘤等导致的椎体病理性压缩骨折;②肺心病、心脏、肝脏、肾脏等重要脏器功能衰竭者。符合上述入选标准及排除标准且获得完整随访资料者87例。男16例,女71例,年龄59~81岁,平均(68.69±4.69)岁。
1.2设备及材料Definition as 64 sliding gantry CT由德国西门子公司提供;FG3002号经皮穿刺针、FG7006号椎体成形导向系统、FG2501号骨导向器由上海凯利泰医疗科技股份有限公司提供;MENDEC骨水泥由意大利Teres S.P.A公司提供。
1.3术中CT精确引导经皮椎体成形术具体操作方法①体位:患者俯卧于CT扫描床上。②入路:胸椎取经椎弓根外途径或经椎弓根途径(图1)。③定位:CT扫描定位穿刺点,测量进针角度、深度,确定手术路线,根据需要采用双侧或单侧椎弓根入路。CT作轴位扫描时扫描架倾斜角度即穿刺针进入的尾倾角(图2)。④穿刺:常规消毒、铺巾,用1%利多卡因作穿刺通道局麻。按预定手术路线进穿刺针,部分进入骨质,再次CT扫描,对穿刺针进行微调,以保证穿刺针沿预定路线进入,待正确达到预定深度后,拔出针芯,插入引导针,再次CT扫描,引导针应位于椎体前缘但未穿出椎体,冠状位及矢状位针尖位于椎体中间,轴位示引导针尖端位于椎体椎弓根平面前中1/4~1/3交界处,表示位置良好。⑤骨水泥注入:用骨水泥填充器将已进入拉丝糊状期的骨水泥加压注入椎体,注射过程进行CT扫描,避免骨水泥进入椎管,一旦发生,及时停止。骨水泥充盈满意后停止注射,注入量2~9 ml,待骨水泥完全凝固后缓慢拔出穿刺针,术毕。手术时间30~40 min。
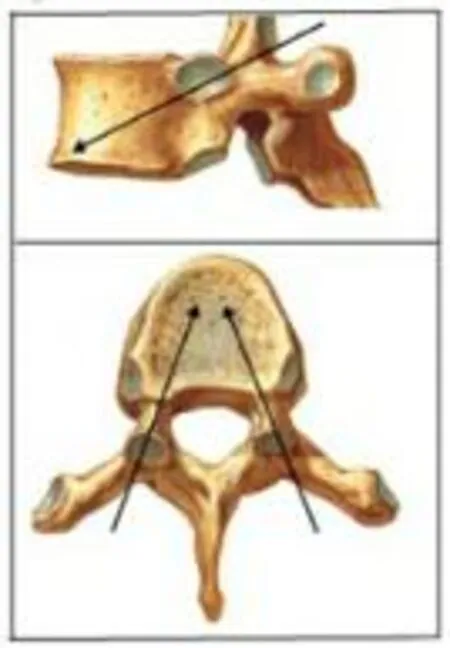
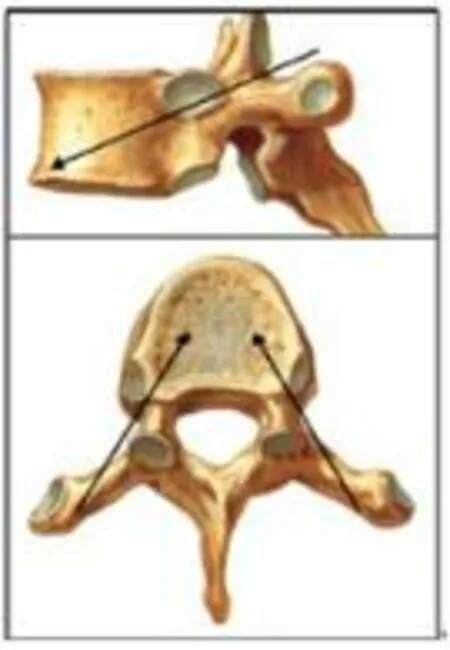
A B
图1术中CT精确引导经皮椎体成形术入路途径
1.4疗效评价记录患者术前和术后3 d、6个月随访时VAS和ODI。远期综合疗效采用WHO标准评价,将疼痛缓解分为完全缓解(complete remission,CR)即无痛;部分缓解(partial remission,PR)为疼痛较术前明显减轻,睡眠基本不受干扰,能正常生活;轻微缓解(minor remission,MR)为疼痛较术前减轻,但有明显疼痛,睡眠受干扰;无效(no remission,NR)则与术前比较无减轻,总有效率=(CR+PR)/总病例数。
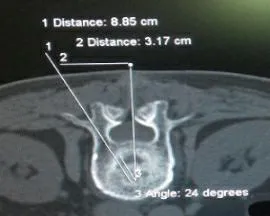
标示线1:穿刺针进针深度8.85 cm;标示线2:进针点距棘突3.17 cm;标示线3:穿刺针进针角度24°。
图2穿刺针进入的尾倾角
2结果
87例患者均在CT三维重建引导下穿刺成功,单侧穿刺83个椎体,双侧穿刺15个,62个椎体经左侧进针,51个椎体经右侧进针,椎体穿刺成功率100.00%;骨水泥注入量2~9 ml,平均(4.17±1.34)ml。共有4例发生骨水泥渗漏(4.60%),仅1例渗漏至椎管前方,导致暂时性神经根性痛。随访6~12个月,平均(10.47±1.68)个月,有2例因其他椎体骨折再行椎体成形术。术后患者VAS评分、ODI指数均较术前有明显改善,差异有统计学意义(P<0.05),见表1。远期综合疗效采用WHO标准评价:CR:87.36%;PR:10.34%;MR:2.30%;NR:0.00%;总有效率为97.70%。

时间nVAS评分/分ODI指数/%术前877.96±0.4872.85±6.84术后3d872.66±0.39a21.24±7.64a术后6月871.89±0.47a9.24±8.30a
注:与术前比较,aP<0.05。
3讨论
3.1术中应用CT的优势自第1例PVP以来,X线透视即为首选的影像引导方式,有学者认为大多数PVP在X线透视监测下实施是安全的[7-8]。但随着PVP的广泛应用,X线透视的影像引导方式越来越满足不了临床需求。主要表现:①操作繁琐,图像显影不佳,使手术的精确度受到一定程度的影响。②无法提供椎体轴位图像,对穿刺针的准确位置了解欠佳。③对骨水泥的早期渗漏监测不佳。由于在骨水泥注射过程中C型臂X线机仅能做到透视侧位,故而可能无法早期发现侧方渗漏与椎体内骨水泥影重叠者。④术者需接受一定量的X线照射,对长期从事此项操作的医务工作者身体不利。
为克服上述不足,近年来我们采用CT三维立体成像引导下的PVP。其优点:①模拟手术路线:CT扫描能清晰显示椎体、神经、脊髓的横断面解剖结构,应用CT计算机软件的二维、三维距离及角度测量工具,可帮助术者准确地设计穿刺针进针点、进针方向、角度及深度,提高穿刺针置入的成功率;且可同时对2个或2个以上椎体进行手术路线的设计。②清晰的影像图像:CT图像可清晰地显示穿刺针尖的具体位置,一方面便于调整方向,另一方面即使穿破了椎弓根的内侧壁也可及时发现,避免了相关并发症的发生。③可以随时扫描观察骨水泥的注入量及其在椎体内的分布情况。④缩短了手术操作时间,使患者在术中所受痛苦减少。⑤操作不需直接暴露于放射线中,对医务人员的健康有利。
3.2并发症的预防骨水泥渗漏为PVP手术最常见并发症。骨水泥渗漏与骨水泥注入量有密切关系。对于PVP术中骨水泥注入量历来都受到争论,有文献报道疼痛缓解与骨水泥注入量无关[9];也有学者认为只要无骨水泥渗漏发生应尽可能增加骨水泥注入量,认为骨水泥量的增加有益于椎体高度恢复和减少PVP后骨折发生[7]。本组病例骨水泥注入量为2~9 ml,疼痛缓解率97.70%,随访期间内除1例出现暂时性神经根性痛,并于术后1周缓解外,其余未出现有症状的并发症。
虽然大多数骨水泥渗漏不会引起相应的临床症状,但有些情况下会发生严重后果如肺栓塞、神经根损伤、脊髓损伤等。为了预防手术并发症,提高手术疗效,我们认为:①精确穿刺路线的设计:选择椎弓根较宽的一侧,以防止穿刺针穿破椎弓根内壁致骨水泥沿刺破口漏出至椎间孔或椎管。注入椎体椎弓根平面前中1/4~1/3交界处,以避开椎内静脉,减少骨水泥进入椎内静脉丛至肺栓塞的发生率。②适时、适量、适速的骨水泥注入:注射骨水泥应在CT监视下、于骨水泥拉丝糊状期适速推注。③清晰的影像设备显影:清晰的影像监测是预防PVP手术并发症的关键。术者能够在CT引导下清晰地看到穿刺针的具体位置,包括其与椎弓根各壁、椎体后壁及椎管的具体位置关系,避免过深、过浅或偏移预定位置,使穿刺针能够准确到位。另外,术者可实时观察到骨水泥的填充情况,可反馈性指导术者灌注骨水泥的速度及量。如骨水泥一旦渗出,亦可准确定位骨水泥渗出位置及范围,为下一步处理提供指导。
参考文献
[1]Li H D,Xu C J,Wang H,et al.Percutaneous vertebroplasty for single osteoporotic vertebral body compression fracture:Results of unilateral 3D percutaneous puncture technique[J].Indian J Orthop,2015,49(2):245-250.
[2]Yi X,Lu H,Tian F,et al.Recompression in new levels after percutaneous vertebroplasty and kyphoplasty compared with conservative treatment[J].Arch Orthop Trauma Surg,2014,134(1):21-30.
[3]Lamy O,Uebelhart B,Aubry-Rozier B.Risks and benefits of percutaneous vertebroplasty or kyphoplasty in the management of osteoporotic vertebral fractures[J].Osteoporos Int,2014,25(3):807-819.
[4]Huwart L,Foti P,Andreani O,et al.Vertebral split fractures:technical feasibility of percutaneous vertebroplasty[J].Eur J Radiol,2014,83(1):173-178.
[5]Guo W H,Meng M B,You X,et al.CT-guided percutaneous vertebroplasty of the upper cervical spine via a translateral approach[J].Pain Physician,2012,15(5):E733-741.
[6]Mathis J M,Barr J D,Belkoff S M,et al.Percutaneous vertebroplasty:a developing standard of care for vertebral compression fractures[J].AJNR Am J Neuroradiol,2001,22(2):373-381.
[7]Kim D J,Kim T W,Park K H,et al.The proper volume and distribution of cement augmentation on percutaneous vertebroplasty [J].J Korean Neurosurg Soc,2010,48(2):125-128.
[8]Peh W C,Gilula L A,Peck D D,et al.Percutaneous vertebroplasty for severe osteoporotic vertebral body compression fractures[J].Radiology,2002,223(1):121-126.
[9]Al-Ali F,Barrow T,Luke K,el at.Vertebroplasty:what is important and what is not[J].AJNR Am J Neuroradiol,2009,30(10):1835-1839.
Clinical efficacy of CT-guided percutaneous vertebroplasty in the treatment of osteoporotic vertebral compression fractures
Xu Yusheng,Zhu Haiyang,Zhong Bin,Cui Hao, Wang Xin,Li Yang
(SixthDepartmentofOrthopaedics,theFirstAffiliatedHospitalofZhengzhouUniversity,Zhengzhou450052,China)
【Abstract】ObjectiveTo assess the clinical efficacy of intraoperative CT-guided percutaneous vertebroplasty (PVP) in the treatment of osteoporotic vertebral compression fractures and prevention of complications. MethodsTotal 98 fracture vertebra of the 87 cases with vertebra accepted optimization of accurate CT-guided percutaneous vertebroplasty. The visual analogue scale, oswestry disability index and long-term curative effect evaluation in preoperation and postoperation were recorded, and the results were statistically analyzed. ResultsThe success rate of optimized CT-guided PVP was 100.00%. Bone cements were injected 2~9 ml, with an average of (4.17±1.34) ml. The average score of VAS were (7.96±0.48) and (1.89±0.47) scores at preoperation and last follow up after the operation respectively. The average scores of ODI were (72.85±6.84) and (9.24±8.30) scores at preoperation and last follow up after the operation respectively. There were significant differences in ODI and VAS between preoperative and postoperative groups(P<0.05). The long term effect: the effective rate was 97.7%. The immediately CT after operation confirmed that 4 patients suffered from asymptomatic bone cement leakage, and 1 of them had a temporary nerve root pain. ConclusionPrecise intraoperative CT-guided can optimize percutaneous vertebroplasty procedure, control the pain caused by vertebral fractures effectively, increase spinal stability and improve the patient’s quality of life. It is a minimally invasive, safe and effective treatment.
【Key words】CT;vertebroplasty;vertebral compression fracture
(收稿日期:2015-08-09)
【中图分类号】R 683.2
doi:10.3969/j.issn.1004-437X.2016.02.008

