蓝耳病病毒抗体ELISA检测试剂盒的“两步法”评价
王 勤,刘晓飞,冯春燕,翟新验,周 智,吴绍强,李晓琳,仇松寅,刘丹丹,林祥梅(.中国检验检疫科学研究院动物检疫研究所,北京 0009;.中国动物疫病预防控制中心,北京 0009)
蓝耳病病毒抗体ELISA检测试剂盒的“两步法”评价
王 勤1,刘晓飞1,冯春燕1,翟新验2,周 智2,吴绍强1,李晓琳1,仇松寅1,刘丹丹1,林祥梅1
(1.中国检验检疫科学研究院动物检疫研究所,北京 100029;2.中国动物疫病预防控制中心,北京 100029)
摘 要:本研究利用“两步法”对蓝耳病试剂盒进行了使用效果评价:第一步,利用18份参考血清对试剂盒进行初筛,淘汰检测准确率低的试剂盒;第二步,利用参考血清和临床样品,分别开展最低检测限、重复性以及诊断敏感性和诊断特异性分析。结果显示,A、B、C、D 4种市售试剂盒的初筛符合率均为100%,诊断敏感性和诊断特异性分别为94.58%和97.14%、94.58%和89.2%、93.1%和90%、96.55%和85%。其中,A和B为通用型试剂盒,能够检测欧洲型和美洲型蓝耳病;C和D均为美洲型检测试剂盒;重复性上,D试剂盒批内与批间变异系数都较小,重复性较好。本研究首次提出了“两步法”试剂盒评价体系并利用这一体系对4种蓝耳病试剂盒进行了评价,不仅为蓝耳病试剂盒的选择提供了依据,也为今后其它动物疫病检测试剂盒的评价提供了参考。
关键词:猪繁殖与呼吸综合征;ELISA检测试剂盒;诊断敏感性;诊断特异性;重复性
资助项目:国家质检总局科技计划项目:猪蓝耳病抗体检测试剂盒贝叶斯方法质量评价模型的建立(2014IK230);中国检验检疫科学研究院基本科研业务费专项资金资助项目:动物检疫风险分析中关键参数的精准估计(2014JK030);国家质检总局科技计划项目《进境高危害病毒性猪病检测方法的系统性研究和完善》(2015IK310)
猪繁殖与呼吸综合征(PRRS)又称“蓝耳病”,是以母猪生殖障碍和仔猪严重呼吸困难和高死亡率为特征的一种高度接触性传染病[1]。本病于1987年首次在美国发现,现流行于世界许多国家和地区,对养猪业构成巨大威胁。近年来,我国也深受其害,2006年PRRS的大规模暴发给我国养猪业造成了毁灭性打击[2]。猪繁殖与呼吸综合征病毒(PRRSV)分为美洲型和欧洲型两种,在我国大陆地区主要为美洲型,近年也分离到少数欧洲型毒株[3]。2008年,我国将高致病性猪蓝耳病列为一类动物疫病。
PRRSV基因组为单股正链RNA,大小为15 kb左右,含有8个开放阅读框,其中ORF1编码非结构蛋白,ORF2-7编码结构蛋白[4]。研究显示,PRRSV感染后M蛋白和N蛋白能够诱导机体产生抗体,但无中和作用。E蛋白和GP5蛋白产生的中和抗体有不定期的保护作用[5]。猪感染PRRSV 后7天开始出现抗体,2周后即可检出抗N蛋白的抗体和基质蛋白M的抗体,4~5周后才出现主要识别囊膜蛋白E特异性中和抗体。目前,针对PRRSV的检测,免疫效果评价以及疫病监测和进出境动物检疫工作中多数使用的是抗体ELISA检测试剂盒。试剂盒的质量成为影响检测结果准确性的关键因素。但目前市售试剂盒良莠不齐,不同品牌试剂盒检测结果间存在差异。
本研究采用两步法,利用参考样品(OIE参考实验室提供)和临床样品,对4种市售的PRRSV抗体ELISA检测试剂盒的检测范围、检测限、诊断敏感性、诊断特异性、重复性几个方面开展了使用效果评价。研究结果为蓝耳病检测试剂盒的选择提供了依据,同时也为其他试剂盒的评价提供了参考。
1 材料与方法
1.1血清
1.1.1参考血清。18份参考血清:由OIE猪繁殖与呼吸综合征参考实验室(中国动物疫病预防控制中心)提供。5种参考血清购自荷兰GD公司,其中REF2为欧洲型血清,REF3为美洲型血清,REF4为美洲型血清,REF5为欧洲和美洲型血清,REF6为美洲型血清。
1.1.2田间样品。343份临床血清样品,包括免疫群血清75份、感染群血清176份、阴性血清92份。
1.2试剂盒
本研究中购买的试剂盒品牌分别为IDEXX、Biochek、LSI、业为基,文中分别用A、B、C、D表示。通过初筛的试剂盒,每个抽取3个批次,每个批次抽3盒进行后续测定。批号见表1。

表1 所用试剂盒品牌和批次号
1.3方法
1.3.1初筛。对OIE猪蓝耳病参考实验室来源的18份参考血清统一编号,严格按照各试剂盒使用说明书进行检测,检测结果均用550型酶标仪按要求的波长读取数值,然后根据各试剂盒提供的标准判定结果。
1.3.2试剂盒最低检测限的确定及试剂盒检测范围的测定。利用荷兰GD公司的5份包含了欧洲型和美洲型的参考血清,进行梯度稀释(1:8、1:16、1:32、1:64、1:128、1:256),进行检测,根据试剂盒说明进行结果判定。
1.3.3试剂盒的诊断特异性、敏感性。利用343份血清临床样品,对4个试剂盒进行检测,判断其诊断敏感性、诊断特异性。对于差异样品,利用IFA方法作为金标准进一步复核。根据测定的结果整理,如表2所示,计算诊断敏感性:DSe= TpDp/(TpDp+TnDp),诊断特异性为:DSp= TnDn/(TnDn+TpDn)。其中,TpDp为真阳性、TnDp为假阴性、TnDn为真阴性、TpDn为假阳性。

表2 2×2列联表
1.3.4重复性测定。试剂盒:每种试剂盒抽取3个批次,每个批次抽取3个试剂盒;样品:选取5份参考血清(4份阳性、1份阴性),见表3。
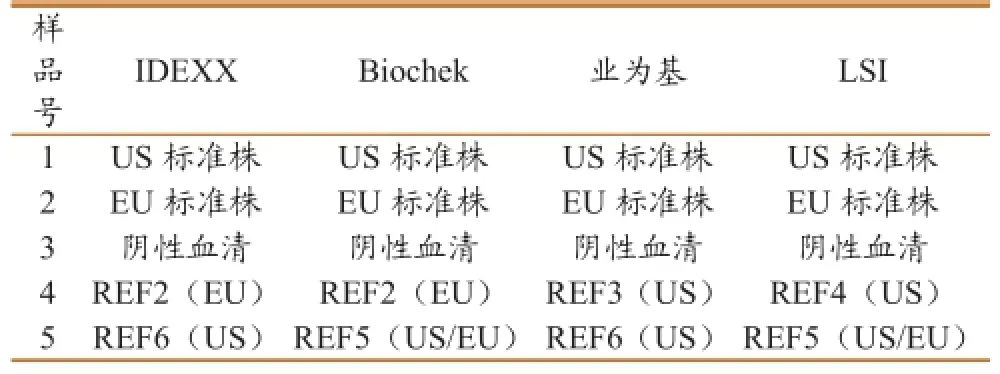
表3 PRRS重复性样品表
2 结果
2.1初筛结果
利用已知的参考样品,对4个试剂盒进行检测。结果发现A、B、C和D的检测结果与18份样品真实状态符合率达100%,检测结果准确,如表4所示。
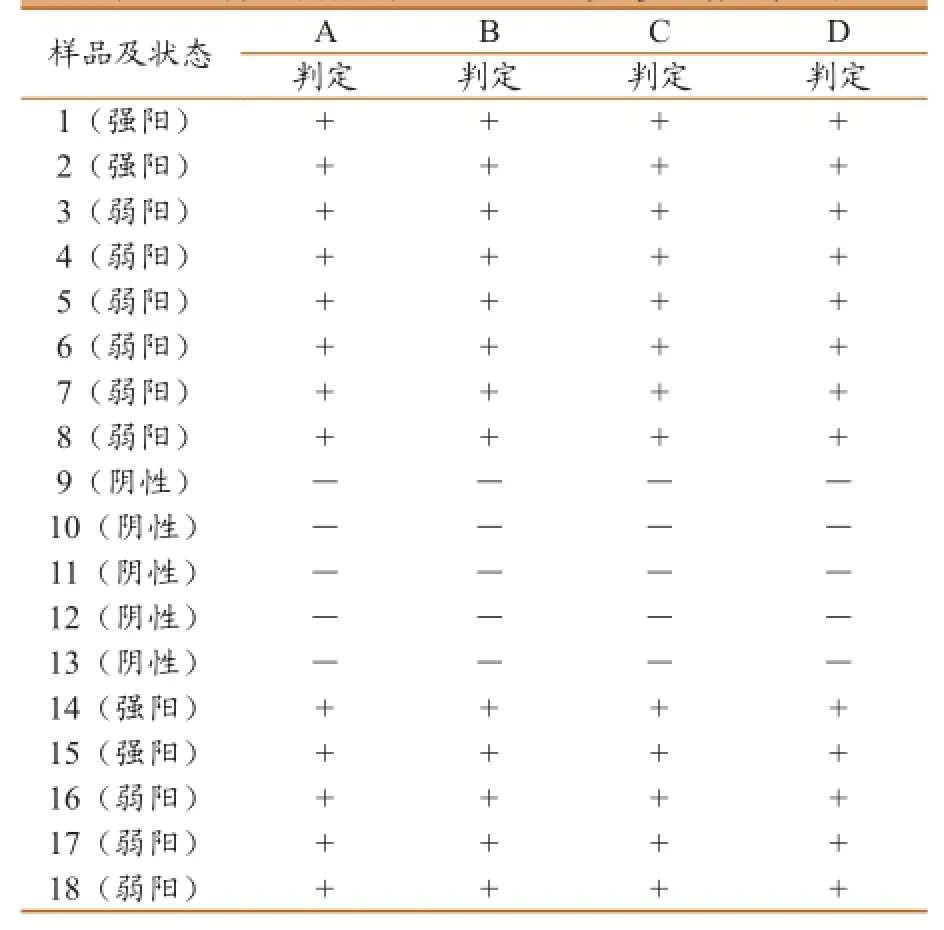
表4 4种试剂盒对PRRSV的参考血清的检测
2.2最低检测限和检测范围测定结果
本研究利用标准血清进行稀释,检测试剂盒能检测到的稀释度(表5)。对于样品REF2,A可检测到1:8,其他试剂盒未检出;对于样品REF3,D可检到1:16,其他试剂盒未检出;对于样品REF4,A可检到1:32,B可检到1:8,D可检到1:64,C未检出;对于样品REF5,A可检到1:16,B和D可检到1:8,C未检出;对于样品REF6,A可检到1:64,B可检到1:32,D可检到1:16,B未检出。
通过4种试剂盒对参考血清样品的检测结果可见,A和B对于欧洲型和美洲型病毒抗体均可检测,为通用型试剂盒;而C和D只能检测美洲型病毒抗体。
2.3诊断敏感性及诊断特异性
利用343份猪血清样品进行试剂盒的Dse和Dsp的测定,结果见表6。4种试剂盒的诊断敏感性都较好,都在90%以上,其中D的诊断敏感性最高,为96.55%;4种试剂盒的诊断特异性均在85%以上,A诊断特异性最高为97.14%,D的诊断特异性最低,为85%。
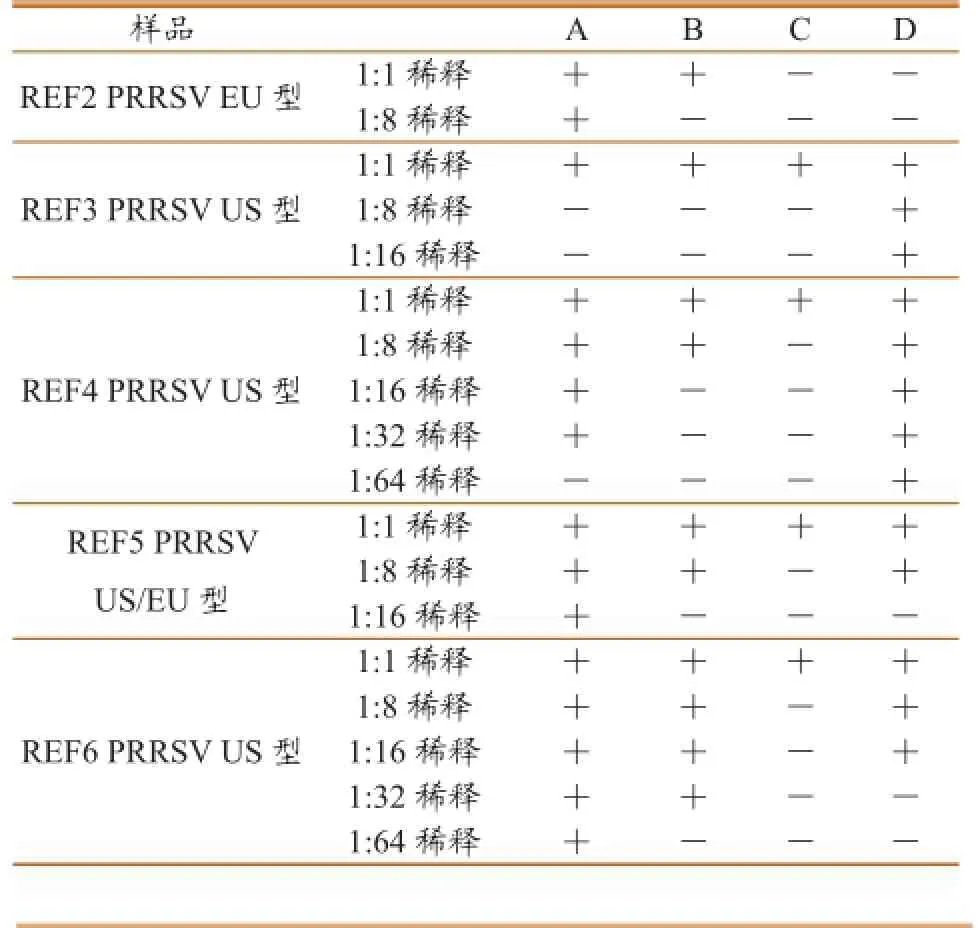
表5 最低检测限测定结果
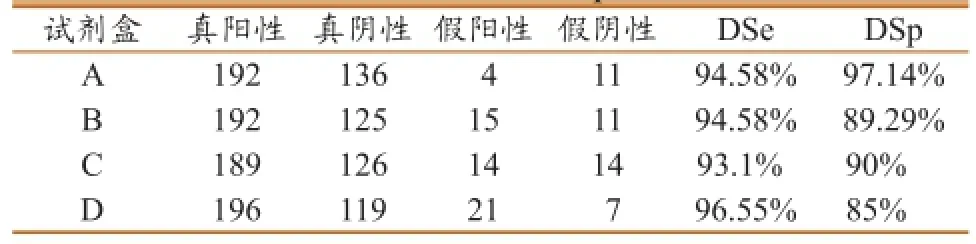
表6 试剂盒的 DSe、DSp测定结果
2.4重复性实验结果
4种试剂盒在批间和批内测定的样品都得到了一致的结果,说明重复性良好,根据各试剂盒得出的S/P值计算批次间及批次内的变异系数。如表7所示,A和B的批次间变异系数分 别为18.23±17.89%和18.20±8.65%,均 大于15%,批次内变异系数分别为7.88±5.68%和11.34±5.60%,说明这两个品牌的试剂盒批内重复性好而批次间的重复性差;D和C的批间变异系数分别为8.07±2.79%和17.22±6.29%,批内变异系数分别为7.34±1.41%和8.66±4.74%,均小于10%,说明两种试剂盒的批内重复性都很好,但批间重复性D优于C。

表7 各试剂盒批间与批内变异系数(CV)
3 结论与讨论
蓝耳病试剂盒具有方便、快速等特点,在体外诊断中被广泛应用。在口岸检疫和国内疫病监测中,蓝耳病检测试剂盒也被广泛应用于疫情判定。据不完全统计,仅国内检验检疫部门每年购买蓝耳病抗体ELISA检测试剂盒的花费已超过百万元。
试剂盒的评价对今后建立和规范国内检测试剂盒的评价、市场准入等管理制度,确保检测试剂盒的质量,具有十分重要的现实意义。国内对动物疫病的试剂盒评价仍然处于起步阶段,如何科学、客观、经济地评价一个试剂盒,成为研究的一个方向。目前已有对弓形虫、丙型肝炎、克伦特罗、商品化支原体液体培养、C-反应蛋白检测试剂盒评价的报道[6-12]。
本研究建立了两步法评价体系,并用其对市售的4种试剂盒进行了使用效果评价。两步法的优点是,先用少量样品,对试剂盒进行初评,能够有效节约评价成本。两步法评价体系分为两个部分(图1):第一步,利用待检试剂盒对参考血清进行检测,筛选出符合程度100%的试剂盒。第二步,对通过初筛的试剂盒,利用参考样品和临床样品对这些试剂盒的检测范围、检测限、重复性、诊断特异性和诊断敏感性进行测定。对测定结果中存在差异的样品,用(相对)金标方法进行复核,以金标方法结果为准,进行结果统计。通过分析比较试剂盒的特异性,敏感性及再现性等参数,对试剂盒的优劣进行评判。其结果可作为口岸检疫、疫病监测等工作试剂盒选择的依据,为提高检测结果的有效性和准确性奠定基础。
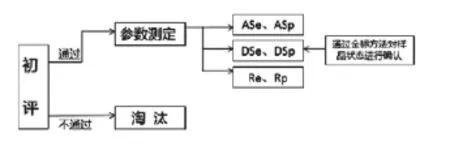
图1 试剂盒评价方案
通过两步法,对4种PRRSV抗体ELISA试剂盒进行检测,可以得出以下结论:PRRSV分为欧洲型(EU)和美洲型(US),因此试剂盒所能检测的病毒类型是一个十分重要的问题。对初筛符合率100%的4个试剂盒进行检测限及检测类型的分析,发现仅有A和B试剂盒可以检出欧洲型血清(REF2),其中A针对REF2的敏感性更高,能检测到1:8个稀释浓度。而在EU/US混合的血清中,1:1稀释的情况下,4种试剂盒均能检出,A的敏感度更高。而对US型的检测,D的敏感性高于C。值得注意的是,在另外3组仅含US型的血清中,敏感性的结果也不相同。在REF3中,D的敏感性最高,其它试剂盒敏感性相同。REF4中,D敏感性也最高,但是A>B> C。在REF6中,A的敏感性最高,而B>D> C。出现这种差异的主要原因很可能是因为每个试剂盒包被的抗原不同,并且包被的抗原的比例不同。而不同血清中,由于个体差异,免疫系统针对不同抗原产生的抗体的含量也不同,因此导致了检测结果的差异。由于缺乏对这些抗体的种类及抗体绝对定量的检测方法,这些差异是否能作为判断试剂盒好坏的标准,还需要进一步研究数据的支持。
在利用大量临床样本进行诊断特异性、诊断敏感性及重复性的测试中,A、B、C、D 等4种试剂盒的诊断敏感性和诊断特异性分别为:94.58%、97.14%、94.58%、89.29%和 93.1%、90%、96.55%和85%,其中,D的诊断敏感性最高,为96.55%,其他3个都在90%以上;A的诊断特异性最高,为97.14%,D的诊断特异性最差,为85%,由于各试剂盒能够检测的蓝耳病抗体不同,需要结合检测目的选择合适的试剂盒使用。从重复性上看,几乎所有试剂盒的批次间差异均显著,大部分试剂盒的批次内差异显著。这说明试剂盒批次间和批次内存在不可忽略的系统误差,从而影响了检测结果。因此,在更换批次之前,建议对试剂盒进行复验后再使用,以保证检测的质量。
参考文献:
[1] Meulenberg J J M. PRRSV,the virus[J]. Veterinary research,2000,31(1):11-21.
[2]Tong G Z,Zhou Y J,Hao X F,et al. Highly pathogenic porcine reproductive and respiratory syndrome,China[J]. Emerging infectious diseases,2007,13(9):1434.
[3]Zhou Z,Ni J,Cao Z,et al. The epidemic status and genetic diversity of 14 highly pathogenic porcine reproductive and respiratory syndrome virus (HP-PRRSV) isolates from China in 2009[J]. Veterinary microbiology,2011,150(3):257-269.
[4]Conzelmann K K,Visser N,Van Woensel P,et al. Molecular characterization of porcine reproductive and respiratory syndrome virus,a member of the arterivirus group[J]. Virology, 1993,193(1):329-339.
[5]Mateu E,Diaz I. The challenge of PRRS immunology[J]. The Veterinary Journal,2008,177(3):345-351.
[6]叶妮,闫小峰. 国内外克伦特罗 ELISA 检测试剂盒评价[J]. 中国兽药杂志,2002,36(10):25-28.
[7]蒋宇富,张述义. 5 种市售弓形虫抗体检测试剂盒的评价[J]. 中国人兽共患病杂志,2003,19(1):97-99.
[8]于恩庶. 对国内市售弓形虫病诊断试剂盒的评价和建议[J]. 中国人兽共患病杂志,2001,17(3):5-6.
[9]黄进梅,郑和平,吴兴中,等. 4 种商品化支原体液体培养试剂盒的质量评价[J]. 国际检验医学杂志,2006,27(6):500-501.
[10]钱高,王红芳,贺文严. C-反应蛋白检测试剂盒评价分析[J]. 国际检验医学杂志,2010,31(12):1474.
[11]邢文革,石向东. 国产丙型肝炎病毒抗体酶免检测试剂盒的质量评价[J]. 中华肝脏病杂志,2001,9(5):314.
[12]周诚,祁自柏. 丙型肝炎病毒抗体酶标试剂盒的评价[J].中华实验和临床病毒学杂志,1998,12(2):115-117.
(责任编辑:朱迪国)
中图分类号:S851.3
文献标识码:B
文章编号:1005-944X(2016)01-0071-05
通讯作者:林祥梅
Evaluation of ELISA Kits for PRRSV Antibody Detection by ‘Two Steps' Method
Wang Qin1,Liu Xiaofei1,Feng Chunyan1,Zhai Xinyan2,Zhou Zhi2,Wu Shaoqiang1,Li Xiaolin1,Qiu Songyin1,Liu Dandan1,Lin Xiangmei1
(1.Chinese Academy of Inspection and Quarantine Institute of Animal Quarantine,Beijing 100029;2.China Animal Disease Prevention and Control Center,Beijing 100125)
Abstract:This study aimed at evaluating four commercial ELISA kits for PRRSV antibody detection by using twosteps for the fi rst time. Firstly,18 reference sera were used to screen. Secondly,6 reference sera were used to detect the limitation of detection(LOD)and repeatability(Re),and 343 fi eld samples were used to test sensitivity and specifi city. The results showed that 4 kits were 100% identical to the reference seras in screening test in the fi rst step,and the sensitivity and specifi city of A,B,C and D were 94.58% and 97.14%,94.58% and 89.2%,93.1% and 90%,96.55% and 85% respectively in the second step. Kit A and B are universal kits for detecting antibody against EU and US type of PRRSV. Kit C and D can only detect US type virus antibody. D kit showed coeffi cient of variation was low among the batches and had good repeatability. The 4 PRRSV kits were varying in detection scale,validity and accuracy. By applying twostep method,this study supplied evidences for the selection of PRRSV antibodies ELISA detection kits,also gave the reference for the evaluation of animal disease detection.
Key Words:PRRS;commercial ELISA diagnostic kit;diagnostic sensitivity;diagnostic specifi city;diagnostic repeatability

