高含硫废水受控氧化的混凝强化研究
王 兵,陈丹丹,任宏洋,李永涛,王丹,林奇,3
(1.西南石油大学化学化工学院,四川成都610500;2.四川省环境保护油气田污染防治与环境安全重点实验室,四川成都610500;3.中石油安全环保技术研究院,辽宁大连116000)
高含硫废水受控氧化的混凝强化研究
王兵1,2,陈丹丹1,任宏洋1,2,李永涛1,2,王丹1,林奇1,3
(1.西南石油大学化学化工学院,四川成都610500;2.四川省环境保护油气田污染防治与环境安全重点实验室,四川成都610500;3.中石油安全环保技术研究院,辽宁大连116000)
以过氧化氢为氧化剂、聚二甲基二烯丙基氯化铵(PDM)为混凝剂对高含硫废水进行控制氧化处理,考察了混凝强化机制对脱硫效果的影响。结果表明,在PDM投加质量浓度为1.0mg/L,初始pH为6,过氧化氢投加量为9mL/L,反应时间为15min的条件下,混凝强化体系中硫化物去除率达99.09%,单质硫产量为1 588.5mg/L,较普通反应体系分别提高了1%和14%;SO42-产量为209.69mg/L,较普通体系降低了8%。
含硫废水;单质硫;氧化历程;混凝强化
无机硫化物是一类常见的环境污染物,在石油天然气开采、炼油、化工、冶金、印染、造纸、制药、皮革加工等行业排放的废水中普遍存在〔1-2〕,尤其在高含硫气田开发过程中,气田水中硫含量高达3 000~5 000mg/L。由于微生物对含硫化合物的分解脱硫作用,在城市污水管道中也普遍存在着硫化物〔3〕。废水中的硫化物具有毒性和腐蚀性,同时其氧化过程能够消耗水体中的氧气,导致水体发黑发臭和水生生物的死亡〔4-6〕,更为严重的是高含硫废水易释放H2S等恶臭气体,会毒害人的神经系统,影响血液循环和消化系统,对人体健康和区域环境造成重大影响〔7-9〕。
目前,针对硫含量较低的废水主要采用微生物脱硫技术将硫化物氧化为单质硫〔10〕。高含硫废水中硫化物的处理方法主要有汽提法〔11〕、氧化法〔12-13〕、混凝沉淀法等〔14-15〕。混凝沉淀法通常是将硫化物转化为难溶的硫化物沉淀加以去除,其产生的含硫污泥容易造成二次污染。传统的氧化法通常是利用强氧化剂将硫化物直接氧化,其氧化产物以高价态硫氧酸根为主,氧化剂加量较大,同时生成的硫氧酸根在底泥等厌氧环境中易被硫酸盐还原菌再次还原成硫化物〔16〕。通过控制反应过程中的氧化还原电位能将硫化物的氧化过程控制在单质硫的阶段〔17〕,同时实现硫化物污染去除和硫磺资源的回收的目标,但硫化物还原性强、氧化过程产物种类较多,初始生成的单质硫较不稳定,容易被进一步氧化。采用化学氧化法将含硫废水中硫化物氧化成单质硫,单质硫回收率较低〔18〕。将混凝-化学氧化相结合,通过混凝强化手段控制氧化反应,提高单质硫生成量的研究还鲜有报道。本试验以提升单质硫的转化率为目标,研究硫化物氧化历程和混凝过程对于受控氧化过程中单质硫回收的影响,考察混凝对脱硫及单质硫回收的强化机制,为高含硫废水中硫化物的污染控制及资源化利用提供基础数据。
1 材料与方法
1.1试剂
采用相对分子质量为20万~35万,质量分数为20%的聚二甲基二烯丙基氯化铵(PDMDAAC,阿拉丁试剂有限公司,以下简称PDM)配成质量浓度为1 000mg/L的溶液;Na2S·9H2O、过氧化氢(30%)、硫代硫酸钠、碘、氢氧化钠、盐酸等均为分析纯试剂,由成都科龙化工试剂厂生产。
1.2装置与仪器
试验采用的脱硫装置主要包括反应器和尾气吸收装置两部分,整个反应在密闭条件下进行,并通过尾气吸收装置(碱液)吸收反应过程中产生的H2S气体;试验所用仪器包括pHS-25型数字式显示酸度计,上海精密科学仪器有限公司;78-1型磁力加热搅拌器,上海双捷实验设备有限公司;SHB-Ⅲ型循环水式多用真空泵,郑州长城科工贸有限公司;PALS/90PLUS型Zeta电位及粒度分析仪,美国布鲁克海文公司。
1.3试验方法
采用Na2S·9H2O配制高含硫模拟废水(质量浓度为1 940mg/L),取200mL含硫废水于250mL三口烧瓶中,加入一定量PDM和过氧化氢后,通过酸式滴定管加酸调节废水初始pH,在50 r/min的转速下搅拌反应15min,并记录pH随时间变化的规律。反应结束后测定反应体系Zeta电位及颗粒粒度,用0.45μm微孔滤膜过滤之后,分别对固相产物和滤液中可溶性产物进行测定。
1.4分析方法
采用碘量法(HJ/T 60—2000)测定废水中硫化物含量;采用重量法(GB 11899—1989)测定反应后滤液中SO42-含量;采用滴定法测定滤液中S2O32-含量;采用Zeta电位及粒度分析仪测量反应体系Zeta电位及颗粒粒度。
产物转化率主要指产物中硫元素占初始硫元素的比例。
2 结果与讨论
2.1混凝强化对脱硫效果的影响
在实验温度为30℃,初始pH为6,过氧化氢投加量为9mL/L,反应时间为15min的条件下,考察PDM加量对脱硫效果的影响,结果如图1所示。

图1 PDM加量对强化脱硫效果的影响
由图1可知,向反应体系投加少量混凝剂PDM能提高硫化物去除率,且硫化物去除率随PDM加量的增加,先小幅升高再小幅降低,在PDM投加质量浓度为1.0mg/L时,达到最大值99.09%。从氧化产物的生成情况来看,过氧化氢氧化脱硫的主要产物为单质硫及少量SO42-,同时还有极少量S2O32-,由于S2O32-不稳定,在产物中所占比例极低,其质量可忽略。当PDM加量从0增加至1.0mg/L时,单质硫产量由1 318.0mg/L增加至1 588.5mg/L,转化率由67.9%提高至81.9%。当PDM投加质量浓度从1.0 mg/L增加至2.0mg/L时,单质硫质量浓度由1 588.5 mg/L降低至1 519.0mg/L,而硫酸根产量随着PDM加量的增加先减小后增大,在PDM投加质量浓度为1.0mg/L时达到最小值209.69mg/L。由此可知,当PDM投加质量浓度为1.0mg/L时强化脱硫效果最理想,此时单质硫产量也达最大值。
上述结果主要与以下几个过氧化氢氧化硫化物的主要反应有关:
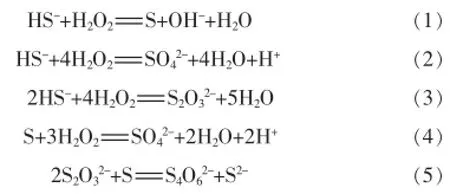
由反应式可知要获得较高的去除率及单质硫的生成量,应将反应(1)作为硫化物氧化过程的目的反应,同时副反应(4)、(5)会消耗体系中氧化产物单质硫,导致单质硫产量下降,应尽量控制。混凝剂PDM的加入能提高硫化物去除率和单质硫产量以及降低SO42-生成量,一方面可能是因为PDM是结构为五元环的线状高分子聚合物,能在刚形成的单质硫表面缠绕附着〔19〕,在一定程度上阻碍了单质硫与其他氧化性分子接触,从而抑制了副反应(4)、(5)的进行;另一方面可能是因为PDM是阳离子型混凝剂,PDM的加入能改变反应体系的Zeta电位,从而影响单质硫颗粒的聚集程度进而影响副反应的进行。
2.2不同pH条件下的混凝强化效果
在实验温度为30℃,过氧化氢投加量为9mL/L,强化体系PDM投加质量浓度为1.0mg/L,反应时间为15min的条件下,考察不同pH下的混凝强化效果,结果如图2所示。
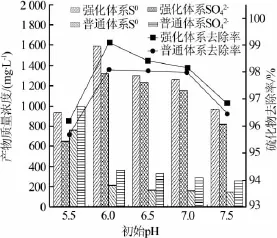
图2 不同pH下的混凝强化效果
由图2可知,两种反应体系均在初始pH为6~7时对含硫废水具有较好的脱硫效果,单质硫的产量相对较高,这主要与过氧化氢的特性有关,过氧化氢在酸性和碱性介质中的标准电极电势分别为1.763、0.867 V〔20〕,可见其在酸性条件下具有更强的氧化性。同时,酸性介质中硫化物主要以HS-、H2S的形式存在,而HS-和H2S转化为单质硫的标准电极电势分别为-0.065、0.142 V,可见HS-更利于单质硫的形成,而过酸的环境会使HS-进一步质子化生成H2S,不利于氧化反应进行的同时也会导致H2S气体逸散,脱离反应体系而被碱液吸收。在碱性过强的介质中,过氧化氢会发生分解,使有效氧化组分减少,从而不利于脱硫反应的进行。另外单质硫在大量OH-存在的情况下会被过氧化氢氧化为SO42-导致单质硫减少,这与O.M.Ilinitch等〔20〕结论相似,即pH<7时,产物以单质硫为主。
混凝强化体系与普通反应体系相比,只在其基础上提高了硫化物去除率和单质硫产量并降低了SO42-生成量,并没有改变反应体系随初始pH变化的趋势和最佳初始pH。在初始pH为6时混凝强化体系单质硫产量及转化率分别为1 588.5 mg/L和81.9%,较普通体系提高了270.5mg/L和14%,SO42-产量较普通体系降低了8%。这主要是由于PDM的特殊结构及带电性质在一定程度上抑制了副反应(4)、(5)的进行,防止了新生态单质硫的继续氧化,从而提高硫化物去除率和单质硫产量以及降低SO42-生成量。
2.3不同氧化剂加量下的混凝强化效果
在实验温度为30℃,初始pH为6,强化体系PDM投加质量浓度为1.0mg/L,反应时间为15min的条件下,考察过氧化氢投加量对混凝强化效果的影响,结果如图3所示。

图3 不同氧化剂加量下的混凝强化效果
由图3可知,两种反应体系均在过氧化氢投加量为9mL/L时具有较好的脱硫效果,单质硫的产量相对最多,而SO42-产量均随氧化剂投加量的增加而增大。由于反应式(1)为硫化物氧化过程的目的反应,当过氧化氢投加量小于9mL/L这一阶段时,随着氧化剂投加量的增大,单位时间发生有效碰撞的分子数大幅增加,反应速率加快,硫化物去除率及单质硫生成量均迅速提高。当过氧化氢投加量超过9 mL/L后,体系中氧化剂相对过量,促进反应(2)~(4)的发生,不仅促进SO42-的生成,还会消耗部分单质硫,导致单质硫产量下降。混凝强化体系同样也没有改变反应体系随氧化剂加量变化的趋势,只在普通反应体系的基础上提高了硫化物去除率和单质硫生由图4可知,随着反应的进行,反应体系pH均呈现先缓慢升高再逐渐下降的趋势,其中普通反应体系pH峰值出现在第6分钟,而混凝强化体系pH峰值则出现在第10分钟,且普通反应体系pH下降更快。
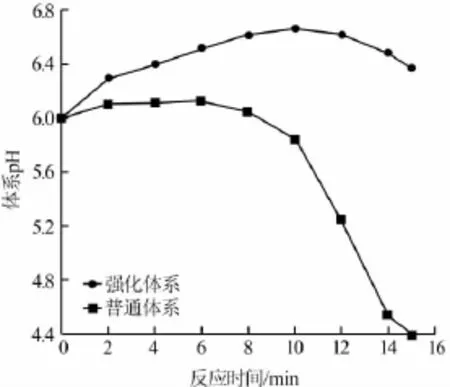
图4 体系pH与反应时间的关系
反应开始时,体系pH会呈上升趋势,主要是因为反应(1)会产生OH-,一段时间后pH逐渐下降,这是由于副反应(4)中单质硫被氧化为高价态硫酸成量,相对单质硫生成量混凝强化体系对硫化物去除率的提高并不明显,最大值为1%,而单质硫产量和SO42-生成量在过氧化氢投加量为9mL/L时分别提高了14%和降低了8%,这是因为混凝强化体系主要是通过控制单质硫的继续氧化来提高单质硫在氧化产物中所占比例,由过氧化氢氧化硫化物的主要反应式可知,这对硫化物去除率的提高影响较小。
2.4硫化物的氧化历程
由反应式(1)可知,当氧化脱硫产物均为单质硫时,每1 L含硫废水需6.20m L 30%过氧化氢;由反应式(2)可知,当产物均为SO42-时,每1 L含硫废水需要24.80mL 30%过氧化氢,而由图3可知,当过氧化氢投加量为9mL/L时,硫化物去除率最高,单质硫产量最大。这说明体系中不仅发生反应(1)和(2),还发生反应(3)、(4),也就是说氧化产物中的高价态硫酸根既来自硫化物的一次性氧化,又来自单质硫的继续氧化。由于氧化产物的变化会引起体系pH的变化,因此为了进一步研究氧化历程,在实验温度为30℃,初始pH为6,过氧化氢投加量为9 mL/L、PDM投加质量浓度为1.0mg/L,反应时间为15min的条件下,考察了反应体系pH随时间的变化关系,结果如图4所示。
2.5混凝强化原理
由硫化物的氧化历程分析可知,混凝强化体系主要通过控制已生成单质硫的继续氧化来提高单质硫产量,为了进一步研究混凝强化机制,考察了反应体系Zeta电位随PDM加量变化的关系,结果如图5所示。

图5 不同PDM加量下体系Zeta电位
由图5可知,在未加PDM的反应体系中Zeta电位为-20.14mV,表明体系中单质硫颗粒表面带负电,由于PDM具有较长的分子链和较多的正电荷点位,因而很容易被带负电的单质硫颗粒吸附,从而有效地中和颗粒表面的负电荷〔22-23〕,因此随着PDM的加入,体系Zeta电位逐渐升高,由最初的-20.14mV升高到16.89mV。Zeta电位是指带电颗粒表面剪切层的电位,是对颗粒之间相互排斥或吸引力强度的度量。Zeta电位绝对值愈大,粒子间相互斥力愈强,颗粒物体系就愈稳定;当Zeta电位接近零时,分散作用减弱,随即趋向聚集〔24〕。由图5可知,当PDM投加质量浓度为1.0mg/L时,体系Zeta电位接近于零,此时颗粒间相互排斥力较弱,更有利于颗粒的团聚,这就是PDM的加入对体系中单质硫产量提高的原因之一。
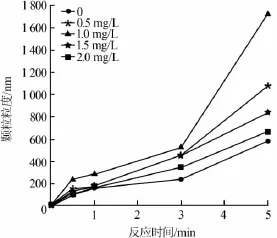
图6 不同PDM加量下颗粒粒度
由图6可知,反应初期单质硫颗粒粒度处于纳米级范围内,并随反应时间的增加而逐渐增大。PDM投加质量浓度为1.0mg/L的反应体系中颗粒粒度明显大于其他反应体系。林奇〔18〕在含硫废水中硫的受控氧化过程研究中指出,过氧化氢氧化含硫废水所生成的单质硫颗粒呈大小不一的球状,因此假设氧化所得单质硫均为球形颗粒,根据球形颗粒比表面积计算公式可知,颗粒比表面积与颗粒粒度呈反比,即颗粒粒度愈大,颗粒比表面积愈小,因此PDM投加质量浓度为1.0mg/L的反应体系中颗粒比表面积相较于其他反应体系明显较小。
结合图5、图6分析,反应体系的Zeta电位的绝对值愈接近于零,反应体系中的颗粒粒度愈大、颗粒比表面积愈小。说明混凝强化体系由于PDM的加入改变了反应体系Zeta电位,使之接近于零,因此促进了单质硫颗粒的团聚,从而使颗粒粒度增大,颗粒粒度愈大,比表面积就愈小,表面能就愈小,因而颗粒表面愈稳定,因此在一定程度上降低了单质硫继续和体系中氧化剂反应的可能性,从而防止了单质硫继续被氧化为高价态硫酸盐。综上所述,混凝强化体系主要是通过提高已生成单质硫颗粒的表面稳定性来控制单质硫的继续氧化,从而提高单质硫转化率,降低硫酸根产量。
为了考察PDM的加入对体系中颗粒团聚行为的影响,考察了前5min内不同PDM加量下颗粒粒度随时间的变化趋势,结果如图6所示。
成量,相对单质硫生成量混凝强化体系对硫化物去除率的提高并不明显,最大值为1%,而单质硫产量和SO42-生成量在过氧化氢投加量为9m L/L时分别提高了14%和降低了8%,这是因为混凝强化体系主要是通过控制单质硫的继续氧化来提高单质硫在氧化产物中所占比例,由过氧化氢氧化硫化物的主要反应式可知,这对硫化物去除率的提高影响较小。
2.4硫化物的氧化历程
由反应式(1)可知,当氧化脱硫产物均为单质硫时,每1 L含硫废水需6.20m L 30%过氧化氢;由反应式(2)可知,当产物均为SO42-时,每1 L含硫废水需要24.80mL 30%过氧化氢,而由图3可知,当过氧化氢投加量为9mL/L时,硫化物去除率最高,单质硫产量最大。这说明体系中不仅发生反应(1)和(2),还发生反应(3)、(4),也就是说氧化产物中的高价态硫酸根既来自硫化物的一次性氧化,又来自单质硫的继续氧化。由于氧化产物的变化会引起体系pH的变化,因此为了进一步研究氧化历程,在实验温度为30℃,初始pH为6,过氧化氢投加量为9 mL/L、PDM投加质量浓度为1.0mg/L,反应时间为15min的条件下,考察了反应体系pH随时间的变化关系,结果如图4所示。

图4 体系pH与反应时间的关系
由图4可知,随着反应的进行,反应体系pH均呈现先缓慢升高再逐渐下降的趋势,其中普通反应体系pH峰值出现在第6分钟,而混凝强化体系pH峰值则出现在第10分钟,且普通反应体系pH下降更快。
反应开始时,体系pH会呈上升趋势,主要是因为反应(1)会产生OH-,一段时间后pH逐渐下降,这是由于副反应(4)中单质硫被氧化为高价态硫酸根时会有H+的产生,导致pH下降。这与毛善成〔21〕在硫化钠氧化的复杂反应动力学与机理中关于硫化物价态变化与pH变化的对应关系有一致的结论,即:S(-Ⅱ)→S(0),pH↑;S(0)→S(Ⅳ),pH↓;S(Ⅳ)→S(Ⅵ),pH↓。由此可以推测,在普通反应体系中,反应前6min时,生成单质硫的反应为主要反应,之后单质硫被继续氧化为高价态硫酸根的反应开始占主导反应,从而使体系的pH逐渐下降。在混凝强化体系中,由于PDM的特殊性质在一定程度上防止了单质硫被继续氧化,因此其出现峰值的时间较前者长,且pH下降趋势也相对较小,这也进一步证明了氧化产物中的高价态硫酸根既由硫化物一次性氧化而得,又由单质硫氧化而得这一观点。因此,控制已生成单质硫的继续氧化有利于提高单质硫的产量。
2.5混凝强化原理
由硫化物的氧化历程分析可知,混凝强化体系主要通过控制已生成单质硫的继续氧化来提高单质硫产量,为了进一步研究混凝强化机制,考察了反应体系Zeta电位随PDM加量变化的关系,结果如图5所示。

图5 不同PDM加量下体系Zeta电位
由图5可知,在未加PDM的反应体系中Zeta电位为-20.14mV,表明体系中单质硫颗粒表面带负电,由于PDM具有较长的分子链和较多的正电荷点位,因而很容易被带负电的单质硫颗粒吸附,从而有效地中和颗粒表面的负电荷〔22-23〕,因此随着PDM的加入,体系Zeta电位逐渐升高,由最初的-20.14mV升高到16.89mV。Zeta电位是指带电颗粒表面剪切层的电位,是对颗粒之间相互排斥或吸引力强度的度量。Zeta电位绝对值愈大,粒子间相互斥力愈强,颗粒物体系就愈稳定;当Zeta电位接近零时,分散作用减弱,随即趋向聚集〔24〕。由图5可知,当PDM投加质量浓度为1.0mg/L时,体系Zeta电位接近于零,此时颗粒间相互排斥力较弱,更有利于颗粒的团聚,这就是PDM的加入对体系中单质硫产量提高的原因之一。
为了考察PDM的加入对体系中颗粒团聚行为的影响,考察了前5min内不同PDM加量下颗粒粒度随时间的变化趋势,结果如图6所示。

图6 不同PDM加量下颗粒粒度
由图6可知,反应初期单质硫颗粒粒度处于纳米级范围内,并随反应时间的增加而逐渐增大。PDM投加质量浓度为1.0mg/L的反应体系中颗粒粒度明显大于其他反应体系。林奇〔18〕在含硫废水中硫的受控氧化过程研究中指出,过氧化氢氧化含硫废水所生成的单质硫颗粒呈大小不一的球状,因此假设氧化所得单质硫均为球形颗粒,根据球形颗粒比表面积计算公式可知,颗粒比表面积与颗粒粒度呈反比,即颗粒粒度愈大,颗粒比表面积愈小,因此PDM投加质量浓度为1.0mg/L的反应体系中颗粒比表面积相较于其他反应体系明显较小。
结合图5、图6分析,反应体系的Zeta电位的绝对值愈接近于零,反应体系中的颗粒粒度愈大、颗粒比表面积愈小。说明混凝强化体系由于PDM的加入改变了反应体系Zeta电位,使之接近于零,因此促进了单质硫颗粒的团聚,从而使颗粒粒度增大,颗粒粒度愈大,比表面积就愈小,表面能就愈小,因而颗粒表面愈稳定,因此在一定程度上降低了单质硫继续和体系中氧化剂反应的可能性,从而防止了单质硫继续被氧化为高价态硫酸盐。综上所述,混凝强化体系主要是通过提高已生成单质硫颗粒的表面稳定性来控制单质硫的继续氧化,从而提高单质硫转化率,降低硫酸根产量。
3结论
(1)采用PDM强化高含硫废水受控氧化过程,在PDM投加质量浓度为1.0mg/L,初始pH为6,过氧化氢投加量为9mL/L,反应时间为15min的条件下,混凝强化体系中硫化物去除率达99.09%,单质硫产量为1 588.5mg/L,较普通反应体系分别提高了1%和14%;SO42-产量为209.69mg/L,较普通体系降低了8%。
(2)过氧化氢氧化处理含硫废水的主要产物为单质硫和SO42-,其中SO42-一部分由硫化物一次性氧化而得,另一部分由单质硫氧化而得。两种反应体系pH随时间变化均呈现先缓慢升高再逐渐下降的趋势,混凝强化体系在一定程度上防止了单质硫被继续氧化为SO42-,因此pH出现峰值的时间相对较长,pH下降趋势也相对较小。
(3)PDM的混凝强化效果主要是通过改变反应体系Zeta电位,使之趋近于零,从而有利于单质硫颗粒的团聚,增大颗粒粒径,降低颗粒比表面积及表面能,使颗粒表面更稳定,在一定程度上控制了单质硫的继续氧化,从而达到含硫废水受控氧化的目的。
[1]姜峰,潘永亮,梁瑞,等.含硫废水的处理与研究进展[J].兰州理工大学学报,2004,30(5):68-71.
[2]席宏波,杨琦,尚海涛,等.纳米铁去除废水中硫离子的研究[J].环境科学,2008,29(9):2529-2535.
[3]张团结.城市排水管网恶臭发生影响因素研究[D].西安:长安大学,2014.
[4]OremW,GilmourC,Axelrad D,etal.Sulfurin theSouth Floridaecosystem:distribution,sources,biogeochemistry,impacts,and manageme[J].CriticalReviewsin EnvironmentalScienceand Technology,2011,41(S1):249-288.
[5]Riesch R,Plath M,Schlupp I,et al.Colonisation of toxic environments drives predictable life-history evolution in livebearing fishes(Poeciliidae)[J].Ecology Letters,2014,17(1):65-71.
[6]袁林,童倚勤,许涛.除硫剂在油田污水中的应用[J].复杂油气藏,2010,3(1):84-86.
[7]李华琴,何觉聪,陈洲洋,等.低温等离子体-生物法处理硫化氢气体研究[J].环境科学,2014,35(4):1256-1262.
[8]MurugananthanM,Raju GB,PrabhakarS.Removalofsulfide,sulfate and sulfite ions by electro coagulation[J].Journalof HazardousMaterials,2004,109(1/2/3):37-44.
[9]刘春霞,马兴,魏国华,等.一种新型“Turn-on”荧光探针用于硫化氢可视化检测[J].环境科学,2015,36(1):343-348.
[10]王庭.硫化物生物氧化为单质硫的研究[D].无锡:江南大学,2008.
[11]屈撑囤,沈哲,杨帆,等.油气田含硫污水处理技术研究进展[J].油田化学,2009,26(4):453-457.
[12]Jung K D,Joo OS,Cho SH,el al.Catalyticwetoxidation ofH2S to sulfuron Fe/MgO catalyst[J].Applied Catalysis A:General,2003,240(1/2):235-241.
[13]杨德敏,袁建梅,谢崇文,等.气田高浓度含硫废水的化学氧化处理[J].环境工程学报,2014,8(11):4757-4761.
[14]洪宗国,张爱清,袁誉洪,等.聚合硫酸铝铁处理含硫油田污水[J].环境化学,2002,21(3):311-312.
[15]段文猛,张太亮,刘莹,等.化学混凝复合超声波处理油气田含硫废水研究[J].石油与天然气化工,2009,38(6):547-550.
[16]翁焕新,高彩霞,刘瓒,等.污泥硫酸盐还原菌(SRB)与硫化氢释放[J].环境科学学报,2009,29(10):2094-2102.
[17]王庭,阮文权,严群,等.ORP控制在硫化物生物氧化成单质硫过程中的应用[J].环境工程学报,2008,2(3):366-369.
[18]林奇.含硫废水中硫的受控氧化过程研究[D].成都:西南石油大学,2014.
[19]贾旭.PDMDAAC合成工艺、聚合反应机理及结构与性质的关系[D].南京:南京理工大学,2011.
[20]Ilinitch OM,Vetchinova YS.Membraneassisted liquid phase catalytic oxidation of sulfides[J].Catalysis Today,1995,25(3/4):423-428.
[21]毛善成.硫化钠氧化的复杂反应动力学与机理[D].徐州:中国矿业大学,2009.
[22]张跃军,李潇潇,赵晓蕾,等.PAC/PDM复合混凝剂用于夏季太湖水混凝脱浊研究[J].环境科学,2008,29(8):2195-2200.
[23]黄曼君,李明玉,任刚,等.PFS-PDM复合混凝剂对微污染河水的强化混凝处理[J].中国环境科学,2011,31(3):384-389.
[24]田秉晖,栾兆坤,潘纲.阳离子聚电解质聚二甲基二烯丙基氯化铵的絮凝机理初探[J].环境科学学报,2007,27(11):1874-1880.
Study on the controlled oxidation of coagulation enhancementused on highly concentrated surfur-bearing wastewater
Wang Bing1,2,Chen Dandan1,Ren Hongyang1,2,LiYongtao1,2,Wang Dan1,Lin Qi1,3
(1.SchoolofChemistry and ChemicalEngineering,Southwest Petroleum University,Chengdu 610500,China;2.Oil and Gas Field Pollution Controland Environmental Security Key Laboratory ofEnvironmental Protection in Sichuan,Chengdu 610500,China;3.Security Environmental Protection Technology Research Instituteof Petrochina,Dalian 116000,China)
Using peroxide as oxidant,and poly dimethyl diallyl ammonium chloride(PDM)as coagulant,controlled oxidation treatmenthasbeen used on thehighly concentrated sulfur-bearingwastewater.The influencesofcoagulation enhancementmechanism on desulfurization effectare investigated.The results show thatunder the following conditions themass concentration of PDM added is 1.0 mg/L,initial pH 6,peroxide dosage 9 mL/L and reaction time 15 min,the sulfide removing rate in the coagulation enhancement system reaches 99.09%,and elemental sulfur output is 1 588.5mg/L,compared with ordinary systems,increasing by 1%and 14%,respectively.The SO42-output is209.69mg/L,compared with ordinary systems,decreasing by 8%.
sulfur-bearingwastewater;elementalsulfur;oxidation process;coagulation enhancement
X703.1
A
1005-829X(2016)07-0029-06
“十二五”国家科技支撑计划项目(2011BAC06B05);中国石油化工集团科技开发项目(114120)
王兵(1979—),教授。E-mail:wangb@swpu.edu.cn。
2016-05-20(修改稿)

