红毛新碱固体分散体的制备及大鼠在体肠吸收研究
邵晓玮,杨晓莹,师亚玲,王嗣岑,卢 闻
(西安交通大学药学院,西安 710061)
·药剂·
红毛新碱固体分散体的制备及大鼠在体肠吸收研究
邵晓玮,杨晓莹,师亚玲,王嗣岑,卢 闻*
(西安交通大学药学院,西安 710061)
目的 采用固体分散体技术改善红毛新碱的溶解度,增加其胃肠道吸收。方法 以聚乙烯吡咯烷酮为载体,正交实验设计优化红毛新碱固体分散体制备工艺;大鼠在体单向肠灌流法考察肠道吸收情况。结果 红毛新碱固体分散体的制备工艺为:红毛新碱和载体质量比为1∶12;溶剂用量比为4∶3;溶剂蒸发温度为65 ℃;冷冻时间为4h;制备工艺优化的固体分散体平衡溶解度为690.2±9.8μg·mL-1,比红毛新碱提高了33倍,1h累积溶出百分率达94 %,比红毛新碱提高近5倍;且固体分散体显著提高了相同质量浓度红毛新碱的在体肠吸收速率常数和表观吸收系数(P<0.05)。结论 固体分散体技术提高了红毛新碱的溶解度和溶出速率,增加了其肠道吸收。
红毛新碱;固体分散体;溶出度;在体单向肠灌流法
陕西七药是我国丰富草药资源的一部分,红毛七(Caulophyllum robustumMaxim)[1]作为陕西七药的一种,主要含有生物碱和三萜皂苷等多种成分[2]。红毛七来源于小檗科牡丹草属植物类叶牡丹的根茎及根。民间用于治疗风湿、类风湿等多种疾病,具有很高的开发价值[3]。红毛新碱是利用细胞膜色谱技术从红毛七中分离得到的一类新的生物碱类化合物[4]。药理研究表明,红毛新碱具有抗心肌缺血的活性,但其具有溶解度低、肠道吸收差和生物利用度低等缺点[5]。因此,改善红毛新碱溶解度、增加体内吸收是进一步明确红毛新碱药理作用的关键步骤。
本文以PVPK30为载体、以平衡溶解度为指标,通过正交实验设计,优化了红毛新碱固体分散体的制备工艺,考察了红毛新碱及其固体分散体的体外溶出度和大鼠在体肠吸收情况。
1 仪器与材料
1.1 仪器 2010AHT型高效液相色谱仪(日本岛津公司);RC-8D溶出度测试仪(天津市国铭医药设备有限公司);BT1-100恒流泵(上海琪特分析仪器有限公司)。
1.2 试药 红毛新碱(实验室自制,HPLC检测质量分数>98%);PVPK30(博爱新开源制药有限公司);甲醇(天津市科密欧化学试剂有限公司);其他试剂均为分析纯。
1.3 动物 健康SD大鼠,雄性,体质量200±20g,由西安交通大学实验动物中心提供,SCXK(陕)2012-003。
2 方法与结果
2.1 固体分散体制备 采用溶剂法制备红毛新碱固体分散体,按照红毛新碱和PVPK30质量比1∶3,1∶6,1∶9,1∶12和1∶15分别称取样品,加入适量无水乙醇溶解,置于水浴中加热,搅拌至溶剂挥发完全,迅速移至-18 ℃冰箱中冷冻,定时取出,减压干燥,粉碎,得固体分散体。另按照比例称定红毛新碱和PVPK30,混匀,过筛,得红毛新碱和载体的物理混合物,备用。
为确定制备工艺参数,采用正交实验设计L9(34)对无水乙醇用量比(无水乙醇体积∶药物与载体总质量和)、溶剂蒸发温度和冷冻时间3个因素进行考察,因素水平见表1。
表1 正交实验因素与水平
Tab.1Factorsandlevelsoftheorthogonaltest
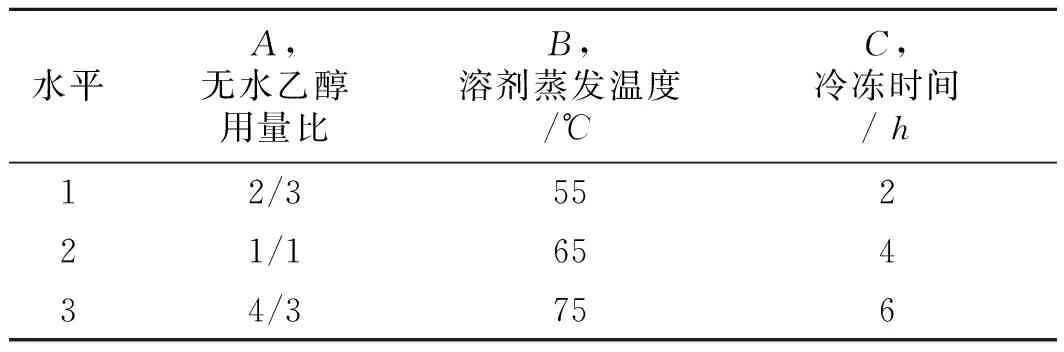
水平A,无水乙醇用量比B,溶剂蒸发温度/℃C,冷冻时间/h12/355221/165434/3756
以平衡溶解度为指标,考察PVPK30不同用量对红毛新碱溶解度的改善情况。随载体比例增加,红毛新碱溶解度逐渐增大,测得平衡溶解度分别为:300.0,345.6,425.4,511.8和513.4μg·mL-1。当载体比例为1∶15,红毛新碱溶解度增加程度明显减小,已接近PVPK30增溶容量。综合考虑增溶效果和载体用量,后续研究选择红毛新碱和PVPK30质量比为1∶12制备固体分散体。
同样以平衡溶解度为评价指标,采用正交实验设计优化了溶剂法制备固体分散体的工艺参数,结果见表2。
表2 正交实验结果
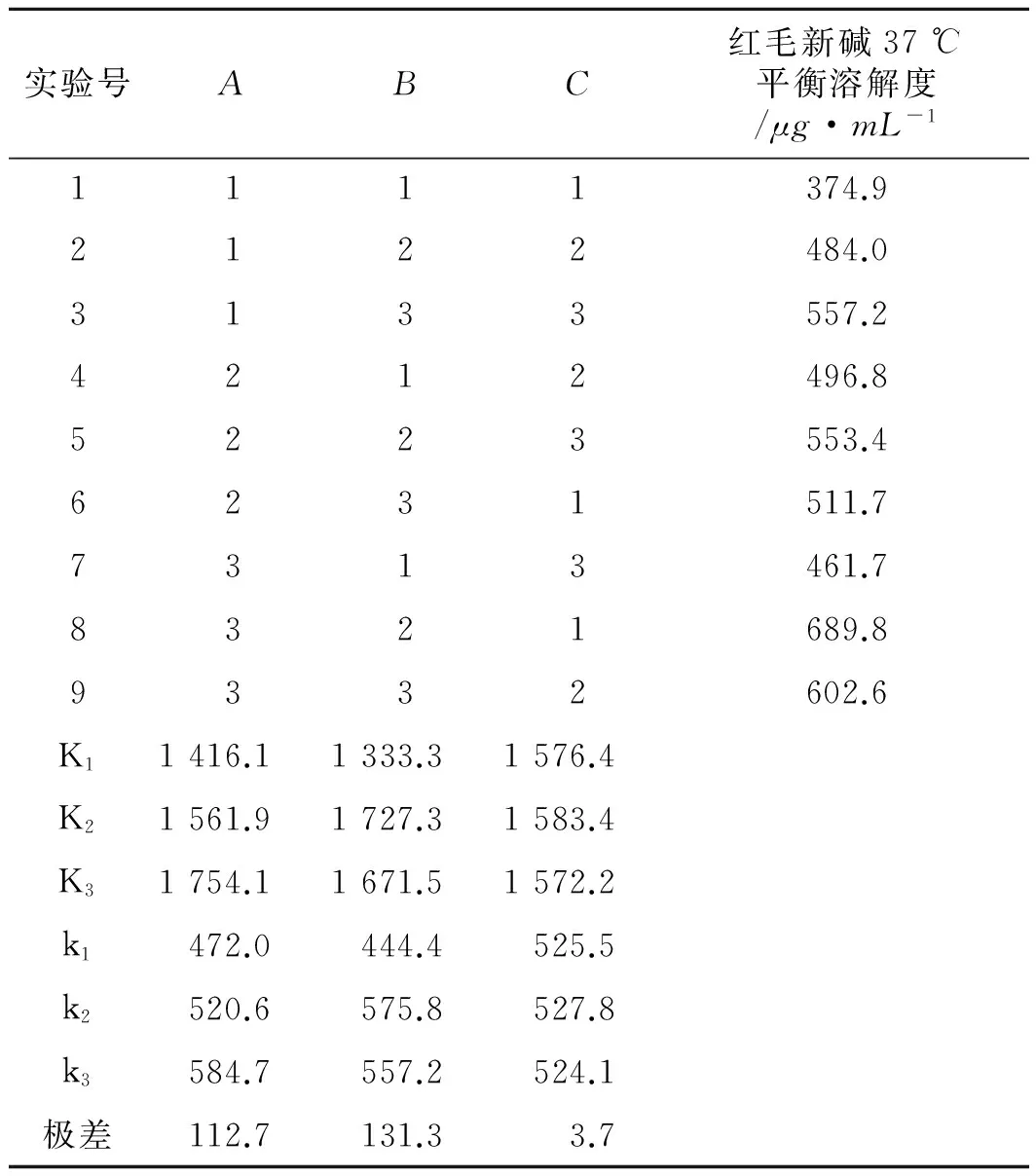
Tab.2 Results of the orthogonal test(n=3)
正交实验直观分析表明,考察因素对平衡溶解度的影响顺序为B>A>C,最佳制备工艺为A3B2C2,即无水乙醇用量比为4/3,溶剂蒸发温度为65 ℃,冷冻时间为4h。以优化工艺制得红毛新碱-PVPK30固体分散体的平衡溶解度为690.2±9.8μg·mL-1,比红毛新碱溶解度提高了近33倍。
2.2 体外溶出度测定
2.2.1 色谱条件 色谱柱:DiamonsilC18(150mm×4.6mm, 5μm);流动相:甲醇-5mL·L-1甲酸溶液(35∶65);流速:1.0mL·min-1;检测波长:267nm;柱温:25 ℃。
2.2.2 标准曲线绘制 取红毛新碱约10mg,精密称定,置于25mL量瓶中,加适量甲醇超声溶解并稀释至刻度,得到质量浓度为400.0μg·mL-1的储备液。精密量取储备液适量,用流动相配制成质量浓度为100.0,50.0,10.0,1.0和0.5μg·mL-1的系列对照品溶液,进行HPLC测定。以红毛新碱质量浓度(X)对峰面积(Y)进行线性回归,得标准曲线方程:Y=128 833 X-2 124.2,r=0.999 9;日内、日间精密度均小于1.2%,准确度为98.8%~99.2%。
2.2.3 溶出度测定 采用《中国药典》2010年版[6]及文献[7]溶出度测定法,以蒸馏水200mL作为溶出介质,温度为37±0.5 ℃,转速为100r·min-1。将红毛新碱、红毛新碱与PVPK30的物理混合物和红毛新碱固体分散体粉末(相当于15mg红毛新碱)均匀洒在液面上,分别于1,5,10,15,20,25,30,40,50和60min取样0.5mL,同时补充同温度的新鲜溶出介质0.5mL。样品经0.45μm微孔滤膜过滤,续滤液10μL进行HPLC测定,以累积溶出百分率对时间作图,绘制溶出曲线,见图1。

图1 红毛新碱及其固体分散体体外溶出曲线
Fig.1Cumulativedissolutionrateofcaulophineanditssoliddispersion
结果表明,红毛新碱溶出较慢,1h的累积溶出百分率仅为19.5 %;物理混合物和固体分散体都能提高红毛新碱的溶出速率,其中物理混合物1h的累积溶出百分率达31%,固体分散体1h的累积溶出百分率达94%,明显高于物理混合物的溶出度。
2.3 大鼠在体肠吸收
2.3.1 色谱条件 色谱柱:DiamonsilC18(150mm×4.6mm,5μm);流动相:甲醇-5mL·L-1甲酸溶液(35∶65);流速:1.0mL·min-1;检测波长:267nm;柱温:25 ℃。
2.3.2 标准曲线 取红毛新碱储备液,精密量取适量,用Krebs-Ringer(K-R)营养液配制系列对照品溶液,进行HPLC测定。以红毛新碱质量浓度(X)对峰面积(Y)进行线性回归,得标准曲线方程:Y=146 129X-1 089.3;r=0.999 9;日内、日间精密度均小于1.7%,准确度在98.4%~99.1%。
2.3.3 红毛新碱在K-R营养液中稳定性考察 以经肠灌流后的K-R营养液配制成质量浓度为10.0μg·mL-1的红毛新碱供试溶液,置于37±0.5 ℃的恒温振荡器中,定时取样,进行HPLC测定。回收率为98.3%~102.5%,表明红毛新碱在经肠灌流液中8h内稳定性良好。
2.3.4 大鼠单向肠灌流 参照文献方法[8-9],向实验前12h禁食的健康雄性大鼠腹腔注射200g·L-1的乌拉坦溶液0.65mL·kg-1。麻醉后,大鼠背位固定,沿腹中线切开腹腔,分离空肠,两端插管并结扎,用37 ℃生理盐水冲净肠道内容物,装好回流装置。先以K-R营养液回流15min平衡肠道,后将红毛新碱供试液以1mL·min-1的流速灌流肠段20min,再以0.2mL·min-1的流速灌流45min,达到稳定状态。在回流15,30,45,60和75min时取样,用HPLC法分析测定样品中的红毛新碱质量浓度,实验中采用重量法校正供试药液流经肠段后因体积变化而导致的质量浓度偏差。按照下式计算试药吸收速率常数(Ka)和表观吸收系数(Papp):
Ka=(1-CoutQout/CinQin)Q/V
Papp=-Qln(CoutQout/CinQin)/2πr2L
Qin和Qout分别为灌入和收集的供试液体积(mL)(经过密度校正);Cin和Cout分别为肠段进口处和出口处灌流液的质量浓度(μg·mL-1);L为灌流肠段长度(cm);r为灌流肠段横截面半径(cm);Q为灌流速度(0.2mL·min-1);V为灌流肠段的体积,可按照πr2L计算。不同红毛新碱供试液肠吸收情况见表3。
因红毛新碱溶解度的限制,在37 ℃、K-R营养液中,低、中、高质量浓度红毛新碱供试液的配制质量浓度分别为1,5和15μg·mL-1;而固体分散体较好地改善了其溶解度,故红毛新碱固体分散体供试液的配制质量浓度分别为15,50 和150μg·mL-1。
对不同红毛新碱供试液空肠段吸收速率常数和表观吸收系数进行方差分析表明,低、中、高质量浓度红毛新碱供试液的Ka和Papp值之间差异无统计学意义(P>0.05);相同质量浓度的红毛新碱供试液和固体分散体供试液的Ka和Papp值之间差异有统计学意义(P<0.05);低、中质量浓度红毛新碱固体分散体供试液的Ka和Papp值之间差异无统计学意义(P>0.05);而低、中质量浓度固体分散体供试液与高质量浓度固体分散体供试液的Ka和Papp值之间差异具有统计学意义(P<0.05)。由结果可知,溶解度是影响红毛新碱肠道吸收的主要因素,当固体分散体提高红毛新碱的溶解度由15μg·mL-1增加到50μg·mL-1时,其肠道吸收程度增大,同时,相同质量浓度的固体分散体较红毛新碱的吸收系数明显提高,说明固体分散体增加了红毛新碱在肠液中的润湿性,而利于被小肠吸收。
表3 红毛新碱供试液空肠段吸收速率常数和表观吸收系数
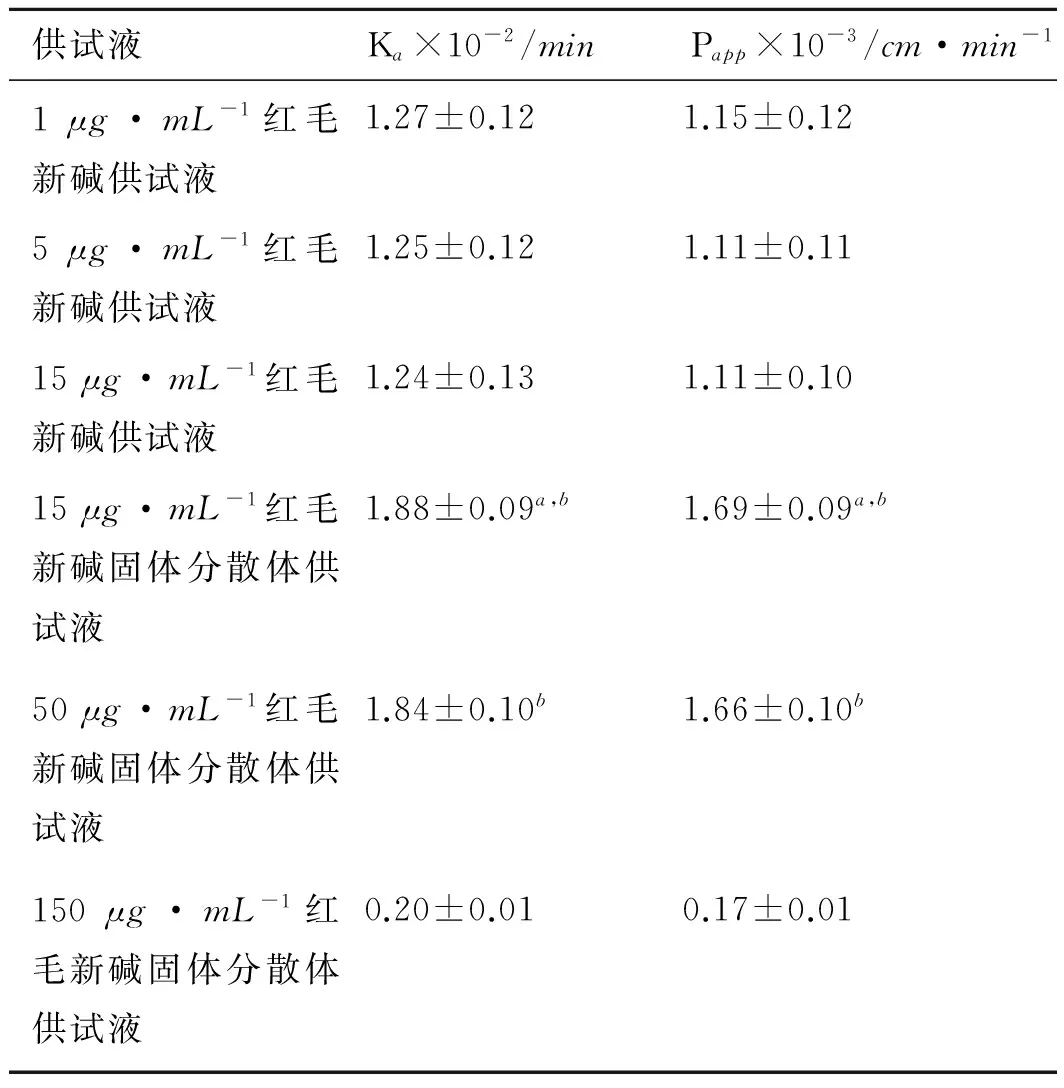
Tab.3 The absorption rate constant and apparent absorption coefficient of caulophine in jejunum(n=3)
注:与15μg·mL-1红毛新碱供试液的吸收速率常数和表观吸收系数比较,aP<0.05;与150μg·mL-1红毛新碱固体分散体供试液的吸收速率常数和表观吸收系数比较,bP<0.05。
3 讨论
红毛新碱固体分散体制备预实验中,考察了其他载体材料[10],如PEG6 000,PEG4 000及Poloxamer188,红毛新碱溶解度只提高了3~4.5倍,而PVPK30作为载体制备的红毛新碱固体分散体的平衡溶解度约提高了33倍。因此,实验选择PVPK30作为载体。
实验采用一定质量浓度的红毛新碱供试液在大鼠的十二指肠、空肠和回肠处分别进行了肠吸收实验,其Ka×10-2值分别为1.26±0.08,1.27±0.12,1.28±0.12;Papp×10-3值分别为1.12±0.08,1.15±0.12和1.14±0.11。方差分析表明,红毛新碱在十二指肠、空肠和回肠的Ka、Papp值之间差异不具有统计学意义,因此实验选用了空肠段进行肠吸收实验。
在体肠吸收实验普遍存在的问题是药液的体积会因肠道吸收或分泌水分而发生变化,从而影响药物的质量浓度,因此需要对药物质量浓度进行校正。药液质量浓度的校正方法有酚红法和重量法,由于在酚红的最大吸收波长处存在红毛新碱背景干扰,因此,本文选择了重量法来校正红毛新碱的质量浓度。
[1] 毛水龙.秦岭七药[M].西安:西安交通大学出版社,2011:158.
[2] 梁俊玉,周峰,陈明忠,等.红毛七的研究进展[J].中国实用医药杂志,2007,7(6):503-505.
[3] 韩省力,任静,王嗣岑.毛细管电泳法研究红毛新碱对HEK293 α1A细胞蛋白表达的影响[J].西北大学学报:自然科学版,2010,40:167-170.
[4]WANGS,WENB,WANGN,etal.FluorenonealkaloidfromCaulophyllum robustumMaxim.withanti-myocardialischemiaactivity[J].ArchPharmRes, 2009,32(4):521-526.
[5] 王嗣岑,陈琴华,尉耀元,等.红毛七超临界提取物化学成分的GS-MS分析 [J].药学学报,2007,42(5):525-528.
[6] 国家药典委员会.中国药典2010年版[S].二部.北京:中国医药科技出版社,2010:303.
[7] 吴瑾,张晓林,彭霞,等.辛伐他汀胃漂浮型缓释片的制备及体外释放研究[J].西北药学杂志,2012,27(2):147-149.
[8] 袁泉,李馨儒,王会娟,等.水飞蓟素微乳大鼠在体小肠吸收的动力学[J].药学学报,2004,39(8):631-634.
[9] 刘建平,杜志永,朱丽. 丹参酮ⅡA固体脂质纳米粒的体外释药和大鼠肠吸收特性的研究[J].中国药理学通报,2005,21(2):186-190.
[10]潘西海,赵丽.固体分散体中常用的载体[J].西北药学杂志,1997,12(6):277-278.
Preparation of caulophine solid dispersion and study on the intestinal absorption in rats
SHAOXiaowei,YANGXiaoying,SHIYaling,WANGSicen,LUWen*
(SchoolofPharmacy,Xi′anJiaotongUniversity,Xi′an710061,China)
ObjectiveToimprovethesolubilityandintestinalabsorptionofcaulophinebysoliddispertiontechnique.MethodCaulophinesoliddispersionwaspreparedwithPVPK30ascarriers.Orthogonaldesignwasappliedtooptimizethesoliddispersionpreparationprocedure.Intestinalabsorptionofcaulophineanditssoliddispersionwereevaluatedbyanin situsingle-passintestinalperfusioninrats.ResultTheoptimizedpreparationprocedureofcaulophinesoliddispersionwasconfirmed,thatis,themassratioofcaulophineandPVPK30 1∶12,theratioofsolventvolumeandsample4∶3,theevaporatingtemperature65 ℃,andthecoolingtime4h.Theequilibriumsolubilityofsoliddispersionpreparedbyoptimizedtechnologywas690.2±9.8μg·mL-1, 33timeshigherthanthatofcaulophine.Thepercentageofaccumulativedissolutionofcaulophinesoliddispersionwas94%in1h, 5timeshigherthanthatofcaulophine.Theabsorptionrateconstantandapparentabsorptioncoefficientsofthesoliddispersionweremuchhigherthanthoseofcaulophinewiththesameconcentrationinsingle-passintestinalperfusion(P<0.05).ConclusionThetechniqueofsoliddispersionsignificantlyimprovedthesolubilityanddissolutionrateofcaulophine,anditsintestinalabsorptioninrats.
caulophine;soliddispersion;dissolution;singlepassintestinalperfusion
“十二五”国家“重大新药创制”专项(编号:2012ZX09103201-054)
邵晓玮,女,硕士研究生
*通信作者:卢闻,女,副教授,硕士生导师
10.3969/j.issn.1004-2407.2016.06.016
R
A
2016-01-11)

