HBsAg酶联免疫吸附试验灰区设置研究*
王 瑞,张 婧,陈 瑜,甄 伟,于 磊,冷 婵,葛红卫
(北京市红十字血液中心检验科 100088)
·论 著·
HBsAg酶联免疫吸附试验灰区设置研究*
王 瑞,张 婧,陈 瑜,甄 伟,于 磊,冷 婵,葛红卫△
(北京市红十字血液中心检验科 100088)
目的 评价与验证该实验室乙型肝炎表面抗原(HBsAg)试验设置0.9倍临界值(CO值)的合理性。方法 参照美国临床和实验室标准协会(CLSI)发布的EP12-A2指南,通过试验确定HBsAg试验C5~C95区间即灰区。对HBsAg灰区标本进行抗体确认试验。绘制受试者工作特征曲线(ROC曲线)确定HBsAg试验最佳CO值。通过实验室既往数据,分析乙型肝炎病毒DNA(HBV-DNA)单阳性标本酶联免疫吸附试验(ELISA)结果分布(S/CO值)与灰区的关系。结果 (C50±20%)水平检测结果阴性数和阳性数均大于或等于95%,(C50-20%)~(C50+20%)水平范围包含C5~C95区间,灰区范围应在0.712~1.103倍CO值区间内。对44例HBsAg灰区标本(S/CO值0.900~0.990)进行中和试验,结果均为无反应性。绘制HBsAg的ROC曲线,曲线下面积(AUC)为0.981,最适CO值为0.063(现用CO值在0.055~0.060)。2010年11月2日至2013年12月31日检测标本研究886 291例患者,HBsAg阳性标本包括135例灰区标本,其中7例核酸检测法(NAT)检测结果均为反应性;共检出HBV-DNA单阳性标本421例,其HBsAg检测结果(S/CO值)分布区间为0.200~0.400,与阴性标本分布区间重叠、距0.9倍CO值较远。结论 该实验室现阶段HBsAg试验设置0.900的CO灰区过于严苛,试验结果支持取消灰区设置。报道所提供的4种灰区评价方法为其他实验室在设置ELISA试验灰区方面提供了1种思路。
乙型肝炎; 酶联免疫吸附测定; 核酸试验; 灰区; 临界值
乙型肝炎病毒(HBV)主要经血液和血制品传播,HBV检测方法有酶联免疫吸附试验(ELISA)、化学发光法、核酸检测法(NAT)等。由于ELISA试验具有价格低廉、试验时间短、操作步骤相对简单等优点,是国内血站筛查实验室检测乙型肝炎表面抗原(HBsAg)的主要方法[1-2]。ELISA检测结果常以阴性和阳性判断,但实际检测工作中经常会遇到某些献血者血液标本光密度值接近临界值(CO值)的灰区标本。为防止弱阳性标本漏检,最大限度确保血液安全,很多实验室设立了“灰区”,将检测值大于或等于灰区界限值标本判定为阳性,其血液做报废处理。但大多试剂生产商并未提供灰区界限值,各血站实验室对灰区的理解及判定规则也未达成共识[3]。随着核酸检测的逐步推广,ELISA设置灰区的效能应重新进行评估。本研究以CO值验证、灰区标本确认试验、绘制受试者工作特征曲线(ROC曲线)、ELISA结果与NAT结果比对分析,评价4种方法对HBsAg灰区设置的合理性,现报道如下。
1 资料与方法
1.1 一般资料 来自本中心无偿献血者标本,包括肝素抗凝标本(ELISA检测用)、乙二胺四乙酸(EDTA)抗凝标本(NAT检测用)。
1.2 仪器与试剂
1.2.1 试剂 HBsAg诊断试剂盒,购自生物梅里埃中国有限公司,批号20120402、20120605。核酸诊断试剂盒,购自诺华诊断公司,联检试剂批号598605,HBV-DNA鉴别试剂批号598605。HBsAg确认试剂盒,购自生物梅里埃中国有限公司,批号B12EA。
1.2.2 质控品 每次进行HBsAg试验采用外部质控品,质控品购自北京康彻斯坦生物有限公司,0.2 U/mL,批号201108003;每次进行NAT联检试验和HBV-DNA鉴别采用外部质控品,质控品购自北京康彻斯坦生物有限公司,30 U/mL,批号2013010019。
1.2.3 仪器 HBsAg检测采用全自动标本处理系统STAR 8CH、全自动酶联免疫分析系统FAME 24/30(哈美尔顿公司);NAT联检试验和HBV-DNA检测采用全自动核酸检测分析系统Tigris(诺华诊断公司)。
1.3 方法
1.3.1 依据EP12-A2《定性试验评价方法用户协议:提议指南》[4-6],确定HBsAg试验C5~C95水平(灰区)。(1)确定HBsAg试验CO值分析物水平(C50):由于试剂盒说明书中未提及C50水平,试剂生产厂商未提供C50标本,故采用EP12-A2文件方案中推荐的层级稀释方法寻找C50水平标本。收集HBsAg试验结果S/CO值大于1.000的阳性标本进行梯度稀释,重复检测各稀释度标本8次,得到阴性、阳性结果概率各占50%的稀释度,以此作为试验本方法的C50水平,再对该稀释度标本进行重复检测(n=40),以验证选定C50的可靠性。(2)确定HBsAg试验C5~C95(灰区):为验证HBsAg的CO值水平血清的稳定性,找出试验方法的灰区,配置(CO±20%)的水平标本,确定C5和C95水平(灰区)。
1.3.2 灰区标本确证试验 收集HBsAg灰区标本(S/CO为0.900~0.990)44例,进行中和试验。以试剂盒诊断标准作为判定标准,结果表达为反应性、无反应性2种。
1.3.3 绘制ROC曲线确定HBsAg试验最适检测CO值 (1)阳性标本来源:挑选本实验室2011年6月至2012年2月常规检测中HBsAg检测阳性标本486例,其中含HBsAg弱阳性标本50例(S/CO值0.900~1.500),进行中和试验。(2)阴性标本来源:HBsAg及NAT检测均为阴性标本292例。(3)绘制ROC曲线,选择最适CO值:以中和试验结果作为“金标准”结果,以检测光密度值为统计变量,绘制ROC曲线分析。选择Youdon指数最大的截断点对应的界值作为试验最适CO值,与现用CO值进行比较,确定灰区范围[7-8]。
1.3.4 HBsAg阳性、HBV-DNA阳性标本结果分析 (1)统计2010年11月2日至2013年12月31日HBV-DNA鉴别试验单阳性即“窗口期”或隐匿性乙型肝炎标本检测情况。“窗口期”或隐匿性乙型肝炎标本的HBsAg检测结果分布距离灰区设定值越近,说明灰区设置越合理;“窗口期”或隐匿性乙型肝炎标本的HBsAg检测结果分布距离阴性标本分布区间越近,说明灰区设置功效越差。(2)统计2010年11月2日至2013年12月31日期间,HBsAg灰区标本核酸检测情况。灰区标本内HBV-DNA阳性检出率越高说明灰区设置越合理,反之则说明灰区设置功效越差。
1.4 质量控制 每次试验外部质控品或内部质控对照,检测结果与预期一致,确认检测系统可靠。
1.5 统计学处理 采用SPSS19.0对数据进行处理。
2 结 果
2.1 依据EP12-A2,确定HBsAg C5、C95水平(灰区)
2.1.1 对初次试验制备C50水平标本进行验证试验 见表1。检测结果合计阳性25例,阴性15例。符合EP12-A2中阳性数量应为14~26例的要求,将此稀释度标本作为C50水平标本进行后续试验。
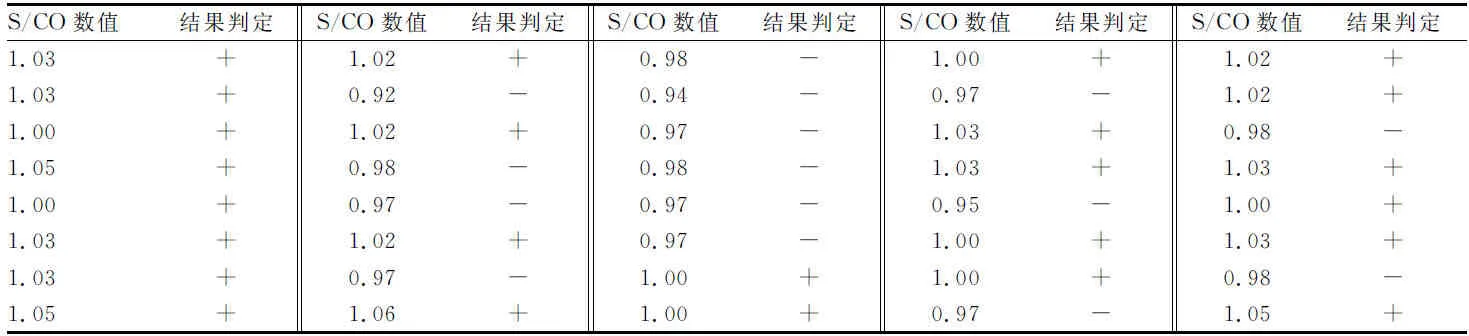
表1 C50水平验证检测结果(n=40)
2.1.2 采用C50稀释度标本 按体积比配制(C50+20%)水平、(C50-20%)水平标本各40例,其检测结果分别为(C50+20%)水平标本阳性40例,阳性率100%,S/CO均值1.103;(C50-20%)水平标本阴性40例,阴性率100%,S/CO均值0.712。由于检测结果阴性数和阳性数大于或等于95%,(-20%)~(+20%)水平范围包含了C5~C95区间,灰区范围落在0.712~1.103倍CO值区间内。见图1。
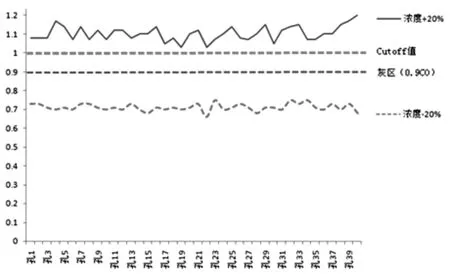
图1 (C50±20%)水平标本检测结果分布曲线
2.2 HBsAg灰区标本确证试验检测结果 对44例灰区标本(S/CO值0.900~0.990)进行中和试验,结果均为无反应性。
2.3 绘制ROC曲线确定HBsAg试验最适检测CO值 以中和试验结果作为“金标准”结果,以检测光密度值为统计变量,绘制ROC曲线。ROC曲线下面积(AUC)为0.981,选择Youdon指数最大的截断点对应的界值作为试验最适CO值为0.063,而试剂厂商建议CO值在0.055~0.060,最适CO值已大于厂商推荐CO值。见图2。
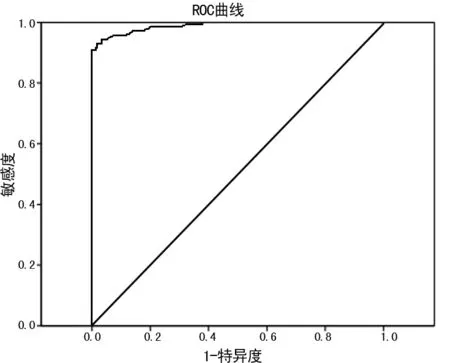
图2 ROC曲线
2.4 对HBsAg阳性、HBV-DNA阳性标本结果分析
2.4.1 实验室在2010年11月2日至2013年12月31日检测标本886 291例,共检出HBsAg“窗口期”或乙型肝炎隐匿性感染标本共计421例,且421例标本HBsAg检测结果S/CO值均小于0.900,其中287例(占68.17%)HBsAg检测结果S/CO值位于0.200~0.400。“窗口期”或乙型肝炎隐匿性感染标本相应HBsAg检测结果距0.9倍灰区CO值较远,与阴性标本分布区间重叠,说明灰区设置功效较差。见图3。
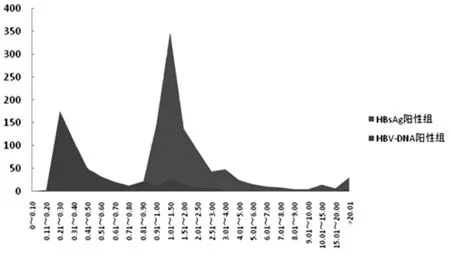
图3 HBsAg阳性组、HBV-DNA阳性组ELISA结果(S/CO值)分布图
2.4.2 实验室在2010年11月2日至2013年12月31日检测标本886 291例,HBsAg阳性中包括135例灰区标本,其中7例NAT检测结果均为阳性。
3 讨 论
我国是HBV感染的高发区。乙型肝炎是目前流行最广泛、危害最严重的病毒性肝炎之一。HBV可经血液和血液制品传播,《世界卫生组织血液筛查建议书》将HBV作为血液筛查实验室必检项目之一[9]。由于ELISA具有价格低廉、试验时间短、操作步骤相对简单等优点,是国内血站筛查实验室检测HBsAg的主要方法。不过,ELISA本身具有一定的局限性、试验过程变异较大。为了防止弱阳性标本漏检,确保输血安全,防止HBV感染,很多实验室设立了“灰区”。血液筛查实验室是否应该设置灰区、如何设置灰区还存在一定争议[10-11]。依据ISO15189的要求,各实验室应对检测系统的分析性能和(或)诊断性能的重要参数进行验证。ELISA的医学决定水平(如改变CO值设置灰区),应有科学依据并经过实验室检测系统验证。
针对方法本身及实验室设备情况,参考其他实验室基础,本实验室将ELISA检测HBsAg方法灰区设定为0.9倍CO值。随着ELISA检测试剂性能不断提高、试验过程管理的精细化及NAT技术的引入,此背景下应重新评估在灰区判定值存在的合理性及有效性。采用4种方法对本实验室HBsAg灰区判定值进行评价。(1)依据EP12-A2评价方法的精密度:结果表明,本实验室ELISA检测HBsAg试验具有良好的重复性和稳定性,因此将灰区界定在0.712~1.103倍CO值区间可确保检测结果的稳定性,现有灰区判定值0.9倍CO值符合其要求。(2)对44例灰区标本进行中和试验未发现有阳性结果,提示应重新审视现用灰区判定值设置的必要性。(3)采用ROC曲线确定HBsAg试验最适诊断CO值:结果显示,ROC曲线下面积为0.981,说明本方法准确性较高;选择Youdon指数最大的截断点对应的界值作为试验最适CO值为0.063,而试剂厂商建议CO值在0.055~0.060,最适CO值已大于厂商推荐CO值,无必要再增设灰区。(4)本实验室自2010年11月起对献血者标本同时进行ELISA检测和NAT检测,经对既往数据分析获知,421例乙型肝炎窗口期或隐匿性感染标本相应ELISA结果与阴性结果分布区间重叠,灰区判定值设定未起到防止漏检的功效。由此可见,灰区不可能解决“窗口期”问题,引入更高级检测技术才是解决问题的关键所在。综上所述,本研究采用4种方法对现用HBsAg灰区设置进行评价,结论为本实验室现阶段HBsAg试验设置0.9倍CO值灰区过于严苛,试验结果支持取消灰区设置。
尽管灰区设定的初衷是加强血液安全,但由于各实验室的依据及尺度不同,部分实验室存在“过度检验”现象。在血液短缺的背景下,造成血液资源不合理浪费、损伤献血者积极性、增加献血者心理负担等。随着实验室管理规范化、检测过程控制精细化及核酸检测技术的引入,检测方法和策略发生了重大变化,实验室应重新审视试验灰区,确保其必要性、科学性和合理性。
[1]陈霞,黄丽丽,姜标.ELISA法检测HBsAg灰区设置的探讨[J].临床输血与检验,2011,13(1):63-66.
[2]陈显,朱绍汶,黄成垠,等.ELISA法检测抗-HCV灰区设置探讨[J].临床输血与检验,2013,15(3):243-244.
[3]周艳萍,倪诗强,黄勇进.酶联免疫吸附试验“灰区”结果探讨[J].检验医学与临床,2008,5(14):876-877.
[4]陈瀑.乙型肝炎病毒表面抗原ELISA试验C50水平的确定及意义[J].现代检验医学杂志,2013,28(1):106-108.
[5]安成,程实,李杰,等.HBeAg化学发光法临界值验证和灰区设定的方法探讨及意义[J].中华检验医学杂志,2012,35(11):1045-1047.
[6]黄文彩,李柳燕,张少丰,等.应用ROC曲线分析确定ELISA检测抗-HBe灰区[J].检验医学与临床,2012,9(19):2426-2429.
[7]唐婧,包建玲,孟存仁,等.ROC曲线对ELISA检测丙型肝炎抗体阳性判断值的确定和分析[J].检验医学,2014,29(8):826-830.
[8]伍伟健,郭如华.ELISA试验灰区设置方法的探讨[J].中国生物制品学杂志,2008,21(10):911-912.
[9]李金明.临床酶免测定技术[M].北京:人民军医出版社,2005:100-105.
[10]李秀,王红丽,马超,等.ELISA定性检测HBsAg灰区和相关实验室结果分析[J].中国试验诊断学,2014,18(2):290-291.
[11]中国合格评定国家认可委员会.CNAS-CL02医学实验室质量和能力认可准则(ISO15189:2012)[M].北京:中国计量出版社,2013:33-34.
The discussion of method for grey area of HBsAg enzyme linked immunosorbent assay*
WANGRui,ZHANGJing,CHENYu,ZHENWei,YULei,LENGChan,GEHongwei△
(DepartmentofClinicalLaboratory,BeijingRedCrossBloodCenter,Beijing100088,China)
Objective To evaluate and verify the rationality of grey area of HBsAg enzyme linked immunosorbent assay(ELISA) in the laboratory.Methods According to CLIS EP12-A2 guide,HBsAg concentration of the range between C5 and C95 concentration were determined as grey area by ELISA test.Samples of HBsAg in grey area were identified by ELISA.Using ROC curve analysis,the optimal CO level of HBsAg test was determined.Combined with previous data,the relationship between disposition of HBV-DNA single positive simple of ELISA results(S/CO value) and grey area were explored.Results Positive and negative results of (C50±20%) concentration were all higher than 95%.(C50-20%) to (C50+20%) concentration range included C5 to C95,gray area of S/CO value was 0.712 to 1.103 times of CO.Forty four cases of HBsAg ELISA grey area samples(S/CO value was 0.900 to 0.990) were confirmed negatively by neutralization confirmatory test.According to ROC curve analysis,AUC was 0.981,the optimal CO level was 0.063(CO level in use was 0.055 to 0.060).And 886 291 samples were tested since November 2,2010 to December 31,2013 in our lab,including 135 grey area samples which were tested out in HBsAg positive samples.Seven samples were reactive by NAT test.A total of 421 cases were HBV-DNA single positive simples,and their distribution interval of ELISA results(S/CO value) were between 0.200 and 0.400,which overlapped the distribution interval of ELISA negative samples and far from 0.9 times of CO level.Conclusion The setting of grey area(0.9 times of CO level) is too strict for the lab,the grey area could be cancelled based on experimental data.In addition,the four evaluation methods of grey area we offered will give other labs idea for setting ELISA grey area.
hepatitis B virus; enzyme linked immunosorbent assay; nucleic acid test; grey area; cut off value
国家卫生和计划生育委员会卫生行业科研专项资助项目(201002005);北京市红十字血液中心中心级课题(BRCBC2012-009)。
王瑞,女,主管技师,主要从事血液传染病筛查、血站实验室质量管理方面的研究。
△通讯作者,E-mail:hwge88@163.com。
10.3969/j.issn.1673-4130.2016.21.003
A
1673-4130(2016)21-2956-03
2016-01-29
2016-04-19)

