纳米多孔β-Li3PS4固体电解质的溶剂脱除法制备及性能
潘亦真, 李宇杰, 陈一民, 郑春满
(国防科技大学航天科学与工程学院, 材料科学与工程系, 长沙 410073)
纳米多孔β-Li3PS4固体电解质的溶剂脱除法制备及性能
潘亦真, 李宇杰, 陈一民, 郑春满
(国防科技大学航天科学与工程学院, 材料科学与工程系, 长沙 410073)
以Li2S和P2S5为反应物, 四氢呋喃为溶剂, 采用溶剂脱除法制备了室温下稳定的高离子电导率β-Li3PS4晶体电解质, 通过粉末X射线衍射、 差热-热重分析、 拉曼光谱、 氮气吸附-脱吸和交流阻抗测试等方法对其性能进行表征, 研究了热处理温度对溶剂脱除程度、 固体电解质结晶状态、 比表面积、 孔隙率和离子电导率的影响. 结果表明, 该方法制备得到的β-Li3PS4晶体可以在室温下稳定存在. 160 ℃加热条件下Li3PS4的离子电导率达到7.44×10-6S/cm. 热处理过程中四氢呋喃分3个阶段脱除, 导致产物颗粒表面和内部产生大量纳米孔. 大量纳米孔洞的存在提高了材料的表面能, 有利于新相形核, 加快了相变速度, 降低了相变温度, 使β-Li3PS4晶体在室温下保持稳定.
固体电解质; 溶剂脱除法; 纳米多孔β-Li3PS4
锂离子电池具有工作电压高、 比能量大、 自放电率低、 循环寿命长、 无记忆效应、 可快速充放电等突出优点, 已成为广泛使用的二次电池. 目前商用锂离子电池所用的电解质材料以有机电解液为主, 但有机电解液存在易燃易爆等安全隐患. 采用锂离子固体电解质制备全固态锂离子电池是解决上述问题的有效途径[1,2], 但全固态锂离子电池的发展仍受电解质离子电导率、 加工性能和电池组装等关键因素制约[3]. Li2S-P2S5体系固体电解质具有离子电导率较高、 电化学窗口宽、 电子电导率低的优点, 是目前已知离子电导率最高的固体电解质体系之一[4], 经掺杂改性后其室温电导率可达10-5~10-2S/cm[5~7], 且电化学窗口大于5 V, 是固态电解质研究的热点[8~12].
Ribes等[13]通过高温烧结技术制备了组分为0.5Li2S·0.5GeS2的无机电解质, 其室温离子电导率为4×10-5S/cm. Mizuno等[6]报道了Li3.25P0.95S4固态电解质, 其室温电导率在10-3S/cm以上. Kamaya等[5]通过对Li2S-P2S5进行掺杂, 将硫化物电解质Li10GeP2S12的电导率提高到了1.2×10-2S/cm, 可以与电解液的导锂性能相媲美, 引起了广泛关注, 但对Li2S-P2S5进行掺杂会影响电解质与锂的化学相容性. 在Li2S-P2S5体系中用Ge部分取代P, 形成Li10GeP2S12, 其中Ge原子导致电解质与金属锂的相容性变差, 只能采用金属铟作为负极[5].
Li3PS4是Li2S-P2S5体系中一类重要的电解质[14~18], 属于含硫快离子导体(thio-LISICON), 有α-Li3PS4,β-Li3PS4和γ-Li3PS43种晶相[19]. Homma等[19]对其进行了X射线衍射和热分析, 发现不同温度下热处理Li3PS4晶体会发生α,β,γ相的转变, 温度超过200 ℃时低温γ相变成中温β相, 在473 ℃时转变为高温α相. 在降温过程中, 低于270 ℃时α相直接转变成了γ相, 没有β相产生, 说明β相在低温下无法稳定存在. 通常未经掺杂改性的晶体由于不含锂离子通道, 室温离子电导率极低, 阻抗在10-7~10-10数量级[20]; 而β-Li3PS4由于其特殊的晶体结构而具有锂离子通道, 离子电导率随测试温度的升高而增大, 在227 ℃时离子电导率高达3.0×10-2S/cm[19]. 除上述原子掺杂外, 采用化学方法构建微纳结构也是提升离子导电率的重要方法之一. Liu等[20]采用化学法合成了纳米多孔β-Li3PS4材料. 其室温锂离子电导率比块状γ-Li3PS4增加了3个数量级.
Li2S-P2S5系固态电解质的合成手段主要为干法, 即对原料粉末进行高能球磨或者高温煅烧, 时间长达数十小时, 能量消耗大, 生产速度慢, 工艺成本高. 此外, 根据Tachez等[21]报道, 煅烧法制备的高电导率β-Li3PS4在室温下难以稳定存在, 在低于195 ℃时β相转变为低电导率γ相.
本文采用构建微纳结构的方法, 通过加热脱除四氢呋喃(THF)溶剂的途径制备出室温下可稳定存在、 且离子电导率为7.44×10-6S/cm的纳米多孔β-Li3PS4晶体. 研究了热处理温度与结晶状态、 比表面积、 离子电导率的关系.
1 实验部分
1.1 试剂与仪器
Li2S(纯度>99.9%, 美国Alfa Aesar试剂公司); P2S5(纯度>99.0%, 上海阿拉丁试剂公司); 四氢呋喃(纯度>99.0%, 天津市富宇精细化工有限公司).
Super(12201750)型氩气手套箱(北京市米开罗那有限公司). 德国Bruker公司AXS D & Advance型X射线衍射仪; 北京恒久公司HCT-1型综合热分析仪; 德国Bruker公司Senterra光栅显微拉曼仪; 日本Hitachi公司S-4800型场发射扫描电子显微镜; 美国康塔公司QuadraSorb SI型氮气吸附-脱附测试仪; 瑞士万通公司Autolab PGSTA30型电化学工作站(以自制不锈钢模具为电极, 离子电导率数据由交流阻抗数据经美国Scribner Associates公司Zview软件拟合并使用公式计算得到).
1.2 实验过程
在氩气手套箱内, 称量摩尔比为3∶1的Li2S和 P2S5, 放入聚乙烯离心试管中, 加入50 mL THF, 混合搅拌12 h后, 离心30 min. 将离心试管移入手套箱, 倒出上层清液, 加入50 mL THF溶剂再次离心, 重复操作3次, 直至上层液由深棕色变为透明. 将离心后的产物干燥24 h后得到白色块状固体, 组成为Li3PS4·xTHF. 将Li3PS4·xTHF置于烧瓶中, 隔绝空气加热1 h(实验设置的热处理温度分别为80, 100, 120, 140, 160, 180, 200 ℃), 并用真空泵排出烧瓶中的气态分解产物, 得到灰白至深褐色块状样品, 样品颜色随加热温度的升高而加深. 将块状样品放入手套箱内研磨得到粉末状样品, 用YP-2型压片机压片得到片状样品. 所有操作在氩气手套箱或隔绝空气条件下进行.
2 结果与讨论
2.1 反应原理
Li3PS4是Li2S-P2S5体系中最稳定的化合物[17]. 用THF作溶剂, Li2S与P2S5反应生成Li3PS4·xTHF:
经过低温热处理, THF从Li3PS4·xTHF中脱除, 得到纯净的Li3PS4:
反应过程及产物转移需要严格隔绝空气, 因为Li2S和P2S5对空气中的微量水敏感, 会发生如下副反应:
Homma等[19]报道了Li3PS4的晶体结构,β-Li3PS4晶体由PS4-LiS4-LiS6单元构成, 每个单元中锂有3种不同的状态[19]. 该晶体属于正交晶系, PS4四面体呈“之”形曲折排列, 存在锂离子通道, 因此具有较高的离子电导率.
2.2 四氢呋喃的脱除
为了研究升温过程中Li3PS4·xTHF的吸、 放热情况和质量变化, 进行了差热-热重分析(图1). 样品在从室温到250 ℃的整个升温过程中出现了3个明显的吸热峰, 产生3次热失重: 在60~90 ℃区间失重14.6%; 在90~130 ℃区间失重21.4%; 在130~150 ℃区间失重6.7%. 3次热失重均对应于THF的脱除. 第三个强吸热峰结束后可观察到1个小的放热峰, 该放热峰在180 ℃处结束, 为Li3PS4由无定形态变为β-Li3PS4的晶型转变放热峰.
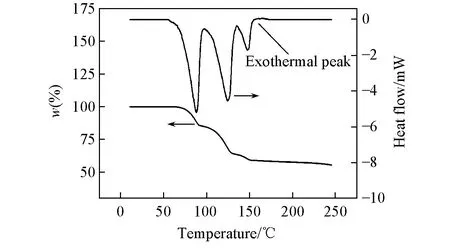
Fig.1 DTA-TGA curves of Li3PS4·xTHF
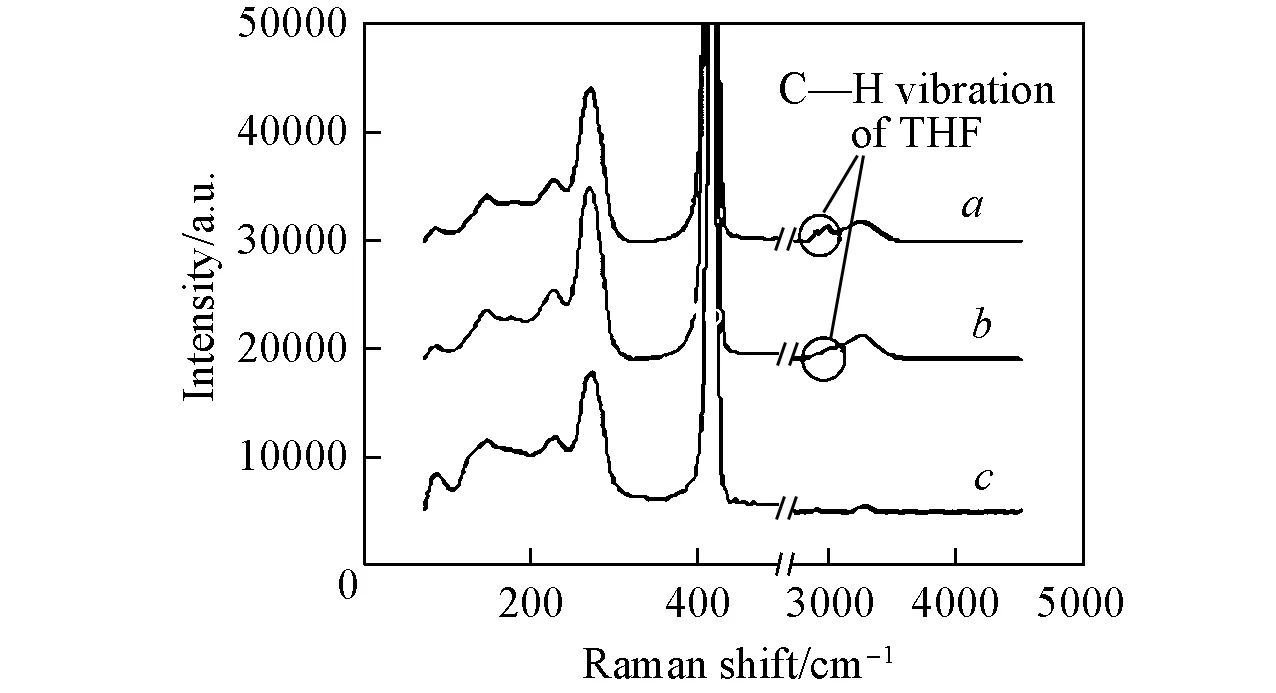
Fig.2 Raman spectra of Li3PS4·xTHF heated at 80 ℃(a), 100 ℃(b) and 160 ℃(c)
为了确定THF是否完全脱除, 对不同温度处理后的样品进行了拉曼光谱测试. 由图2可见, 各热处理温度下Li3PS4·xTHF样品都在415 cm-1处出现强峰, 此为νs(PS4)的特征峰[20]. 由于拉曼光谱测试需要暴露在空气中进行, 样品会迅速吸收水分, 因此出现水的特征峰, 即3000~3300 cm-1处的弱峰. 80 ℃热处理的样品在2880和2970 cm-1处各有1个明显的小峰, 对应于THF分子结构中4个亚甲基的C—H伸缩振动峰[20]. 随着热处理温度的升高, 该峰强度降低, 100 ℃热处理的样品中, 亚甲基的C—H伸缩振动峰大幅度减弱. 随着热处理温度的继续升高, THF不断被脱除, 160 ℃热处理后, 亚甲基的C—H伸缩振动峰消失, 此时THF完全脱除, 表明样品由Li3PS4·xTHF转化为Li3PS4.
2.3 Li3PS4的结晶状态和晶粒尺寸分析
图3为制备的Li3PS4·xTHF经不同温度热处理1 h后的粉末XRD谱图. 由于Li3PS4·xTHF极易与空气中的水反应, XRD测试时样品表面需覆盖一层聚酰亚胺薄膜(无定形态), 该薄膜的存在会使XRD谱线产生馒头宽峰, 但不会对XRD衍射峰测试结果产生影响.
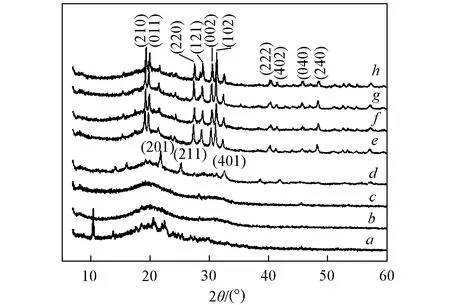
Fig.3 XRD patterns of Li3PS4·xTHF heated at different temperatures Temperature/℃: a. 25; b. 80; c. 100; d. 120; e. 140; f. 160; g. 180; h. 200.
由图3可见, 随着热处理温度的升高, 样品的晶型发生转变, 与差热-热重分析中的晶型转变放热峰相对应. 未进行热处理(25 ℃)的Li3PS4·xTHF在2θ=8.6°处有1个尖峰, 说明Li3PS4·xTHF中含有结晶相[17], 但此时并未形成晶态Li3PS4. 热处理温度为80和100 ℃时, 样品未出现明显的衍射峰, 呈现非晶态. 热处理温度为120 ℃时出现了宽衍射峰, 说明晶粒已经成核, 但结晶程度较弱, 此时Li3PS4的(201), (211), (401)晶面优势生长. 热处理温度为140 ℃时, XRD谱图中出现清晰的衍射峰, 衍射谱线与β-Li3PS4的标准PDF卡片(PDF#76-0930, 样品由Mercier在高温下制备[22])相一致, 说明已形成β-Li3PS4. 热处理温度从140 ℃升高到200 ℃的过程中, 半峰宽变窄, 晶粒长大. 根据Tachez等[21]的报道, 当加热温度高于195 ℃时, 采用煅烧法制备出的γ-Li3PS4转变为高离子电导率的β-Li3PS4, 而在低于195 ℃时高离子电导率的β相恢复到γ相, 即β相在室温下难以稳定存在. 而经过140 ℃热处理的样品在室温条件下显示出清晰的β-Li3PS4衍射峰, 说明溶剂脱除法不仅可以在较低温度下(低于195 ℃)制备出β-Li3PS4晶体, 而且所制备的β-Li3PS4晶体在室温下可以稳定存在而不转变为γ相.
表1为不同热处理温度下制备的Li3PS4的X射线衍射三强线数据. 由表1可知, 随着Li3PS4·xTHF样品热处理温度的升高, 峰位发生了偏移, 晶面间距d也在改变, 晶格常数发生了变化; 在加热温度从140 ℃升高到200 ℃的过程中, (102), (210), (220)晶面的衍射峰半峰宽不断减小, 垂直于晶面的厚度在增加. 据此可知样品晶粒大小随着热处理温度的升高而增大.
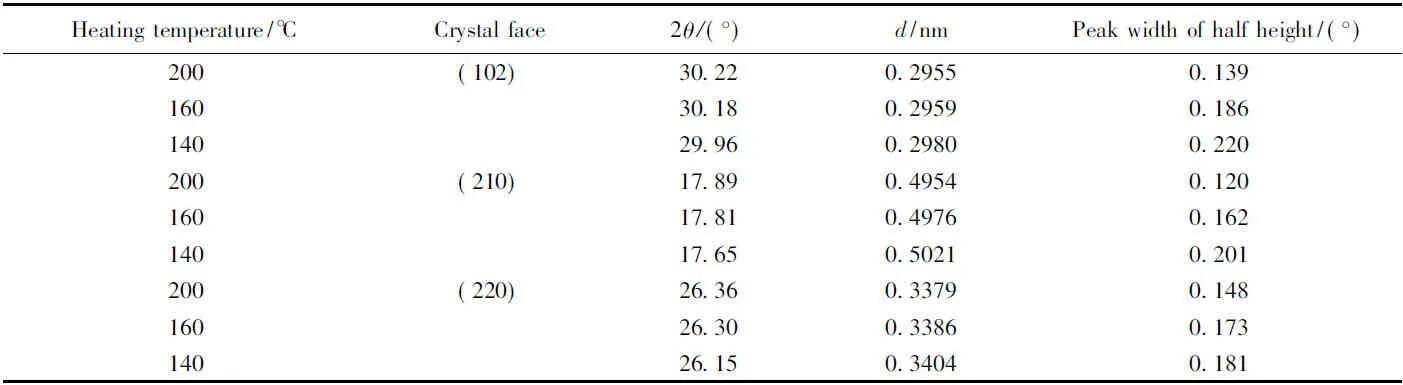
Table 1 XRD data of Li3PS4 heated at different temperatures
2.4 Li3PS4·xTHF的微纳结构分析
图4(A)和(B)为未热处理的Li3PS4·xTHF样品的SEM照片. 可见, 未经热处理的Li3PS4·xTHF表面孔隙较少, 颗粒大且较完整. 由差热-热重分析可知, 此时THF未从样品中脱除. 图4(C)和(D)为160 ℃热处理后Li3PS4样品的SEM照片, 可见, 热处理后样品呈现微米和纳米结构共存的形貌. 微米颗粒表面布满纳米颗粒, 且颗粒表面有大量孔洞.

Fig.4 SEM images of Li3PS4·xTHF before(A, B) and after(C, D) 160 ℃ heat treatment
热处理使Li3PS4·xTHF中THF脱除而出现大量孔隙和裂纹, 使样品比表面积增大, 而热处理温度的持续升高又会使晶粒长大, 导致比表面积下降. 对不同热处理温度下制备的Li3PS4粉末样品进行了比表面积测试, 研究了Li3PS4的比表面积的变化趋势.
从图5可知, 样品比表面积的变化趋势与热重分析的结果有良好的对应性. 未经过热处理的Li3PS4·xTHF的比表面积最小, 说明常温下颗粒呈完整的块状, THF尚未脱出. 80 ℃热处理的Li3PS4比表面积最大, 可能是因为脱除THF导致样品产生大量孔隙所致. 热处理温度为80~100 ℃时, 样品比表面积骤降, 推测可能是样品中比表面能高的孔隙和裂纹处产生大量微晶, 导致微孔减少, 比表面积降低. 热处理温度为100~140 ℃时, 样品比表面积逐渐减小, 说明一方面Li3PS4·xTHF经历了第二个THF的脱除过程, 产生新的孔隙和裂纹; 另一方面随着温度的升高, 晶粒形核长大, 填补孔隙和裂纹. 两个因素共同作用的结果使比表面积减小. 热处理温度为140~160 ℃时, 根据图1可知, 此温度下为THF脱除的第三阶段, THF的脱除占主导作用, 使孔隙率上升. 热处理温度为160, 180和200 ℃的样品已完全脱除THF, 晶粒不断长大, 孔隙和裂纹显著减少, 从而使比表面积有轻微下降.
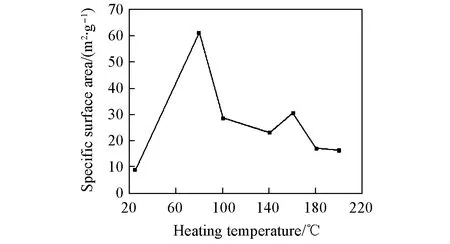
Fig.5 Relationship between heating temperature and specific surface area
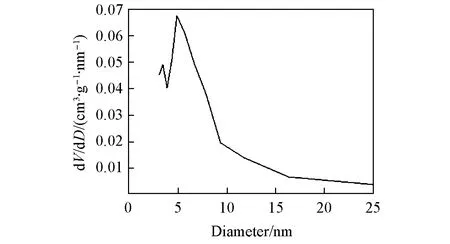
Fig.6 Pore diameter distribution of 160 ℃- heated Li3PS4
对160 ℃热处理的Li3PS4样品进行氮气吸附-脱吸测试, 得到的孔径分布曲线如图6所示. 该曲线表明Li3PS4呈现纳米多孔结构, 主要为4~8 nm的介孔, 对应于THF去除时留下的孔隙. 大量纳米孔对于降低β-Li3PS4相变温度有重要作用. 晶型转变是固态相变, 晶体中原子的迁移往往很慢, 所以固态相变通常需要较高的温度. 本文所采用的溶剂脱除法可以在加热过程中使固体颗粒表面产生大量结晶态THF脱除时留下的缺陷——纳米孔. 大量缺陷的存在可以提高材料的表面能, 有利于新相形核, 从而加快相变速度, 降低相变温度. 所以140 ℃热处理的Li3PS4样品的XRD谱图中已出现明显的β-Li3PS4的特征峰, 相比高温煅烧制备β-Li3PS4的相变温度低55 ℃.
2.5 Li3PS4的离子电导率
将Li3PS4粉末压成电解质片(25 MPa), 在自制不锈钢模具内组装成Li3PS4半电池进行室温(25 ℃)交流阻抗测试, 得到的典型Nyquist曲线如图7所示. 高频端不规则半圆代表电解质的体电阻, 可以拟合成晶粒阻抗和晶界阻抗两部分; 低频端直线反映固体电解质阻塞电极表面, 阻碍离子迁移. 用Zview软件按照图7中的等效电路拟合, 可得到电解质阻抗模拟值并计算离子电导率. 等效电路中R1为晶粒阻抗,R2为晶界阻抗, 电解质体电阻R=R1+R2, CPE1为恒相元件,W1为Warburg阻抗. 电导率的计算公式为σ=L/AR, 其中σ为离子电导率,L为电解质片厚度,A为电解质片面积,R为交流阻抗谱拟合得到的电解质体电阻.
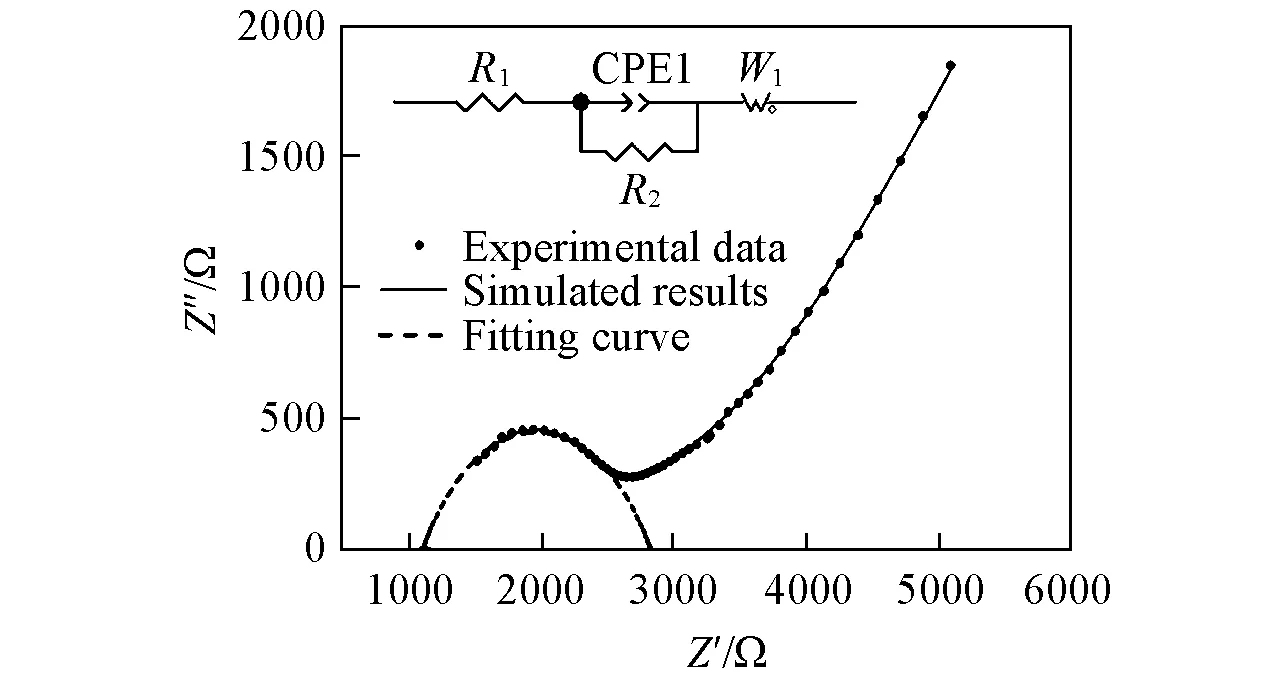
Fig.7 Impedance plot from the symmetrical cell containing 160 ℃-heated Li3PS4 Inset: equivalent circuit.
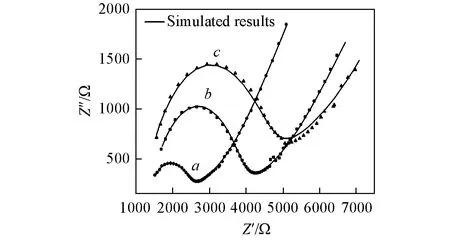
Fig.8 Impedance plots from the symmetrical cell containing 160 ℃-(a), 180 ℃-(b) and 200 ℃-(c) heated Li3PS4
图7为160 ℃热处理后得到的Li3PS4电解质压片后的交流阻抗图, 图中虚线为高频阻抗弧部分的模拟结果, 实线为整个阻抗谱的拟合结果. 160, 180, 200 ℃热处理制备的Li3PS4晶体电解质的晶粒阻抗拟合结果分别为1200, 1160, 930 Ω. 这说明随着热处理温度的升高, 晶格常数增大, 晶粒阻抗降低. 由图8可知, 随着热处理温度的升高, 阻抗弧的直径增大,R2增大, 说明晶界阻抗增大. 结合XRD谱图数据可知, 这可能是因为热处理温度升高导致晶粒尺寸增大, 同样压力下片状样品的致密度降低, 晶界阻抗增大.
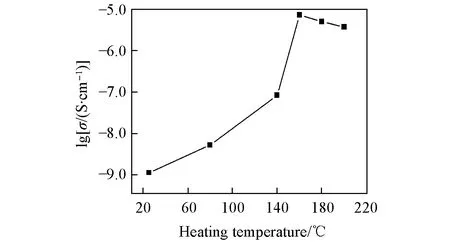
Fig.9 Logarithmic relationship between ionic conductivity and heating temperature
将不同温度下的电解质阻抗拟合值(R1+R2)代入σ=L/AR计算得到电解质片的离子电导率. 图9为离子电导率与热处理温度的对数关系曲线. 其中热处理温度为100和120 ℃时, Li3PS4·xTHF中未形成高离子电导率的β-Li3PS4, 交流阻抗谱未显示出有规律的数据点, 离子电导率极低, 难以通过软件进行阻抗拟合, 无法计算其离子电导率. 这是由于反应温度处于Li3PS4晶型转变的温度范围, 反应后样品中并未形成锂离子通道, 与XRD测试中该温度下Li3PS4呈现无定形态的测试结果相一致. 由于所制备的β-Li3PS4未进行掺杂, 晶体缺陷较少, 因此晶粒阻抗比掺杂的固体电解质高. 本文采用手动压片后直接进行交流阻抗测试, 与通常先压片后高温固相烧结所得电解质片相比, 手动压片得到的片状样品致密度较低, 因此样品的晶界阻抗较高. 综合以上2个因素, Li3PS4的离子电导率较低. 但是离子电导率经过加热脱除溶剂后仍有较大提升, 从图9可以看出, 室温下的Li3PS4·xTHF离子电导率约为10-9S/cm, 而160 ℃时形成结晶良好的β-Li3PS4, 离子电导率最高, 达到7.44×10-6S/cm, 比室温下制得的Li3PS4·xTHF提高了近4个数量级.
3 结 论
采取溶剂脱除法制得常温下稳定的高离子电导率β-Li3PS4晶体, 研究了β-Li3PS4晶体的形成过程以及结晶形态、 微纳结构、 电导率性能与热处理温度的关系. 结果表明, 热处理温度为80和100 ℃时Li3PS4·xTHF呈现无定形态, 120 ℃时开始晶化, 140 ℃时出现β-Li3PS4, 160 ℃时THF完全脱除. 随着THF的脱除, Li3PS4表面出现大量纳米孔. 热处理温度从140 ℃升至200 ℃时β-Li3PS4的离子电导率呈先升高后下降的趋势, 160 ℃热处理后离子电导率最高, 达到7.44×10-6S/cm, 相比未进行热处理的Li3PS4·xTHF提升了4个数量级. 溶剂脱除法通过增加纳米孔隙的方法帮助新相形核, 在更低的温度下完成相变, 相比高温烧结法, 溶剂脱除法具有能耗低、 步骤简单、 效率高等优点, 为低温制备高离子电导率的Li2S-P2S5体系固态电解质提供了一种新方法, 也为制备其它类型的固态电解质提供了新的思路.
[1] Yu T., Han Y., Wang H., Xiong S. Z., Xie K., Guo Q. P.,Chem.J.ChineseUniversities, 2016, 37(2), 306—315(余涛, 韩喻, 王珲, 熊仕昭, 谢凯, 郭青鹏. 高等学校化学学报, 2016, 37(2), 306—315)
[2] Ren X. M., Gu H., Chen L. Q., Wu F., Huang X. J.,Chem.J.ChineseUniversities, 2002, 23(7), 1383—1385(任旭梅, 顾辉, 陈立泉, 吴锋, 黄学杰. 高等学校化学学报, 2002, 23(7), 1383—1385)
[3] Xu X. X., Qiu Z. J., Guan Y. B., Huang Z., Jin Y.,EnergyStorageScienceandTechnology, 2013, 2(4), 331—341(许晓雄, 邱志军, 官亦标, 黄祯, 金翼. 储能科学与技术, 2013, 2(4), 331—341)
[4] Liu J., Xu J. Y., Lin Y., Li J., Lai Y. Q., Yuan C. F., Zhang J., Zhu K.,ActaChim.Sinica, 2013, 71(6), 869—878(刘晋, 徐俊毅, 林月, 李劼, 赖延清, 袁长福, 张锦, 朱凯. 化学学报, 2013, 71(6), 869—878)
[5] Kamaya N., Homma K., Yamakawa Y., Hirayama M., Kanno R., Yonemura M., Kamiyama T., Kato Y., Hama S., Kawamoto K., Mitsui A.,Nat.Mater., 2011, 10(9), 682—686
[6] Mizuno F., Hayashi A., Tadanaga K., Tatsumisago M.,SolidStateIonics, 2006, 177(26), 2721—2725
[7] Cui G. J., Han Y., Xu J.,GuangzhouChemicalIndustry, 2014, 42(17), 71—73(崔广军, 韩喻, 许静. 广州化工, 2014, 42(17), 71—73)
[8] Yamada T., Ito S., Omoda R., Watanabe T., Aihara Y., Agostini M., Ulissi U., Hassoun J., Scrosati B.,Electrochem.Soc., 2015, 162(4), A646—A651
[9] Agostini M., Aihara Y., Yamada T., Scrosati B., Hassoun J.,SolidStateIonics, 2013, 244, 48—51
[10] Nagao M., Hayashi A., Tatsumisago M.,Electrochim.Acta, 2011, 56(17), 6055—6059
[11] Hayashi A., Ohtomo T., Mizuno F., Tadanaga K., Tatsumisago M.,Electrochim.Acta, 2004, 50(2), 893—897
[12] Hayashi A., Ohtomo T., Mizuno F., Tadanaga K., Tatsumisago M.,Electrochem.Commun., 2003, 5(8), 701—705
[13] Barrau B., Ribes M., Maurin M., Kone A., Souquet J. L.,Non-Cryst.Solids, 1980, 37(1), 1—14
[14] Li G. R., Li Z. P., Zhang B., Lin Z.,FrontEnergyRes., 2015, (3), DOI: 10.3389/fenrg.2015.00005
[15] Lin Z., Liu Z. C., Dudney N. J., Liang C. D.,ACSNano, 2013, 7(3), 2829—2833
[16] Lin Z., Liu Z. C., Fu W. J., Dudney N. J., Liang C. D.,Adv.Funct.Mater., 2013, 23(8), 1064—1069
[17] Lin Z., Liu Z. C., Fu W. J., Dudney N. J., Liang C. D.,Angew.Chem.Int.Ed., 2013, 125(29), 7608—7611
[18] Dathar G. K. P., Kent P. R., Rondinone A. J., Ganesh P.,TheElectrochemicalSocietyMeetingAbstracts, Orlando, Florida, USA, 2014, Vol.MA2014-01, 49
[19] Homma K., Yonemura M., Kobayashi T., Nagao M., Hirayama M., Kanno R.,SolidStateIonics, 2011, 182(1), 53—58
[20] Liu Z. C., Fu W. J., Payzant E. A., Yu X., Wu Z. L., Dudney N. J., Kiggans J., Hong K. L., Rondinone A. J., Liang C. D.,J.Am.Chem.Soc., 2013, 135(3), 975—978
[21] Tachez M., Malugani J. P., Mercier R., Robert G.,SolidStateIonics, 1984, 14(3), 181—185
[22] Mercier R., Malugani J. P., Fahys B., Robert G., Douglade J.,ActaCrystallogr.Sect.B:Struct.Sci., 1982, 38(7), 1887—1890
(Ed.: S, Z, M)
Performance of Nano-porousβ-Li3PS4Prepared by Solvent Removing Method†
† Supported by the National High Technology Research and Development Program of China(No.2014AA8095078B).
PAN Yizhen, LI Yujie*, CHEN Yimin, ZHENG Chunman
(DepartmentofMaterialScienceandEngineering,CollegeofAerospaceScienceandEngineering,NationalUniversityofDefenseTechnology,Changsha410073,China)
Room temperature-stable and highly ionic conductive crystal electrolyteβ-Li3PS4was fabricatedviasolvent-removing method using Li2S and P2S5as reactants, tetrahydrofuran as solvent. Thenβ-Li3PS4was analyzed through X-ray diffraction, differential thermal analysis and thermogravimetry analysis, Raman spectrometry, N2adsorption-desorption analysis and electrochemical impedance spectroscopy. Effects of heat treatment temperature on solvent removing, crystallization, specific surface area, porosity, and ionic conductivity were investigated. The results show that solvent-removing method successfully stabilizesβ-Li3PS4at room temperature. When heated at 160 ℃, Li3PS4reaches its highest ionic conductivity, 7.44×10-6S/cm. During the heating treatment, tetrahydrofuran solvent was removed in 3 stages, generating numerous nanopores at both surface and interior of the Li3PS4particles. Those nanopores increase surface energy, which helps new phase nucleate, expedites crystalline transition, reduces phase transition temperature, and stabilizesβ-Li3PS4to room temperature.
Solid electrolyte; Solvent-removing method; Nanoporousβ-Li3PS4
2016-05-12.
日期: 2016-06-27.
国家高技术研究发展计划项目(批准号: 2014AA8095078B)资助.
10.7503/cjcu20160333
O611; O646; TQ174
A
联系人简介: 李宇杰, 男, 博士, 讲师, 主要从事正极材料和电解质材料研究. E-mail: powerlyj@163.com

