大豆蛋白自组装纤维聚集体的界面及乳化性质研究
王金梅 陈燕琼 王梦萍 杨晓泉
(华南理工大学轻工与食品学院食物蛋白工程研究中心,广州 510640)
大豆蛋白自组装纤维聚集体的界面及乳化性质研究
王金梅 陈燕琼 王梦萍 杨晓泉
(华南理工大学轻工与食品学院食物蛋白工程研究中心,广州 510640)
大豆分离蛋白(SPI)经酸性热处理后可自组装形成具有交叉β-折叠结构的纤维聚集体,研究了SPI纤维化对其界面吸附动力学、界面膜扩张流变特征及乳化性质的影响。由于纤维化过程中伴随的蛋白水解,酸性热处理明显改善了SPI在等电点附近的溶解度,但中性pH处溶解度明显下降。SPI纤维化过程中,蛋白表面压增加速度和Ed值明显增强,说明其拥有较高的界面活性,且增强了蛋白分子在界面上的相互作用,易于在界面形成较厚的多层结构。纤维聚集体的形成使蛋白乳液粒径随加热时间延长而不断增加,但其pH稳定性明显增强,明显抑制了其在中性条件下的絮凝,这一改善受加热时间强烈影响。
大豆蛋白 自组装 纤维聚集 界面性质 乳化性质
蛋白质在低pH(2.0)和低离子强度下加热会发生自组装形成纤维聚集体,其具有典型的交叉β-折叠结构(crossβ-sheet)[1]。研究者针对这一普遍现象进行形成机制研究,以期通过调控(抑制或促进)蛋白聚集进程来开发其优异的功能性质[1-2]。近年来,蛋白纤维以其刚性的β-sheet结构和良好的流变学特性(特别是弹性)引起了生物医药和材料等领域研究者的广泛关注,扩展蛋白纤维聚集体应用范围成为研究热点。Cherny等[3]综述了蛋白纤维作为功能性结构单元在材料科学中潜在的用途。蛋白纤维材料拥有较其他生物材料更高的强度,表现更好的优越性,可用于构建水凝胶体系,例如热响应型水凝胶[4]。另外,在生命科学领域,蛋白纤维结构可用做支架或者配基结合体应用于器官移植等医药应用[5]。
在食品工业中,蛋白纤维聚集体因其良好的流变学性质,主要用作增稠剂和凝胶填充物[6]。在其理论研究领域也主要集中于纤维凝胶的构建,表征其微结构和流变学特性[7-9]。目前,蛋白纤维聚集体的界面吸附性质及其在乳液体系中的应用等领域报道较少见,且仅限于动物蛋白。Mezzenga研究团队报道了β-乳球蛋白及其蛋白纤维在油水和汽水界面的吸附和剪切流变性质,发现蛋白纤维聚集体可以有效地稳定界面。研究者利用探针颗粒跟踪技术深入揭示了蛋白纤维稳定界面的可能机制[10-11]。另外,有报道通过多层静电沉积方法在乳液液滴构建甲氧基果胶/纤维多层结构来强化微胶囊,并对柠檬烯进行控制释放[12-13]。
目前已证实,大豆蛋白在酸性pH加热可形成纤维聚集体,且7S球蛋白聚集能力高于11S球蛋白,静电屏蔽可以有效改善其纤维化聚集进程[14-15]。考虑到蛋白质的界面及乳化性质对于食品体系的重要指导意义,以大豆分离蛋白(SPI)为原料,着重探讨蛋白纤维聚集体的形成对界面(界面吸附及界面膜扩张流变性质)和乳化性质的影响,为扩展蛋白纤维聚集体的开发利用提供参考。
1 材料与方法
1.1 材料与设备
低温脱脂豆粕:山东禹王公司;Florisil分子筛(60~100目):Sigma公司;牛血清白蛋白(BSA)和Folin-Ciocalteu’s 试剂:北京鼎国试剂公司;金龙鱼玉米油:市售;其他试剂均为分析纯。
OCA20视频光学接触角测量仪、ODG20P界面黏弹测量仪:德国Dataphysics公司;DMA35N便携式密度计:奥地利Anton Paar公司;CR22G型冷冻离心机:日本HITACHI公司;Dumas定氮仪:法国Elementar公司;T25高速剪切机:德国IKA公司;M-110EH-30高压微射流纳米均质机:美国MFIC公司; Mastersize2000粒度分布仪:英国Malvern公司。
1.2 试验方法
1.2.1 SPI的制备
以料液比1∶10向低温脱脂豆粕加入去离子水,调节其pH为8.0,室温搅拌2 h后10 000 g离心20 min。将上清液pH调至4.5进行酸沉,10 000 g离心10 min后的蛋白沉淀重新溶于去离子水中,调节pH至中性后进行透析和冻干。Dumas法测得SPI蛋白含量为[(85.79±0.70)%, N× 5.71]。
1.2.2 SPI纤维聚集的诱导
将冻干的蛋白分散于去离子水中(2%,m/V),室温搅拌2 h后,调节其pH至2.0,置于4 ℃水化过夜。蛋白溶液经过10 000 g离心20 min后,采用Lowry法测定上清液的蛋白含量,以BSA为标准蛋白。使用预调至pH 2.0的去离子水稀释蛋白浓度至1%。将蛋白样品置于带有密封盖的小瓶中,于85 ℃加热不同时间,定时取样,立即冷却到室温以终止蛋白纤维化。电镜图片证实,大豆蛋白在pH 2.0条件下加热诱导20 h后,形成了“蠕虫状”扭曲螺旋的蛋白纤维聚集体。
1.2.3 溶解度
将纤维化的蛋白溶液经过室温10 000 g离心20 min后,采用Lowry法测定上清液的蛋白含量,以BSA为标准蛋白制作标准曲线。
溶解度=上清液蛋白质质量/样品蛋白质质量×100%。
1.2.4 界面张力的测定
选择玉米油为油相,考虑到其含有少量表面活性成分可能影响测试,使用前对其纯化处理,具体参见Gaonkar[16]方法:向100 mL玉米油中加入3 g Florisil吸附剂,搅拌、静置和离心后,再加入新的吸附剂,重复操作,直至去离子水界面张力在30 min内不发生明显变化。纯化玉米油密度为0.915 6 g/cm3,去离子水的界面张力为(25.5±0.5) mN/m。
采用动态滴形分析法检测纤维化蛋白在O/W界面上的界面张力(σ)随吸附时间(θ)的变化,步骤参考Wang等[17]方法。将连接在毛细管上的不锈钢针(外径1.65 mm,内径1.19 mm)插入盛有油相的玻璃槽内。将蛋白溶液(1 mg/mL)置于注射器中,静置至样品温度平衡,由电动注射单元通过毛细管推入样液,在针尖上形成15 μL的液滴。在室温下,视频摄像系统立即连续采集液滴的外形图象,计算获得σ随θ的变化,采集时间持续 180 min。动态界面张力为表面压力(π) 随吸附时间的变化,π=σ0-σ,式中:σ为蛋白样品的表面张力;σ0为缓冲液的值,室温条件测得σ0=(25.5 ± 0.5) mN/m。
1.2.5 界面膜扩张流变性质的测定
采用动态滴形分析结合振荡滴技术,研究纤维化蛋白在O/W界面上的界面扩张模量(E)、界面扩张弹性模量(Ed)及界面扩张黏性模量(Ev)随吸附时间(θ)的变化,方法详见Wang 等[17]方法。将蛋白溶液(1 mg/mL)置于注射器中,注射形成10 μL液滴后,使用ODG振荡发生器对其施以周期性正弦振荡,液滴的表面积(A)发生扩张应变,从而引起σ的变化(扩张应力)。O/W界面形成1 min后开始收集σ,每个测量点是5个周期(50 s)内的平均值,测试在室温下进行,重复2次,其界面张力检测结果误差为±0.5 mN/m,相应地扩张模量检测结果误差为± 4 mN/m。液滴在适当的频率(f)和振幅(ΔA/A0)条件下正弦规律振荡,本试验f恒定为0.1 Hz,ΔA/A0为10%,处于线性黏弹性范围内,试验持续180 min。
线性黏弹性界面扩张模量(E, mN/m)是评定膜抗形变能力的参数,其绝对值是材料对弹性形变和黏性形变的总形变阻力,定义为界面张力(σ, mN/m)变化与界面面积(A, m2)相对变化的比值见式(1)。界面扩张模量由2个独立的部分组成,即弹性模量(Ed, mN/m)和黏性模量(Ev, mN/m),扩张模量可写作复数形式,见式(2)。
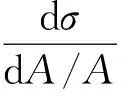
(1)
E=|E|cosθ+i|E|sinθ=Ed+iEv
(2)
1.2.6 乳液的制备及表征
将一定量不同加热时间的SPI纤维聚集体(pH 2.0)与玉米油混合,并加入0.02%(m/V) 叠氮钠抑制微生物生长。常温下,混合物经预乳化后 (5 000 r/min, 2 min)进行微射流处理二次(40 MPa),制备成蛋白含量为0.5 g/100 mL,含油量为10%(m/V)的乳液。将乳液pH调节至设定值(2.0、4.5和7.0)待测。
采用Mastersizer 2000 粒度分布仪测定乳液液滴的粒径。参数为:颗粒折射率:1.520;颗粒吸收率:0.001;分散剂:水;分散剂折射率:1.330。试验采用体积平均直径(d43)表征液滴粒度的大小。乳液的絮凝率(FD%)=(d43-d43SDS)/d43SDS×100[18],其中d43SDS为加入SDS所测得的d43。
2 结果与分析
2.1 蛋白纤维化过程中溶解度的变化
蛋白质溶解性与其乳化性质密切相关,溶解性较好样品一般具有较好的乳化性。明确酸性条件热处理蛋白的溶解情况将有助于其在食品加工中的合理利用,对SPI纤维化进程中溶解度的变化进行监测,结果见图1。随着加热时间的延长,在等电点附近 (pH 5.0) 的溶解度不断上升,而在中性(pH 6.0~8.0)范围内不断减小,特别是加热12 h,纤维聚集体在pH 8.0仍具有较低的溶解性。可以从蛋白质在酸性条件下发生水解和随之产生的蛋白纤维化聚集角度来理解此现象[14-15]。纤维化过程中部分发生聚集,部分以多肽形式存在,这导致了蛋白在等电点处溶解度的升高,随着水解的加剧,溶解度逐渐上升,而纤维聚集体这一刚性结构的形成则降低了溶解度。
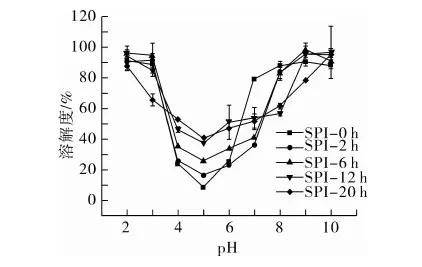
图1 SPI纤维化过程中溶解度的变化
2.2 界面吸附动力学
图2为SPI纤维聚集体在O/W界面上的表面压随时间的变化。整体来看,样品间差异较明显。天然SPI在吸附初期拥有最小的π值,随着吸附时间增加而逐渐上升,且上升速度慢慢趋于平缓,这表明蛋白不断在界面上完成吸附。在初始吸附阶段,纤维聚集体出现了较高的π值,且随着加热时间延长而逐渐升高,且吸附后期π值也不断升高。这说明,酸性条件下热处理使蛋白质的界面活性明显提高。从能垒角度考虑,这可能是由于伴随加热发生的蛋白水解使其结构处于去折叠状态,降低了蛋白在O/W界面上吸附的能垒,克服了因聚集体尺寸变大而带来的扩散速度减小,进而引起表面压的整体提高。另外,蛋白水解产生的小分子量多肽也可能促进了表面压的快速增加。Jung等[10]对β-乳球蛋白纤维聚集体的O/W界面吸附进行表征,发现酸热处理蛋白的高表面活性主要来自于加热过程中未转化成纤维聚集体的多肽。
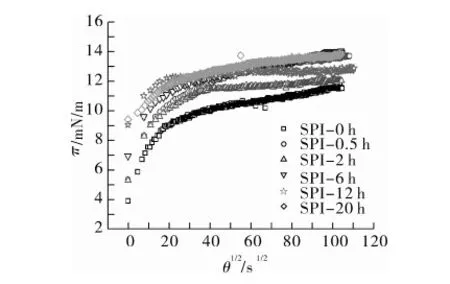
注:SPI-0h表示天然SPI,体相蛋白质量浓度1 mg/mL。
图2 SPI纤维聚集体在O/W界面随吸附时间变化(θ1/2)的表面压变化(π)
2.3 界面膜扩张黏弹特性
图3反映了不同时间加热诱导纤维聚集体的界面膨胀模量E随π值增加的变化情况,以反映界面上蛋白分子的结构特征和分子间相互作用。E-π曲线斜率的增加往往代表界面上吸附分子间相互作用的增强。由图3可知,随着蛋白不断吸附到O/W界面上(π值的增加),所有样品的E都不断增加,且扩张弹性模量(Ed) 明显大于黏性模量(Ev)(数据未列出),这说明蛋白质在界面上形成了黏弹性吸附膜,且蛋白分子间相互作用的存在和增强。纤维聚集体的形成明显地增加了E-π曲线的斜率,且随着加热时间的延长而上升,意味着SPI纤维的生长增强了界面上蛋白分子间的相互作用。另外,长时间加热诱导的纤维聚集体自身拥有更有序的结构,导致其流变学特性的增强,当它在O/W界面上吸附也就导致了其界面黏弹性的增加。

注:SPI-0h表示天然SPI,体相蛋白质量浓度1 mg/mL,测试频率为0.1 Hz,振幅为10%。
图3 SPI纤维聚集体在O/W界面上的扩张黏弹模量(E)随表面压 (π) 的变化
当加热时间延长到20 h后,出现明显不同的E-π曲线变化趋势。π值增加到16 mN/m时,E值达到最大,随着π值的持续增加,E值却逐渐下降。这可能是由于纤维聚集体在界面上发生的去折叠和随之而来的构象改变也许导致了蛋白聚集体固有刚性结构的破坏[19-20]。Freer等[19]曾研究了溶菌酶在十六烷/水界面上吸附膜的扩张流变特性,研究发现,在吸附初期,伴随着蛋白在界面发生部分去折叠和聚集而出现界面黏弹模量随π值增加而逐渐增加,经过长时间的吸附,蛋白质在界面形成了多层结构引起了界面黏弹模量的剧烈下降。以上所述现象与此结果一致,由此可推测,SPI纤维聚集体较为疏松的空间状态可能导致其在O/W界面上形成较厚的界面吸附层,纤维聚集体可能在界面上定向排列,导致多层界面结构的出现。
图4为纤维聚集体的界面吸附层膨胀弹性模量(Ed)随时间的变化情况。不同加热时间样品的Ed随时间变化明显不同。天然SPIEd值表现为逐渐增加的趋势,与其他球蛋白一致[21]。短时间加热没有改变Ed值变化趋势,长时间加热形成的纤维聚集体在吸附初期就表现了较高的Ed值,可能说明蛋白分子间快速发生相互作用。随着吸附时间延长,纤维聚集体Ed值迅速增加,这可能来自于纤维聚集体本身固有的有序刚性结构。有报道称,β-乳球蛋白纤维可以有效地稳定O/W界面,且认为蛋白纤维的稳定机制明显不同于天然蛋白,可以将蛋白纤维理解为具有表面活性的纳米胶体颗粒,这种颗粒的刚性结构可以使蛋白在界面吸附的过程中诱发二维结晶相的形成,进一步增强了界面稳定性[10-11]。

注:SPI-0h表示天然SPI,体相蛋白质量浓度1 mg/mL,测试频率为0.1 Hz,振幅为10%。
图4 SPI纤维聚集体的O/W界面吸附层的膨胀弹性模量随时间的变化
2.4 蛋白纤维聚集体的乳化性质
鉴于蛋白酸性热处理后具有较快的降低表面张力的能力,且蛋白在界面上形成的吸附膜具有较强的膨胀黏弹模量,这些特征都有利于蛋白对O/W界面的稳定。因此,本文尝试验证是否纤维聚集体的形成有利于其乳化性质的提高。图5为蛋白纤维聚集体稳定乳液的粒径分析。短时间加热会轻微减小蛋白乳液的粒径。遗憾的是,随着加热时间延长,尽管界面活性显著提高(图2),但纤维聚集体的形成使蛋白乳液粒径随加热时间延长而不断增加,未能改善其乳化性质。高压均质乳化时,由于大粒径分子具有较高的对流传质速度,均质产生的巨大湍流可促进蛋白聚集体在界面上的优先吸附。因此,纤维聚集体的空间位阻作用可能导致蛋白分子不能很好的覆盖油滴,阻止油滴的重新聚结,最终表现为较大的液滴粒径[22]。由此可知,可以通过控制蛋白的加热时间来调控纤维聚集体乳液的粒度。需要指出,所有乳液粒径都小于1 μm,可以认为纤维聚集体乳液仍是一个较为稳定的乳液体系。
图6为不同pH条件下乳液粒度和絮凝率的变化。所有乳液在pH 2.0时均有较小的粒度和絮凝率。调节乳液pH至4.5时,乳液粒径和絮凝率均明显增加,这可能是由于蛋白在等电点附近,其表面电荷减小导致液滴之间的静电排斥力减弱,发生絮凝。值得注意的是,纤维聚集体乳液的粒径和絮凝率明显小于天然SPI(0 h),且随加热时间延长呈现逐渐减小的趋势。这可能归因于蛋白在等电点处溶解度的提高(图1)。当乳液pH为7.0时,乳液粒度和絮凝率均明显下降。长时间加热诱导的纤维聚集体乳液较天然SPI乳液拥有更小的粒径和絮凝率,这说明纤维聚集体的形成明显抑制了蛋白乳液在中性条件下的絮凝,这一改善受加热时间强烈影响。值得注意的是,纤维聚集在pH 7.0溶解度小于天然SPI,因此溶解度可能不是乳液絮凝改善的直接原因,乳液界面结构也许与之相关。纤维聚集体增强的界面膜黏弹特性支持了以上推断(图3、图4)。

注:SPI-0h表示天然SPI。
图5 SPI纤维聚集体稳定乳液的液滴粒径大小(d43)
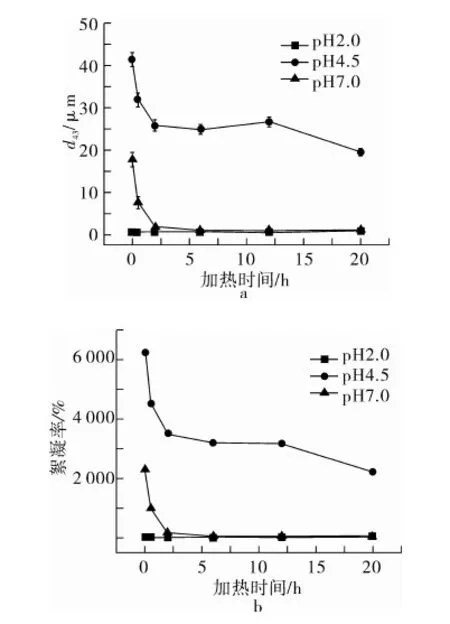
图6 pH对SPI纤维聚集体乳液粒度(d43)和絮凝率的影响
3 结论
SPI经酸性条件热处理后,等电点附近的溶解度明显改善,但中性pH处溶解度明显下降。蛋白的表面压增加速度和幅度随着热处理时间的延长明显增强,证实其拥有较高的界面活性。界面扩张特征参数变化证实,大豆蛋白纤维聚集体的Ed值及其增长速度明显高于天然SPI,且随加热时间的延长而不断提高,说明纤维聚集体的形成和生长增强了蛋白分子在界面上的相互作用,长时间吸附后,E值慢慢下降,易于形成多层界面结构。纤维聚集体的形成使蛋白乳液粒径随加热时间延长而不断增加,但其pH稳定性明显增强,明显抑制了蛋白乳液在中性条件下的絮凝,这一改善受加热时间强烈影响。以上理解将有利于拓展蛋白纤维聚集体在真实乳液食品体系中的应用。
[1]Lara C, Adamcik J, Jordens S, et al. General self-assembly mechanism converting hydrolyzed globular proteins into giant multistranded amyloid ribbons [J]. Biomacromolecules, 2011, 12 (5): 1868-1875
[2]Jones O G,Mezzenga R. Inhibiting, promoting, and preserving stability of functional protein fibrils [J]. Soft Matter, 2012, 8(4): 876-895
[3]Cherny I,Gazit E. Amyloids: not only pathological agents but also ordered nanomaterials [J]. Angewandte Chemie International Edition, 2008, 47 (22): 4062-4069
[4]Bakota E L, Aulisa L, Galler K M, et al.Enzymatic cross-linking of a nanofibrous peptide hydrogel [J]. Biomacromolecules, 2011, 12 (1): 82-87
[5]Jung J P, Gasiorowski J Z, Collier J H. Fibrillar peptide gels in biotechnology and biomedicine [J]. Biopolymers, 2010, 94(1): 49-59
[6]Van der Linden E. From peptides and proteins to micro-structure mechanics and rheological properties of fibril systems [J]. 2012, 26(2): 421-426
[7]Sagis L M C, Veerman C, Ganzevles R, et al. Mesoscopic structure and viscoelastic properties ofβ-lactoglobulin gels at low pH and low ionic strength [J]. Food Hydrocolloids, 2002, 16(3): 207-213
[8]Weijers M, Sagis L M C, Veerman C, et al. Rheology and structure of ovalbumin gels at low pH and low ionic strength [J]. Food Hydrocolloids, 2002, 16(3):269-276
[9]Zhang Y H, Tang C H, Wen Q B, et al. Thermal aggregation and gelation of kidney bean (Phaseolus vulgaris L.) protein isolate at pH 2.0: Influence of ionic strength [J]. Food Hydrocolloids, 2010, 24(4): 266-274
[10]Jung J M, Gunes D Z, Mezzenga R. Interfacial activity and interfacial shear rheology of nativeβ-lactoglobulin monomers and their heat-induced fibers [J]. Langmuir, 2010, 26(19): 15366-15375
[11]Isa L, Jung J M, Mezzenga R. Unravelling adsorption and alignment of amyloid fibrils at interfaces by probe particle tracking [J]. Soft Matter, 2011, 7(18): 8127-8134
[12]Rossier-Miranda F J, Schro⊇n K, Boom R. Mechanical characterization and pH response of fibril-reinforced microcapsules prepared by layer-by-layer adsorption [J]. Langmuir, 2010, 26(24): 19106-19113
[13]Humblet-Hua K N P, Scheltens G, van der Linden E, et al. Encapsulation systems based on ovalbumin fibrils and high methoxyl pectin [J]. Food Hydrocolloids, 2011, 25(4): 569-576
[14]Tang C H,Wang C S. Formation and characterization of amyloid fibrils from soy β-conglycinin and glycinin [J]. Journal of Agricultural and Food Chemistry, 2010, 58(20): 11058-11066
[15]Tang C H, Wang C S, Huang Q. Improvement of heat-induced fibril assembly of soy β-conglycinin (7S Globulins) at pH 2.0 through electrostatic screening [J]. Food Research International, 2012, 46(1): 229-236
[16]Gaonkar A G. Interfacial tensions of vegetable oil/water systems: Effect of oil purification [J]. Journal of the American Oil Chemists' Society, 1989, 66(8): 1090-1092
[17]Wang J M, Xia N, Yang X Q, et al. Adsorption and dilatational rheology of heat-treated soy protein at the oil-water interface: relationship to structural properties. Journal of Agricultural and Food Chemistry, 2012,60(12), 3302-3310
[18]Kim D A, Cornec M, Narsimhan G. Effect of thermal treatment on interfacial properties of β-lactoglobulin [J]. Journal of Colloid Interface Science, 2005, 285(1): 100-109
[19]Freer E M, Yim K S, Fuller G G, et al. Interfacial rheology of globular and flexible proteins at the hexadecane/water interface: comparison of shear and dilatation deformation [J]. Journal of Physical Chemistry B, 2004, 108(12): 3835-3844
[20]Freer E M, Yim K S, Fuller G G, et al. Shear and dilatational relaxation mechanisms of globular and flexible proteins at the hexadecane/water interface [J]. Langmuir, 2004, 20(23): 10159-10167
[21]Patino J M R, Nino M R R, Sanchez C C. Adsorption of whey protein isolate at the oil-water interface as a function of processing conditions: A rheokinetic study [J]. Journal of Agricultural and Food Chemistry, 1999, 47(6): 2241-2248
[22]Guilmineau F,Kulozik U. Impact of a thermal treatment on the emulsifying properties of egg yolk. Part 1: effect of the heating time [J]. Food Hydrocolloids, 2006, 20(8): 1105-1113.
Interfacial and Emulsifying Properties of Self-Assembly Fibrillar Aggregates from Soy Protein
Wang Jinmei Chen Yanqiong Wang Mengping Yang Xiaoquan
(Research and Development Center of Food Proteins, Department of Food Science and Technology,South China University of Technology, Guangzhou 510640)
Soy protein isolate (SPI) could convert to fibrillar aggregates with crossβ-sheet structure under self-assembly upon acidity heating treatment at pH 2.0. The influence of SPI fibrillation on the interfacial (adsorption at the oil-water interface and dilatational rheology of interfacial layers) and emulsifying properties of SPI was evaluated. The solubility of fibrillar aggregates at near isoelectric point was obviously improved due to polypeptide hydrolysis during the fibrillation of SPI, while the solubility was significantly decreased at neutral pH. During the fibrillation of SPI, higher interfacial activity was supported by the increase in the increase speed of protein surface pressure and Ed value, and interactions between protein molecules on the interface was enhanced,leading to the formation of the thicker multilayer structure. The formation of fibrillar aggregates maked protein emulsion particle diameter increased with the prolonging of heating time, but its pH stability was enhanced significantly, which significantly suppresses the flocculation under nuetural conditions, while such improvements were influenced by heating time.
soy protein, self-assembly, fibrillar aggregates, interfacial properties, emulsifying properties
TS201.1
A
1003-0174(2016)12-0033-06
国家自然科学基金(31301432, 31371744)
2015-05-12
王金梅,女,1982年出生,讲师,植物蛋白加工与利用
杨晓泉,男,1965 年出生,教授,植物蛋白加工与利用

