紫杉醇脂质体用于乳腺癌新辅助化疗的疗效与安全性
陈雪姣,周凤杰,赵伟锋,仓顺东#
(1.河南省人民医院肿瘤科,河南 郑州 450003; 2.锦州医科大学研究生院,辽宁 锦州 121000)
紫杉醇脂质体用于乳腺癌新辅助化疗的疗效与安全性
陈雪姣1*,周凤杰2,赵伟锋1,仓顺东1#
(1.河南省人民医院肿瘤科,河南 郑州 450003; 2.锦州医科大学研究生院,辽宁 锦州 121000)
目的:探讨紫杉醇脂质体用于乳腺癌新辅助化疗的疗效与安全性。方法:选取2013年3月—2015年2月河南省人民医院收治的行新辅助化疗与手术治疗的乳腺癌患者259例进行回顾性研究,根据治疗方法的不同,将患者分为A组118例、B组141例。A组患者采用紫杉醇脂质体联合表柔比星、环磷酰胺治疗,B组患者采用多西他赛联合表柔比星、环磷酰胺治疗。比较两组患者的临床疗效、2年生存情况与不良反应发生情况的差异。结果:A组患者的总有效率、疾病控制率分别为80.5%(95/118)、95.8%(113/118),B组分别为79.4%(112/141)、92.9%(131/141),两组的差异均无统计学意义(P>0.05)。两组患者2年生存率的差异无统计学意义(P=0.368)。A组患者Ⅲ—Ⅳ级中性粒细胞减少症、Ⅲ—Ⅳ级白细胞减少症、过敏反应、体液潴留、口腔黏膜炎、皮肤指甲毒性反应的发生率明显低于B组,差异均有统计学意义(P<0.05)。结论:紫杉醇脂质体用于乳腺癌新辅助化疗的疗效与多西他赛相当,但紫杉醇脂质体减少了溶剂降解引起的过敏反应,不良反应更少。
紫杉醇脂质体; 乳腺癌; 疗效; 不良反应
紫杉醇是乳腺癌和卵巢癌的化疗药,但其水溶性极低且来源有限,极大限制了其在临床上的应用[1]。且其采用聚氧乙基代蓖麻油作为溶剂,患者易发生不良反应。多西他赛的抗肿瘤活性显著优于紫杉醇,但其同样具有脂溶性小且难溶于水的缺点[2-3]。目前,多西他赛多采用乙醇和吐温80作为溶剂,易引发超敏反应、神经毒性等不良反应。脂质体是一种人工膜,可用于药物的制备,具有双分子层囊状结构。脂质体制剂具有特殊的药物缓释靶向性功能,可增加药物稳定性,减少毒性[4]。2003年,注射用紫杉醇脂质体在我国研制成功,本研究回顾性分析紫杉醇脂质体与多西他赛分别用于乳腺癌新辅助化疗的疗效,现报告如下。
1 资料与方法
1.1 资料来源
选取2013年3月—2015年2月河南省人民医院收治的行新辅助化疗与手术治疗的乳腺癌患者259例进行回顾性研究。纳入标准:(1)经病理诊断为原发浸润性乳腺癌的女性患者;(2)年龄≥18岁;(3)符合美国癌症联合委员会乳腺癌分期标准的Ⅱ—Ⅲ期,且未经过乳腺癌治疗;(4)无远处转移,无明显的内脏器官功能障碍。排除标准:(1)患自身免疫性疾病或其他疾病而长期服用免疫抑制剂或激素者;(2)严重神经或精神疾病者。根据治疗方法的不同,将患者分为A组118例、B组141例。A组患者中,年龄≥35岁108例;未绝经75例;美国东部肿瘤协作组评分:0分97例,1分21例;腋窝淋巴结阳性91例;临床分期:Ⅱ 期41例,Ⅲ 期77例;T2期49例,T3期53例,T4期16例;分子分型:Luminal A型37例,Luminal B型47例,原癌基因人类表皮生长因子受体2(HER-2)过表达型15例,三阴性乳腺癌19例。B组患者中,年龄≥35岁126例;未绝经88例;美国东部肿瘤协作组评分:0分115例,1分26例;腋窝淋巴结阳性108例;临床分期:Ⅱ 期39例,Ⅲ期102例;T2期47例,T3期69例,T4期25例;分子分型:Luminal A型41例,Luminal B型66例,HER-2过表达型12例,三阴性乳腺癌22例。两组患者基线资料的均衡性较高,具有可比性。
1.2 方法
A组患者给予注射用紫杉醇脂质体135~175 mg/m2、注射用盐酸表柔比星60 mg/m2、注射用异环磷酰胺500 mg/m2,21 d为1个治疗周期,共治疗6个周期。B组患者给予多西他赛注射液75 mg/m2、注射用盐酸表柔比星60 mg/m2、注射用异环磷酰胺500 mg/m2,21 d为1个治疗周期,共治疗6个周期。每个治疗周期结束后,对患者进行血常规检查,如出现Ⅲ度及以上骨髓抑制,则预防性给予口服抗菌药物或皮下注射粒细胞集落刺激因子。
1.3 观察指标与疗效评定标准
比较两组患者的临床疗效:完全缓解,患侧乳房无可触及肿块,腋窝无触及肿大淋巴结;部分缓解,肿瘤最大径之和减少≥30%;稳定,肿瘤最大径之和减少<30%或增加<20%;进展,肿瘤最大径之和增加≥20%或化疗后患侧乳房其他部位发现新病灶,或化疗前腋窝未触及肿大淋巴结而化疗后可触及肿大淋巴结。总有效率=(完全缓解病例数+部分缓解病例数)/总病例数×100%,疾病控制率=(完全缓解病例数+部分缓解病例数+稳定病例数)/总病例数×100%。比较两组患者2年生存情况。采用美国国家癌症研究所不良事件评定标准评价不良反应。
1.4 统计学方法
采用SPSS 20.0统计学软件分析数据,计数资料采用率(%)表示、进行χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 两组患者临床疗效比较
两组均无停药或减量的患者。两组患者总有效率、疾病控制率的差异均无统计学意义(P>0.05),见表1。

表1 两组患者临床疗效比较[例(%)]Tab 1 Comparison of clinical efficacy between two groups [cases(%)]
2.2 两组患者2年生存情况比较
经过2年的随访,A组患者2年生存率为76.3%(90/118),B组患者为71.6%(101/141),两组的差异无统计学意义(P=0.368)。
2.3 两组患者不良反应发生情况比较
A组患者Ⅲ—Ⅳ级中性粒细胞减少症、Ⅲ—Ⅳ级白细胞减少症、过敏反应、体液潴留、口腔黏膜炎、皮肤指甲毒性反应的发生率明显低于B组,差异均有统计学意义(P<0.05),而两组患者其他不良反应发生率的差异无统计学意义(P>0.05),见表2。
3 讨论
19世纪末,Halsted提出了乳腺癌根治术,对乳腺癌的治疗由手术切除发展为目前的全身性综合治疗,新辅助化疗是乳腺癌综合治疗的重要部分,为切除困难或不可切除的局部晚期乳腺癌患者带来了福音[5-6]。蒽环类及紫杉烷类药物是目前乳腺癌新辅助化疗的标准药物。大规模Ⅲ期临床研究结果显示,多西他赛+阿霉素+环磷酰胺(TAC)方案能降低乳腺癌患者的病死率和复发率[7]。美国国立综合癌症网络指南将TAC方案推荐为乳腺癌化疗与新辅助化疗的备选方案之一。紫杉烷类药物能抑制微管蛋白的解聚,促进聚合,保持微管蛋白的稳定,进一步抑制细胞的有丝分裂,达到抗肿瘤的目的[8-9]。但紫杉醇及紫杉醇的半合成衍生物多西他赛也有诸多缺点,如水溶性较差、溶剂会造成严重不良反应(包括过敏反应、神经毒性、骨髓抑制、心血管毒性、肠道反应等),限制了其的临床应用[10-11]。
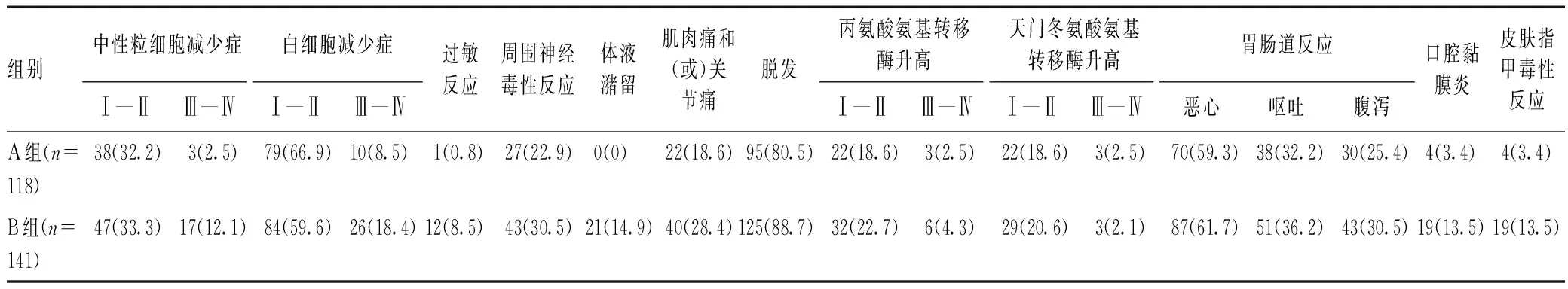
表2 两组患者不良反应发生情况比较[例(%)]Tab 2 Comparison of adverse drug reactions between two groups[cases(%)]
随着科学技术进步,紫杉醇脂质体剂型研发成功并迅速应用于临床。该药以载体卵磷脂包裹紫杉醇,增强了药物的稳定性,延长了药物在体内的平均滞留时间和半衰期,降低了溶剂的过敏反应和药物毒性[12]。相关药物毒副作用研究结果表明,传统紫杉醇的半数致死量为33.0 mg/kg,而紫杉醇脂质体为69.8 mg/kg[13-15]。多西他赛、紫杉醇注射液与紫杉醇脂质体治疗乳腺癌的疗效相当,但紫杉醇脂质体对患者心脏与骨髓的毒性更小,不良反应发生率明显更低。
本研究结果显示,两组患者总有效率、疾病控制率、2年生存率的差异均无统计学意义(P>0.05);A组患者Ⅲ—Ⅳ级中性粒细胞减少症、Ⅲ—Ⅳ级白细胞减少症、过敏反应、体液潴留、口腔黏膜炎、皮肤指甲毒性反应的发生率明显低于B组,差异均有统计学意义(P<0.05),提示紫杉醇脂质体的不良反应较少、程度较轻。
综上所述,紫杉醇脂质体用于乳腺癌新辅助化疗的疗效与多西他赛相当,但紫杉醇脂质体减少了溶剂降解引起的过敏反应,不良反应更少。
[1]杨振磊,张四喜,黄桂华.抗肿瘤药紫杉醇载体的研究进展[J].中国生化药物杂志,2015,35(9):183-185.
[2]净晓龙,陈建明.紫杉醇给药系统的研究进展[J].中国新药与临床杂志,2011,30(9):650-657.
[3]杨庄青,董凤萍,张杰,等.累计超大剂量紫杉醇脂质体维持治疗晚期乳腺癌一例[J].中国肿瘤临床与康复,2015,22(12):1525-1526.
[4]谢秋芬,赵侠,周颖,等.脂质体制剂的Ⅰ期临床药代动力学研究进展[J].临床药物治疗杂志,2014,12(4):18-22.
[5]Sousa MS,Peate M,Jarvis S,et al.A clinical guide to the management of genitourinary symptoms in breast cancer survivors on endocrine therapy[J].TherAdv Med Oncol,2017,9(4):269-285.
[6]张厚云,赵凌云.乳腺癌内分泌治疗研究进展[J].中国普通外科杂志,2014,23(5):1-6.
[7]Mackey JR,Martin M,Pienkowski T,et al.Adjuvant docetaxel,doxor-ubicin,and cyclophosphamide in node-positive breast cancer: 10-year follow-up of the phase 3 randomised BCIRG 001 trial[J].Lancet Oncol,2013,14(1):72-80.
[8]李伟,杨敏,张海燕.紫杉烷类药物与蒽环类药物用药顺序对乳腺癌患者近期疗效的影响[J].现代中西医结合杂志,2016,25(24):2699-2701.
[9]陈坤成,冯思良,刘克良.紫杉烷类抗肿瘤药物临床研究进展[J].国际药学研究杂志,2013,40(3):271-276.
[10]Berger MJ,Vargo C,Vincent M,etal.Stopping paclitaxel preme-dication after two doses in patients not experiencing a previous infu-sion hypersensitivity reaction[J].Support Care Cancer,2015,23(7):2019-2024.
[11]Ouchi A,Ouchi A,Asano M,et al.A patient with paclitaxel hype-rsensitivity treated with nab-paclitaxel[J].GanTo Kagaku Ryoho,2014,41(7):889-891.
[12]Ling L,Du Y,Ismail M,et al.Self-assembled liposomes of dual paclitaxel-phospholipid prodrug for anticancer therapy[J].Int J Pharm,2017,526(1-2):11-22.
[13]张兰,李彦辉,王彩霞,等.紫杉醇脂质体的制备及初步毒性、药效学研究[J].中国药学杂志,2013,48(6):446-449.
[14]白凤丽.康复护理对紫杉醇脂质体治疗乳腺癌患者生活质量及心理状态的影响[J].中国药业,2015,24(23):128-129.
[15]陈涵,王娟,张静.紫杉醇脂质体与多西紫杉醇对乳腺癌疗效及安全性临床观察[J].临床荟萃,2016,31(11):1206-1208.
Efficacy and Safety of Paclitaxel Liposome in Neoadjuvant Chemotherapy for Breast Cancer
CHEN Xuejiao1,ZHOU Fengjie2,ZHAO Weifeng1,CANG Shundong1
(1.Dept.of Oncology,People’s Hospital of Henan,Henan Zhengzhou 450003,China; 2.Graduate College,Jinzhou Medical University,Liaoning Jinzhou 121000,China)
OBJECTIVE:To probe into the efficacy and safety of paclitaxel liposome in neoadjuvant chemotherapy for breast cancer. METHODS:259 patients with breast cancer accepting neoadjuvant chemotherapy and operation admitted into People’s Hospital of Henan from Mar. 2013 to Feb. 2015 were selected to be divided into group A (118 cases) and group B (141 cases) via the different treatment methods,retrospective analysis was conducted on two groups. Patients in group A were treated with paclitaxel liposome combined with epirubicin and cyclophosphamide,while patients in group B
docetaxel combined with epirubicin and cyclophosphamide. Differences of clinical efficacy,2-year survival rate and incidence of adverse drug reactions of two groups were compared. RESULTS:The total effective rate,disease control rate of group A were respectively 80.5% (95/118) and 95.8% (113/118),and the data in group B were respectively 79.4%(112/141) and 92.9% (131/141),without any statistically significant difference between two groups(P>0.05). There was no statistical significance between two groups in the 2-year survival rate(P=0.368). The incidences of Ⅲ-Ⅳ grade of neutrophilic granulocytopenia,Ⅲ-Ⅳ grade of leukopenia,anaphylaxis,fluid overload,oral mucositis and toxic reaction of skin,hair and nails in group A were significantly lower than those in group B,with statistical significance difference(P<0.05). CONCLUSIONS:The efficacy of paclitaxel liposome is equivalent to docetaxel,yet paclitaxel liposome can reduce the allergic reactions caused by degradation of solvent and has fewer adverse drug reactions.
Paclitaxel liposome; Breast cancer; Efficacy; Adverse drug reactions
R979.1
A
1672-2124(2017)08-1058-03
DOI 10.14009/j.issn.1672-2124.2017.08.020
2017-05-16)
*主治医师。研究方向:恶性肿瘤的综合治疗。E-mail:chesjz@163.com
#通信作者:主任医师。研究方向:肺癌综合治疗。E-mail:luoshiyougz@163.com

