植物颜色“大师”
刘欣晔 蒋郸骥


摘要:紫薯是生活中的常见食材,从紫薯中提取的紫薯色素富含易溶于水的花青素,其颜色随溶液pH变化而变化;酸性Na2SO3水溶液能有效地使紫薯色素褪色,并且通过调节溶液的pH可以使该褪色过程“可逆”地进行;用紫外可见光谱比较系统地分析了紫薯色素在不同pH以及Na2SO3褪色前后分子结构的变化特征;据此,设计了有趣且有明显颜色变化的小实验,并将中学阶段涉及到的“酸碱指示剂”、“SO2的漂白作用”、“化学平衡移动”、“盐的水解”和“肥皂去污”等化学知识渗透其中,边玩边学,有效提升师生科学素养。
关键词:紫薯色素;花青素;pH指示剂;“可逆”褪色;“化学”密信
文章编号:1008-0546(2018)12-0082-04中图分类号:G633.8文献标识码:B
doi:10.3969/j.issn.1008-0546.2018.12.027
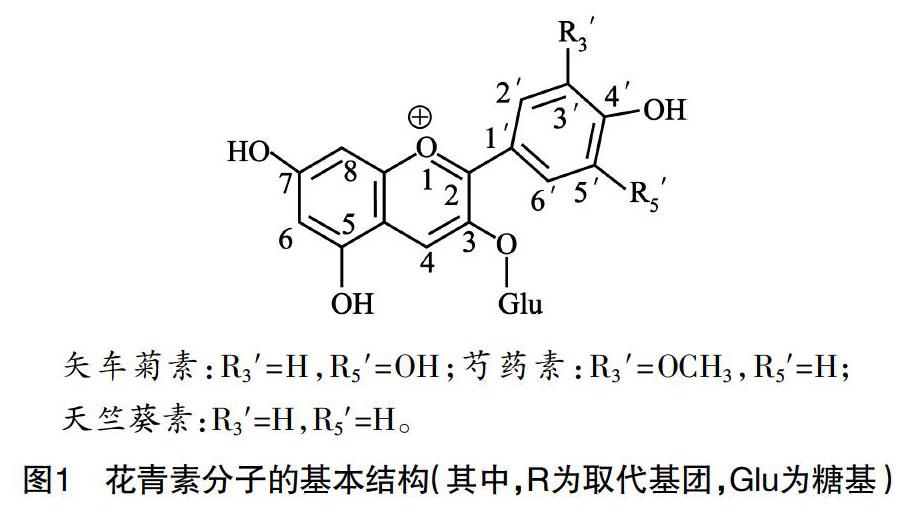
花青素是广泛存在于花朵和果实、能够赋予花朵和果实以丰富颜色的多种天然化合物的统称。从化学角度看,花青素属于类黄酮类物质,它们的分子结构中都具有图1所示的“C6-C3-C6三环”结构 [1,2]。自然界中的花青素超过300种,广泛分布于接骨木红、越橘、紫甘薯、蓝莓、葡萄、黑加仑、紫胡萝卜和紫甘蓝等果蔬中。植物中的花青素是混合物,种类各异和多种成份组合,从而表现出丰富的色彩,因此,花青素是自然界植物的颜色“大师”。紫薯花青素的主要成分是矢车菊素、芍药素及少量天竺葵素的3-O-糖基化合物。天然花青素大多在水和乙醇中具有良好的溶解性,尚没有发现其有明显的毒副作用,因此,作为天然色素被广泛应用于饮料、糖果、果酱等食品中 [3];有研究表明,花青素还具有良好的抗氧化性质,在生物体内,花青素具有抗自由基、抑制癌细胞等重要的生理活性和功能 [4]。
化学,是以实验为基础的自然科学。丰富有趣的化学实验,不仅有助于激发学生学习化学的兴趣,而且有助于学生练习和掌握化学实验操作技能,从而有效提升师生科学素养。基于紫薯花青素丰富的颜色变化,我们设计了一些有趣且伴有颜色变化的小实验,以帮助中学生学习和理解“酸碱指示剂”、“SO2的漂白作用”、“化学平衡移动”、“盐的水解”和“肥皂去污”等知识点 [5]。
一、实验设计
1.实验试剂与仪器
紫薯色素(食品级),湖北紫鑫生物科技有限公司;盐酸、NaOH、十四酸、CCl4、石油醚、Na2SO3和氨水,均为分析纯,国药集团化学试剂有限公司;TU-1950紫外可见分光光度计,北京普析通用仪器有限公司;ZF-7A紫外检测灯,上海宝山顾村电光仪器厂;PHS-3C雷磁pH计,上海仪电科学仪器有限公司。
2.实验方法
去离子水配制0.5%和1%紫甘薯色素溶液;分别用盐酸和NaOH配制pH为1~13的水溶液,各取5mL不同pH的水溶液,滴加0.5%紫薯色素溶液0.1mL并用pH计检测和调节溶液pH,观察颜色随pH的变化并测定紫外可见光谱;配制0.5%的Na2SO3水溶液并将其pH调为3;用棉签蘸取1%紫薯色素在滤纸上书写“化学”密信。
3.实验结果与讨论
(1)紫薯色素颜色的pH效应
早在1996年,紫甘蓝色素用作pH指示剂就有文献报导。在pH 6.8~7.8时,天然紫甘蓝色素由紫红变绿;在pH约7.5时,紫甘蓝色素呈蓝色,相当于一种混合pH指示剂 [6]。紫甘蓝色素属于花青素,而紫薯色素也属于花青素,因此,紫薯色素的颜色也应当随pH改变而改变。图2是不同pH紫薯色素水溶液的照片,可见在不同pH条件下,紫薯色素水溶液的颜色呈现多种色彩。pH为1~4时,紫薯色素溶液呈洋红色,pH为5~7洋红色逐渐变浅,pH为8~10变成淡紫蓝色,pH为11呈蓝色,pH为12时呈蓝黄色,pH为13时呈土黄色。可见,紫薯色素水溶液的颜色也表现出明显的pH效应。
物质分子结构决定其性质,反之,性质变化也反映出分子结构的改变。为此,我们测定了不同pH紫薯色素水溶液的紫外可见光谱(图3)。pH为1~10范围内,紫薯色素在290nm和320nm处有很强的吸收,结合530nm处的吸收峰,这是紫薯色素分子结构中具有花青素结构(图1)的特征吸收 [7],表明紫薯色素属于花青素;pH为11~13范围内,290nm和320nm处的两个吸收峰消失,但在380nm处出现新的较强吸收峰;在pH为1~13范围内,紫薯色素在200nm~350nm范围内的吸光度高于其在400nm~700nm范围内的吸光度,说明紫薯色素对紫外光有很好的吸收,具有抗紫外線的潜能。
可以用紫薯色素分子结构随pH改变而改变的示意图(图4) [8]分析图2和图3所观察到的结果。pH为1~3时,溶液中紫薯色素主要呈红色的黄烊盐AH+形态;随着pH增加,红色黄烊盐失去H+形成蓝紫色的醌碱A;随着pH进一步增大时,醌碱A进一步失去H+变成醌碱阴离子A-。所以,随着pH增加,紫薯色素溶液的颜色发生洋红色-淡洋红色-淡紫色-蓝色-蓝黄色-土黄色递次转变(图2)。
(2)紫薯色素的水溶性及其用作pH指示剂
基于紫薯色素水溶液的颜色随pH改变呈现丰富的颜色变化,我们设计了两个小实验用以验证“紫薯色素水溶性及其用作pH指示剂”的性质。
①实验一
在一个容积为15mL的玻璃瓶中,加入等体积(3mL)的CCl4、水和石油醚,再加入少量紫薯色素,混合均匀后观察到如图5A所示状态。CCl4、水和石油醚彼此间互不相溶,再根据三者的密度(ρ)可知,ρ(CCl4)>ρ(水)>ρ(石油醚),不难判断图5A中,最下层液体为CCl4,中间层液体为水,最上层液体为石油醚;再根据图5A中三层液体只有中间层为紫红色,由此判明,紫薯色素是水溶性的,不能在CCl4和/或石油醚中溶解。向图5A中滴加稀盐酸溶液,可观察到盐酸液滴通过上层石油醚溶入中间水层,且中间层颜色变成鲜艳的洋红色(图5B);若向图5A中滴加稀NaOH溶液,可观察到NaOH液滴通过上层石油醚溶入中间水层,且中间层颜色变成鲜艳的蓝色(图5C);若向图5A中交替滴加稀盐酸和稀NaOH溶液,可观察到中间层的颜色在红色和蓝色之间交替变换。
②实验二
在苏教版普通高中课程标准实验教科书化学2专题3的第二单元中,介绍了肥皂的去污作用。肥皂中起去污作用的主要成分是长链脂肪酸钠,比如十四酸钠,它是弱的有机脂肪酸十四酸与强碱NaOH中和反应得到的有机酸盐、属于强碱弱酸盐。而强碱弱酸盐在水溶液中会因为部分水解反应使溶液的pH>7。
向浓度为1%的十四酸钠水溶液中滴加几滴紫薯色素水溶液,可以观察到十四酸钠水溶液呈蓝色(图6 A1,A2为未滴加色素的十四酸钠水溶液),可见,十四酸钠水溶液呈碱性。十四酸钠是一种阴离子型表面活性剂,除了有去污作用,也有良好的泡沫性质,简单振摇十四酸钠水溶液,可以觀察到明显的泡沫(图6 A1);向十四酸钠溶液中滴加盐酸至溶液呈红色(图6 B1,B2为未滴加色素的十四酸钠水溶液),此时溶液显酸性,图6B中观察到有白色不溶物出现,该白色不溶物为十四酸;加入盐酸,使十四酸钠水溶液中的水解反应向生成十四酸的方向进行(该过程也可以理解为强酸生成弱酸),而十四酸是难溶于水的物质,所以出现白色不溶物;此时,振摇溶液,观察不到有泡沫产生;向十四酸钠溶液中交替加入盐酸和NaOH,可观察到溶液分别呈现红色和蓝色、无泡沫(有不溶物)和有泡沫的现象。
(3)Na2SO3对紫薯色素的可逆褪色作用
在苏教版普通高中课程标准实验教科书化学1专题4的第一单元中提到:“实验证明,SO2能漂白某些有色物质(如品红),这是由于它能与某些有色物质反应,生成不稳定的无色物质。”实际上,紫薯色素也有类似的效果。在SO2漂白品红的过程中,SO2先与水结合形成H2SO3,H2SO3进而与品红反应。因此,本文实验中用酸性Na2SO3水溶液代替“向水溶液中通入SO2”,避免制取有刺激性和毒副作用的SO2气体。
由图7A可见,在pH=3时加入Na2SO3后,原先红色的紫薯色素溶液(图7 A1)明显褪色(图7 A2),原本在530nm处的吸收明显减弱,并且在可见光区的最大吸收波长有明显红移,说明经过酸性Na2SO3作用后,紫薯色素在可见光区的吸收减弱导致其褪色。图7B是花青素与NaHSO3反应过程中分子结构变化的示意图,花青素分子中含氧杂环的3,4-双键与NaHSO3反应,4-C接入磺酸基(SO3H) [9],导致含氧杂环原有的共轭双键改变,所以紫薯色素的光谱吸收性质发生图7A所示的改变。此外,图7B中示意的花青素与NaHSO3反应,其反应进行的方向容易随反应体系的pH改变而改变;若是pH进一步降低,该反应过程向反方向进行,即已经褪色的紫薯色素又可以逐步恢复其红颜色;反之,pH再次升高,红色的紫薯色素又将再次褪色(图7C)。因此,Na2SO3对紫薯色素的颜色具有“可逆”的褪色作用。
(4)基于紫薯色素-NaHSO3“可逆”褪色作用制作“化学密信”
利用酚酞遇碱变色的原理,可以制作化学密信 [10]。基于图7中所得实验结果,利用NaHSO3对紫薯色素的“可逆”褪色作用,我们也可以制作“化学密信”,所得“化学密信”的显色过程见图8。配制紫薯色素溶液,并将其pH调为3,用棉签蘸取色素溶液在滤纸片上书写“化学”(图8A),向图8A纸片上喷洒pH=3的Na2SO3溶液,几分钟后,纸片上紫红色字迹褪去(图8B);由图7B可知,这是由于酸性Na2SO3与色素反应形成无色加合物的结果。将图8B无色纸片置于浓盐酸瓶口约10秒钟,纸片上的字迹重新显现且呈红色(图8C),这是由于浓盐酸瓶口会有盐酸酸雾逸出,酸雾与图8B纸片接触,相当于在图8B纸片上喷洒盐酸,依据图7B不难理解,在盐酸作用下,紫薯色素与酸性Na2SO3反应形成的无色加合物重新转变为红色的紫薯色素。将图8C纸片放置在浓氨水瓶口,红色字迹慢慢褪去,约20秒钟后字迹全无(图8D),这是由于浓氨水瓶口有氨气逸出,遇到图8C酸性纸片,发生酸碱中和反应,图8C表面过量的盐酸会逐步被中和,在酸性Na2SO3的作用下,红色紫薯色素逐渐褪色(图7C)。此外,从图3和图7紫外可见光谱可知,无论是pH改变还是Na2SO3褪色,紫薯色素在紫外区的吸收没有显著减弱,因此,将图8B纸片放置于紫外灯下,已经因Na2SO3褪色而隐藏的字迹又清晰可见(图8E)。由此可见,用紫薯色素制作的“化学”密信,可以用多种手段解密。
二、结论
水溶性紫薯色素可以方便地溶于水中形成溶液,其颜色随着溶液pH的变化而变化,可作为酸碱指示剂用于中学化学实验教学;与典型花青素物质类似, 酸性Na2SO3水溶液可以有效地使紫薯色素褪色,并且通过调节溶液的pH可以使褪色过程“可逆”进行,据此性质,可以用作 “化学”密信制作等趣味实验;本文基于紫薯色素设计的小实验,实验现象比较明显,可以用作学生课外兴趣实验和教师课堂演示实验。可见,化学联系生活,学科素养基于实验创新。世界上不是缺少美,而是缺少发现的眼睛。
参考文献
[1] J. M. Bueno, F. Ramos-Escudero, P. Sáez-Plaza, A. M. Muńoz, M. J. Navas, A. G. Asuero. Analysis and antioxidant capacity of anthocyanin pigments Part I [J]. Critical Reviews in Analytical Chemistry, 2012, 42:102-125
[2][8] J. M. Bueno, P. Sáez-Plaza, F. Ramos-Escudero, A. M. Jiménez, R. Fett, A. G. Asuero. Analysis and antioxidant capacity of anthocyanin pigments Part II [J]. Critical Reviews in Analytical Chemistry, 2012, 42:126-151
[3] 孙鹏尧,周芳宁,李喜层,曹燕华,袁素辉,牟德华.紫甘薯饮料中花青素的稳定性研究[J].食品工程,2014,3:28-32
[4] 罗春丽,王林,李杏,张子程,张久亮.紫薯花青素体外抗氧化及对H2O2诱导HepG2细胞氧化损伤的保护作用[J].食品科学,2015,36(17):225-230
[5] 王祖浩主编.普通高中课程标准实验教科书·化学(必修,选修)[M].南京:江苏教育出版社,2007
[6] 卢玉振,袁勋模.一种天然指示剂——紫甘蓝色素[J].贵州科学,1996,14(3):53-57
[7] 周培剑.紫甘蓝和紫甘薯色素提取及酸碱指示真丝织物的制备[D].杭州:浙江理工大学,2012
[9] 毛建霏,付成平,郭灵安,仲伶俐,雷绍荣.可见分光光度法测定紫甘薯总花青素含量[J].食品与发酵科技,2010,46(2):101-104
[10] 窦星星,刘雄,王秋月,等.化学密信送情报[J].中学化学教学参考,2016,4:65-66

