沸腾氯化生产TiCl4工艺分析及氯化废料的综合利用
田 键,张 祥,黄季宇,朱艳超,黄红旗
(1.湖北大学,湖北 武汉 430062)(2.湖北大学天沭新能源材料工业研究设计院,湖北 武汉 430062)
0 引 言
TiCl4是生产金属钛及其化合物的重要中间体,是生产海绵钛和氯化法钛白的主要原料,也是乙烯聚合催化剂的重要组分,同时可作为溶解合成树脂、橡胶、塑料等多种有机物的良好溶剂[1]。TiCl4生产过程主要由配料、氯化与精制3部分构成,其中氯化工段根据氯化方式的不同,又分为沸腾氯化、熔盐氯化和竖炉氯化3种[2]。目前,竖炉氯化已被淘汰,熔盐氯化工艺落后于沸腾氯化工艺,但由于沸腾氯化不能有效处理含高钙镁(CaO+MgO质量分数大于3%)的原料,使得部分企业还在采用熔盐氯化工艺。
沸腾氯化工艺因具有气-固相之间传质传热条件好、炉型结构简单、“自热”方式生产、氯渣可回收利用等优点,被世界上多数海绵钛生产企业所采用[3]。但是,TiCl4生产过程中,会产生大量的氯化废料。由于这些氯化废料产量大、组分复杂、性质难界定等,一直以来如何对其进行安全可靠的处理都是探讨的热点[4]。
此外,随着工业化进程的加剧,若不能系统解决氯化废料的处理与利用问题,势必会导致大量废渣堆积。一方面,经露天风干陈化产生扬尘会污染大气环境;另一方面,经雨水溶出有害物渗流进地下水会污染水资源。
本研究则从TiCl4生产工艺流程入手,根据各过程的反应机理,以及影响沸腾氯化效果的因素,列出其中所产生的氯化废料,再针对各种氯化废料的特点,制定出综合处理利用的方法,以期能够最大限度的发挥原料潜能,提高原料利用率,降低三废排放,减少环境污染。
1 沸腾氯化工艺分析
1.1 反应机理
沸腾氯化工艺制取粗TiCl4的基本原理是把富钛料与石油焦按一定比例配制成混合料,加入沸腾炉内与氯气在沸腾状态下进行氯化反应[5],主要反应式如下:

(1)

(2)

(3)
由于富钛料的氯化反应为放热反应,故当达到反应的起始温度后,靠氯化放出的热量可使富钛料的氯化反应一直持续进行[6]。根据热力学计算,反应(1)式和(2)式在1 000 K时的热效应分别为214.64 kJ和46.44 kJ。当氯化温度低于980 K时,反应主要按(1)式和(3)式进行,生成CO2;高于980 K时,反应主要按(2)式进行,生成CO。具体工艺流程如图1所示。
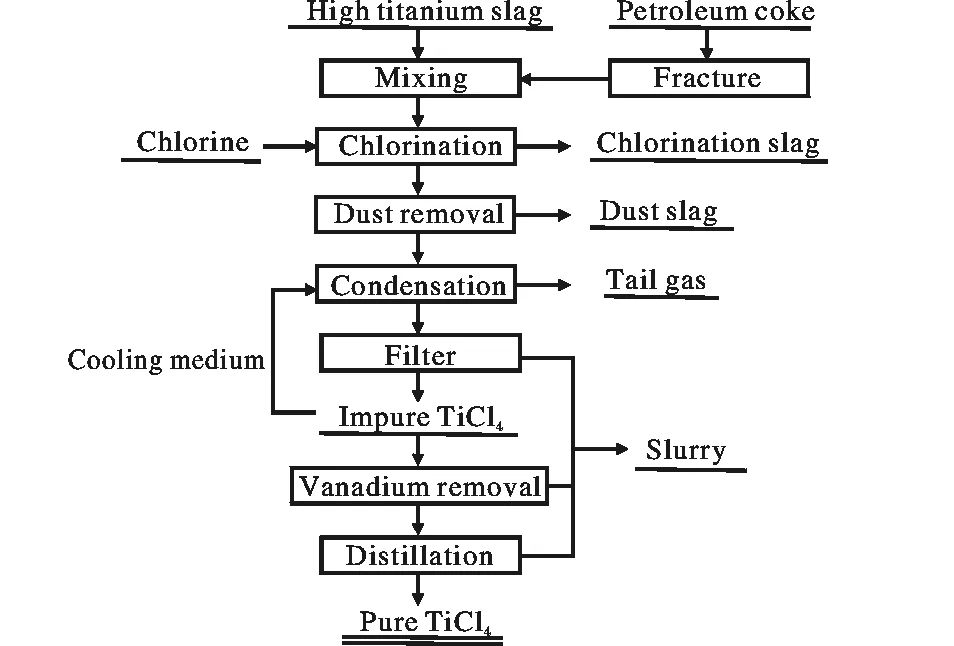
图1 沸腾氯化生产TiCl4工艺流程图Fig.1 Process flow diagram of producing titanium tetrachloride by fluidized bed chlorination
1.2 影响因素
1.2.1 富钛料种类
天然金红石、人造金红石和高钛渣是生产TiCl4的常用原料。天然金红石纯度高(一般TiO2含量在95%以上)、沸腾氯化效果好,是生产TiCl4的最优原料,但由于其在地壳中储量较少,且不同地区储量差异较大,因此更多的是使用人造金红石或高钛渣制备TiCl4。对于同等品位的人造金红石和高钛渣,人造金红石的价格较高,所以工业中大多采用高钛渣。高钛渣品位的高低直接关系到产品的产量和质量,以及沸腾氯化生产是否能够正常进行。从理论上讲,高钛渣品位越高,沸腾氯化反应的效果越好,产品产量越高[7]。表1为不同品位高钛渣的成分标准。

表1 不同品位高钛渣的成分标准(w/%)Table 1 Standard of high titanium slag constituent
1.2.2 原料粒度分布
富钛料密度一般在3.5~4.2 g/cm3之间,而石油焦密度一般在1.2~1.5 g/cm3之间。为了使高钛渣和石油焦在流化床中保持良好的流化状态,在同一气流速度下获得相近的速度,流化时不至于分层,必须对2种物料粒度分布进行调整,使其与平均粒径的固体颗粒质量相近[8-9]。假设固体颗粒为球形,则理论计算公式如下:
(4)
设ρ高钛渣=3.9 g/cm3,ρ石油焦=1.3 g/cm3,计算可得d石油焦∶d高钛渣≈1.44,即石油焦与高钛渣的理论粒径比为1.44。但实际生产过程中,高钛渣和石油焦颗粒均为非规则形状,生产实践表明,最好使用颗粒粒径较大(0.15~0.4 mm)且分布窄的富钛料,这样可使工艺的可控操作范围加大。
1.2.3 钙镁含量
钛矿反应产生的金属氯化物中CaCl2和MgCl2具有很高的沸点,能在床层中积累[10]。在加碳高温氯化过程中,CaO、MgO几乎可以完全氯化,不可避免的会生成较多的CaCl2、MgCl2。对于熔沸点较高的CaCl2、MgCl2(CaCl2的熔沸点分别为772、1 935 ℃,MgCl2的熔沸点分别为714、1 412 ℃)来说,其在氯化炉中是以熔融态形式存在的。当粘稠物达到一定浓度后,会导致流化床黏度急剧增加,床层压降增大,正常沸腾被破坏,直至死炉[11]。所以要求钛渣中CaO和MgO的总含量不得超过1.5%;CaO、MgO和MnO2的总含量不得超过3%。
1.2.4 配碳比
由(1)、(2)、(3)式可知,氯化反应进行时会产生CO和CO2,因此,考虑2种极端情况,根据理论计算可得:假设无CO生成,或者生成的CO全部参与(3)式反应,按(1)式计算,配碳比为100 ∶ 15; 假设无CO2生成,按(2)式计算,配碳比为100 ∶ 30。因此,理论配碳比在100 ∶ (15~30)之间。
但是,实际生产过程中配碳比一般为理论值的105%~110%。当含碳量不足时,会使高钛渣反应不完全,一部分进入炉渣中造成原料的浪费;当含碳量严重过剩时,过多的碳会影响扩散过程,降低氯化率,不但造成浪费,还会加快床压增长速度,增大扒渣频率,降低产能[8]。而稍过量的碳不仅能起到稀释CaCl2、MgCl2浓度的作用,还可以通过包裹CaCl2、MgCl2颗粒,阻止其相互粘连成团[9]。
1.2.5 氯气的浓度和流速
氯化反应速率随氯气分压提高而增加,提高氯气浓度和加大氯气流速有利于增加炉内氯气分压,进而可提高氯化速率[12]。实际生产中,氯气流速和浓度与氯化率成正态分布关系,在一定范围内,氯化率随氯气浓度和流速的增大而增大,当达到最大氯化率时,再增大氯气浓度和流速反而会降低氯化率。
2 氯化废料综合利用
2.1 废料来源及成分
不同的原料、配碳比、氯化工艺等,均会导致氯化废料各组分含量的差异,但废料类型基本相同[13-14]。这些废料中都含有相当部分的TiCl4,处理时应尽可能的回收利用。由图1可以看出,氯化废料的主要来源包括:①从沸腾氯化炉底排放的氯化废渣,主要成分是未反应的石油焦以及一定含量的TiO2,其次是Ca、Fe、Mg等金属氯化物;②收尘冷却器排放的收尘渣,主要成分是高沸点的金属氯化物,例如FeCl3、FeCl2、MgCl2、CaCl2、AlCl3、MnCl2等,以及少量的TiCl4;③从氯化炉逸出的炉气经收尘、淋洗、冷凝后的尾气,主成分为CO、CO2、O2、N2、HCl、Cl2、COCl2;④在过滤、除钒和蒸馏过程中形成的泥浆,含有大量的TiCl4和一些收尘器未能收集到的高沸点氯化物,例如FeCl3、AlOCl、VOCl2等。
2.2 废料综合利用
2.2.1 氯化炉渣的处理
为保证沸腾氯化炉内良好的流态化状态,当炉内料层较厚、阻力较大时,必须排炉渣。目前,处理氯化炉渣的方法主要有固化填埋和深井灌注2种,但这2种方法不仅会造成原料的浪费,增加处理成本,而且如果处理不当,会导致地下水污染,进而危害人身健康。
φ1 200 mm沸腾氯化炉正常生产时每天产生的炉渣量约为1.5~1.8 t。炉渣中的主要成分为未反应的金红石和固定碳,正常情况下,炉渣TiO2含量应小于10%,炉况不正常时,TiO2含量可达25%左右,甚至更高,固定碳含量则为45%~50%。因此,氯化炉渣有较大的潜在利用价值空间,可通过调控氯化工艺参数,将此部分废渣重新返回氯化炉回收利用[15]。
根据金红石和碳密度的差异,可采用重选选矿法将二者分离,并洗去炉渣中的可溶性氯化物。结合不同的重选方法及反应后的废料组成、粒径分布和回收效益等,工业生产中可使用摇床进行分选。在摇床往复运动和水流的作用下,达到分选的要求,然后将分选后的物料干燥脱水,重新返回氯化炉。如果选出的金红石中TiO2含量达到89%以上,亦可作为电焊条药皮敷料出售。
综合考虑炉渣中TiO2与碳的含量及回收利用率,预计每日可回收TiO2140~160 kg,石油焦650~750 kg左右。
2.2.2 收尘渣的处理
TiCl4制备过程中,随着CO、CO2、N2等气体的排出,会产生一定量的收尘渣,其化学成分复杂,并且Fe、Al、Mn的氯化物含量较高。收尘渣表面还覆有少量TiCl4,在空气中易潮解放热,遇大量水会溶解形成酸性水溶液,并放出有刺鼻性气味且有毒的腐蚀性烟气[16-18]。具体反应如下:

(5)
若收尘渣处置不当,随意堆放,将会直接对环境造成一次污染,遇到雨水淋洗时还会对土壤及地下水造成二次污染。
由于收尘渣的成分主要以金属氯化物为主,虽然金属可回收利用,但排放后的氯离子始终不会消失,如果只进行简单的水洗,会造成淋洗液中氯离子浓度不符合国家排放标准。因此,可先将氯化收尘渣加水制成泥浆,收尘渣表面的TiCl4与H2O反应生成HCl气体,将其用水吸收制备盐酸,之后再将泥浆送入尾气燃烧炉,加热至500~550 ℃使其高温水解,残渣则为Fe、Mn、Al等不溶于水的金属氧化物,可用作炼铁原料,Ca、Mg氯化物仍留在处理后的余渣中[19]。
此外,由于收尘渣中含有Ca、Fe、Al等氯化物,可提供硅酸盐矿物胶凝材料所需成分,还可先用石灰水冲洗收尘渣,以反应掉其表面的TiCl4,并调节pH至弱碱性,再经压滤机压滤得到滤饼,滤饼可用作生产水泥或建筑砖制品的原料。
2.2.3 尾气的处理
氯化炉尾气中需要首先处理的可回收物为Cl2和HCl,其中HCl含量较高,必须加以回收。如果不对HCl进行回收,只经水洗后直接排入酸性废水中和池,中和难度过大。因此,可通过多级稀酸淋洗后再经碱液中和处理废液[20]。
具体处理方法为:将尾气引入循环水洗涤吸收塔,为提高吸收率,可配合使用稀酸淋洗。由于水在吸收HCl气体时,是放热反应,致使循环淋洗液的温度达到60~70 ℃,严重影响循环淋洗液的吸收效果,故而可采用石墨冷却器冷却降温。经该方法处理后,盐酸浓度可富集到31%~33%。具体工艺流程见图2。
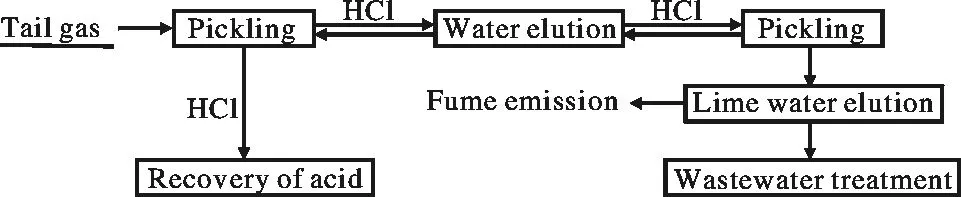
图2 尾气处理工艺流程图Fig.2 Process flow diagram of exhaust gas treatment
HCl气体被逐级吸收,富集为盐酸,当浓度达27%~31%时,可输送到盐酸储罐自用或出售。未被洗涤除去的CO、CO2、O2、N2等气体,经尾气调节阀调节风量用空气稀释后经风机排空。根据物料平衡计算,φ1 200 mm沸腾氯化炉每小时可回收浓度31%的盐酸150~180 kg。
2.2.4 泥浆的处理
由(4)式可知,经冷凝、沉降、过滤产生的含TiCl4泥浆,TiCl4最终可溶解于反应生成的稀HCl中,因此具有很高的回收价值。理论上讲,处理泥浆的最好方法是将泥浆返回氯化炉,使TiCl4蒸发回收[21-22]。但实际生产中,沉淀泥浆返回氯化炉会导致炉况不稳定,操作不易控制,无法正常作业,所以不能轻易将泥浆加入氯化炉,特别是在大规模工业生产中。由于TiCl4沸点较低,为136.4 ℃,故可采用熔盐蒸馏法对泥浆中的TiCl4进行回收,这种技术回收率高,经济效益好,且清洁环保[23]。
具体的处理方法为:沉淀泥浆由浓密机绞龙进入转运罐中,加入一定量的熔盐络合物(NaCl-AlCl3)后,搅拌放入液固分离器中分离得到上清液和泥渣。沉淀泥浆经过2次逆流溶出后,溶出渣放入泥渣蒸发器中,蒸发回收其中残留的溶剂;低浓度溶出剂经提取液储槽和提取液高位槽返回下一次溶出,高浓度提取液经提取液储槽和提取液高位槽进入反应釜中,经过蒸馏分离得到提取液和粗TiCl4产品;提取液返回提取液贮槽,粗TiCl4则收集在TiCl4贮槽中,溶剂可采用冷凝法回收重复利用[23-24]。最后的蒸馏残渣,可以经过干燥后和收尘渣一同进行处理。
利用该方法可使TiCl4回收率达到95%以上。经计算,1 t TiCl4沉淀泥浆可回收粗TiCl4400 kg左右。
3 结 论
(1)TiCl4生产过程中,应综合考虑各种工艺影响因素,根据生产情况,合理选择原料及配比,最大限度的减少排渣量,提高氯化率。
(2)氯化炉渣中含有未反应的TiO2,可采用摇床水洗重选的方法分离出TiO2,使其回炉二次反应;泥浆中含有反应生成的TiCl4,可采用熔盐蒸馏法富集粗TiCl4产品。对含Ti料的回收利用,可节约企业生产成本,且减少环境污染。
(3)收尘渣中含有Ca、Fe、Al、Mg等金属的离子,可经水洗煅烧后用作炼铁原料,亦可通过碱洗压滤制备水泥或建筑砖等。
(4)氯化尾气具有较高的回收价值,可采用多级弱酸淋洗的方法对其回收。φ1 200 mm沸腾氯化炉每小时可回收浓度31%的盐酸150~180 kg。
[1] 刘立文. 四氯化钛生产工艺探讨[J]. 无机盐工业, 2013, 45(2):36-38.
[2] 顾荣良. 四氯化钛的生产和市场研究[J]. 上海化工, 2008, 33(1):35-38.
[3] 陈辉. 沸腾氯化生产四氯化钛工艺技术[J]. 现代机械, 2010(5):68-70.
[4] 赵海涛. 沸腾氯化法四氯化钛生产中固体废物的综合利用[J]. 有色金属工程, 2015, 5(1):94-96.
[5] 傅崇说. 有色冶金原理[M]. 2版. 北京: 冶金工业出版社, 1987.
[6] 王亚锋, 李俊峰, 于振才. 沸腾氯化生产四氯化钛的热平衡分析[J]. 河南科学, 2016, 34(1):20-24.
[7] 商黔丽, 田建强. 不同品位高钛渣对沸腾氯化工艺的影响[J]. 钛工业进展, 2007, 25(3):26-28.
[8] 王岷, 邢生智. 沸腾氯化工艺影响因素及改进措施[C]. 第22届全国铁合金学术研讨会论文集. 吉林:中国金属学会铁合金分会,2013.
[9] 王亚锋, 李俊峰, 张兵兵,等. 高钛渣沸腾氯化制备四氯化钛工艺研究[J]. 河南科技, 2014(2):36-37.
[10] 熊雪良, 杨智, 欧阳红勇,等. 沸腾氯化用高品质金红石的生产工艺[J]. 中国有色金属学报, 2010, 20(专辑1):981-985.
[11] 胡元金. 沸腾氯化原料特性分析[J]. 四川冶金, 2014, 36(2):45-47.
[12] 邓国珠. 钛冶金[M]. 北京: 冶金工业出版社, 2010.
[13] 朱辉. 沸腾氯化渣无害化处理试验研究[J]. 山东化工, 2015, 44(20):154-156.
[14] 李建军, 刘建良, 史勤恺. 氯化法钛白粉工业化生产三废处理与利用[J]. 云南冶金, 2013, 42(2):59-63.
[15] 马海青, 张素超. 四氯化钛生产过程中废渣处理工艺研究[J]. 金川科技, 2014(4):6-8.
[16] 姚泉. 氯化收尘渣无害化处理的研究[D]. 沈阳:东北大学, 2013.
[17] 金芳荣, 李卫红, 尚东,等. 四氯化钛生产工艺中的新型尾气处理装置[J]. 工业安全与环保, 2014(12):75-76.
[18] Wang T H, Navarretelópez A M, Li S, et al. Hydrolysis of TiCl4:initial steps in the production of TiO2[J]. Journal of Physical Chemistry A, 2010, 114(28):7561-7570.
[19] 张兵兵, 李俊峰, 张鹤,等. 四氯化钛生产中氯化收尘渣资源利用及无害化处理[J]. 河南科技, 2015(11):110-112.
[20] Turnbaugh D T, Morris A J, Perkins J B. Method for the analysis of gas produced by a titanium tetrachloride fluidized bed reactor:US7183114 B2[P]. 2007.
[21] Shon H K, Vigneswaran S, Kim I S, et al. Preparation of titanium dioxide(TiO2) from sludge produced by titanium tetrachloride(TiCl4) flocculation of wastewater[J]. Environmental Science & Technology,2007,41(4):1372-1377.
[22] 王鹃. 海绵钛冶炼过程中从泥浆回收四氯化钛的方法研究与应用[J]. 有色冶金节能, 2015, 31(5):35-38.
[23] 向小艳, 王学文, 王明玉,等. 熔盐蒸馏法回收粗四氯化钛沉淀泥浆中的TiCl4[J]. 稀有金属, 2016, 40(1):57-63.
[24] 任惠锋. 熔盐法处理四氯化钛沉淀泥浆工艺研究[D]. 天津:天津大学, 2014.

