三氧化二砷脂质体的制备及银盐法含药量测定△
刘春秀,王存杨,张斯杰,马佳,王绍宁*
(1.沈阳药科大学 药学院,辽宁 沈阳 110016;2.沈阳药科大学 制药工程学院,辽宁 沈阳 110016;3.中国中药有限公司,北京 102600)
中药砷剂有剧毒,《本草纲目》指出:“砒乃大热大毒之药,而砒霜之毒尤烈”。但在“以毒攻毒”的理论指导下砒霜却成为最早被应用于治疗恶性肿瘤的传统药物[1]。三氧化二砷(As2O3)是砷剂砒霜的主要成分。20世纪70年代,哈尔滨医科大学第一临床医学院率先用As2O3治疗急性早幼粒细胞白血病(Acute promyelocytic leukemia,APL),取得巨大成功。目前欧洲白血病国际专家委员会已认为As2O3是“APL疗法中最具生物学活性的单体”[2]。由于As2O3具有快速的肾清除率和剂量限制毒性的特点,限制了其在其他肿瘤治疗中的应用[3-4]。脂质体以其独特的类细胞结构和载药特点成为抗肿瘤药物的优良载体,可改变药物在体内的分布并降低毒性[5]。本课题组采用醋酸铜梯度主动载药法制备了三氧化二砷脂质体,建立银盐法测定砷的含量及葡聚糖凝胶微柱离心-银盐法测定脂质体包封率的方法,为制剂评价提供依据。
1 仪器与试药
1.1 仪器
PHS-25型pH计(上海精科雷磁);BS124s电子分析天平(德国赛多利斯公司);UV-1801型紫外-可见分光光度计(瑞利分析仪器有限公司,中国);DF-101S磁力搅拌器(巩义市英峪予华仪器厂);UV-260紫外扫描仪(日本Shimadzu);Anke TDL80-2B离心机(上海安亭科学仪器厂);Nicomp-380激光粒度测定仪(美国Particle Sizing Systems公司);JM-1200EX透射电镜(日本JEOL);JY92-2D超声波细胞粉碎机(宁波新芝科器研究所)。
1.2 试药
氢化大豆磷脂(HSPC,德国Lucas Meyer);亚砷酸钠(NaAsO2,成都西亚化工股份有限公司,纯度≥96%);胆固醇(CH,南京新百药业有限公司);聚乙二醇单甲醚2000-二硬脂酰磷脂酰乙醇胺(mPEG2000-DSPE,美国Genzyme公司);无水乙醇(药用,安徽安特生物化学有限公司);氢氧化钠(NaOH,天津博迪化工有限公司);碘化钾(KI,天津市凯信化学工业有限公司);氯化亚锡(SnCl2,天津博迪化工有限公司);无砷锌粒(天津博迪化工股份有限公司);醋酸铅棉花(实验室自制);二乙氨基二硫代甲酸银(国药集团化学试剂有限公司);三乙醇胺(天津博迪化工股份有限公司);三氯甲烷、浓硫酸(天津市凯信化学);醋酸铜[Cu(OAc)2·H2O,天津博迪化工股份有限公司];葡聚糖凝胶G-50(美国Sigma公司);ZB-1型Na+型阳离子交换纤维(国药集团化学试剂有限公司)
2 方法与结果
2.1 脂质体的制备
将HSPC、CH及mPEG2000-DSPE按3∶1∶1(w/w/w)的比例混合,加入0.3 mL无水乙醇,于65 ℃水浴中加热溶解,开盖搅拌1.5 min以挥除大部分乙醇。加入预热至相同温度的水化介质[200 mmol·L-1的Cu(OAc)2溶液],65 ℃水浴搅拌30 min,得空白脂质体初品。以超声波细胞粉碎机处理所得脂质体(200 W×2 min,400 W×6 min,工作1 s,间歇1 s)后,依次通过0.8、0.45和0.22 μm微孔滤膜各3遍进行整粒,得空白脂质体混悬液(磷脂质量浓度约为50 mg·mL-1)。
取空白脂质体混悬液0.1 mL,上样于经离心预处理的2 mL阳离子交换纤维,同时加入0.1 mL重蒸水,停留10 min,2000 r·min-1离心4 min,再于柱顶端加入0.05 mL 5%葡萄糖,2000 r·min-1离心4 min洗脱,合并洗脱液,混匀,得最终磷脂浓度约为20 mg·mL-1的具有Cu(OAc)2跨膜离子梯度的脂质体混悬液。
取梯度脂质体混悬液适量,按药脂比1∶30(w/w)加入药物溶液,60 ℃恒温孵育30 min,冰水浴终止载药,即得三氧化二砷脂质体(含砷量0.3 mg·mL-1)。
2.2 脂质体的表征
2.2.1 形态 取重蒸水稀释后的三氧化二砷脂质体,滴至镀碳支持膜铜网上,用滤纸从边缘吸去多余液体。将醋酸双氧铀染液滴至支持膜上染色,用滤纸吸去多余的染液,干燥3 h,置于透射电镜下观察。见图1。

图1 三氧化二砷脂质体透射电镜图片
由图1可以看到脂质体双层结构明显,大小分布均较均匀,未见脂质体聚集。
2.2.2 粒径与Zeta电位 取三氧化二砷脂质体适量,用重蒸水行稀释,使光密度值在250~350,放入样品池内,采用Nicomp-380粒径/Zeta电位测定仪对粒径和Zeta电位进行测定。测定条件:光源为He-Ne激光(空气冷却);波长λ为632.8 nm;功率为75 mW;温度为23 ℃。粒径检测结果见图2。粒径为110.8 nm,粒径分布呈高斯分布,PDI值为0.133。脂质体Zeta电位为-21.97 mV(见图3),呈负电性,有利于脂质体的稳定。

图2 三氧化二砷脂质体粒径分布
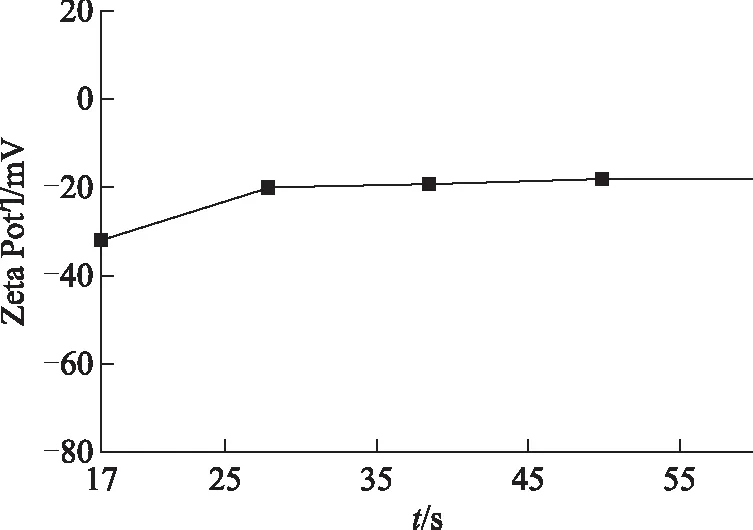
图3 三氧化二砷脂质体的Zeta电位测定
2.3 砷含量的测定
2.3.1 溶液的配制 吸收液(二乙胺基二硫代甲酸银-三乙醇胺三氯甲烷溶液):称取0.25 g二乙胺基二硫代甲酸银[(C2H5)2NCS2Ag,Ag-DDC]粉末,移入100 mL量瓶中,加入1.8 mL三乙醇胺,再用三氯甲烷溶解稀释至100 mL,放置过夜,滤入棕色瓶中贮存。
硫酸溶液:将浓硫酸与蒸馏水等体积混合后即得。
400 g·L-1氯化亚锡溶液:称取40 g氯化亚锡溶于40 mL盐酸中,加蒸馏水稀释至100 mL,投入数粒锡粒,此溶液质量浓度为400 g·L-1。
砷标准溶液:精确称取亚砷酸钠17.32 mg至100 mL量瓶中,加重蒸水溶解并稀释至刻度,贮于棕色瓶中,此溶液每毫升相当于0.1 mg砷。使用时吸取此溶液1.0 mL于100 mL量瓶中,加1 mL 10%硫酸,加水至刻度,此溶液每毫升相当于1 μg砷。
2.3.2 测定方法 准确吸取砷标准液适量置于砷化氢发生器中,加入硫酸溶液10 mL,加蒸馏水至50 mL。加入150 g·L-1的碘化钾溶液5.0 mL及400 g·L-1的氯化亚锡5滴,混匀,放置15 min。于吸收管中加入5 mL吸收液,插入塞有乙酸铅棉花的导气管。依次向各发生瓶中加入5 g无砷锌粒,塞紧瓶塞,室温下反应1 h,用三氯甲烷将吸收液体积补充至5.0 mL,以空白吸收液为参比,对反应后的吸收液进行全波长扫描。见图4。

图4 砷与Ag-DDC的复合物的UV-VIS吸收光谱
由图4可知,吸收液中砷与Ag-DDC的复合物在510 nm处有最大吸收波长,因此选择510 nm为后续测定的波长。
2.3.3 标准曲线的绘制 准确吸取砷标准使用液(1 μg·mL-1)4.0、8.0、12.0、16.0、20.0、24.0 mL,分别置于砷化氢发生器中,加蒸馏水至50 mL,配成标准系列。按2.3.2项下操作,以空白吸收液为参比,510 nm处测定其吸光度,以吸光度值A对砷量(μg)进行线性回归,得线性方程Y=0.023 5X+0.014 3,r=0.999 1,表明砷在4.0~24.0 μg呈线性良好。
2.3.4 精密度 准确吸取砷标准溶液4.0、16.0、24.0 mL,按2.3.2和2.3.3项下测定吸光度值,连续进样3次,计算日内日间精密度。结果为日内相对标准差(%)为1.0、1.48、1.31,日间相对标准差(%)为1.75、1.03、1.22,说明此方法精密度良好。
2.3.5 回收率 取亚砷酸钠溶液(含砷0.6 mg·mL-1)与空白脂质体等体积混合,得砷对照液及砷-空白脂质体混合液(含砷0.3 mg·mL-1)。分别取上述混合溶液0.3、0.4、0.5 mL于10 mL量瓶中,甲醇溶解并稀释至刻度,摇匀。取上述溶液1.0 mL于砷化氢发生器中,按2.3.2项下方法测定吸光度值,将所得吸光度值由标准曲线计算药物浓度,计算低、中、高3个浓度的回收率。回收率(%)分别为98.0、99.4、98.7,RSD(%)分别为2.7、1.5、2.2,表明脂质体中的其他成分(脂质及铜离子)对测定无影响,回收率良好。
2.3.6 脂质体中砷含量的测定 取制备的三氧化二砷脂质体0.4 mL,用甲醇溶解并稀释至10 mL。取上述溶液1.0 mL于砷化氢发生器中,按2.3.2项下方法测定吸光度值,带入标准曲线,计算药物含量为0.296 mg·mL-1。
2.4 脂质体包封率的测定
2.4.1 葡聚糖凝胶柱的制备 将葡聚糖凝胶Sephadex G-50浸泡在蒸馏水中过夜,充分溶胀。装于2.5 mL注射器内,待水分自然流下,2000 r·min-1离心3 min除水,制备凝胶柱,柱高约为1.0 cm,备用。
2.4.2 葡聚糖凝胶微柱对空白脂质体的吸附 采用浊度法考察葡聚糖凝胶微柱对空白脂质体的截留情况。取2.1项下空白脂质体0.1 mL 4份,分别标记为A、B、C和D。A直接转移入5 mL量瓶中。B、C和D均上样于葡聚糖微柱顶端。B在2000 r·min-1离心3 min后收集洗脱液于5 mL量瓶。C离心后继续加0.1 mL 5%葡萄糖溶液于葡聚糖凝胶微柱顶端,2000 r·min-1离心3 min进行洗脱,收集经离心后的洗脱液于5 mL量瓶。D重复洗脱2次后,收集经离心的洗脱液于5 mL量瓶。将量瓶中A、B、C和D分别用蒸馏水稀释至刻度,摇匀,并于510 nm处测定吸光度值,记为Atotal、A0、A1、A2。按公式Rn(%)=An/Atotal×100%计算脱吸附率,结果见表1。

表1 洗脱次数对空白脂质体的脱吸附率的影响(n=3)
由表1可知,经2次洗脱后96%以上的空白脂质体被洗脱下来。
2.4.3 葡聚糖凝胶微柱对砷溶液的吸附 分别取砷溶液(0.3 mg·mL-1)0.1 mL各4份,按照2.4.2方法处理,收集于5 mL量瓶中,蒸馏水稀释到刻度,摇匀,按2.3.2项下操作,在510 nm处,测定其吸光度,记为Atotal、A0、A1和A2,带入标准曲线计算药物量,记为Wtotal、W0、W1和W2,考察洗脱次数对药物吸附的影响。脱吸附率根据公式Rn(%)=Wn/Wtotal×100%。

表2 洗脱次数对三氧化二砷脱吸附率的影响(n=3)
注:“—”为吸光度值未测出。
结果表明,药物在Sephadex G-50凝胶柱上吸附能力较强,经2次洗脱后仅有1.46%的药物被洗脱下来。结合空白脂质体的洗脱结果(表2),我们确定分离脂质体与游离药物洗脱次数为2次。
2.4.4 脂质体包封率的测定 取三氧化二砷脂质体0.1 mL两份。一份用甲醇稀释至5 mL,摇匀。按2.3.2项下操作后,测定吸光度值,计算总药量(Wtotal)。第二份上样于葡聚糖凝胶微柱顶端,2000 r·min-1离心3 min,继续加0.1 mL 5%葡萄糖溶液于葡聚糖凝胶柱顶端,2000 r·min-1离心3 min,合并洗脱液用甲醇稀释至5 mL,摇匀,精密量取1.0 mL于砷化氢发生器中,按2.3.2项下操作后,测定吸光度值,计算包封于脂质体中的药物量(记为Wlip)。根据公式EE(%)=Wlip/Wtot×100%计算包封率为83.54%。
3 讨论
脂质体(liposomes)是磷脂等类脂质分散于水相中所形成的封闭囊泡,因其具有良好的组织相容性与细胞亲和性而广泛应用于生物学领域,具有其他载体无法替代的独特优势。脂质体是抗肿瘤药物的理想载体,可以通过高通透性长滞留效应(EPR)提高药物在肿瘤中的滞留,增加癌细胞对药物的摄取量,降低给药剂量,减少药物对系统和特定部位的毒副作用(如心脏毒性、肾脏毒性)。目前多种抗肿瘤药物的脂质体已上市或进入临床,如盐酸阿霉素脂质体(Doxil®)、阿糖胞苷脂质体(DepoCyt®)、紫杉醇脂质体(力扑素®)等。三氧化二砷作为中药砷剂的有效单体,虽然具有抗肿瘤活性,但毒性大、治疗窗窄的缺陷限制了其在其他肿瘤治疗中的应用。本研究利用三氧化二砷具有弱酸性的特点,利用醋酸铜梯度法制备了三氧化二砷脂质体,包封率可达83.54%,以期降低毒性、提高疗效,实现在临床肿瘤治疗中的应用。
银盐法的检测原理为,碘化钾、氯化亚锡将五价砷还原为三价砷后经历如下反应:
H3AsO3+3Zn+6HCl=AsH3↑+ZnCl2+3H2O
AsH3+6Ag(DDC)=AsAg3·3AgDDC+3HDDC
AsAg3·3AgDDC+3NR3+3HDDC=6Ag+As(DDC)3+3(NR3H)(DDC)
由原理可知,砷化氢产生的速度是影响吸收液吸光度值的关键因素。产生速度过慢(每3 s产生气泡数少于1个)或过快(每3 s产生气泡数超过9个)都不利于砷化氢的吸收,导致方法重复性不好,所得精密度不符合规定。砷化氢的产生速度受锌粒体积、酸度以及温度3个因素的影响。参考文献[7-9],我们选择13~20粒/g的无砷锌粒,将硫酸用量定为10 mL,温度控制在27~30 ℃,方法重复性良好。
测定脂质体中的药物,首先要将其中的药物释放出来,即破坏脂质双分子膜。马满玲等[9]采用Triton X-100作为破膜剂测定三氧化二砷脂质体的包封率,但本研究发现,向砷化氢发生器中加入Triton X-100时,吸收液的吸光度无法测出。这可能是由于Triton X-100是一种表面活性剂,砷化氢发生器中不断产生气泡,就等同于在晃动整个发生器,所以体系中会产生大量的泡沫。产生的气体进入气泡中,使得新生态氢无法与砷结合生成砷化氢,同时生成的砷化氢进入气泡中,不能通过导气管被吸收液吸收。采用甲醇作为破膜剂,脂质体中砷含量的测定不受影响,因此本研究采用甲醇作为破膜剂。
测定包封率时,脂质体与游离药物的分离方法多种多样,例如阳离子交换树脂吸附法[11]、超滤法[12-13]、超速离心法[14]、葡聚糖凝胶柱层析法[15]等。本文采用的葡聚糖凝胶微柱-离心法是对于葡聚糖凝胶柱层析法的改进,通过离心加速药物与脂质体分离的过程,同时减少了对脂质体样品的稀释。实验中发现,一次洗脱后即可分离完全脂质体与游离三氧化二砷,简便快捷。
4 结论
醋酸铜梯度法适用于制备三氧化二砷脂质体,包封率较高。同时,将银盐法与葡聚糖凝胶微柱-离心法相结合用于三氧化二砷脂质体包封率的测定,方法简单易行,可操作性强。

