光动力疗法治疗晚期消化道肿瘤的临床研究
熊超亮 吴裕文 钟谷平 范惠珍
【摘要】 目的:探討光动力疗法治疗晚期消化道肿瘤的临床效果。方法:选取本院2015年1月-2018年5月收治的26例晚期消化道肿瘤患者,均给予光动力疗法,观察近期疗效、吞咽困难评分、生活质量评分、毒副反应的发生情况、生存状况。结果:26例患者光动力治疗后1个月显效率57.69%、有效率88.46%,不同部位、不同病理类型的晚期消化道肿瘤患者的显效率、有效率比较,差异均无统计学意义(P>0.05);光动力治疗4周后患者的吞咽困难评分(1.77±0.63)分,低于治疗前的(3.23±0.74)分(t=7.660,P<0.05);生存患者治疗后3个月生活质量各项评分均高于治疗前,治疗后6、12个月生活质量各项评分均低于治疗后3个月,且治疗后12个月生活质量各项评分均低于治疗后6个月,差异均有统计学意义(P<0.05);26例患者光动力治疗后17例出现不同程度的局部疼痛或不适,12例出现不同程度的反酸/胃灼热症状,3例出现低度发热,2例食管癌患者在第2次进行激光照射时肿瘤组织表面有少量出血,经对症处理后均明显好转;26例患者中位生存期为9个月,其中KPS评分≥70分的患者生存期为(11.23±2.39)个月,长于KPS评分<70分的(6.17±1.43)个月,差异有统计学意义(t=6.232,P<0.05)。结论:光动力疗法治疗晚期消化道肿瘤的临床效果良好。
【关键词】 光动力疗法 消化道肿瘤 吞咽困难 生活质量 毒副反应
[Abstract] Objective: To explore the clinical effect of photodynamic therapy in the treatment of advanced gastrointestinal cancer. Method: From January 2015 to May 2018, 26 patients with advanced gastrointestinal cancer were treated with photodynamic therapy. The short-term efficacy, dysphagia score, quality of life score, the occurrence of side effects and survival status were observed. Result: After photodynamic therapy 1 month, the marked improvement rate was 57.69%, and the effective rate was 88.46%. The comparison of marked improvement rate and effective rate of patients with advanced gastrointestinal cancer in different parts and pathological types were compared, the differences were not statistically significant (P>0.05). The score of dysphagia after photodynamic therapy was (1.77±0.63) points, lower than (3.23±0.74) points of before photodynamic therapy (t=7.660, P<0.05).The each score of quality of life in 3 months after treatment were higher than those of before treatment, and those in 6 and 12 months after treatment were lower than those in 3 months after treatment, and those in 12 months after treatment were lower than those in 6 months after treatment, the differences were statistically significant (P<0.05).After photodynamic therapy, 17 patients had local pain or discomfort of different degrees, 12 patients had acid regurgitation/heartburn symptoms of different degrees, 3 patients had fever of low degree, 2 patients with esophageal cancer had a small amount of bleeding on the surface of tumor tissue during the second laser irradiation, all of which improved significantly after symptomatic treatment. The median survival time of 26 patients was 9 months, and the median survival time of patients with KPS ≥70 was (11.23±2.39) months, longer than (6.17±1.43) months with KPS <70, the difference was statistically significant (t=6.232, P<0.05). Conclusion: The clinical curative effect of photodynamic therapy is good on advanced gastrointestinal cancer.
在我国的恶性肿瘤分布中,消化道肿瘤的发病率与死亡率都很高,但是由于消化道肿瘤早期症状一般都不具有特异性,故而早期诊断率很低,大部分患者就诊时已进入晚期阶段,预后较差。手术治疗是消化道肿瘤的首选方式,结合放化疗可提高早中期患者的生存率。但是以上治疗方式对于晚期患者无明显治疗效果。光动力疗法是一种联合应用光敏剂及相应光源,诱发强烈的光化学反应,选择性破坏肿瘤组织的新型微创技术。临床研究表明,光动力疗法临床优势在于破坏肿瘤组织的同时能够最大限度地保护正常组织,其选择性杀瘤作用在现有肿瘤微创治疗手段中最强[1-2]。目前有关光动力疗法治疗晚期消化道肿瘤的临床研究鲜有报道。本研究选取本院2015年1月-2018年5月收治的26例晚期消化道肿瘤患者,旨在探讨光动力疗法治疗晚期消化道肿瘤的效果,以期为晚期患者临床治疗方案的选择提供科学的依据。现报道如下。
1 资料与方法
1.1 一般资料 选取2015年1月-2018年5月本院收治的26例晚期消化道肿瘤患者,按病变部位可分为食管癌10例、胃癌8例、直肠癌8例;按病理类型分鳞癌12例、腺癌14例;Karnofsky(卡氏,KPS,百分法)功能状态评分标准≥70分15例、<70分11例。(1)纳入标准:①均经过经病理学证实为晚期消化道肿瘤;②均失去手术最佳时机,不符合手术指征;③TNM分期为T3~4及N1~2部分已达M1,预计生存期≥3个月;④患者依从性良好,能配合治疗;⑤患者临床病例资料完整。(2)排除标准:①重要脏器严重功能不全患者;②存在其他脏器原发性或转移性恶性肿瘤者;③合并严重感染或恶病质患者;④过敏体质或对光敏剂过敏患者;⑤存在光动力治疗禁忌证患者;⑥经放化疗治疗失败或术后复发患者。患者及其家属知晓光动力治疗的目的、注意事项以及并发症相关情况,治疗前均已签署光动力治疗同意书。本研究已经院伦理委员会审核批准。
1.2 方法 患者均给予光动力疗法,将患者安置于避光病房中,光敏剂PHOTOFRIN(加拿大药业有限公司,规格:100 mg/瓶),按照2 mg/kg溶于0.9%氯化钠注射液100 mL中,持续静脉输入1 h,48 h后行光动力治疗,治疗仪器为氩离子泵浦染料激光器(中国科学院电子学研究所),激光波长630 nm。术前禁食水6 h,采取静脉全身麻醉,持续心电监测。电子纤维内镜(日本Olympus公司)事先寻找、观察病灶,距离病灶1 cm时,在其引导下导入柱状光导光纤(深圳雷迈科技公司),根据病变范围以及病灶大小选取不同长度的光导纤维,设置不同功率及照射范围和时间。治疗时发光部需超出肿瘤边缘1~2 cm以确保照射范围充分覆盖病灶。术后行止血、抑酸等对症治疗,禁食24 h,给予静脉营支持。48 h后经内镜清除坏死组织,用同样方法对原有病灶和新发现病灶进行第2次照射。嘱患者4~6周内严格避光,严禁阳光及日光灯照射,4周后复查。
1.3 观察指标及判定标准 (1)分析患者的近期疗效,比较不同部位、不同病理类型晚期消化道肿瘤患者的近期疗效。患者4周后复查内镜,对比治疗前内镜结果,根据肿瘤变化情况进行客观疗效判定,分为完全缓解(CR,肿瘤完全消失,持续超过4周)、明显缓解(SR,肿瘤最大径和其垂直或肿瘤高度的乘积缩小50%以上,并持续4周以上)、稍有缓解(MR,上述乘积缩小不足50%,并持续4周以上)、无效(NR,肿瘤无缩小甚至增大),显效=CR+SR,有效=CR+SR+MR[3]。(2)分析患者治疗前后临床症状(吞咽困难)改善情况,治疗前后对患者进行吞咽困难程度评分,5分:不能进食任何东西,包括唾液;4分:不能进流食;3分:不能吞咽固体食物,但能够进流食;2分:吞咽固体食物比较困难,但能吞咽半固体食物;1分:无吞咽困难症状[4]。(3)生活质量:采用世界卫生组织生活质量测定量表简表(SF-36评分)中国版,分别在治疗前及治疗后3、6、12个月对生存患者进行调查,得分越高表明生活质量越好[5]。(4)毒副反应:光动力治疗结束后观察和记录患者的毒副反应发生情况,主要包括疼痛、反酸、胃灼热、发热、肠道梗阻状况以及光过敏反应等。(5)生存状况:患者光动力治疗结束开始进入为期12个月的随访期,随访方式包括电话随访以及查阅患者复查就诊的电子病案记录。生存期计算由治疗日开始至死亡或末次随访日止。
1.4 统计学处理 使用SPSS 20.0软件对所得数据进行统计分析,计量资料用(x±s)表示,组间比较采用t检验,组内比较采用配对t检验;计数资料以率(%)表示,比较采用字2检验。以P<0.05为差异有统计学意义。
2 结果
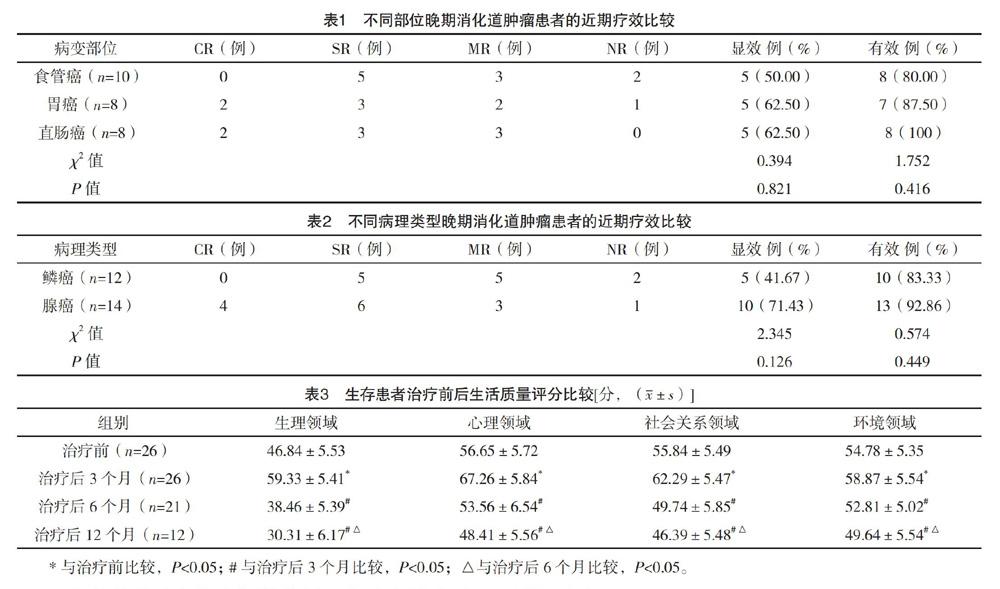
2.1 患者的近期疗效分析 患者光动力治疗后1个月CR 15.38%(4/26)、SR 42.31%(11/26)、MR 30.77%(8/26)、NR 11.54%(3/26),显效率57.69%(15/26),有效率88.46%(23/26);不同部位、不同病理类型的晚期消化道肿瘤患者的显效率、有效率比较,差异均无统计学意义(P>0.05),见表1、2。
2.2 患者临床症状改善情况 光动力治疗后10例食管癌、8例胃癌患者上消化道梗阻癥状明显改善,8例直肠癌患者肠道刺激症状、排便习惯改变、便血以及不完全性肠梗阻等症状得以明显改善;光动力治疗4周后26例患者的吞咽困难评分(1.77±0.63)分,低于治疗前的(3.23±0.74)分,差异有统计学意义(t=7.660,P<0.05)。
2.3 生存患者治疗前后生活质量评分比较 生存患者治疗后3个月生活质量各项评分均高于治疗前,治疗后6、12个月生活质量各项评分均低于治疗后3个月,且治疗后12个月生活质量各项评分均低于治疗后6个月,差异均有统计学意义(P<0.05)。见表3。
2.4 患者毒副反应发生情况分析 光动力治疗后,17例患者出现不同程度的局部疼痛或不适,给予非甾体类消炎药物治疗后均得以缓解,2~5 d后症状消失;12例患者出现不同程度的反酸/胃灼热症状,给予质子泵抑制剂抑酸、胃黏膜保护剂治疗5~7 d后有效缓解;3例患者出现术后低度发热,未经特殊治疗,指导患者进行物理降温后缓解;2例食管癌患者在第2次进行激光照射时,肿瘤组织表面有少量出血,术后给予常规止血药物治疗,48 h后复查内镜示食管壁充血水肿明显,经过延长禁食时间并给予抗感染治疗,1周后出院,4周后复查内镜食管壁无明显异常。本研究纳入患者未出现穿孔、瘘等严重并发症,治疗后均严格按照要求采取避光措施,未见皮肤色素沉着,无光敏反应如皮肤红斑、瘙痒等症状发生,治疗后复查血常规及肝肾功能无明显改变。
2.5 26例患者生存状况分析 26例患者中位生存期为9个月,其中KPS评分≥70分的患者生存期为(11.23±2.39)个月,长于KPS评分<70分的(6.17±1.43)个月,差异有统计学意义(t=6.232,P<0.05)。
3 讨论
近年来消化道肿瘤发病率逐年上升,据有关中国癌症方面的报告,我国消化道肿瘤占全部癌症发病率的43.3%。消化道肿瘤主要为恶性肿瘤,癌占绝大部分,多见于食管、胃和大肠。晚期消化道肿瘤患者预计生存期较短,一般为数月,多数死于肿瘤的浸润生长和广泛转移[6]。目前临床上治疗晚期消化道肿瘤以减轻患者痛苦、提高其生活质量以及延长生存时间为主[7]。光动力学疗法不受细胞病理类型、细胞异质性及耐药等的影响,光动力反应生成的ROS成分可以直接作用于底物,如细胞质膜、线粒体、溶酶体、内质网、高尔基体等,诱导肿瘤细胞的坏死或凋亡,治疗效果显著的同时可最小化治疗毒性。近年来随着光敏剂及光源不断更新,光动力疗法凭借其卓越的杀伤深度和杀伤效率,已广泛应用于晚期消化道肿瘤的治疗中[8]。临床研究表明,光动力学疗法可特异性地杀伤肿瘤细胞,能以重复剂量应用而无总剂量限制,且毒副反应少[9-10]。
本研究结果显示,26例晚期消化道肿瘤患者光动力治疗后1个月显效率57.69%、有效率88.46%,不同部位、不同病理类型的晚期消化道肿瘤患者的显效率、有效率比较,差异均无统计学意义(P>0.05)。提示光动力疗法不受细胞病理类型影响,对不同部位、不同组织病理类型的肿瘤治疗效果相当。本研究结果显示,光动力治疗后26例患者主要临床症状得到明显改善,表明光动力治疗效果良好。光动力治疗4周后26例患者吞咽困难评分低于治疗前(P<0.05),表明光动力疗法可有效缓解上消化道肿瘤患者的吞咽困难症状,食管癌和胃癌患者治疗后在无吞咽困难期间可正常饮食,有助于其生理机能的恢复。本研究结果显示,患者治疗后3个月生活质量各项评分均高于治疗前(P<0.05),提示光动力疗法能够明显改善患者近期的生活质量。郝璐等[11]在光动力疗法在食管癌治疗中的作用中表明光动力疗法能缩小肿瘤,缓解吞咽困难,提高中晚期食管癌患者的生活质量。本研究中,治疗后6、12个月生活质量各项评分均低于治疗后3个月,且治疗后12个月生活质量各项评分均低于治疗后6个月,差异均有统计学意义(P<0.05)。这与恶性肿瘤的浸润生长和广泛转移有关,但结果提示在临床实践中结合生活质量评分有助于医师推测患者病情变化和判断光动力疗法的治疗效果,为接下来治疗方案的选择提供一定的依据。
光动力治疗的并发症主要包括皮肤光毒反应、消化道症状反应、发热反应以及过敏反应[12]。皮肤光毒反应仅发生在激光照射区,持续时间较短,且引起的组织破坏作用过程缓和,对痛觉神经理化刺激很轻[13],本研究中17例患者出现不同程度的局部疼痛或不适,给予非甾体类消炎药物止痛后均得以缓解,2~5 d后症状消失;消化道症状反应主要表现为上腹疼痛或灼热、腹胀、恶心、呕吐或伴有上腹压痛,本研究中12例患者出现不同程度的反酸/胃灼热症状,给予质子泵抑制剂抑酸、胃黏膜保护剂治疗5~7 d后有效缓解;患者在严格避光条件下均未出现明显的光过敏反应;发热反应一般在静脉给予光敏剂后出现,发生率约3%,一般38 ℃左右[14],本研究中出现发热3例,给予物理降温后缓解;本研究中2例患者在行第2次激光照射时发现肿瘤组织表面有出血,这可能与患者既往行放射治疗导致肿瘤组织的血管壁受到破坏有关。本研究中26例患者均未出现穿孔现象,这与光动力治疗中根据病变范围以及病灶大小选取不同长度的光导纤维、设置不同功率及照射范围和时间有关,故而达到最佳治疗效果的同时可最大限度保护正常管壁组织。本研究结果提示光动力治疗毒副反应较轻微,与国内其他研究一致[15]。
KPS评分是肿瘤患者功能状态评分标准之一,研究报道KPS评分得分越高表明肿瘤患者健康状况越好,对于治疗给身体带来的毒副作用耐受程度越高,是临床上考虑是否接受彻底治疗的评判标准之一[16],既往研究已证实KPS评分>70分者术后状态较好,存活期较长[17]。本研究根据KPS评分对患者进行分层分析,结果显示,26例患者中位生存期为9个月,其中KPS评分≥70分的患者生存期长于KPS评分<70分者(P<0.05),提示KPS评分状态对晚期患者的生存期有显著性影响,与既往研究结果一致[18-19]。
综上所述,光动力疗法治疗晚期消化道肿瘤效果良好,可以有效缓解患者的临床症状,提高其生活質量,且毒副反应较小。本研究不足之处在于样本数量较少,可能会对结果造成一定的统计学误差,但本研究为晚期消化道肿瘤患者的临床治疗和预后提供了一定的理论支持。
参考文献
[1] El-Daly S M,Abba M L,Gamal-Eldeen A M.The role of microRNAs in photodynamic therapy of cancer[J].Eur J Med Chem,2017,142:550-555.
[2] Duan X,Chen B,Cui Y,et al.Ready player one? Autophagy shapes resistance to photodynamic therapy in cancers[J].Apoptosis,2018,23(11-12):587-606.
[3]刘慧龙,王飞,王莉,等.血卟啉衍生物介导的光动力疗法治疗上消化道癌的临床研究[J].中国激光医学杂志,2017,26(6):303-308.
[4]张明,赵静,李珊,等.光动力治疗联合顺铂对食管癌Eca-109细胞增殖、凋亡及p38 MAPK通路的影响[J].中国临床研究,2019,32(1):13-17,22.
[5]骆莉萍,娄继滨,游红杏.不同光敏剂诱导的光动力疗法在结直肠癌治疗中应用效果[J].中华实用诊断与治疗杂志,2017,31(10):1014-1016.
[6] Rodrigues J,Amorim R,Silva M,et al.Photodynamic Therapy at Low-Light Fluence Rate:in vitro Assays on Colon Cancer Cells[J].IEEE Journal of Selected Topics in Quantum Electronics,2018,33(99):1-12.
[7]曾嘉,梅世文,邹博远,等.胃肠道肿瘤的光动力治疗及其进展[J].中国普通外科杂志,2017,26(6):795-800.
[8] Candido N M,de Melo M T,Franchi L P,et al.Combining Photodynamic Therapy and Chemotherapy:Improving Breast Cancer Treatment with Nanotechnology[J].J Biomed Nanotechnol,2018,14(5):994-1008.
[9] Zhang Y,Wang F,Liu C,et al.Nanozymes Decorated Metal-Organic Frameworks for Enhanced Photodynamic Therapy[J].ACS Nano,2018,12(1):651-661.
[10] Tsai W H,Yu K H,Huang Y C,et al.EGFR-targeted photodynamic therapy by curcumin-encapsulated chitosan/TPP nanoparticles[J].Int J Nanomedicine,2018,13(12):903-916.
[11]郝璐,邱海霞,毛永平,等.光动力疗法在食管癌治疗中的作用[J].中国激光医学杂志,2018,27(2):33.
[12]顾静,王付亮,王来群,等.氨基酮戊酸光动力疗法对鳞状细胞癌细胞株A43蛋白激酶D1及其磷酸化位点的影响[J].中华皮肤科杂志,2018,51(2):96-100.
[13]闫炫炫,李多富,李汛.光动力疗法在不可切除肝门部胆管癌中的应用[J].中国普外基础与临床杂志,2018,25(4):488-492.
[14]王颖,顾瑛.肿瘤靶向光动力疗法的临床研究与应用新进展[J].中国激光医学杂志,2017,26(5):279-287.
[15]王凌翔,吴正春,文宇,等.肿瘤干细胞的光动力治疗研究进展[J].激光生物学报,2017,26(1):1-8.
[16]樊曉静,史志涛,孙昕.活血健脾中药联合顺铂化疗对直肠癌患者肿瘤相关指标、Karnofsky评分及ECOG评分的影响分析[J].中华中医药学刊,2017,35(11):2969-2972.
[17]张鑫彤,祁兴顺,郭晓钟.卡氏评分预测肝硬化患者出院后死亡风险[J].临床肝胆病杂志,2017,33(2):363.
[18]靳义,康聪,郭占领,等.光动力疗法联合奈达铂和5-Fu治疗顺铂耐药性晚期食管癌患者的疗效[J].医学临床研究,2018,35(1):155-157.
[19]马杜丰.胃镜下光动力疗法治疗上消化道肿瘤分析[J].中外医学研究,2015,13(1):137-138.
(收稿日期:2019-08-19) (本文编辑:董悦)

