基于色度传感器探究乙酸乙酯的水解反应
纪政 吴峰


摘要:探究了基于色度传感器的乙酸乙酯水解反应实验,尝试将实验从定性层面上升到定量层面,发展成为乙酸乙酯水解反应的探究性和创新性实验,希望能为传感器技术应用于高中化学实验教学提供一些借鉴和思考。
关键词:色度传感器;乙酸乙酯;水解反应;探究实验
文章编号:1008-0546(2019)01-0089-03 中图分类号:G633.8 文献标识码:B
doi:10.3969/j.issn.1008-0546.2019.01.028
鲁科版《化学2(必修)》[1]中研究乙酸乙酯在不同酸碱度下的水解情况,通过闻乙酸乙酯气味消失的时间判断水解的快慢,香味消失的时间越短,水解反应速率越快。但是不同的人观测时会存在一定的误差,所以用观察法误差较大,只能作定性判断。
利用色度传感器,笔者尝试将水层染色,通过观测水层的透光率变化,可以精确反映乙酸乙酯在不同酸碱度时的水解情况。
一、实验装置与药品
装置:色度计传感器、数据采集器、计算机(如图1所示)。
药品:乙酸乙酯(AR)、蒸馏水、红墨水溶液、pH分别为4、7、10的溶液。
二、实验原理
1.色度传感器的工作原理
色度传感器是一種测量某种波长的光透过溶液程度(即透光率,T)的仪器。溶液吸光度(A)与透光率(T)之间的关系为A=lg(1/T),可由色度传感器直接测得。根据朗伯比尔定律有:A=εbc(ε为摩尔吸光系数,b为液层厚度)。因此,在一定的浓度范围内,吸光度A与溶液浓度c呈线性关系。
2.乙酸乙酯水解的探究原理
实验的大致思路为:向不同酸碱性的介质溶液中滴入1—2滴红墨水溶液,观察乙酸乙酯水解时,溶液透光率改变的快慢,从而确定乙酸乙酯在何种酸碱度条件下水解的速率较快。
由于乙酸乙酯水解产生乙醇和乙酸,而乙醇和乙酸与水任意比互溶,将导致水层溶液稀释,从而颜色变浅,因此,可以观察单位时间内水层变浅的多少来衡量乙酸乙酯在不同酸碱度时的水解快慢。
三、实验步骤与结果讨论
1.实验步骤
(1)连接好数据采集器、色度传感器等相关实验装置。
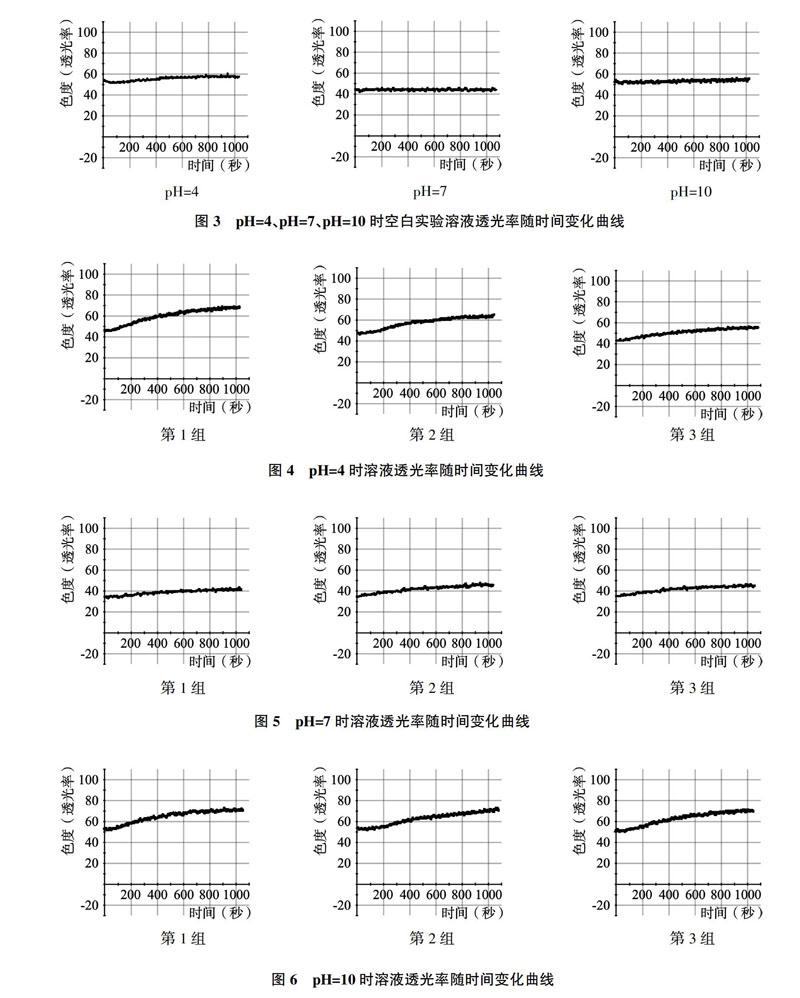
(2)选择蓝色光为透射光,分别使用黑色和透明的比色皿进行两点校准,设置好采集时间为不限定,样本取样频率为1个/s;向比色皿中加入2mL pH=4的溶液,滴加2滴红墨水溶液,混合均匀,放入55℃恒温箱中。三组空白实验溶液透光率变化如图3所示。
(3)选择蓝色光为透射光,分别使用黑色和透明的比色皿进行两点校准,设置好采集时间为不限定,样本取样频率为1个/s;向比色皿中加入2mL pH=4的溶液,滴加2滴红墨水溶液,混合均匀,再加入1mL乙酸乙酯,放入55℃恒温箱中。三组平行实验溶液透光率变化如图4所示。
(4)同样的操作完成pH=7、pH=10乙酸乙酯水解时的水层透光率变化,如图5、图6所示。
2.实验结果
将pH分别为4、7、10时,不加入乙酸乙酯做空白实验,红墨水溶液的透光率变化的三组曲线图,设置成相同缩放比例。具体如下图3所示。
将pH分别为4、7、10时,红墨水溶液的透光率随着乙酸乙酯的水解而变化的三组曲线图,设置成相同缩放比例。具体如下图4、图5和图6所示。
四、几点思考
1.关于水层染色物质的选择
文献显示[2],水层染色物质有甲基橙、石蕊等指示剂,其目的在于清晰界分酯层与水层,通过一段时间酯层的减少量,来衡量乙酸乙酯水解的快慢。而本案例设计的思路是,通过观察酯层透光率变化的多少,从而判断乙酸乙酯水解的快慢。
本案例选择的是红墨水溶液,可不可以选择甲基橙或石蕊染色呢?事实证明是不行的,因为案例中设计的三组对比实验分别是pH=4、pH=7、pH=10的不同溶液,无论是甲基橙还是石蕊在不同酸碱度条件下的颜色都不同,对应溶液的起始透光率也肯定各不相同。而且,随着乙酸乙酯的水解,生成的乙酸越来越多,必然导致溶液pH的变化,从而引起溶液透光率的变化;另外由于水解产物逐渐溶于水,溶液被稀释,透光率也会逐渐变大,两种因素都会导致电导率的变化,变量不可控,故不可选酸碱指示剂作为水层染色剂。
综上所述,在水层染色剂的选择需满足以下原则:
(1)不能与乙酸乙酯水解产物发生反应而导致水层颜色的变化。
(2)不能易溶于乙酸乙酯而导致水层颜色变化。
(3)不能与乙酸乙酯发生反应导致水层颜色变化。
考虑实验药品的易得性原则,本实验最终确定用教学中常用的红墨水作水层染色剂,从实验效果来看,红墨水是比较理想的水层染色剂。
2.关于对比实验的选择
本实验设置了三组对比实验,分别是在温度约55℃时pH分别为4、7、10的硫酸溶液、蒸馏水和氢氧化钠溶液。本实验的目的主要是为了从定量的角度描述乙酸乙酯在不同pH值时的水解情况,因此,笔者选取了三组pH相差3的溶液,从定量的角度说明了乙酸乙酯在碱性条件下水解较容易,反应速率较快。
3.关于实验变量的控制
本实验的自变量是时间,因变量是水层透光率的变化,因此,其他无关变量都要控制相同。
(1)温度。实验是在温度约为55℃下进行的,实验过程中,配制的硫酸溶液和氢氧化钠溶液均已加热至55℃,乙酸乙酯也是在55℃恒温箱内预热后量取的,因此,三组对比实验温度基本控制相同。
(2)水层体积和酯层体积。实验时控制加入水的体积为2mL,乙酸乙酯的体积为1mL,基本控制三组对比实验水层体积和酯层体积相同。为防止实验过程中酯层的挥发,笔者设计了一个与比色皿内径刚好嵌合且具有良好弹性的发泡塑料,如图7。很好地防止了因挥发导致的酯层减小,控制了实验过程中的变量相同。
参考文献
[1] 王磊,普通高中标准实验教科书:化学2(必修)(3版)[M].济南:山东科学技术出版社,2007:81-82
[2] 相虎.酯的水解实验的改进[J].化学教育,2003(4)

