采用高灵敏共振光散射技术检测食品中残留的卡马西平
江虹,庞向东,吴小燕,程丹,李娜
(长江师范学院 化学化工学院,长江师范学院武陵山片区绿色发展协同创新中心,重庆,408100)
食品中的药残分析,对保障人体健康、及时采取防病防毒措施具有重意义。我国农业部在176 号公告中规定,严禁在动物饲料和饮用水中添加镇静、抗惊厥药物,在动物源食品中也不得检出此类药物[1]。卡马西平属二苯并氮杂类抗癫痫、镇痛药物,具有抑制神经兴奋、减少机体运动和安眠镇静等作用。当用药过量时,年老者可引起精神错乱、激动不安、焦虑、房室传导阻滞或心动过缓等(卡马西平使用说明书中特别强调);由于卡马西平能透过胎盘屏障,通过乳汁进行分泌,因此对妊娠孕妇及哺乳期妇女均有影响。畜牧业中,为了对所饲养的畜禽达到快速增重、催肥、谋取更多经济利益的目的,饲养过程中,有的饲养者擅自在动物饲料或饮水中加入了卡马西平等镇静药物,导致此类药物在动物源食品中的残留,从而对消费者人体健康造成一定危害。由此可见,对动物源性食品中残留的卡马西平进行研究具有一定的必要性和重要性。目前,国内外测定卡马西平的方法主要有高效液相色谱法[2-8],液质联用[9-11],荧光法[12-13],分光光度法[14-15],电化学法[16-17]等。这些方法中,有的所用仪器价格较贵,不易普及,有的选择性不好或灵敏度不高,有的条件要求苛刻等。本工作是在用吸收光谱法研究卡马西平之后,发现用共振光散射(resonance light scattering,RLS)技术研究肉食品中残留的卡马西平,有更高的灵敏度,比吸收光谱法约高4~5个数量级,并且有很好的选择性。该方法用于肉食中残留卡马西平的测定,结果满意。
1 材料与方法
1.1 材料与试剂
卡马西平(CMA)(99.7%,对照品批号:100142-201105),中国食品药品检定研究院;考马斯亮蓝(CMS)(分析纯),临海市亿达贸易有限公司;三羟甲基氨基甲烷(Tris,99.9%),齐一生物科技(上海)有限公司;溴代十六烷基吡啶(CPB,99%),武汉易泰科技有限公司上海分公司;猪肉(1#~2#)、鸡肉(3#~4#), 市售;水,二次蒸留水。
卡马西平标准溶液:准确称取CMA对照品适量,加少量甲醇溶解后转移至100 mL容量瓶中,用水定容,配成236.3 mg/L贮备液,冰箱4 ℃ 保存;临用时取贮备液稀释100倍。考马斯亮蓝溶液:1.00×10-4mol/L。溴代十六烷基吡啶溶液:称取适量的CPB,加少量无水乙醇溶解后用水稀释配成5.00×102mg/L。pH 3.0~8.5 Tris-盐酸溶液:适量0.10 mol/L盐酸与适量0.20 mol/L Tris溶液混合,用酸度计测定而配成。
1.2 仪器与设备
F-2500型荧光光度计,日本日立公司;pHS-3C 型精密酸度计,上海虹益仪器仪表有限公司。
1.3 样品处理
取生鲜猪肉和鸡肉洗净、切条并搅成肉末。准确称取各样品15 g左右(精确至0.000 1 g),置于离心试管中,加甲醇10 mL,搅匀,超声提取40 min,再离心分离(4 000 r/min)20 min,分出上清液。按上述操作再重复提取1次。2次上清液合并后,加入20 mL甲醇,超声提取30 min,再离心分离(4 000 r/min)30 min,上清液转入一小烧杯中,在通风橱内100 ℃恒温水浴浓缩至约3 mL即为待测样品溶液(各平行处理5份)。
1.4 实验方法
在10 mL具塞比色管中,顺序加入适量2.363 mg/L CMA标准溶液、2.50 mL 1.00×10-4mol/L CMS溶液、0.30 mL 5.00×102mg/L CPB溶液和 0.50 mL pH 3.46 Tris-盐酸溶液,用二次蒸馏水定容、摇匀,15 min后,于荧光仪上(设λex=λem=220 nm,测定狭缝5 nm)同步扫描RLS光谱,记录344 nm波长处体系和试剂空白的RLS强度IRLS及I0,并计算他们的强度差值ΔIRLS=IRLS-I0。
2 结果与讨论
2.1 CMA-CPB-CMS的RLS光谱
按1.4的方法扫描体系各不同组合的RLS光谱,见图1。

1-0.236 mg/L CMA;2-2.50×10-5 mol/L CMS;3-15.0 mg/L CPB;4-2.50 ×10-5 mol/L CMS,pH 3.46;5-15.0 mg/L CPB,pH 3.46;6-0.236 mg/L CMA-2.50×10-5 mol/L CMS,pH 3.46;7~12-0.0、0.047 3、0.094 5、0.142、0.189、0.236 mg/L CMA-2.50×10-5 mol/L CMS-15.0 mg/L CPB,pH 3.46图1 CMA-CMS-CPB 的RLS光谱Fig.1 RLS spectra of CMA-CMS-CPB
从曲线1~6可知,单独的CMA、CMS、CPB溶液的RLS信号十分微弱,CMS的酸性溶液(pH 3.46)、CPB的酸性溶液(pH 3.46)及CMS与CMA在酸性溶液(pH 3.46)中反应后的RLS信号也很微弱。但当CMS与CPB在酸性溶液(pH 3.46)中共存时,RLS信号有显著增强,见曲线7,这说明CPB可以增敏CMS;当CMA、CMS、及CPB三物质在酸性溶液(pH 3.46)中共存时,体系RLS信号随着CMA质量浓度的增加而增强,当CMA处于一定浓度范围内,体系的ΔIRLS与CMA的质量浓度呈线性关系,可用于卡马西平的定量测定。
可能的反应机理:从CMA、CPB及CMS的分子结构式(图2)可见,CMA上的氮原子可接受质子,以阳离子形式存在于溶液中;CPB分子结构上的Br-离去后以阳离子预胶束聚集体形式存在于溶液中;CMS分子结构上的Na+离去后以阴离子形式存在于溶液中。

图2 结构式Fig.2 Structural formula
带负电荷的CMS可聚集在带正电荷的CPB聚集体的表面,导致RLS信号急剧增强。可见,CMS不仅可与CMA反应还可与CPB反应,即体系中存在竞争反应。他们的可能反应为:带负电荷的CMS先与带正电荷的CPB以静电引力结合生成带负电荷的缔合颗粒,再与带正电荷的CMA结合(静电引力)生成电中性的三元离子缔合物;或CMS先与CMA以静电引力结合生成带负电荷的缔合颗粒,再与CPB结合(仍为静电引力)生成电中性的三元离子缔合物。无论以哪种方式结合,最终生成的三元离子缔合物有其较大的摩尔质量,导致RLS显著增强。
2.2 反应条件
2.2.1 介质及酸度
按1.4的实验方法分别考察了不同浓度的HCl、NaOH及不同pH的Tris-盐酸作介质时对体系ΔIRLS的影响。结果显示,用pH 3.46 Tris-盐酸作反应介质时体系有较大的ΔIRLS(见图3误差线图),且有较好的重现性。

图3 pH值的影响Fig.3 Effect of buffer pH on ΔIRLS
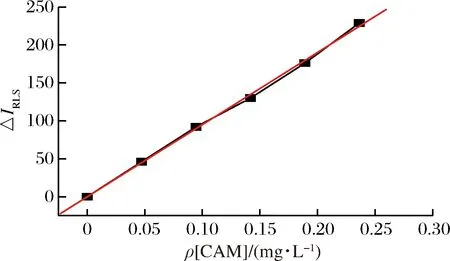
而用不同浓度的盐酸或NaOH作反应介质时,其体系的IRLS和试剂空白的I0均较小,ΔIRLS 2.2.2 CMS溶液的浓度 按1.4的实验方法,考察了不同用量的1.00×10-4mol/L CMS溶液对体系ΔIRLS的影响。结果显示,CMS溶液的浓度在2.2×10-5~ 2.8×10-5mol/L,体系有较大ΔIRLS(见图4误差线图)。 图4 考马斯亮蓝浓度对体系ΔIRLS的影响Fig.4 Effect of coomassie brilliant blue concentration on ΔIRLS 在此范围外,ΔIRLS均有不同程度的降低,灵敏度随之降低。降低原因:当CMS的浓度小于2.2×10-5mol/L时,CMA、CMS及CPB间的反应不完全,使ΔIRLS有所降低;当CMS的浓度大于2.8×10-5mol/L时,由于CMS分子间的聚集,使ΔIRLS降低。故实验选用CMS溶液的浓度为2.50×10-5mol/L(即取2.50 mL 1.00×10-4mol/L CMS溶液于10 mL比色管中)。 2.2.3 表面活性剂及用量 按1.4的实验方法,考察了阴离子表面活性剂(十二烷基硫酸钠、十二烷基磺酸钠)、阳离子表面活性剂(溴代十六烷基吡啶、溴化十六烷基三甲基铵) 及非离子表面活性剂(Tween-20、Triton X-100) 等对体系ΔIRLS的影响。结果显示,在浓度和用量相同的情况下,使用溴代十六烷基吡啶(CPB)作增敏剂有较好的效果,其ΔIRLS相对较高(ΔIRLS=205)。当5.00×102mg/L CPB的用量为0.30 mL时,体系的RLS信号相对最强,此时的ΔIRLS=225,体系有较高灵敏度,如图5所示。故实验用0.30 mL 5.00×102mg/L CPB溶液。 图5 CPB 溶液用量的影响Fig.5 Effect of CPB solution dosage on ΔIRLS 2.2.4 试剂加入顺序 考察了反应体系中各试剂加入顺序对体系ΔIRLS的影响。结果显示,试剂加入的最佳顺序为CMA、CMS、CPB、Tris-盐酸。按此顺序加入时,体系的RLS信号相对最强,ΔIRLS较大,灵敏度较高。故实验按试剂的最佳加入顺序进行。 2.2.5 反应时间及稳定性 按1.4的实验方法,考察了反应时间对体系ΔIRLS的影响,如图6所示。 图6 时间对ΔIRLS的影响Fig.6 Effect of time on ΔIRLS 结果显示,该体系在15 min内即可反应完全。15 min前,随着反应的进行,体系的ΔIRLS随时间增加而逐渐增大,曲线表现为一条逐渐上升的斜线,由此表明此时CMA、CMS及CPB间的反应并未完全;15 min后,体系的ΔIRLS随时间的增加不再增大,即ΔIRLS基本处于同一平台上,由此表明此时CMA、CMS及CPB间的反应已进行完全。故实验选在15 min后进行测定,稳定时间的1.5 h。 按1.4的实验方法,配制CMA标准系列溶液,扫描RLS光谱,以ΔIRLS为纵坐标,CMA的质量浓度ρ(mg/L)为横坐标,绘制344 nm波长处CMA的工作曲线,见图7。 图7 CAM 的工作曲线Fig.7 Working curve of carbamazepine 该工作曲线的线性回归方程为ΔIRLS=-0.194 2+951.0ρ,相关系数r=0.999 1,CMA在0.006~0.33 mg/L与ΔIRLS呈线性关系,检出限(3Sb/S)为0.005 6 mg/L,定量限为0.012 mg/kg。 考察了相对误差≤±5% 时,某些可能存在的干扰物质对测定0.236 mg/L CMA的影响,结果见表1。结果显示,氨基酸、糖类及常见阴、阳离子均不干扰测定,故该法有很好的选择性。 表1 共存物质的影响Table 1 Effect of coexistent substance 取1#~4# 待测液,按1.4实验方法,以样液代替标液,扫描RLS光谱。实验结果表明,在344 nm处,均未检出卡马西平。为了考察该方法的准确度和精密度,以空白肉样为样品,分别进行3个不同加标梯度(即不同水平)的回收试验,每个加标水平平行测定5份,最后根据回收率和相对标准偏差判断该方法的准确度和精密度,结果见表2。 在pH 3.46 Tris-盐酸及CPB存在下,以CMS作探针测定肉食品中痕量CMA的RLS法具有高的灵敏度和选择性、较高的准确度和精密度及较宽的线性范围。该法简便、快速,操作简单,所用仪器为一般的荧光分光光度计,易于普及。适于肉食品中残留CMA的测定。


2.3 工作曲线及相关参数
2.4 共存物质的影响

2.5 样品分析
3 结论

