PD-1抑制剂所致甲状腺毒症1例报告
孙潇泱, 蒋晶晶, 蔡青青, 余一祎, 刘天舒, 高 鑫*
1. 复旦大学附属中山医院内分泌科,上海 200032 2. 复旦大学代谢性疾病研究所,上海 200032 3. 复旦大学附属中山医院药剂科,上海 200032 4. 复旦大学附属中山医院肿瘤内科,上海 200032
近年来,随着抗肿瘤药物研发水平的迅速发展,新型抗肿瘤药物免疫检查点抑制剂(immune checkpoint inhibitors,ICIs)的应用越来越广泛。但此类药物应用的同时可能会造成免疫相关不良反应(immune-related adverse events,irAEs),常见的内分泌相关irAEs包括垂体炎、甲状腺功能障碍、糖尿病、肾上腺功能减退等[1]。所有ICIs单药治疗过程中,最易引起甲状腺功能障碍的是程序性死亡受体-1(programmed death-1, PD-1)抑制剂[2]。PD-1抑制剂主要包括纳武单抗(nivolumab)和帕博利珠单抗(pembrolizumab)。本文报告了1例转移性鳞癌患者应用PD-1抑制剂帕博利珠单抗过程中出现甲状腺毒症的临床表现和诊治情况,以提高临床对该类疾病的认识,提升诊治水平。
1 病例资料
1.1 一般资料 患者女,45岁,颈部淋巴结活检与PET/CT检查结果提示多发性转移性鳞癌,原发灶不明。2019年1月5日起开始肿瘤免疫治疗,使用PD-1抑制剂帕博利珠单抗(pembrolizumab),每21 d静脉注射1次,剂量为200 mg。患者首次用帕博利珠单抗18 d后出现胸闷、心悸、多汗、食欲增加。无腹泻、手抖及性格改变,体质量无明显变化。首次使用帕博利珠单抗之前,患者抗甲状腺球蛋白抗体(antithyroglobulin autoantibody,TgAb)阳性,甲状腺相关激素水平及其他自身抗体水平处于正常范围(表1)。甲状腺B超:甲状腺右叶40 mm×12 mm×12 mm,左叶36 mm×13 mm×12 mm,峡部2 mm。甲状腺内部回声均匀,甲状腺内血流分布尚正常。患者于2019年1月25日至我院肿瘤内科进一步治疗。体格检查:体温36.5℃,呼吸19次/min,血压130/84 mmHg(1 mmHg=0.133 kPa),心率105次/min,体质指数(body mass index, BMI)24.6 kg/m2。头部皮肤多汗,无眼睑水肿及突眼。甲状腺Ⅰ度肿大,质地软,触之无压痛,未及结节,未闻及震颤及血管杂音。心率105次/min,律齐,未闻及病理性杂音。肺部及腹部查体无特殊。手心多汗,双下肢无水肿。实验室检查:白细胞计数 4.29×109/L, 中性粒细胞0.69, 血红蛋白 126 g/L,血小板计数 167×109/L;白蛋白47 g/L,丙氨酸氨基转移酶31 U/L,门冬氨酸氨基转移酶 46 U/L,肾功能未见异常,葡萄糖6.1 mmol/L,糖化血红蛋白 5.5%。甲状腺功能相关指标见表1。
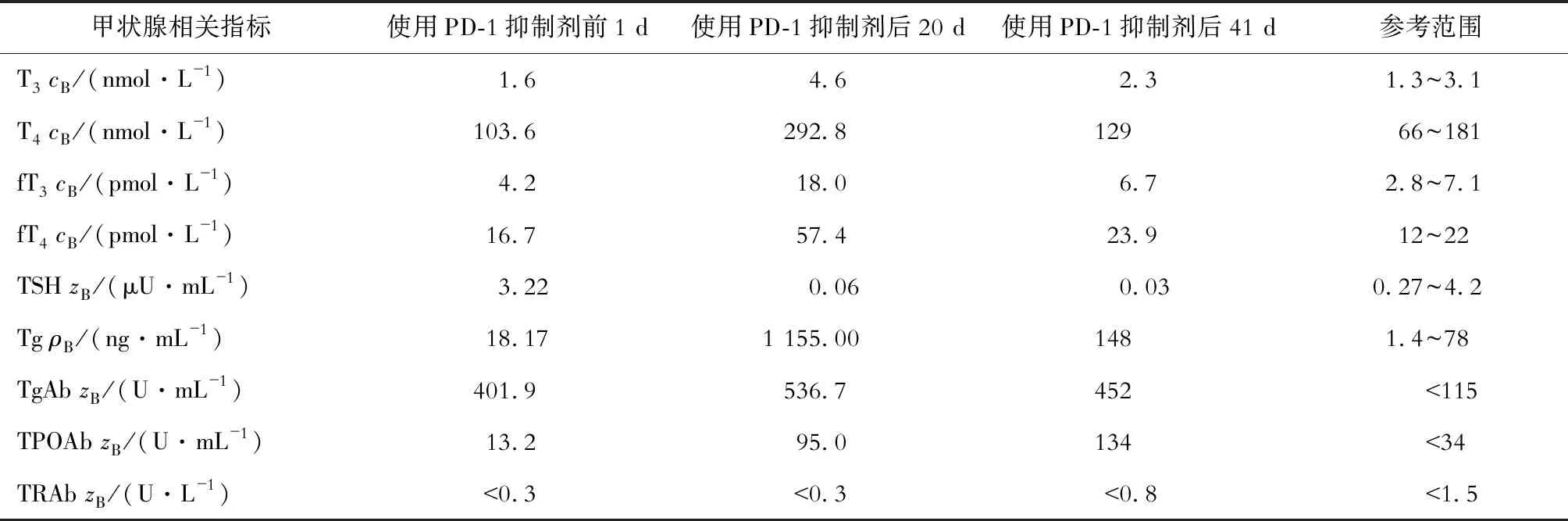
表1 该患者首次使用PD-1抑制剂前后的甲状腺功能相关指标
T3:三碘甲状腺原氨酸(triiodothyronine); T4:甲状腺素(thyroxine); fT3:游离三碘甲状腺原氨酸(free T3); fT4:游离甲状腺素(free T4); TSH:超敏促甲状腺激素(thyroid-stimulating hormone); Tg:甲状腺球蛋白(thyroglobulin); TgAb:抗甲状腺球蛋白抗体(antithyroglobulin autoantibody); TPOAb:抗甲状腺过氧化物酶抗体(antithyroid peroxidase autoantibody); TRAb:促甲状腺激素受体抗体(TSH receptor autoantibody)
1.2 诊断及治疗 患者用帕博利珠单抗前甲状腺激素水平正常,用该药后出现高代谢症候群,T3、T4、fT3、fT4明显升高,TSH降低,即出现甲状腺毒症。患者Tg明显升高,TgAb及TPOAb阳性,TRAb阴性,病因考虑为PD-1抑制剂诱发的自身免疫性甲状腺炎。2019年1月26日起给予美托洛尔片25 mg 每日3次口服改善临床症状,帕博利珠单抗治疗方案不变。治疗3周后至我院随诊,心悸、多汗等症状好转,心率控制在80次/min,复查甲状腺相关指标的结果见表1,目前仍规律随访中。
2 讨 论
本文报告了1例甲状腺毒症患者,其病因考虑为PD-1抑制剂诱发的自身免疫性甲状腺炎。ICIs可使免疫系统过度激活,损伤正常内分泌腺体组织,其中甲状腺较易受累[1]。PD-1抑制剂引起的甲状腺相关不良反应中,甲状腺功能亢进(简称甲亢)、甲状腺功能减退(简称甲减)和自身免疫甲状腺炎均有报道。PD-1抑制剂引起甲减的发生率约7.2%,而甲亢的发生率约3.1%[3]。其中帕博利珠单抗引起的甲减发生率与纳武单抗相似(7.9%vs6.5%),而甲亢发生率显著高于纳武单抗(3.8%vs2.5%,P=0.04)[3]。而PD-1抑制剂引起的甲状腺炎报道较少。一项对93例应用帕博利珠单抗的患者的回顾性分析显示,甲状腺炎的发生率为7.5%[4]。纳武单抗诱发甲状腺炎的发生率则为6.1%[5]。本例患者的病因考虑为自身免疫性甲状腺炎,因为其发生甲状腺毒症时伴随TgAb及TPOAb阳性,TRAb阴性。在后一次随访中患者T3、T4、fT3、fT4水平均较上一次明显下降,甲状腺毒症减轻,符合甲状腺炎引起的甲状腺毒症常为一过性的特点。为进一步鉴别诊断自身免疫甲状腺炎与Grave病,应行甲状腺131I摄碘率检查。而本例患者在肿瘤诊断过程中曾行增强CT检查,碘造影剂的使用可能影响甲状腺131I摄碘率检查的准确性[1],故未进行该项检查。值得注意的是,本例患者在帕博利珠单抗治疗后18 d即发生了甲状腺毒症,略早于既往文献[6]报道的21~59 d(中位时间32 d)。这提示在使用帕博利珠单抗后应尽早开始监测甲状腺激素水平。
PD-1抑制剂引起甲状腺炎的发病机制尚不明确。本例患者在帕博利珠单抗治疗后Tg水平明显增加,说明甲状腺受到了较严重的炎症损伤。帕博利珠单抗治疗后TPOAb转为阳性,TgAb水平较基线进一步升高,与甲状腺毒症同时发生,提示甲状腺自身抗体可能参与了PD-1抑制剂引起的甲状腺炎的发生发展。但也有研究[4]认为PD-1抑制剂引发甲状腺功能障碍的机制涉及T细胞、自然杀伤细胞及单核细胞相关通路,而与甲状腺自身抗体无关。根据该领域首个多学科指南《免疫检查点抑制剂引起的内分泌急性并发症管理》(2018年)[7],使用β受体阻滞剂改善患者心悸等症状。大多数ICIs引起的甲状腺功能障碍均较轻微,无需因此调整ICIs用药[2]。随访至目前,该患者的甲状腺毒症已持续21 d,而帕博利珠单抗引起的甲状腺毒症可持续21~60 d(中位时间27 d)[6]。使用PD-1抑制剂的患者经历甲状腺毒症之后,其甲状腺功能可能恢复正常[4,6],但更多转归为甲减[6,8-9]。因此应继续观察本例患者甲状腺功能的变化,若转归为甲减,则应根据临床症状和TSH水平考虑长期采用甲状腺激素替代治疗[10]。开始甲状腺激素替代治疗之前应排除肾上腺皮质功能减退症[7]。
该病例提示临床需提高对PD-1抑制剂引起的甲状腺功能障碍的认识,对该类患者的管理需加强多学科合作。在用PD-1抑制剂之前,若有条件应行甲状腺自身抗体检查及甲状腺131I摄碘率检查;用药后应加强监测甲状腺相关指标,尤其在治疗最初1~2个月,以及时发现、鉴别甲状腺功能异常的病因,给予适当治疗,改善患者预后。

