不同剂量脐带间充质干细胞在针刀镜下定植治疗强直性脊柱炎患者病变髋关节的临床观察
曲海洪,李晓昊,张军
1.广州莱德尔生物科技有限公司,广东 广州 510643;2.中国人民解放军南部战区总医院,广东 广州 510000;3.暨南大学,广东 广州 510632
强直性脊柱炎是临床常见的慢性炎性脊柱关节病[1],以侵犯骶髂关节和中轴关节为特征[2],好发于年轻人,约有1/3患者可因髋关节受累而致残[3],目前尚缺乏有效治疗措施。本课题组应用微创针刀镜联合脐带间充质干细胞定植治疗AS髋关节病变患者30例,并随访至24周,旨在研究治疗前后各组别AS患者病变髋关节功能和疾病相关炎性指标的变化,比较不同剂量组脐带间充质干细胞的疗效及评估不同组别安全性。
1 资料与方法
1.1 诊断标准 参照ACR/EULER2009强直性脊柱炎分类诊断标准[4]。
1.2 纳入标准 ①符合AS诊断标准;②有单侧或双侧髋关节疼痛症状,按照Bath AS异常髋关节X线分类标准[5]骨盆平片符合II级-III级损害特征或是骨盆平片符合0级-I级损害特征并且髋关节MRI提示滑膜炎并对应关节腔存在积液;③入组前经正规治疗6个月以上,未能控制髋关节症状;④年龄18-60岁;⑤患者知情同意。
1.3 排除标准 ①不符合病例纳入标准者;②妊娠期或近期准备妊娠妇女,哺乳期妇女;③有严重心、脑、肾、血液系统原发疾病者;④同时患有其他血清阴性脊柱关节病或合并其他风湿免疫系统疾病者;⑤传染病患者,或近期与传染病患者有密切接触者;⑥精神病患者;⑦对人血白蛋白和脐带间充质干细胞培养体系主要成分如青霉素、链霉素过敏者。
1.4 一般资料 选取2016年5月-2017年5月于南部战区总医院中医风湿科住院治疗的符合纳入标准的AS患者共30例,其中男20例(29髋),女10例(16髋),年龄18-41岁,平均(28.10±7.58)岁;病程7-85个月,平均(26.73±21.22)月。
1.5 脐带间充质干细胞分离和培养[6]经南部战区总医院伦理委员会批准,选取南部战区总医院妇产科健康剖腹产产妇(经检测其乙肝抗原、抗HCV抗体、抗HIV抗体、抗梅毒螺旋体抗体、支原体、抗巨细胞病毒抗体等均为阴性,孕期各项检查包括TORCH、唐氏筛查等均正常,经孕产妇及家属同意且签署自愿捐献脐带志愿书),选取经腹剖腹产新生儿脐带,自手术台上取下脐带后,用含抗生素的生理盐水浸泡,保持4 ℃恒温储存。在洁净操作台中将脐带用PBS反复冲洗,洗净残余血液后用剪刀和止血钳剔除脐静脉、脐动脉并剪碎。随后将其置入体积相同的II型胶原酶于37 ℃恒温消化2-3小时,待上述物质呈现胶冻状态,再采用PBS将其稀释为50 mL,用离心机离心5分钟,静止后取上清液,再次离心5分钟后,弃其上清液,采用Stem cells专用培养基重悬其沉淀物,移入6孔板中。隔2日换液1次。在显微镜下观察其细胞覆盖80%的培养瓶底时传代,移除旧的培养液,采用PBS洗涤3次。取1 mL的0.25%胰蛋白酶消化液进行消化,显微镜下观察到细胞突起消失、细胞变圆即加入培养液使消化终止。将贴壁细胞吹打为单细胞悬液,采用一定比例进行分瓶传代,调整恒温培养箱参数为37 ℃并5%CO2,将细胞置于其中进行培养。第2日更换培养液后将检测合格的培养细胞收集成MSCs悬液,分别为:低剂量MSCs组20 mL(含MSCs数为0.7×107-1×107个)、中剂量组30 mL(含MSCs数为1.4×107-2×107个)、高剂量组40 mL(含MSCs数为2×107-3×107)。
1.6 治疗方案[6]按手术流程进行术前准备,患者取可保持患侧髋关节伸展的平卧位,以前入路口为手术入口,取15 mL利多卡因行局麻后,用手术刀切开前入路口皮肤,再用平刀逐层切开皮下筋膜层、肌层及关节囊。换用钝性拨针进行扩口和疏通,建立手术通路,将针刀镜合体套管置入,待其抵达关节面拔出套管芯,将针刀合体光镜置入,打开灌洗液连接通道后将灌洗液灌入。于镜下观察髋臼及股骨头病变情况,清理病变滑膜组织及软骨碎屑,修整髋臼及股骨头坏死骨面,反复以生理盐水进行冲洗。再采用自主研发的4毫米克氏针以多方向扇形在避开正常软骨面的情况下钻入骨坏死区。于可视微创针镜引导下,采用套筒器械把各剂量组MSCs悬液分别注入钻孔区域。然后拔除关节腔内器械,将腔内积液清除,活动患肢无异常后行术口缝合,覆盖无菌纱布并以弹力绷带进行包扎。术后须将制动患肢1日,一般无需行围手术期抗生素治疗。
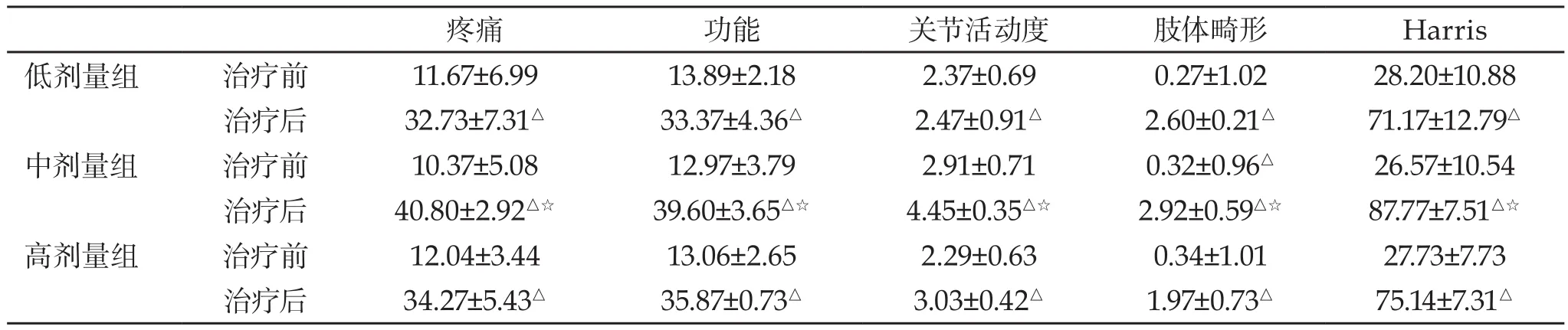
表1 不同剂量组治疗前后Harris评分(Mean±SD)
1.7 观察项目和检测方法
1.7.1 髋关节功能评估 分别在治疗前、治疗后6月进行Harris髋关节评分[7]。
1.7.2 AS疾病炎性指标 分别在治疗前、治疗后6月抽取患者静脉血检测血沉(ESR)、C-反应蛋白(CRP)水平。
1.8 评估治疗方案安全性 分别于治疗前、治疗后1月、3月、6月检测患者三大常规及生化指标,行心电图检查,并及时记录研究中的不良事件。
1.9 数据统计方法 用SPSS 17.0统计软件进行数据分析:用(Mean±SD)表示计量资料,组间同一时间节点比较及同组中治疗前后的比较,采用t检验处理符合正态分布的数据,采用非参数检验处理不符合正态分布的数据。
2 结果
2.1 一般资料 本研究纳入36例伴有髋关节病变AS患者,全部完成观察,无一脱落、剔除。
2.2 患者髋关节功能评估 治疗6月后,低、中、高剂量组患者疼痛、功能、关节活动度、肢体畸形及Harris总分均较治疗前有明显升高,差异有统计学意义(P<0.05)。中剂量组治疗后疼痛、功能、关节活动度、肢体畸形及Harris总分高于低剂量组、高剂量组(P<0.05),三组治疗前各评分差异无统计学意义(P>0.05)(见表1)。
2.3 患者炎症指标评估 治疗6月后,低、中、高剂量组别患者的相关炎性指标(血沉、C反应蛋白)水平较治疗前均有明显降低,其差异具有统计学意义(P<0.05)。其中,中剂量组别治疗后的ESR、CRP水平低于低剂量组、高剂量组(P<0.05),三组治疗前ESR、CRP水平差异无统计学意义(P>0.05)(见表2)。
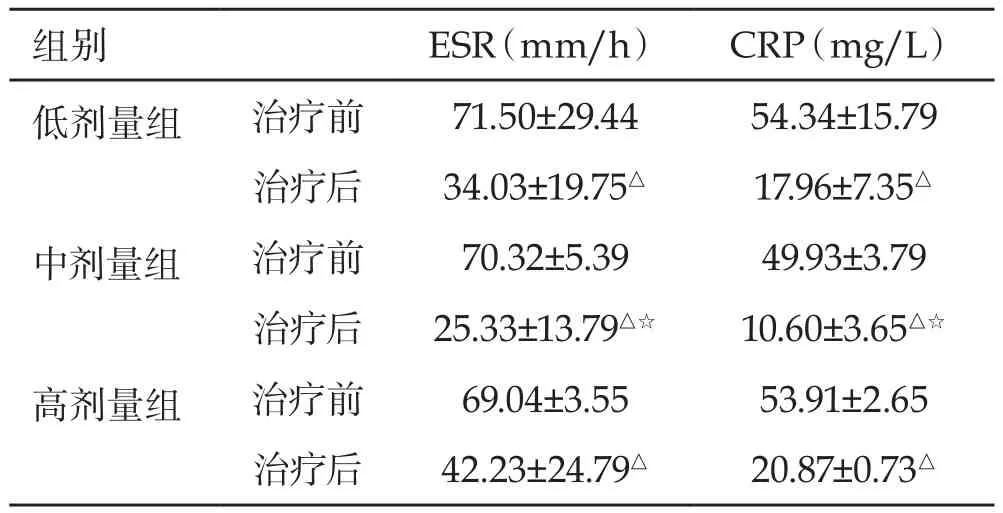
表2 不同剂量组治疗前后ESR、CRP水平比较(Mean±SD)
2.4 不良反应 监测36例患者心电图、血常规、肝肾功能等指标,均未见异常。有2例患者术后出现伤口局部红肿、愈合延迟,给予换药护理后,术口愈合。
3 讨论
AS髋关节早期病变以滑膜炎症为主,病理显示滑膜增生、淋巴样浸润及血管翳形成,接着血管翳可逐渐覆盖软骨使其变性和降解,形成骨破坏,损害关节功能[7]。由于缺乏血管,髋关节软骨组织损伤后难以再生修复。
目前并无特异性有效治疗措施[8],近年来间充质干细胞的研究成为热点。MSCs自我更新以及在特定微环境下多向分化的生物特性,成为当前修复软骨缺损、恢复关节结构并促进关节功能恢复、阻断骨破坏有效治疗策略之一。然而,在干细胞移植的方法和干细胞的临床治疗剂量上还没有形成固定的标准。局部移植在准确性及安全性方面均优于静脉移植,但局部移植,通常为关节腔注射,也同样面临一些问题,如:种子细胞的主动转运和归巢能力不足,难以附着在软骨损伤部位发挥修复作用,并且关节液的流动性和稀释作用也可能影响种子细胞在损伤部位的定植,从而治疗效果受到影响[9]。其次,粘附于其他部位的细胞,或者游离于关节液中,还可能诱发炎性反应,引起滑膜增生,形成游离体、瘢痕组织等,增加了并发症的风险。第三,AS患者关节腔内为炎性环境[10],不仅影响MSCs的软骨形成能力,还可能引起新生软骨的降解。因此,如何将种子细胞在良好的环境下精确、高效地定植于目标区域,需要临床上探索出一种新的技术。
微创针刀镜技术,为南部战区总医院中医风湿科韦嵩教授及其团队的原创技术,该技术以《内经》“九针十二原”等篇章为基础,结合现代医学“内窥镜”技术,通过自主研发的系列微型器械在可视条件下进行组织微透析、灌洗、关节腔内滑膜组织清理等操作,可改善腔内炎性环境[11]。我们将此项技术用于探索AS髋关节病变不同剂量干细胞局部定植,临床结果显示,治疗后6月,低、中、高剂量组患者疼痛、功能、关节活动度、肢体畸形及Harris评分均较治疗前升高,且中剂量组治疗后疼痛、功能、关节活动度、肢体畸形及Harris总分高于低剂量组、高剂量组;治疗6月后,低、中、高剂量组患者ESR、CRP水平均较治疗前有明显下降,且中剂量组治疗后ESR、CRP水平低于低剂量组、高剂量组。低、中、高剂量组安全性评价指标均为出现异常。
综上所述,不同剂量组MSCs于微创针刀镜可视条件下定植治疗AS病变髋关节对髋关节功能的改善和疾病炎性指标的降低方面均有积极意义,具有良好的临床疗效和安全性。其中中剂量组可以更加迅速缓解患者临床症状,更大幅度地降低疾病活动度,更好地改善病变髋关节活动功能,是临床治疗的较佳剂量。

