当归调经颗粒(无糖型)的质量标准研究
唐靖雯 卢礼平 李娇娇 杨桃 潘梅

【摘 要】目的:建立当归调经颗粒(无糖型)的质量标准,有效地控制产品质量。方法:采用薄层色谱法对制剂中当归、川芎、甘草、黄芪、白芍进行定性鉴别,以白芍中芍药苷作为指标性成分,采用高效液相色谱法测定其含量。色谱柱为Agilent TC-C18(250mm×4.6mm,5μm),流动相为乙腈-0.1%磷酸溶液(12∶ 88),流速为1.0mL/min,检测波长为230 nm,柱温为25 ℃,进样量为10μL。结果:当归、川芎、甘草、黄芪、白芍的TLC法鉴别专属性强,且阴性均无干扰;含量测定结果显示,芍药苷浓度在(4.38~140.16)μg/mL内与峰面积呈良好的线性关系(r=0.9998),平均加样回收率为99.45%,RSD=1.97%(n=6)。结论:该方法操作简单、结果准确、专属性强、重复性好,可用于当归调经颗粒(无糖型)的质量控制。
【关键词】当归调经颗粒(无糖型);质量标准;薄层色谱法;高效液相色谱法
【中图分类号】R284【文献标志码】A【文章编号】1007-8517(2019)20-0040-05
Abstract:Objective The quality standard of Angelica regulating granule (sugar-free type) was established to effectively control the quality of products.Methods TLC was used to identify the radix angelicae sinensis, rhizoma chuanxiong, radix glycyrrhiza root, radix astragalus root and radix paeoniae alba. The content of paeoniflorin in radix paeoniae alba was determined by HPLC. The column was Agilent TC-C18(250 mm×4.6mm,5μm), the mobile phase was acetonitrile-0.1% phosphoric acid solution (12∶ 88, V/V), the flow rate was 1.0mL/min, the detection wavelength was 230nm, the column temperature was 25℃, and the injection volume was 10μL.Results The TLC method of angelica sinensis, ligusticum chuanxiong, licorice root, astragalus root and paeoniae alba has strong specificity and no interference. The results showed that the concentration of paeoniflorin in (4.38 ~ 140.16)μg/mL had a good linear relationship with the peak area (r=0.9998), and the average recovery rate was 99.45%, RSD=1.97% (n=6).Conclusions The method is simple, accurate, specific and repeatable, and can be used for the quality control of Angelica regulating granule (sugar-free type).
Keywords:Angelica regulating granule(sugar-free type);Quality standards;TLC;HPLC
当归调经颗粒由当归、熟地黄、川芎、党参、白芍、甘草、黄芪等7味药材组成,收载入《中国药典》2015年版。具有补血助气、调经的功效,用于贫血衰弱、病后、产后血虚以及月经不调、痛经。本研究在当归调经颗粒含糖型基础上,完成了其无糖型产品的质量标准研究并建立了企业内控质量标准,为广大患者提供了一个治疗痛经的产品。为保证临床用药的安全、有效以及更好地控制产品质量,本研究采用薄层色谱法对制剂中当归、川芎、甘草、黄芪、白芍等5味药材进行定性鉴别;建立了以制剂中白芍的主要活性成分芍药苷为指标性成分的HPLC含量測定方法。
1 仪器与材料
1.1 仪器 Agilent 1260高效液相色谱仪,包括二极管阵列检测器、ChemStation色谱工作站、1200型自动进样器(美国Agilent公司);AG135型电子天平(瑞士Mettler-Toledo公司);CH-250型超声波清洗机(天津恒奥科技公司,功率:250W,频率:40KHz);硅胶G(青岛海洋化工厂分厂,批号:20150701)。
1.2 药品与试剂 无糖型当归调经颗粒(批号:170501、170502、170503,贵州威门药业股份有限公司);芍药苷对照品(批号:110736-201741,中国食品药品检定研究院);磷酸(批号:10015408,国药集团化学试剂有限公司);乙腈为色谱纯;乙酸乙酯、三氯甲烷、冰醋酸、环己烷、无水乙醇均为分析纯;水为超纯水。
2 方法与结果
2.1 定性鉴别
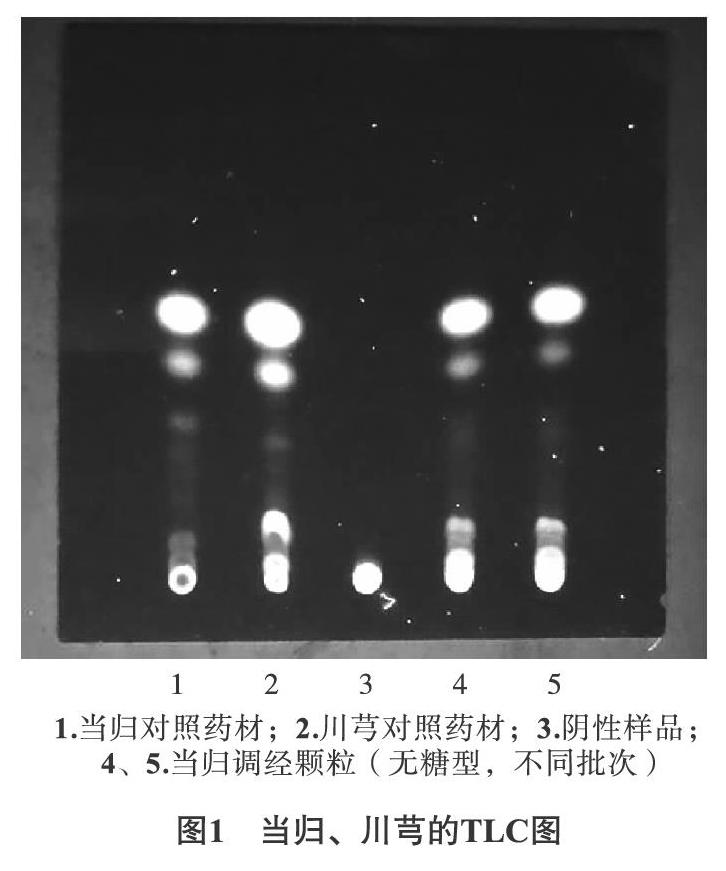
2.1.1 当归、川芎的鉴别 取本品10 g,研细,加水30 mL使溶解,用乙醚振摇提取2次(水液备用),每次使用20mL,将两次乙醚提取液合并,挥干乙醚提取液,残渣加lmL甲醇使完全溶解,作为供试品溶液。分别取当归、川芎药材,按照供试品溶液的制备方法分别制成当归、川芎对照药材溶液。另按制剂的处方比例称取适量缺当归、川芎药材的其他各味药材,按该制剂的制备工艺制成颗粒,取颗粒适量,按上述制备供试品溶液的操作方法制成缺当归、川芎药材的阴性样品。照薄层色谱法(2015年版中国药典四部,通则0502),分别依次吸取上述当归对照药材、川芎对照药材、阴性样品、供试品溶液各4μL,分别依次点于同一硅胶G薄层板,选用正己烷-二氯甲烷-乙酸乙酯-甲酸(4∶ 1∶ 1∶ 0.1)的溶液为展开剂进行展开,取出硅胶板后放置晾干,将晾干的硅胶G薄层板置紫外光灯(365nm)下检视。结果,当归的TLC图中,不同批次供试品溶液所呈现的斑点完全一致,在与对照药材色谱相应的位置上显相同颜色的荧光斑点,且阴性无干扰。如图1所示。
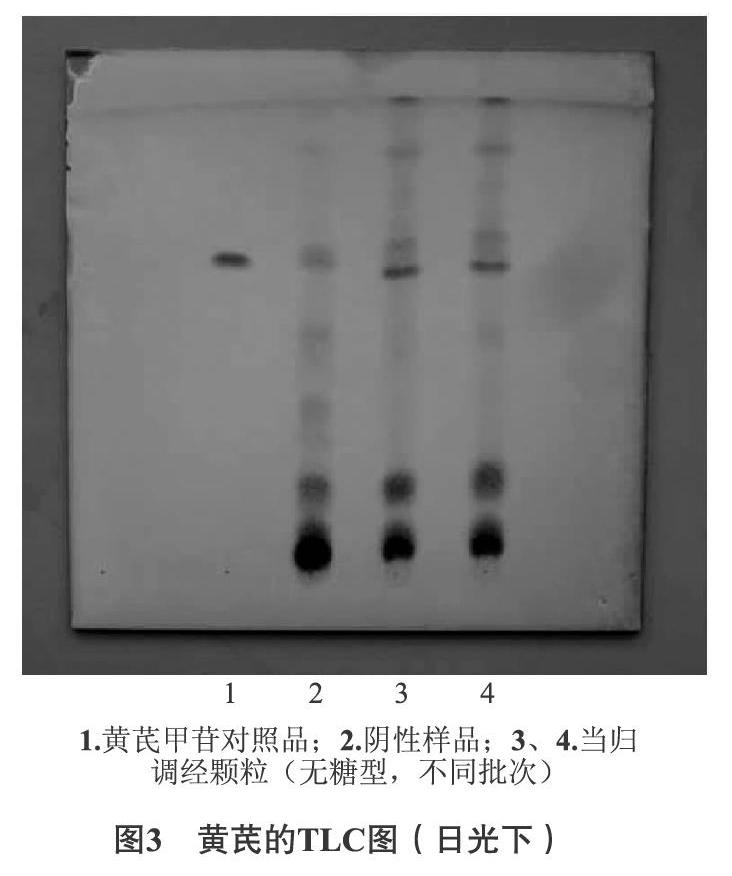
2.1.2 甘草的鉴别 取本品10g,研细,加乙醚40mL,超声处理30min,滤过,弃去乙醚液,残渣挥干乙醚,加水40mL使溶解,用水饱和的正丁醇振摇提取2次,每次30mL,合并正丁醇液,用正丁醇饱和的水洗涤2次,每次20mL,分取正丁醇液,回收溶剂至干,残渣加甲醇lmL使溶解,作为供试品溶液。另取甘草药材及缺甘草的阴性样品适量,按上述供试品溶液的制备方法分别制成甘草对照药材溶液、缺甘草的阴性样品溶液。照薄层色谱法(2015年版中国药典四部,通则0502),分别吸取上述甘草对照药材、阴性样品、供试品溶液各6μL,分别依次点于同一硅胶G薄层板,选用乙酸乙酯-甲酸-冰醋酸-水(15∶ 1∶ 1∶ 2)的溶液为展开剂进行展开,取出硅胶板后放置晾干,将晾干的硅胶G薄层板置紫外光灯(365nm)下检视。结果,当归的TLC图中,不同批次供试品溶液所呈现的斑点完全一致,且阴性无干扰。如图2所示。2.1.3 黄芪的鉴别 取“2.1.1”项下的备用水溶液,用水饱和的正丁醇振摇提取2次,每次30mL,合并正丁醇提取液,用氨试液洗涤2次,每次20mL,分取正丁醇液,回收溶剂至干,残渣加甲醇l mL使溶解,作为供试品溶液。取黄芪甲苷对照品,加甲醇制成每lmL含0.5mg的溶液,作为对照品溶液。另取缺黄芪的阴性样品适量,按上述供试品溶液的制备方法制成缺黄芪的阴性样品溶液。照薄层色谱法(2015年版中国药典四部,通则0502),分别吸取上述黄芪苷对照品、阴性样品、供试品溶液各6μL,分别依次点于同一硅胶G薄层板,选用三氯甲烷-甲醇-水(13∶ 7∶ 2)的下层溶液作为展开剂,取出硅胶板后放置晾干,喷以10%硫酸乙醇溶液,在105℃加热至斑点显色清晰,分别在日光及紫外光(365nm)下检视。结果,黄芪的TLC图中,不同批次供试品溶液所呈现的斑点完全一致,日光下显相同颜色的斑点,紫外光下显相同颜色的荧光斑点,且阴性无干扰。如图3、图4所示。
2.1.4 白芍的鉴别 取本品10g,加乙醇10mL,振搖5min,滤过,滤液蒸干,残渣加乙醇lmL使溶解,作为供试品溶液。取芍药苷对照品,加乙醇制成每lmL含lmg 的溶液,作为对照品溶液。另取缺白芍的阴性样品适量,按上述供试品溶液的制备方法制成缺白芍的阴性样品溶液。照薄层色谱法(2015年版中国药典四部,通则0502),分别吸取上述芍药苷对照品、阴性样品、供试品各10μL,分别依次点于同一硅胶薄层板,选用三氯甲烷-乙酸乙酯-甲醇-甲酸(40∶ 5∶ 10∶ 0.2)为展开剂进行展开,取出硅胶板后放置晾干,喷以5%香草醛硫酸溶液,加热至斑点显色清晰。结果,白芍的TLC图中,不同批次供试品溶液所呈现的斑点完全一致,与芍药苷对照品相应的位置上,显相同的斑点,且阴性无干扰。如图5所示。
2.2 芍药苷的含量测定
2.2.1 色谱条件 色谱柱:Agilent TC-C18(250mm×4.6mm,5μm);乙腈-0.1%磷酸溶液(12∶ 88,V/V);流速:1.0mL/min;检测波长:230nm;柱温:25℃;进样量:10μL。
2.2.2 溶液的制备
2.2.2.1 供试品溶液[2] 取装量差异项下的本品,研细,从中取约2.5 g药物粉末,精密称定,置具塞锥形瓶中,精密加入70%乙醇10 mL使溶解,密塞,称定重量,超声处理(功率250 W,频率50 kHz)30 min,放冷,再称定重量,用70%乙醇补足减失的重量,摇匀,滤过,取续滤液,即得。
2.2.2.2 对照品溶液 取芍药苷对照品适量,精密称定,用甲醇配制成每1 mL含35 μg的溶液,既得。
2.2.2.3 缺白芍的阴性样品 按处方称取缺白芍的群药,按上述供试品溶液的制备方法制成缺白芍的阴性样品溶液。
2.2.3 系统适用性试验[3-5] 精密吸取“2.2.2”项下对照品溶液、供试品溶液、缺白芍的阴性样品溶液各10 μL,按“2.2.1”项下色谱条件进行测定。理论板数按芍药苷峰计算>3000,分离度>1.5。色谱如图6所示。
2.2.4 线性关系 取芍药苷对照品适量,精密称定,用甲醇溶解并稀释制成0.2192mg/mL的溶液,分别精密量取0.5、1、2、4、8、16μL至25mL的容量瓶中,加甲醇稀释刻度。按“2.2.1”项下色谱条件,各进样10μL,记录峰面积,以各对照品溶液的浓度为横坐标,峰面积为纵坐标绘制标准曲线,进行线性回归。回归方程:A= 14.254C-25.694,r=0.9998。结果表明,对照品溶液浓度在(4.38~140.16)μg/mL范围内,与峰面积呈良好的线性关系。
2.2.5 精密度试验 取样品(批号170501),按“2.2.2”项下方法制成供试品溶液,精密吸取10 μL,按“2.2.1”项下色谱条件重复进样6次,记录芍药苷的峰面积。结果,峰面积RSD为0.28%,表明仪器精密度较好。
2.2.6 稳定性试验 取样品(批号170501),按“2.2.2”项下方法制成供试品溶液,按“2.2.1”项下色谱条件,分别于0、2、4、6、8、10h进样测定记录色谱峰。结果,峰面积的RSD为1.72%,表明供试品溶液在10h内稳定。
2.2.7 重复性试验 取同一批样品(批号170501)6份,精密称定,按“2.2.2”项下方法制成供试品溶液,按“2.2.1”项下色谱条件进行测定,以外标一点法计算芍药苷的含量。结果,含量的RSD为1.96%,表明本方法的重复性良好。
2.2.8 加样回收率试验 取已知芍药苷含量的当归调经颗粒(无糖型,批号:170501,含量为0.3427mg/g),采用加样回收法,测定本方法的回收率。精密称取本批次当归调经颗粒1.25g,分别精密吸取芍药苷对照品溶液(35.20μg/mL)10 mL,按“2.2.2”项下的方法制成供试品溶液,按“2.2.1”项下色谱条件,计算白芍苷的加样回收率,结果详见表1。
2.2.9 样品含量的测定 取3批样品(批号170501、170502、170503)各适量,按 “2.2.2”项下方法制成供试品溶液,精密吸取10 μL注入HPLC仪,按“2.2.1”项下色谱条件记录色谱图;另取“2.2.2”项下对照品溶液,同法测定。按外标法以峰面积计算供试品的含量,结果详见表2。
3 讨论
研究对制剂中当归、川芎进行TLC 定性鉴别时,按照文献方法:分别用正己烷-乙酸乙酯(9∶ 1)、正己烷-乙酸乙酯(4∶ 1)作为展开剂进行TLC定性鉴别,结果供试品色谱中均未显示斑点。在多次尝试的基础下发现,以两种溶剂作为展开剂时始终无法获得理想的展开效果,故最终选择采用正己烷-二氯甲烷-乙酸乙酯-甲酸(4∶ 1∶ 1∶ 0.1)的4种溶剂作为展开剂,所得的供试品色谱中斑点也较为清晰。
制劑中当归、白芍的主要活性成分分别为阿魏酸、芍药苷,在含量测定的指标性成分如何选取过程中,考虑到君药当归中阿魏酸含量较低,故选择含量较高、成分较稳定的活性成分芍药苷作为指标性成分,采用高效液相色谱法测定白芍中芍药苷的含量。但由于中药制剂成分复杂且该制剂中白芍所占比例小等因素,仅以白芍中芍药苷作为指标性成分来控制该制剂质量明显不足,因此在后续的研究中,应优化臣药中阿魏酸的提取方法,增加制剂中阿魏酸提取量,建立多指标性成分的含量测定方法,以更有效地控制该制剂的质量。
综上,本研究建立的质量控制分析方法,经过对多批产品的验证,结果表明该质量控制方法简便、准确,可用于当归调经颗粒(无糖型)生产过程质量控制,能有效地保证产品临床用药的安全性、有效性和可控性。
参考文献
[1]卫生部药典委员会.中华人民共和国卫生部药品标准[S].北京:人民卫生出版社,1998 : 165.
[2]国家药典委员会.中华人民共和国药典(一部)[S].北京:中国医药科技出版社,2015:842-843.
[3]叶丛丛,傅红兴,周伟忠,等.RH-HPLC法同时测定自制复方雷帕霉素栓剂中雷帕霉素和他克莫司的含量[J].中国药房,2015,26(3): 388.
[4]许舒瑜,彭军,陈小玲,等.金牧感冒片的质量标准研究[J].中国药房,2014, 25(39):3682.
[5]丁菊英,夏晓君,黄新刚,等.清肺止咳胶囊的质量标准研究[J].中国药房,2014,25(27): 2553-2556.
(收稿日期:2019-08-29 编辑:陶希睿)

