白藜芦醇聚合物胶束的制备及质量评价
周韵秋,冀素平,刘聪,颜雄,典灵辉
论著
白藜芦醇聚合物胶束的制备及质量评价
周韵秋,冀素平,刘聪,颜雄,典灵辉
523808 东莞,广东医科大学药学院
制备白藜芦醇(RES)聚合物胶束并对其进行质量评价。
采用薄膜分散法,以聚乙烯己内酰胺-聚乙酸乙烯酯-聚乙二醇接枝共聚物(SPS)和 D-α 生育酚聚乙二醇 1000 琥珀酸酯(TPGS)为载体材料,制备白藜芦醇聚合物胶束(RES-SPS-TPGS-PMs);采用纳米粒度分析仪、差示扫描量热法(DSC)及傅立叶变换红外光谱法(FTIR)对其进行表征;采用高效液相色谱法测定聚合物胶束的包封率和载药量;采用动态膜透析法考察载药胶束的体外释放特性。
制备的胶束平均粒径为(52.4 ± 0.66)nm,多分散指数为 0.06 ± 0.01,包封率为(97.12 ± 9.08)%,载药量为(2.37 ± 0.22)%。白藜芦醇在聚合物胶束中可能以无定型或分子的形式存在,且白藜芦醇与载体材料之间形成了氢键。体外释放结果表明白藜芦醇聚合物胶束具有明显的缓释效果。
该胶束制备工艺简单,其粒径、包封率、载药量可控,具有缓释作用。
白藜芦醇; 聚合物胶束; Soluplus; 质量评价; 体外释放
白藜芦醇(resveratrol,RES)是一种天然的多酚类化合物,富含于葡萄、花生和浆果等[1-3],具有抗氧化、抗炎、抗癌、抗糖尿病、抗衰老和心脏保护的作用[2-4]。但由于其疏水性导致口服生物利用度低,严重影响临床应用[5-6]。有报道采用不同的方法提高其口服生物利用度,比如制备成脂质体、固体分散体、纳米乳剂等,但作用效果不显著。聚合物胶束是一种新型的口服递药系统,倍受广泛关注。聚合物胶束具有核-壳结构,疏水性内核可以包载疏水性药物,增加药物的稳定性[7]。胶束材料具有较小的纳米尺寸,可通过肿瘤组织的 EPR 效应(enhanced permeability and retention effect)在肿瘤部位蓄积,从而实现药物的被动靶向[8]。聚合物胶束具有良好的稳定性,尤其是两亲性结构的聚乙烯己内酰胺-聚乙酸乙烯酯-聚乙二醇接枝共聚物形成的胶束Soluplus。Soluplus 具有较低的临界胶束浓度值(CMC)(约 10-8mol/L),当其浓度超过 CMC 时,会自动形成胶束,将疏水性药物包载在疏水核心,进而提高胶束的包封率和载药量,并且其分子结构中羰基与药物分子的羟基形成氢键,大大提高胶束的稳定性[9-10]。D-α 生育酚聚乙二醇 1000 琥珀酸酯(TPGS)具有促口服吸收作用[11],可作为混合胶束材料。因此本实验以 Soluplus 和 TPGS 为纳米载体材料,采用薄膜分散法制备功能化的白藜芦醇混合胶束,并对其进行体外质量评价,为后期体内研究提供理论基础。
1 材料与方法
1.1 材料
1.1.1 试剂 白藜芦醇(纯度≥ 99%)购自上海麦克林生化科技有限公司;Soluplus 购自德国 BASF 公司;TPGS 购自美国 Sigma 公司;甲醇(色谱纯)购自天津市四友精细化学品有限公司;其他试剂均为分析纯;超纯水自制。
1.1.2 仪器与设备 SZ-100 纳米粒度分析仪购自日本 Horiba 公司;UV-650 紫外可见分光光度计购自上海美谱达仪器有限公司;Agilent 1260 高效液相色谱仪购自美国安捷伦科技有限公司;Scientz-10ND 普通型冷冻干燥机购自宁波新芝生物科技股份有限公司;Discovery DSC25 热分析仪购自美国 TA Instruments 公司;WQF-510A 傅立叶变换红外光谱仪购自北京瑞利分析仪器有限公司。
1.2 方法
1.2.1 白藜芦醇聚合物胶束的含量测定方法

1.2.1.2 白藜芦醇标准曲线的建立 精密称量白藜芦醇 5.0 mg,用甲醇溶解并定容至 50 ml,配制成 100 μg/ml 的溶液作为储备液。吸取白藜芦醇储备液适量,用甲醇分别稀释成 1、2、5、10、20、30、40、50、100 μg/ml 的工作液,按“1.2.1.1”项下色谱条件进样,记录各浓度对应的峰面积(A),以峰面积(A)为纵坐标,浓度(C)为横坐标,进行线性回归,求出线性回归方程。
1.2.1.3 精密度实验 精密移取白藜芦醇储备液适量,无水乙醇稀释配制低、中、高 3 个浓度的对照品溶液(5、20、50 μg/ml),按“1.2.1.1”项下色谱条件进样,测定峰面积,一天内连续测定3 次,连续测定 3 d,计算日内和日间精密度。
1.2.1.4 回收率实验 按处方比例,精密吸取相应比例的空白聚合物胶束溶液各 3 份,加入白藜芦醇储备液,用甲醇稀释至浓度分别为 5、20、50 μg/ml,按“1.2.1.1”项下色谱条件进样,测定峰面积。代入标准曲线方程计算回收率。
1.2.2 白藜芦醇聚合物胶束的处方工艺研究
1.2.2.1 聚合物胶束的制备方法 称取适量白藜芦醇,40 mg Soluplus 溶于 1.0 ml 甲醇中,磁力搅拌至完全溶解;旋转蒸发除去甲醇得到均匀的含药薄膜,加入一定量的 TPGS 水溶液,涡旋 5 min,磁力搅拌一段时间,过 0.22 μm 滤膜,最终得到白藜芦醇聚合物胶束溶液。以粒径和包封率为考察指标,筛选出胶束的最佳制备工艺。
1.2.2.2 投药量对聚合物胶束的影响 固定 TPGS 的浓度、Soluplus 浓度、磁力搅拌时间、磁力搅拌速度及水化量,考察投药量为 1、2、3 mg 对聚合物胶束粒径及包封率的影响。
1.2.2.3 TPGS 浓度对聚合物胶束的影响 固定其他条件不变,考察 TPGS 的浓度为 0.01、0.02、0.03、0.04、0.05 μg/ml 对聚合物胶束粒径和包封率的影响。
1.2.2.4 磁力搅拌速度对聚合物胶束的影响 固定其他条件不变,考察磁力搅拌速度为500、600、700、800 r/min对聚合物胶束粒径和包封率的影响。
1.2.2.5 磁力搅拌时间对聚合物胶束的影响 固定其他条件不变,考察磁力搅拌时间为 1、1.5、2、2.5、3 h 对聚合物胶束粒径及包封率的影响。
1.2.2.6 水化量对聚合物胶束的影响 固定其他条件不变,考察水化量为 1、2、3、4 ml 对聚合物胶束粒径及包封率的影响。
1.2.3 白藜芦醇聚合物胶束的质量评价
1.2.3.1 白藜芦醇聚合物胶束粒径的测定 将白藜芦醇聚合物胶束用超纯水稀释到适当浓度,测定其平均粒径和 PDI,测试温度为 25 ℃,重复检测 3 次。
1.2.3.2 聚合物胶束的包封率和载药量测定 采用滤膜过滤法进行聚合物胶束药物包封率的测定。滤膜过滤法能够将包封和未包封的药物分开;因白藜芦醇难溶于水,未包封的药物大多会以游离微晶形式存在,故可被滤膜截留;取 250 μl 白藜芦醇聚合物胶束溶液,过 0.22 μm 滤膜,用甲醇破坏胶束结构并定容至 5 ml,用 HPLC 法测定,计算胶束中包封的药物的含量。按照以下公式计算包封率(EE)和载药量(DL):EE(%)= 胶束中包封的药物的质量/加入药物的质量 × 100%,DL(%)=胶束中包封的药物的质量/(加入药物的质量+ 加入的载体材料的质量)× 100%。
1.2.3.3 差示扫描量热法(DSC) 分别取白藜芦醇原料药、空白聚合物胶束冻干粉、白藜芦醇与空白聚合物胶束的物理混合物、白藜芦醇聚合物胶束冻干粉 6 mg 置于铝坩埚中,以空白铝坩埚为对照。在氮气保护下,升温速率为 10 ℃/min,扫描区间温度为30 ~ 300 ℃,记录吸收曲线。
1.2.3.4 红外光谱(FTIR) 将白藜芦醇原料药、空白聚合物胶束冻干粉、白藜芦醇与空白聚合物胶束的物理混合物、白藜芦醇聚合物胶束冻干粉分别与 KBr 压片后,在 4000 ~ 400 cm-1范围内进行红外光谱扫描。
1.2.3.5 聚合物胶束的体外释放及机制的考察 采用动态膜透析袋法考察白藜芦醇聚合物胶束的体外释放行为。以磷酸盐缓冲液(pH 7.4,0.5% Tween80)为释放介质。取适量的白藜芦醇聚合物胶束溶液,平行 3 份,每份白芦藜醇的含量均为 1.0 mg,置于处理过的透析袋(MWCO 为 10 000)内;将含药透析袋两端扎紧后浸入 20 ml 已超声脱气的释放介质中。在(37 ± 0.5)℃、100 r/min 的条件下进行释放实验,分别于 0.5、1、2、3、4、5、6、8、9、10、12、24、36、48、72、96、120 h 时取出全部释放介质,每次取出释放介质后立即补入等温等体积的新鲜释放介质。将取出的液体经0.22 μm 微孔滤膜过滤后,按照“1.2.1.1”项下色谱条件进样,记录峰面积,得到不同时间点的药物浓度,从而计算出累积释放百分数(Q),绘制累积释放曲线。
2 结果
2.1 白藜芦醇聚合物胶束的含量测定结果
白藜芦醇在 1 ~ 100 μg/ml 范围内峰面积和浓度呈良好的相关性,线性回归方程为A = 46.16C – 31.327(2= 0.9995)。低、中、高 3 个浓度的日内精密度分别为 114.57%、100.91%、101.31%,RSD 分别为 1.58%、1.52%、1.44%;日间精密度分别为 116.14%、103.65%、104.39%,RSD 分别为 1.09%、1.57%、1.37%,表明精密度符合方法学要求。低、中、高 3 个浓度的回收率分别为 110.45%、99.10%、100.21%,RSD 为 0.84%、0.13%、0.06%(n = 3),表明回收率符合方法学要求。
2.2 白藜芦醇聚合物胶束的处方工艺研究
2.2.1 投药量对聚合物胶束的影响 结果如图 1所示,粒径随着投药量的增加,呈缓慢增加的趋势;而包封率随着投药量的增加逐渐降低;当投药量达到 3 mg 时,粒径急剧增加,包封率骤减。当投药量达到 2 mg 时,粒径为(80.17 ± 0.38)nm;PDI 为(0.16 ± 0.02);包封率 88.86%;大于 80%,所以确定投药量为 2 mg。
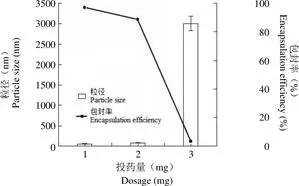
图 1 投药量对聚合物胶束粒径和包封率的影响
Figure 1 Effect of dosage on particle size and encapsulation efficiency of polymeric micelles
2.2.2 TPGS 浓度对聚合物胶束的影响 随着 TPGS 浓度的增加,粒径变化趋势不显著;而包封率大致呈增加趋势(图 2)。当浓度为 0.05 mg/ml时,粒径为(79.50 ± 0.66)nm;PDI 为(0.20 ±0.02);包封率为 94.50%。而当浓度为 0.03 mg/ml 时,粒径为(77.40 ± 0.26)nm;PDI 为(0.18 ± 0.01);包封率为 90.51%。综合考虑,确定 TPGS 浓度为 0.03 mg/ml。
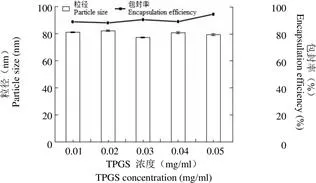
图 2 TPGS 浓度对聚合物胶束粒径和包封率的影响
Figure 2 Effect of TPGS concentration on particle size and encapsulation efficiency of polymeric micelles
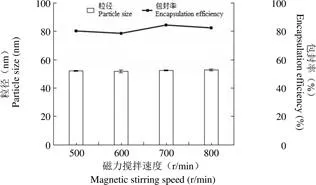
图 3 磁力搅拌速度对聚合物胶束粒径和包封率的影响
Figure 3 Effect of magnetic stirring speed on particle size and encapsulation efficiency of polymeric micelles
2.2.3 磁力搅拌速度对聚合物胶束的影响 磁力搅拌速度的改变对粒径的影响较小,当磁力搅拌速度达到700 r/min 时,包封率最高,为 84.55%;再增加磁力搅拌速度,包封率反而减小。综合考虑,选定磁力搅拌速度为 700 r/min(图 3)。
2.2.4 磁力搅拌时间对聚合物胶束的影响 粒径随着磁力搅拌时间的延长而波动较小;包封率的变化与磁力搅拌时间也不成正相关。当时间为 1 h 时,包封率最大,为 93.92%(图 4)。综合以上分析,确定磁力搅拌时间为 1 h。
2.2.5 水化量对聚合物胶束的影响 粒径随着水化量的增加呈逐渐增加的趋势,而包封率逐渐减小(图 5)。故选定水化量为 1 ml。
2.2.6 最佳制备工艺的确定 经综合分析,确定最佳制备工艺的投药量为 2 mg;Soluplus 的量为 40 mg;TPGS 浓度为 0.03 mg/ml;水化量为 1 ml;在磁力搅拌速度为 700 r/min条件下搅拌 1 h。
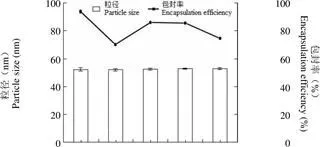
图 4 磁力搅拌时间对聚合物胶束粒径和包封率的影响
Figure 4 Effect of magnetic stirring time on particle size and encapsulation efficiency of polymeric micelles
2.3 白藜芦醇聚合物胶束的质量评价
2.3.1 白藜芦醇聚合物胶束的外观形态 如图 6 所示,白藜芦醇(RES + H2O)混悬液呈白色、混悬状。本实验以最佳工艺制备的白藜芦醇聚合物胶束(RES-SPS-TPGS-PMs)溶液呈蓝色乳光,为澄明透亮的均一、稳定溶液。此外观是聚合物胶束制备成功的一个标志。
2.3.2 白藜芦醇聚合物胶束粒径的测定 纳米粒粒径的大小是评价药物制剂的一个关键指标。将最佳工艺制备的聚合物胶束加入适量水稀释,用激光粒度仪测定粒径和 PDI,分别为(52.4 ± 0.66)nm和(0.06 ± 0.01),说明制备的胶束溶液粒度小且分布均匀(图 7)。
2.3.3 差示扫描量热法(DSC) 由图 8可知,白藜芦醇原料药在 271 ℃有吸收峰存在,该点是白藜芦醇的熔融峰,说明原料药具有晶体的性质。白藜芦醇聚合物胶束冻干样品中,白藜芦醇的特征吸收峰消失,说明白藜芦醇在聚合物胶束中,晶型已经发生了改变,可能以无定型或分子的形式存在。物理混合物中,在白藜芦醇熔融峰附近并非平滑曲线,说明一部分白藜芦醇仍为晶体形式,进一步说明胶束中药物晶型发生了改变。
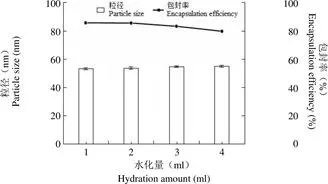
图 5 水化量对聚合物胶束粒径和包封率的影响
Figure 5 Effect of hydration amount on particle size and encapsulation efficiency of polymeric micelles

图 6 白藜芦醇混悬液(左)和白藜芦醇聚合物胶束溶液(右)的外观图
Figure 6 Appearance of resveratrol suspension (left) and resveratrol polymeric micelles solution (right)
2.3.4 红外光谱 由图 9可知,白藜芦醇粉末在 3250 cm-1处出现酚羟基的特征吸收峰;966 cm-1为反式 C=C 的特征峰;1610 cm-1、1510 cm-1处为苯环的特征吸收峰。从白藜芦醇聚合物胶束的红外谱图中可以看出白藜芦醇的部分特征吸收峰发生改变,说明白藜芦醇被包载在胶束材料中。空白胶束冻干粉与白藜芦醇的物理混合物的红外光谱中,既有空白胶束的特征吸收峰,也有芹菜素的特征吸收峰;此外,在空白胶束中出现了 C=O 的特征吸收峰(1729 cm-1、1623 cm-1),白藜芦醇聚合物胶束中也出现了 C=O 的特征吸收峰(1727 cm-1、1616 cm-1),相较于空白胶束位移发生了稍许改变。由此也表明了在聚合物胶束中,白藜芦醇的羟基与载体中的羰基之间形成了氢键,从而有较高的载药量与包封率。
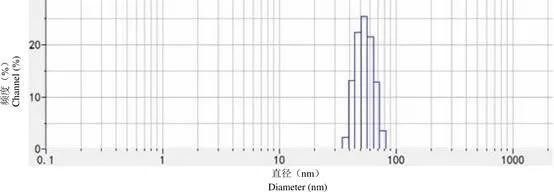
图 7 白藜芦醇聚合物胶束的粒径分布图
Figure 7 Particle size distribution of resveratrol polymeric micelles
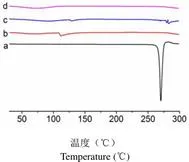
a:白藜芦醇原料药;b:空白聚合物胶束冻干粉;c:空白胶束与白藜芦醇原料药的物理混合物;d:白藜芦醇聚合物胶束冻干粉
Figure 8 Differential scanning calorimetry of resveratrol polymeric micelles
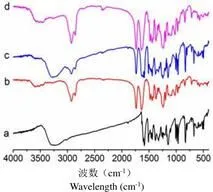
a:白藜芦醇原料药;b:空白聚合物胶束冻干粉;c:空白胶束与白藜芦醇原料药的物理混合物;d:白藜芦醇聚合物胶束冻干粉
Figure 9 Infrared absorption spectrum of resveratrol polymer micelles
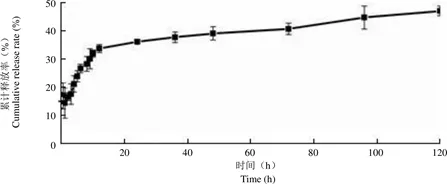
图 10 白藜芦醇聚合物胶束的累积释放
Figure 10 Cumulative release of resveratrol polymeric micelles
2.3.5 聚合物胶束的体外释放及机制的考察 白藜芦醇聚合物胶束的释放曲线如图 10 所示。白藜芦醇聚合物胶束在 120 h 内仅仅释放 45.83%,显示达到明显的缓释效果,说明 Soluplus 作为聚合物胶束释药系统的载体具有缓释作用。分别用零级动力学方程、一级动力学方程、Higuchi 方程对胶束的体外释放度进行拟合度分析,结果见表 1。结果显示,聚合物胶束的体外释放曲线更符合 Higuchi 方程,表明其体外释放以扩散为主。可能由于白藜芦醇分子结构上的羟基与载体材料结构上的羰基形成了氢键,致使药物从聚合物胶束的疏水核心扩散到释放介质的过程更加缓慢。

表 1 白藜芦醇聚合物胶束的不同释放模型拟合方程
3 结论
常用的聚合物胶束的制备方法有直接溶解法、透析法、微相分离法、溶剂挥发法、薄膜分散法等。薄膜分散法往往制备简单,具有较高的包封率和载药量。本研究采用薄膜分散法制备白藜芦醇聚合物胶束,制备的胶束包封率与载药量较高。纳米粒粒径的大小是评价药物制剂的一个关键指标。用于口服的聚合物纳米尺寸通常小于 100 nm,本试验制备的白藜芦醇聚合物胶束的粒径约 52 nm,符合口服吸收对粒径大小的要求[12]。白藜芦醇聚合物胶束的 DSC 结果显示,白藜芦醇在聚合物胶束中,晶型已经发生了改变,可能以无定型或分子的形式存在。从 FTIR 分析结果可以得出,白藜芦醇与载体之间形成了氢键,由于氢键的存在,大大提高了聚合物胶束的包封率、载药量及稳定性。载药胶束的释放采用动态透析袋法。在满足漏槽条件的前提下,选择磷酸盐缓冲液(pH 7.4,0.5% Tween80)为释放介质考察白藜芦醇聚合物胶束的释放特性;由体外释放曲线可知,白藜芦醇聚合物胶束具有显著的缓释效果,达到了长循环的目的,说明白藜芦醇几乎完全包封于胶束中。白藜芦醇聚合物胶束的释放行为更符合 Higuchi 扩散方程,说明聚合物胶束中药物的释放主要以扩散为主。本研究为白藜芦醇口服制剂的开发提供理论依据。
[1] Ramprasath VR, Jones PJ. Anti-atherogenic effects of resveratrol. Eur J Clin Nutr, 2010, 64(7):660-668.
[2] Meng J, Guo F, XU H, et al. Combination therapy using co-encapsulated resveratrol and paclitaxel in liposomes for drug resistance reversal in breast cancer cells in vivo. Sci Rep, 2016, 6:22390.
[3] Bilia A, Piazzini V, Guccione C, et al. Improving on nature:The role of nanomedicine in the development of clinical natural drugs. Planta Med, 2017, 8(5):366-381.
[4] Li TP, Wong WP, Chen LC, et al. Physical and pharmacokinetic characterizations of trans-Resveratrol (t-rev) encapsulated with self-assembling lecithin-based mixed polymeric micelles (saLMPMs). Sci Rep, 2017, 7(1):10674.
[5] Qiu C, Wang J, Zhang H, et al. A novel approach with controlled nucleation and growth for green synthesis of size-controlled cyclodextrin-based metal-organic frameworks based on short-chain starch nanoparticles. J Agric Food Chem, 2018, 66(37):9785-9793.
[6] Mont KV, Yvonne I. Increasing solubility of poorly water soluble drug resveratrol by surfactants and cyclodextrins. Adv Mater Res, 2012, (418-420):2231-2234.
[7] Prakash J, Bothiraja C, Pawar A. Resveratrol-piperine loaded mixed micelles:formulation, characterization, bioavailability, safety and in vitro anticancer activity. RSC Adv, 2016, 6(114):112795-112805.
[8] Hitesh K, Deep P, Shweta S, et al. Cyclic-RGDfK peptide conjugated succinoyl-TPGS nanomicelles for targeted delivery of docetaxel to integrin receptor over-expressing angiogenic tumours. Nanomedicine, 2015, 11(6):1511-1520.
[9] Yen CC, Chang CW, Hsu MC, et al. Self-nanoemulsifying drug delivery system for resveratrol:enhanced oral bioavailability and reduced physical fatigue in rats. Int J Mol Sci, 2017, 18(9):E1853.
[10] Dian LH, Hu YJ, Lin JY, et al. Fabrication of paclitaxel hybrid nanomicelles to treat resistant breast cancer via oral administration. Int J Nanomedicine, 2018, 13:719-731.
[11] Zhang Z, Tan S, Feng SS. Vitamin E TPGS as a molecular biomaterial for drug delivery. Biomaterials, 2012, 33(19):4889-4906.
[12] Feng S, Mei L, Anitha P, et al. Poly(lactide)-vitamin E derivative/montmorillonite nanoparticle formulations for the oral delivery of docetaxel. Biomaterials, 2009, 30(19):3297-3306.
Preparation and quality evaluation of resveratrol loaded polymeric micelles
ZHOU Yun-qiu, JI Su-ping, LIU Cong, YAN Xiong, DIAN Ling-hui
To prepare resveratrol-soluplus-TPGS-polymeric micelles (RES-SPS-TPGS-PMs) and evaluate its quality.
The RES-SPS-TPGS-PMs were prepared by the thin film hydration method, and the micelles were characterized by the nanoparticle analyzer, differential scanning calorimeter (DSC) and Fourier transform infrared spectroscopy (FTIR). The HPLC method was established for determining the encapsulation efficiency and drug loading capability. Therelease of resveratrol from polymeric micelles was evaluated by dialysis method.
The particle size and polymer dispersity index (PDI) of RES-SPS-TPGS-PMs were (52.4 ± 0.66) nm and (0.06 ± 0.01), respectively. Encapsulation efficiency and drug loading were (97.12 ± 9.08)% and (2.37 ± 0.22)%, respectively. Resveratrol possibly existed in an amorphous or molecular form in the polymer micelles and the hydrogen bonds were formed between resveratrol and polymer. The release profile showed that resveratrol-loaded polymeric micelles were sustained-release formulations.
The preparation process of RES-SPS-TPGS-PMs was simple, its particle size, entrapment efficiency and drug loading capacity could be controllable, and it possesses a slow drug-release effect.
Resveratrol; Polymeric micelles; Soluplus; Quality evaluation; Vitro release
DIAN Ling-hui, Email:dianlh@163.com
10.3969/j.issn.1673-713X.2020.01.006
Author Affiliation:College of Pharmaceutical Sciences, Guangdong Medical University, Dongguan 523808, China
广东省东莞市社会科技发展(重点)项目(2017507152463);广东医科大学重点培育项目(Z2017002);广东省教育厅青年创新人才类项目(2018KQNCX093);广东省科技计划项目(2014A020212296);广东省大学生创新创业训练计划项目(201610571016、201710571055、201810571084)
典灵辉,Email:dianlh@163.com
2019-08-26

