谷物中锗的干灰化-氢化物发生-原子荧光光谱法测定
刘海涛 林建奇 姚梦楠 炼晓璐 魏洪敏
[摘要]建立一种干灰化-氢化物发生-原子荧光光谱法测定谷物中锗的方法。采用控温程序的干灰化为前处理方式,实现谷物中锗的原子荧光光谱法测定。灰化程序:第一步,200℃保持10min;第二步,500℃保持20min的条件下,称样2g的谷物样品灰化效果良好。优化仪器参数和试剂浓度条件,考察灯电流、负高压、载气、酸浓度、还原剂浓度等对锗荧光强度的影响。结果表明,锗元素浓度0~30μg/L,線性相关r为0.999,方法检出限为0.12μg/kg,方法精密度(n=7)在3.9%~5.8%,加标回收率为94.5%~104.5%。该方法操作简单、高效、稳定性良好,适用于谷物中锗的批量检测。
[关键词]谷物;锗;干灰化;氢化物发生;原子荧光光谱法
中图分类号:TS210.7 文献标识码:A DOI:10.16465/j.gste.cn431252ts.202002
锗是一种典型的稀散金属元素。它在地壳里的含量约为1.5ppm,土壤样品中锗约含0.2μg/g。在诸多矿物中,它常常以伴生形式存在,常和铅、铝等元素混在一起[1]。痕量锗是动植物必需的营养元素,它对生理作用起着重要的作用,具有生物电解质作用,能够加快血液循环,提高代谢并促进身体的自然治愈力等[2-3]。近年来,对于锗的分布以及含量的研究逐渐被关注。王岙等[4]研究了保健品锗的石墨炉法测定,锗元素以有机锗的形式被广泛用于药物、保健品等产品,但长期使用或服用易引起中毒。因此对于富锗产品,不宜过于盲从,应该科学理性对待。
自古以来,“民以食为天”。谷物作为人类每天食用的主食,涵盖的范围较广,包括大米、小麦、玉米、豆类等及其他杂粮。由于锗的存在很分散且土壤中含有痕量的锗,作为赖以土壤生长的谷物,有必要进行锗元素检测,可为人类的健康提供参考。目前的测试方法主要有:电感耦合等离子质谱法、分光光度法、原子吸收光谱法、原子荧光光谱法、极谱法、离子色谱法等。对于样品的前处理,李丹等[5]、邢银娟等[6]采用HF+H3PO4+HNO3或者HF+H3PO4+HNO3+H2SO4对样品电热板湿法消解、微波消解、高压密封罐消解等,费时费力且存在易引入误差干扰。还有巩海娟等[10]以氧化性混合酸为消解介质,利用高通量密闭微波处理,结果良好但是依然步骤较为繁琐。因此笔者建立了干灰化法处理,磷酸溶解,快速测定的氢化物-原子荧光光谱法测定,该方法简便、准确、快速,为谷物中锗的检测方法提供完善和参考。
1 原理
样品经马弗炉一定温度下灰化,在磷酸酸性介质中,溶液中的Ge4+和硼氢化钾还原剂进行氧化还原反应,如(1)、(2)反应式,生成挥发性的气态氢化物锗化氢(GeH4),在氩气作为载气的作用下进入原子荧光原子化器进行原子化。在锗空心阴极灯释放特殊光源谱线的照射下,原子化后的基态锗原子被激发至高能态,由于在高能态的锗原子很不稳定,在去活化的过程中以发射出特征波长的锗原子荧光回到基态,在一定锗元素浓度下,发射出的荧光强度和浓度符合朗伯-比尔定律,两者呈线性关系。以此为基准,通过外标法对未知样品的锗元素进行定量测试。
KBH4+3H2O+H+=H3BO3+K++8H* (1)
8H*+Ge4+=GeH4(g)+2H2(g) (2)
式中:H*为活化性氢。
2 材料与方法
2.1 仪器设备
原子荧光光谱仪(AFS-8510):北京海光仪器有限公司;锗空心阴极灯:北京有色金属研究院;万分之一电子天平:北京赛多利斯科学仪器有限公司;超纯水机(UPW-20N):北京历元仪器公司;研钵、电热板(EH35A plus):北京莱伯泰科有限公司;TE系列一体式陶瓷纤维马弗炉:北京盈安美城科学仪器有限公司;移液枪(100μg/L、1 000μg/L):大龙科技;陶瓷坩埚(20mL,带盖)、筛网(80目)、大米/大豆标准物质(GSB-1/GSB-4):地球物理地球化学勘察研究所。
2.2 试剂及耗材
锗标准液(1 000mg/L):中国计量院;磷酸(优级纯)、硫脲(分析纯)、硼氢化钾(优级纯)、氢氧化钠(优级纯):国药试剂;分析用水(超纯水);氩气(99.99%纯度)。
还原剂溶液:于50mL烧杯中依次加入5g氢氧化钠,20mL高纯水,溶解。再加入30g的硼氢化钾,溶解。采用高纯水将以上混合溶液转移至1 000mL容量瓶,并定容,混匀。
载流溶液:于1 000mL容量瓶中,加入30mL磷酸,并定容,混匀。
硫脲溶液:于50mL烧杯中称量10g硫脲,加入30mL纯水,于电热板上加热并搅拌至溶解,移入100mL容量瓶,并用纯水定容,摇匀待用。
2.3 样品
谷物中,以大米、大豆、玉米为主,于北京顺义区超市采购,随机选取三种样品。
2.4 样品前处理以及试验方法
除了玉米,大米和大豆均是风干好的。将采购的玉米棒包裹的叶子剥掉,于通风处风干1周(按北京天气)。通过四分法,分别取三种样品100g。通过研钵进行研磨,分别过80目筛网,塑封袋保存待用。
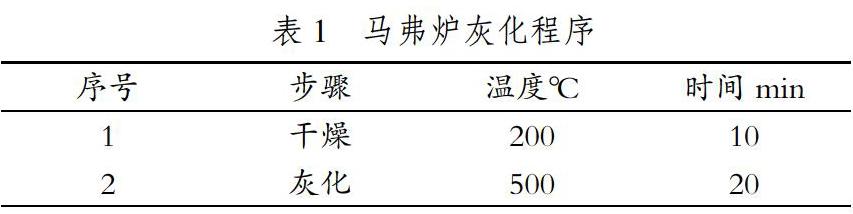
于陶瓷坩埚中,称取2g样品,带上盖子;将称好样品的陶瓷坩埚放置于马弗炉中,设置马弗炉灰化程序(见表1),启动灰化。灰化结束,取出冷却。
在灰化后的谷物样品中,加入7.5mL磷酸,沿坩埚内壁淋洗确保所有样品灰彻底溶解,并用纯水多次清洗转移入25mL比色管。接着,加入5mL硫脲溶液,纯水定容至刻度,摇匀待测。同时,做试剂空白试验。
2.5 仪器参数条件
锗空心阴极灯电流80mA,光电倍增管负高压270V,炉高8mm,氩气载气流量500mL/min,氩气屏蔽气流量1 000mL/min,延迟时间5s,读数时间12s,进样体积1.0mL。
2.6 标准曲线配制
将锗标准液稀释成1mg/L。取7个25mL比色管,依次加入10mL纯水,7.5mL磷酸,5.0mL硫脲溶液。再用移液枪依次加入0L,25L,50L,125L,250L,500L,750L的1mg/L铅标准溶液,高纯水定容,摇匀。得到的标准曲线系列浓度依次为0μg/L,1μg/L,2μg/L,5μg/L,10μg/L,20μg/L,30μg/L。
2.7 方法學评价
方法学的评价涉及试验方法的准确性和可靠性,是验证试验方法是否可行的关键[7-9]。因此结合本试验方法实际,笔者分别设计了以下试验验证项目:准确性、加标回收率、精密度以及检出限,并对这些验证项目的结果进行分析,以此作为评估方法学的可行依据。
3 结果与讨论
3.1 测试条件优化
原子荧光光谱仪采用一定负高压下的仅对近紫外光源敏感的日盲光电倍增管(PMT)作为检测器,检测的稳定性与负高压大小息息相关。负高压决定日盲光电倍增管的光电信号放大倍数,直接影响仪器的噪声。并且经原子化后的基态原子,能否最大限度地跃迁并释放较强的原子荧光,取决于特殊光源的空心阴极灯的光源强度,而这个光源强度强弱来源于给空心阴极灯供电的电流大小。作为原子荧光光谱仪分析,必须把硬件的状态调至最佳,才能保证整体的测试是稳定的。笔者分别对负高压以及灯电流进行了梯度试验:固定灯电流为默认电流80mA,负高压从250V、260V、270V、280V、290V、300V、310V、320V、330V、340V,锗的荧光强度逐渐上升,340V负高压状态下荧光强度最高,但是稳定性不是很理想(相对标准偏差大于15%)。基于此,每个负高压条件下均进行稳定性试验,最后选择负高压270V(相对标准偏差1.2%),电流为空心阴极灯出厂默认值,配合负高压调整至足够的荧光强度以及较好的稳定性[10-12]。
除此之外,氢化物发生原理是一个实时、在线、动态的氧化还原的化学反应过程,当产生了稳定的氢化物之后,应确保原子化过程是正常的,基态原子激发后去活化产生的荧光不猝灭而被检测器检测到,这就要求屏蔽气足够而且稳定。本试验过程,笔者为保证屏蔽气防止荧光猝灭,将屏蔽气调整至1 000mL/min,调整载气大小:300mL/min、400mL/min、500mL/min、600mL/min,以此试验稳定性。载气大小影响着能否及时彻底地促进氧化还原反应以及彻底地将产生的氢化物气态物质送入原子化器,避免氢化物残留至管壁引起记忆效应带来的不稳定。结果表明,当载气在500mL/min时,稳定性比较理想(相对标准偏差小于1%),过大的气流量使得流路过程产生湍流现象,反而引起氧化还原反应的不稳定,最终影响仪器测定的稳定性。因此,最后选择载气500mL/min,屏蔽气1 000mL/min作为谷物中锗的测定参数条件[13-16]。
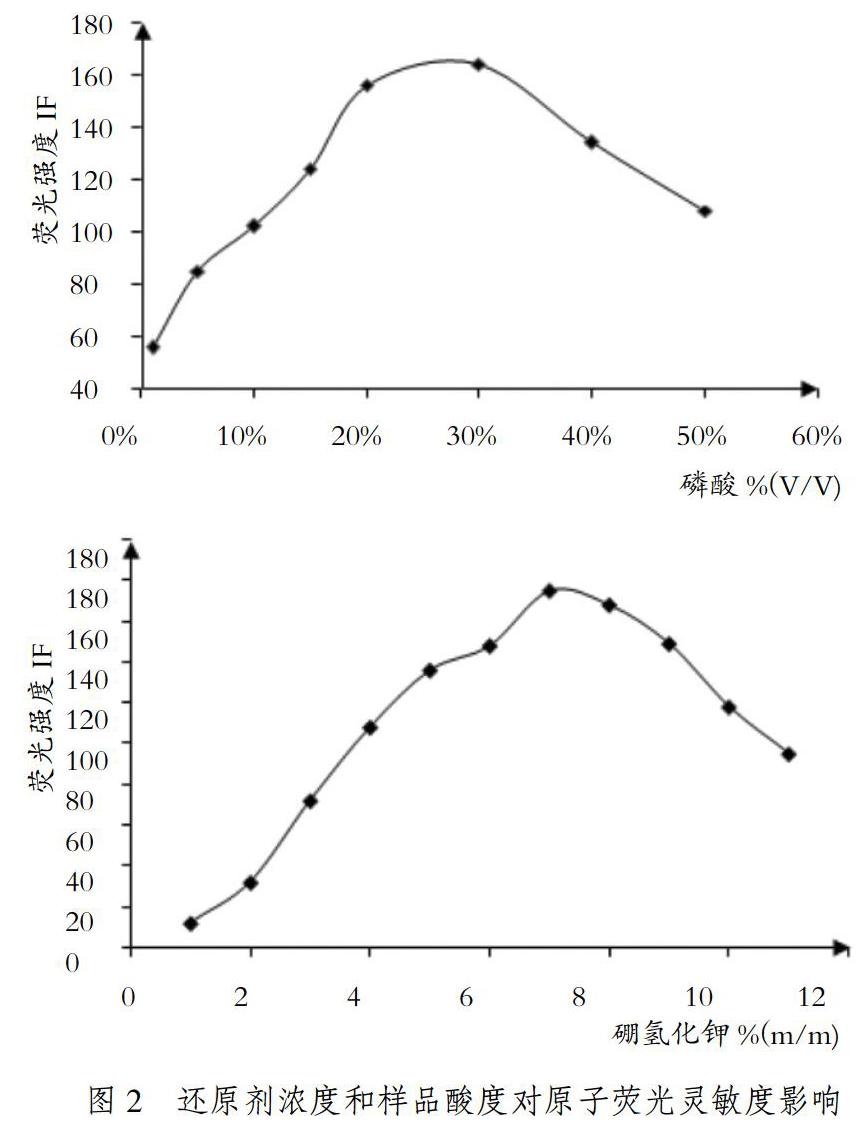
3.2 还原剂浓度和样品酸度的选择
在条件优化中提到了仪器硬件方面的调整,对于原子荧光光谱分析原理中,锗之所以可以采用该仪器进行分析,主要的一个化学特性就是酸化的四价锗离子可以和还原剂硼氢化钾氧化还原成气态氢化锗。所以这是锗元素分析的核心特性,涉及酸介质、酸介质浓度、还原剂浓度是否匹配。本试验选择磷酸为酸介质,主要原因是磷酸可以和四价锗离子反应成络合物而相对稳定地存在于溶液中,便于检测。在对磷酸和还原剂浓度的梯度试验中,见图2。本试验选择30%的磷酸(V/V)以及3%的硼氢化钾(m/m)以确保锗的氢化物反应顺利进行,并得到准确稳定的分析数据。
3.3 干扰实验
谷物中的Fe、Cu、Mn、Zn、Ca等金属元素含量较高ppm级别[17-18]。在氢化物发生反应过程,过高含量的这些元素总是对检测存在影响,试验发现,Cu大于500ppm使得锗的检测结果严重偏低。笔者采用一定浓度的硫脲进行掩蔽试验,发现改善效果明显。故在灰化过后的溶样中加入2%的硫脲(m/m)以起到信号掩蔽剂的作用。
3.4 干灰化条件摸索
由于锗属于低温挥发性元素,锗的化合物易于挥发,用石墨炉原子吸收法测锗,为避免锗在灰化阶段以挥发性GeO(710℃升华)形式损失,需加入基体改进剂,起到稳定锗的作用。还有研究表明,锗的化合物如GeCl4以及其他卤素化合物是挥发性气体。所以,在灰化过程需试验并考虑灰化温度以及样品中是否含有大量的卤素元素、是否在灰化过程对锗的挥发起到作用。试验初期,选取灰化温度为300℃、350℃、400℃、450℃、500℃、550℃、600℃、650℃、700℃,在干净的坩埚中加入1mL的10g/L的锗标准溶液分别在不同灰化温度下进行试验,发现在550℃以上锗的含量开始损失5%,700℃时锗的含量损失20%。因此,为了保证彻底灰化且不损失,灰化温度定为500℃,保持20min。由于实际灰化样品时,出现了谷物样品粉末在升温过程容易爆燃现象,因此为缓解该现象设置了干燥步骤200℃,保持10min,并配备盖子,有效缓解升温灰化过程造成损失,确保所有样品彻底灰化,以达到准确测试的目的。
3.5 标准曲线以及方法检出限
按1.6标准曲线点,依次测试拟合,一次线性回归方程为:y=182.36x+12.28,线性相关r=0.999 2。方法检出限采用连续测试11次样品空白浓度值,并计算11次空白浓度的标准偏差SD=0.08μg/L,最后方法检出限以DL=3×SD计算,得到检出限为0.24μg/L,AFS-8510原子荧光光谱仪的进样体积为1mL,而实际样品称样重量为2g,那么换算后本方法的方法检出限为0.12μg/kg。
3.6 准确度试验
查询谷物相关的标准物质,选取大米/大豆标准物质:GSB-1(标准值Ge:5μg/kg)、GSB-4(标准值Ge:2.5μg/kg)。通过灰化,磷酸直接溶解上机检测,结果实测值:GSB-1,4.82μg/kg;GSB-4,2.64μg/kg。相比之下,实测结果和标准值相当,准确度良好。
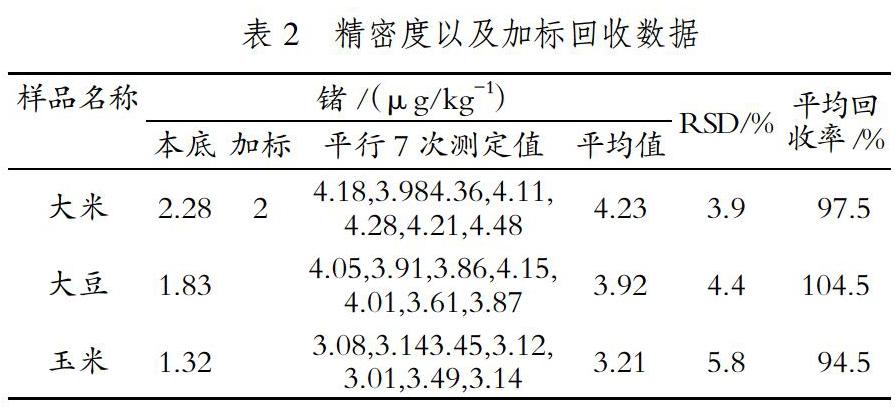
3.7 精密度以及加标回收试验
考察实际样品的加标回收率和精密度,以验证稳定性以及灰化处理是否可靠。同准确度测试方法,分别对大米、大豆、玉米样品进行检测,由于谷物中锗的含量均较低,因此加标回收试验选择加标2μg/kg(通过加入标准溶液换算),每个加标平行7次试验,得出结果计算精密度。得出精密度3.9%~5.8%,回收率为94.5%~104.5%,两者数据均符合实际样品检测需求(见表2)。
4 结 论
相比混酸消解的前处理方式,本文应用马弗炉控温程序的干灰化处理-磷酸直接溶解的氢化物发生-原子荧光光谱法对谷物中锗的检测,分析结果良好,检出限、精密度、回收率均满足检测需求,为谷物中锗元素的分析提供方法参考。另外,锗是人体必需的元素,通过本试验的分析,常规谷物中均含有一定痕量的锗,可为人们日常的饮食健康提供参考。
参考文献
[1] 胡瑞忠,苏文超.锗的地球化学、赋存状态和成矿作用[J].矿物岩石地球化学通报,2000,19(4):215-217
[2] Li Zaijun,Zhou Xia,Liu Huizhen.Development of spectro photometric method for determination of germanium[J].Analy tical Chemistry,2007,26(1):23-41.
[3] Winkler,Clemens.Mittheilungen über des Germanium. Zweite Abhandlung[J].Prak Chemie,1887(36):177–209
[4] 王岙,于文海.硝酸镍作基体改进剂用石墨炉原子吸收光谱法测定保健食品中锗[J].中国卫生检验杂志,2002,12(3):279-282.
[5] 李丹,李彪.痕量锗的分析进展[J].冶金分析,2010,30(12): 33-38.
[6] 邢银娟,杨军红.锗化学分析技术研究进展[J].分析化学计量, 2019(6):125-129.
[7] 魏丽娜,李明晓.电感耦合等离子体原子发射光谱法测定煤中的锗[J].理化检验(化学分册),2019(10):1219-1221.
[8] 朱传翔,白龙律.氢化物原子荧光光谱法对长白山人参锗含量的测定[J].现代食品,2019(19):149-151.
[9] 张笑言,刘涛.原子荧光法测定调味品中锗的不确定度来源分析[J].中国调味品,2014(7):99-102.
[10] 巩海娟,谢芸欣,王佳丽.高通量密闭微波消解-ICP-MS测定食品中的锗含量[J].食品研究与开发,2019(15):160-164.
[11] 叶英植,刘少陵.氢化物分离苯基荧光酮-氯化十六烷基吡啶光度法测定微量锗[J].理化检验.化学分册,1984(2):21-24.
[12] 柳志龙.石墨炉原子吸收法测定焙烧烟尘和渣中锗[J].理化检验.化学分册,1988(5):288-289.
[13] 程良娟,張旭,沈庆峰,等.微分脉冲极谱法测定锌电解液中微量锗[J].分析试验室,2017(7):837-840.
[14] 段艳文,王培根,王震,等.苯芴酮分光光度法测定粉煤灰中的微量锗[J].安徽化工,2015(6):86-88.
[15] 杨树泉,陈吉祥,莫平英.X-射线荧光光谱仪快速测定酸浸渣中铅、镉、砷、铜、锗、银、硫含量[J].世界有色金属,2015(7): 51-54.
[16] 高向阳,高遒竹,王长青,等.微波消解-石墨炉原子吸收法测定小麦中锗的生物吸收比[J].食品科学,2014(8):249-252.
[17] 高锦红.常见谷物及红枣中特征金属元素分析研究[J].科学技术与工程,2011(3):51-54.
[18] 鲁晶晶.长春市市售谷物制品中重金属含量研究与安全评价[D].长春:吉林大学,2019.
Determination of Germanium in Grain By Dry Ashing-Hydride Generation-Atomic Fluorescence Spectrometry
Liu Haitao,Lin Jianqi,Yao Mengnan,Lian Xiaolu,Wei Hongmin
(Beijing Haiguang Instrument Co.,Ltd.,Beijing 101312)
Abstract:Method for the determination of germanium in grain by dry ashing-hydride generation-atomic fluorescence spectrometry was established. The determination of germanium in grain by atomic fluorescence spectrometry (afs) was realized by dry ash pretreatment with temperature control program. In the ashing process: in the first step, keep it at 200℃ for 10min; In the second step, under the condition of keeping at 500℃ for 20min, the grain sample of 2g had good ashing effect. The influence of lamp current, negative high voltage, carrier gas, acid concentration and reducing agent concentration on the fluorescence intensity of germanium was investigated. The results showed that the concentration of germanium was 0~30μg/kg, linearly correlated was better than 0.999, the detection limit of the method was 0.12g/K, the method precision(n=7)was between3.9%~5.8%,and the standard recovery was between 94.5%~104.5%.The method is simple, efficient and stable, and is suitable for the bulk detection of germanium in grain.
Key Words:grain,germanium,dry ash,hydride generation,AFS
收稿日期:2020-02-14
作者简介:刘海涛,男,硕士,高级工程师,主要从事项目管理。

