罗沙司他共晶的合成、表征与理化性质研究
徐巾超,陈勇,2,叶辉青,张杰,张霁,2,罗忠华,2
(1 广东东阳光药业有限公司,广东东莞523871; 2 抗感染新药研发国家重点实验室,广东东莞523871)
引 言
难溶性是制约候选药物成为临床药物的关键因素之一[1],近年来进入市场有不少新药,但变得愈来愈普遍的是,研发中的候选药物水溶性不好[2]。据估计,大约有40%的口服速释药物被归类为几乎不溶[3]。通过组合筛选程序鉴定的70%或更多的新化学实体(new chemical entity,NCE)水溶性也很差[4]。改善药物的溶解性,从而提升生物利用度是难溶性药物成药的重要手段。在药物产品的研发过程中,药物中活性成分的物理化学性质必须优化,如溶解性、生物利用度和稳定性等[5-8]。药物共晶能够改善药物的一些重要物理化学性质,也有利于药物合成和生产工艺的绿色化。文献报道的可用于研发改善药物物理化学性质的潜在方法手段有形成共晶、多晶型、溶剂化物、水合物和盐[9-12]。美国药物管理局(food and drug administration,FDA)在2016 年发布的《药物共晶监管分类指南》[13]中明确给出了共晶的定义“共晶是两种或多种不同分子以同样晶格构成的结晶物质,通常是药物和共晶配体。它们不同于盐而更像溶剂化物,虽然都是一个晶格中含有多于一个的组分”。从物理化学性质角度看,共晶可看作是溶剂化物和水合物的特殊情形,其中第二组分共晶配体是非易失形的。
近年来,药物共晶[14-18]作为一种新兴的药物晶型,通过引入共晶配体(co-crystal coformers,CCF)可改变其活性药物成分(active pharmaceutical ingredient,API)的诸多理化性质[19-23]。2015 年,诺华的EntrestoTM(代号LCZ696)获得了FDA 的批准,用于治疗慢性心衰竭[24],是有限的几个被FDA 批准的药物共晶之一。EntrestoTM由沙库巴曲单钠盐、缬沙坦二钠盐和水组成[25],临床数据证明,不仅显著降低死亡率且在患者耐受性上与依那普利相似。另一个共晶药物是埃格列净-L-焦谷氨酸共晶(ertugliflozin)[26],于2017 年12 月由FDA 批准用于治疗糖尿病的新型药物。这些共晶药物的获批上市进一步提升了研究者和制药公司对共晶开发的关注,通过共晶研究来改善药物的理化性质或者生物利用度以达到提早应用的目的。
罗沙司他(爱瑞卓Roxadustat,RDXT),由珐博进(FibroGen)、阿斯利康(AstraZeneca)和安斯泰来(Astellas)联合开发,是全球首个开发的小分子低氧诱导因子脯氨酰羟化酶抑制剂类治疗肾性贫血(chronic kidney disease,CKD)的药物。2017年12月,罗沙司他胶囊被中国药审中心纳入优先审评公示名单,并于2018 年12 月17 日获批上市。该药是首个在中国本土孵化、首个率先在中国获批的全球首创原研药,用于透析依赖的慢性肾衰性贫血。目前全世界范围慢性肾病的发生率达8%~16%,在中国慢性肾病发生率达10.8%,大约有1.2 亿人,CKD 已成为一个重要的全球医疗保健问题,代表着一个庞大且日益增长的未满足的医疗需求。最近,RDXT在治疗非透析慢性肾脏病患者贫血的Ⅲ期临床研究也达到了主要终点[27-28]。
然而,RDXT 的水溶性较差,在水中的溶解度仅为1.71 mg/L[29]。据专利报道[30],RDXT原研晶型与盐型专利中包含了游离酸的晶型A、B、C、D,以及钠盐、钾盐、赖氨酸盐等,其中原研上市的晶型为A。目前未见有RDXT 共晶的报道,对RDXT 开展多晶型筛选有重要意义。设计了数百组实验,最终只得到若干溶剂合物,没有得到令人满意的游离酸晶型,于是开展了共晶研究。本研究选用RDXT 为模型药物,对一系列CCF 进行500多组实验的筛选,先后制备出RDXT与烟酰胺、肉桂酰胺、苯甲酰胺和脯氨酸四种共晶并进行表征,对其溶出速率、溶解性和稳定性进行研究。根据FDA 的指南,设计新共晶的药物被认为是类似于API 的新固体形态,有别于成盐的方式。
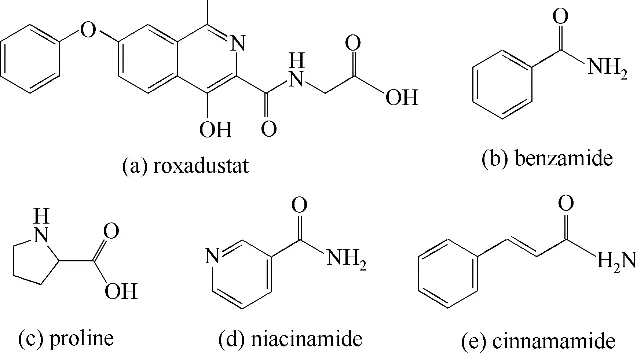
图1 罗沙司他以及CCF的化学结构式Fig.1 Chemical structures of roxadustat(RDXT)and CCF
1 实验材料和方法
1.1 材料
RDXT 购自上海再启生物技术有限公司,纯度≥98%,通过XRD 对原料进行表征,可知原料晶型为晶型A[29]。烟酰胺和苯甲酰胺(aladdin)纯度≥99%,肉桂酰胺(energy chemical)纯度≥97%,脯氨酸(accela)纯度≥98%,所有试剂(西陇化学)均为分析纯,实验用水为去离子水。
1.2 方法
1.2.1 罗沙司他共晶的制备 罗沙司他-烟酰胺共晶(RDXT-N)的制备实验:采用溶液冷却结晶法,40~60℃下将烟酰胺和RDXT溶于丙酮中,CCF和API的投料摩尔比为2∶1,溶清后缓慢降温至0℃,析出固体,养晶后过滤、真空干燥得到罗沙司他-烟酰胺共晶。罗沙司他-肉桂酰胺共晶(RDXT-C)的制备实验:采用溶液混悬结晶法,室温条件下将肉桂酰胺溶于丙酮中,加入RDXT,CCF 和API 的投料摩尔比为2∶1,溶液混悬搅拌2~12 h 过滤、真空干燥得到罗沙司他-肉桂酰胺共晶。罗沙司他-苯甲酰胺共晶(RDXT-B)的制备实验:采用反溶剂溶析结晶法,室温条件下将等物质的量的苯甲酰胺和RDXT溶于良溶剂1,4-二氧六环中,搅拌溶清后,滴加反溶剂正庚烷,有大量固体析出,搅拌2~12 h 过滤、干燥得到罗沙司他-苯甲酰胺共晶。罗沙司他-脯氨酸共晶(RDXT-P)的制备实验:采用反溶剂溶析结晶法,室温条件下将等物质的量的脯氨酸和RDXT溶于甲醇和乙二醇二甲醚的混合溶剂中,溶清后滴加反溶剂正庚烷,有大量固体析出,搅拌2~12 h 后过滤、干燥,得到罗沙司他-脯氨酸共晶。
1.2.2 罗沙司他共晶的表征 四种RDXT 共晶的X射线粉末衍射法(XRD)(Empyrean,PANalytical,荷兰)测试条件为:Cu Kα为光源,电压45 kV,电流40 mA,扫描范围3°~40°,扫描步长0.0168°。差式扫描量热法(DSC)(Q2000,TA Instruments,美国)的测试方法为:在氮气保护下将2~5 mg 样品置于铝坩埚中,测试温度范围为室温~300℃,升温速率为10℃/min。热重分析法(TGA)(Q500,TA Instruments,美国)的测试方法为:在氮气保护下将5~10 mg 样品置于铝坩埚中,测试温度范围为室温~300℃,升温速率为10℃/min。傅里叶红外光谱分析[31](FTIR)(TENSORⅡ,Bruker,德国)采用KBr 压片,扫描范围为4000~400 cm-1。核磁共振氢谱分析法(1H NMR)(AdvanceⅢHD 600,Bruker,瑞士)中样品用氘代DMSO 溶解后进行1H NMR测试。
1.2.3 固有溶出速率测试 API 的固有(特性)溶出速率可以预测潜在的生物利用度问题,本研究参照USP 附录<1087>固有溶出速率的测定方法,分别检测了RDXT 四种共晶和API 在pH 4.5 和pH 6.8 缓冲液中的固有溶出速率并进行对比。实验方法:称取适量粉末置于溶出模具中,用压片机(digital hydraulic press 数显手动液压压片机,PIKE,美国)按压力55 kN 压片、保持30 s,将压制好的片与模具置于溶出杯中,采用桨法,溶出介质900 ml,转速50 r/min,温度(37 ± 0.2)℃,使用在线光纤紫外检测系统(Rainbow,PION,美国)在线实时监测浓度变化[32],全波长200~720 nm 扫描,采样间隔由最初的密集取样20 s、30 s、1 min(0~40 min)逐渐变为5 min(40~100 min)、10 min(100~700 min)、20 min(11~41 h),计算溶出度并绘制溶出曲线。测试完成后,将剩余的样品过滤,干燥。
1.2.4 平衡溶解度测试 本研究借助水浴恒温振荡器(SHZ-B,常州国立)充分溶解RDXT 及其共晶:在离心管中称取过量的样品,加入4.5 ml 水并置于37℃下的恒温振荡器中振摇24 h后取样检测。采用紫外可见分光光度计(Cary 60,Agilent,美国)检测浓度,测定纯水中的平衡溶解度。方法如下:首先扫描得到RDXT 的特征吸收波长为387 nm,在该波长下四种CCF 都无紫外吸收峰。接着在387 nm 波长下利用浓度和吸收强度的关系绘制RDXT溶液的标准曲线,其相关度为99.99%。依据标准曲线和吸光度来计算RDXT和共晶在水中的溶解度。每个样品平行测量2 次取平均值。测试完成后,将剩余的样品过滤,干燥。
1.2.5 影响因素稳定性测试 分别取RDXT 和四种共晶的样品适量,平铺于洁净培养皿中,摊成厚度≤5 mm 的薄层,分别在高温(60±2)℃、高湿((90%±5%)RH)、光照(可见光(4500±500)cm-1,紫外线不低于0.7(W·h)/m2,(25 ± 2)℃,(60% ± 5%)RH)条件下进行影响因素稳定性实验,敞口放置15 d,用XRD检测样品的晶型。
2 实验结果与讨论
2.1 共晶表征与分析
RDXT晶型A和四种共晶产品的XRD表征如图2 所示,谱图中新特征峰的出现可以确认新晶型的形成。图2(a)中RDXT-C 共晶在6.22°±0.2°、10.46°±0.2°、14.57°±0.2°、25.30°±0.2°等处出现新的特征峰,而晶型A 中位于8.41°±0.2°、11.39°±0.2°、16.25°±0.2°、21.56°±0.2°、22.90°±0.2°等的特征峰消失;在图2(b)中 晶 型A 中 位 于11.39°±0.2°、12.83°±0.2°、22.90°±0.2°、25.80°±0.2°等处的特征峰消失,在RDXT-N 共 晶 中 出 现 了6.30°±0.2°、10.90°±0.2°、14.31°±0.2°、20.54°±0.2°等处的新峰;在图2(c)图中晶型A 中位于8.41°±0.2°、11.39°±0.2°、18.90°±0.2°、25.80°±0.2°等处的特征峰消失,在RDXT-B 共晶中出现了6.71°±0.2°、10.64°±0.2°、11.11°±0.2°、18.14°±0.2°、25.32°±0.2°等处的新峰;最后在图2(d)中晶型A 中 位 于8.41°±0.2°、12.83°±0.2°、16.25°±0.2°、22.59°±0.2°、24.66°±0.2°等处的特征峰消失,在RDXT-P 共 晶 中 出 现 了3.63°±0.2°、7.15°±0.2°、10.75°±0.2°、14.31°±0.2°、20.39°±0.2°等处的新峰。
DSC 曲线如图3所示,RDXT 晶型A 的熔融峰峰值温度为223.4℃,四种共晶都只有单一的熔融峰,均低于晶型A的熔点。其中RDXT-C共晶的熔融峰值温度为167.7℃,RDXT-N 共晶为156.2℃,RDXTB共晶为172.7℃,RDXT-P共晶为188.4℃。
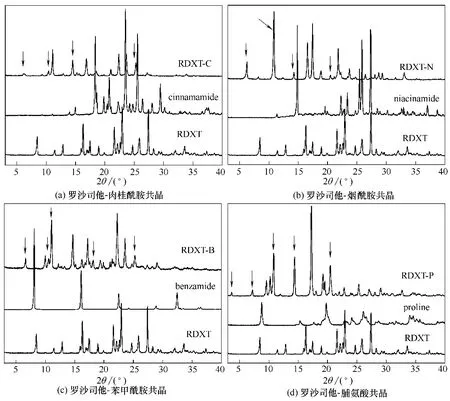
图2 罗沙司他四种共晶的XRD谱图Fig.2 XRD patterns of RDXT co-crystals
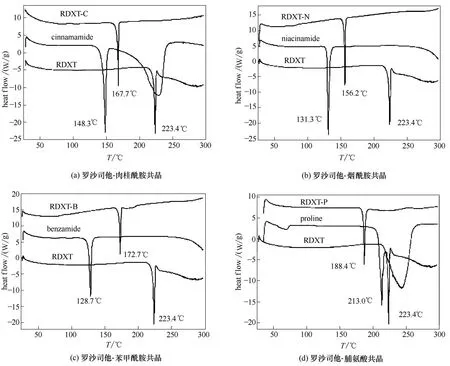
图3 罗沙司他四种共晶的DSC谱图Fig.3 DSC curves of RDXT co-crystals
图4 是共晶的IR 谱图,由图4(a)可以看出,RDXT 位于1728 cm-1羧酸中的C====O 伸缩振动峰在RDXT-C共晶中向较低波数转移,转移至1718 cm-1,肉桂酰胺归属3374 cm-1的N—H 伸缩振动峰,在RDXT-C共晶中向高波数转移,转移到了3400 cm-1,由此推测RDXT 分子是通过氢键C====O…H—N 与肉桂酰胺形成共晶;这种迁移在RDXT-B 共晶[图4(c)]中同样存在,即预测RDXT 分子亦是通过氢键C====O…H—N 与苯甲酰胺形成共晶。在图4(b)中可以看到,RDXT位于1728 cm-1的C====O伸缩振动峰在RDXT-N 共晶中位移不变,而位于1639 cm-1的C====O 振动在共晶中迁移至1590 cm-1,推测出烟酰胺分子中的氨基与RDXT酰胺基团中的羰基形成氢键N—H…O====C,而非羧酸中的羰基形成氢键。图4(d)图中RDXT 位于1728 cm-1的羧基中的C====O 振动峰在RDXT-P 共晶中偏移至低波1712 cm-1处,并且脯氨酸位于3381 cm-1的N—H 伸缩振动峰在RDXT-P 共晶中并无偏移,因此推测出脯氨酸分子中的羟基通过氢键O—H…O====C 与RDXT 形成共晶。
核磁共振氢谱如图5 所示,四个共晶的谱图显示均没有发生质子转移,证明了形成的是共晶而非成盐;通过核磁共振氢谱分析,计算出四个共晶分子中API和CCF的摩尔比均是1∶1。
2.2 固有溶出速率研究
RDXT 及其四种共晶在pH 4.5 和pH 6.8 的缓冲液中的固有溶出速率分别如图6 和图7 所示。从图6 中可以看出,在pH 4.5 缓冲液中,四种共晶的固有溶出速率都比RDXT 晶型A 的大,其中RDXT-C 的溶出速率最大,达到溶出平台后的溶解度将近RDXT 晶型A 的10 倍,其次溶出较快的是RDXT-N和RDXT-B 共晶。从图7 中曲线斜率可以明显看出,在pH 6.8 缓冲液中溶出速率的大小顺序为:RDXT-C 共 晶>RDXT-B 共 晶>RDXT 晶 型A>RDXT-P共晶>RDXT-N共晶。
2.3 平衡溶解度研究
在纯水中37℃条件下溶解度数据如图8 所示,溶解度相对大小为:脯氨酸共晶>肉桂酰胺共晶>烟酰胺共晶>苯甲酰胺共晶>RDXT 晶型A。其中脯氨酸共晶的溶解度最大,为RDXT 晶型A 溶解度的5.3倍;肉桂酰胺共晶的溶解度为RDXT 晶型A 溶解度的5.2 倍;烟酰胺共晶的溶解度是RDXT 晶型A 的4倍;苯甲酰胺共晶的溶解度是RDXT 晶型A 的3.7倍。
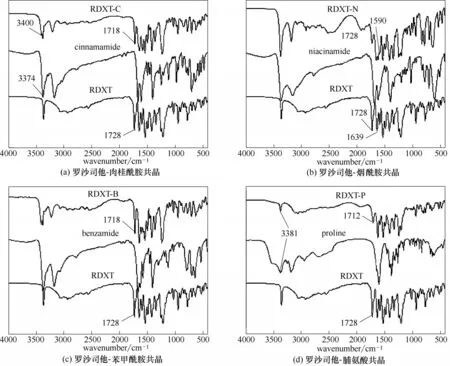
图4 罗沙司他四种共晶的IR谱图Fig.4 Infrared spectra(IR)of RDXT co-crystals
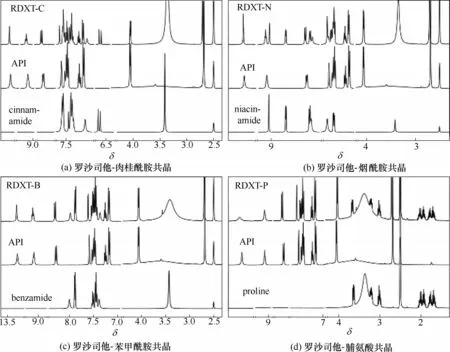
图5 罗沙司他四种共晶的1H NMR谱图Fig.5 1H NMR spectrum of RDXT co-crystals
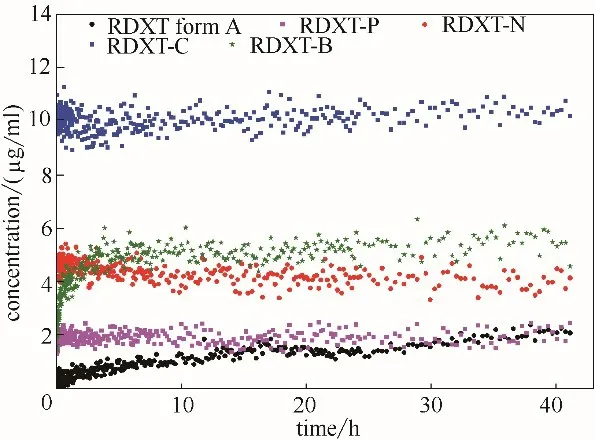
图6 罗沙司他四种共晶和晶型A在pH 4.5缓冲液中的固有溶出曲线Fig.6 Intrinsic dissolution rate of RDXT co-crystals and form A in pH 4.5 buffer
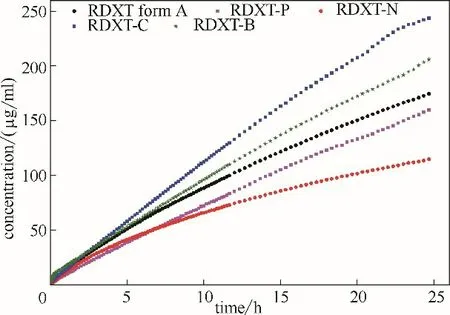
图7 罗沙司他四种共晶和晶型A在pH 6.8缓冲液中的固有溶出曲线Fig.7 Intrinsic dissolution rate of RDXT co-crystals and form A in pH 6.8 buffer
虽然脯氨酸共晶、烟酰胺共晶和苯甲酰胺共晶在达到平衡时都已转化为晶型A,但它们仍具有提高溶解度的效果,其中脯氨酸共晶在这四个共晶中的溶解度最大,这是由于脯氨酸这种CCF 有较好的水溶解性,使得共晶更易与水亲和溶解。在溶液中,固态形式的转变是介稳晶型的溶解和稳定晶型析出的平衡过程,最初的溶解的共晶在达到平衡时不一定全部析出转变为晶型A,所以各个共晶的平衡溶解度也不一定和晶型A 保持一致,本研究的四种共晶都达到了提升溶解度的效果[33]。
2.4 影响因素稳定性研究
在高温(60 ± 2)℃、高湿((90% ± 5%) RH)、光照(可见光(4500 ± 500)cm-1,紫外线不低于0.7 (W·h)/m2,(25 ± 2)℃,(60% ± 5%) RH)条件下放置15 d,其中罗沙司他-肉桂酰胺共晶和烟酰胺共晶的XRD 谱图与0 d 数据无差异,晶型未发生改变。苯甲酰胺共晶在高温条件下5 d后出现晶型A的特征峰,其余条件下晶型均未变化;脯氨酸共晶在高湿条件下转成晶型A,在高温和光照条件下稳定。
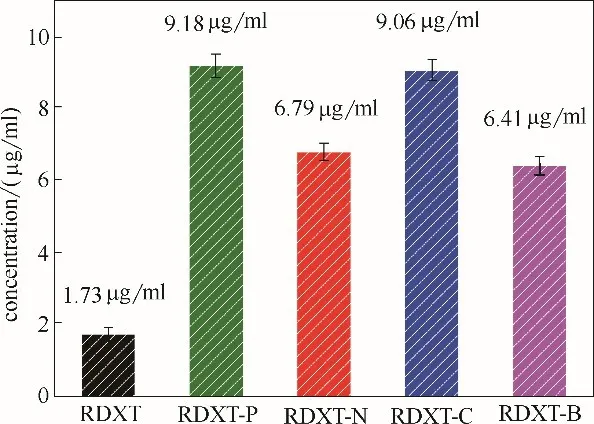
图8 罗沙司他四种共晶和晶型A在纯水中的平衡溶解度(37℃)Fig.8 Solubility of RDXT co-crystals and form A in water at 37℃
3 结 论
(1)通过溶液结晶法制备了罗沙司他-肉桂酰胺、罗沙司他-烟酰胺、罗沙司他-苯甲酰胺和罗沙司他-脯氨酸四种共晶,并通过XRD、DSC、TGA、FTIR和1H NMR的表征确认了共晶的形成。
(2)固有溶出实验证明:在pH 4.5 缓冲液中,四种共晶的固有溶出速率均比晶型A 的溶出速率快,罗沙司他-肉桂酰胺共晶的溶出速率将近晶型A 的10 倍;在pH 6.8 缓冲液中,罗沙司他-肉桂酰胺和罗沙司他-烟酰胺共晶的溶出速率高于晶型A。在纯水中37℃条件下,脯氨酸共晶的溶解度最大,为晶型A 溶解度的5.3 倍,显著提高了罗沙司他的溶解度。
(3)结合影响因素稳定性数据,烟酰胺共晶和肉桂酰胺共晶有着良好的稳定性,在高湿、光照、高温条件下晶型均保持不变。
(4)上述研究结果表明,罗沙司他-肉桂酰胺、罗沙司他-烟酰胺、罗沙司他-苯甲酰胺和罗沙司他-脯氨酸四种共晶能有效地提高溶解度和溶出速率,并且有着良好的稳定性。因此制备出的罗沙司他四个共晶对于新剂型、新药的开发具有重要意义。

