市政脱水污泥生物炭对阿莫西林的吸附研究
贺月莛,杨灿,郭钰,刘亚利
(南京林业大学土木工程学院,江苏南京210037)
阿莫西林属于β-内酰胺类抗生素,被广泛用于临床医学、农业和畜牧业,但其吸收率较低[1]。大量阿莫西林排入水体,会导致水质恶化,甚至会对水生态系统和人类健康构成威胁[2-3]。为此,各种水处理技术被用来去除水中的阿莫西林[4-5]。吸附因具有简单快速、无二次污染等优点,被认为是处理阿莫西林的最佳方法[6]。近年来,为了克服市售活性炭价格高的问题,农业、林业、市政等废弃物被用作生产生物炭的原材料,以实现废水处理和固废资源化利用的双赢[7-9]。
污泥是污水处理厂生物处理工艺不可避免的副产物。据《中国污泥处理处置深度调研与投资战略规划分析报告》统计,预计2020年我国污泥产生量将超7000 万t。传统的污泥处理处置技术(如垃圾填埋场,焚化场和土地施用)会对环境和人类健康造成危害。以污泥为原料制备生物炭,是污泥可持续管理的重要方法。污泥生物炭对磺胺甲恶唑、加替沙星等抗生素具有很好的吸附效果[10-11],但污泥生物炭对阿莫西林的吸附研究相对较少。
本文以市政污水厂的脱水污泥为原料制备生物炭,并采用扫描电镜(SEM)、傅里叶红外光谱(FTIR)等手段对生物炭进行表征。同时,研究不同的投加量、初始浓度、pH、接触时间、温度等条件下,生物炭对阿莫西林的吸附性能,以确定最佳的吸附条件。最后,采用吸附动力学和吸附等温线模型对实验数据进行拟合和分析。
1 材料和方法
1.1 实验材料
本实验所用的脱水污泥取自南京江心洲污水处理厂,其中,挥发性固体(VS)62.01%,灰分37.99%,含水率78.86%,C、H、N的含量分别为26.5%、6.24%和4.08%。将脱水污泥在105℃的GZX-9140MBE型电热鼓风干燥箱中烘干至恒重后,粉碎、筛分,得到粒径小于0.42mm 的粉末,将其储存于封口袋中干燥备用。
1.2 实验试剂和设备
本实验所采用的氯化锌、浓盐酸、阿莫西林、氢氧化钠等化学药品均为分析纯。
GZX-9140MBE型电热鼓风干燥箱,SHA-BA型恒温振荡器,JW-2017HR 型离心机,SX-12-10型箱式电阻炉,PHS-3C型pH计,Vario EL cube型自动元素分析仪,V-Sorb 2800型比表面积及孔径分析仪,QUANTA 200 型SEM显微镜,IR-360 型FTIR 光谱仪。
1.3 活性炭的制备
将污泥粉末置于250 mL 烧杯中,加入5 mol·L-1的ZnCl2溶液,固液比为1∶3。将烧杯置于25℃的恒温振荡器中,100 r·min-1条件下震荡24h。将混合液在4000 r·min-1的离心机中离心3min 后,将沉淀部分于105℃下烘干至恒重。将活化后的污泥放入550℃的箱式电阻炉中热解45min,冷却至室温。用1mol·L-1的HCl溶液对其进行洗涤,并用纯水冲洗至中性后,烘干、粉碎,过0.42mm 筛,得到实验所需的污泥生物炭。
1.4 吸附试验
1.4.1 阿莫西林溶液的配制
取一定量的阿莫西林在100℃下干燥2h 后,称取100mg 溶解于1L 超纯水中,制备成阿莫西林贮备液。
1.4.2 吸附试验
本实验研究了投加量(2.0~8.0 g·L-1)、初始浓度(10~90 mg·L-1)、温度(15~40℃)、pH(2.0~10.0)和接触时间(60~420 min)等参数对吸附效果的影响。温度通过恒温摇床进行控制,pH采用1.0mol·L-1的HCl或NaOH进行调整。
取100 mL 不同浓度的阿莫西林溶液于250 mL锥形瓶中,将不同质量的生物炭加入溶液中,调节pH后置于恒温振荡器中振荡至预定时间后,取样分析阿莫西林的浓度。
1.5 分析方法
挥发性固体、含水率等指标按照《水和废水分析检测方法》(第4 版)进行分析[12]。阿莫西林浓度的分析方法按参考文献[13]进行。pH采用pH计进行测定。C、H、N采用自动元素分析仪进行测定。生物炭的比表面积及孔径采用比表面积及孔径分析仪进行测定。表面形态用SEM显微镜观察。利用FTIR 光谱仪分析表面官能团,波长范围为400cm-1~4200cm-1。
1.6 数据分析
吸附容量q(mg·g-1)和去除率η(%)的计算公式如式(1)和式(2)所示。
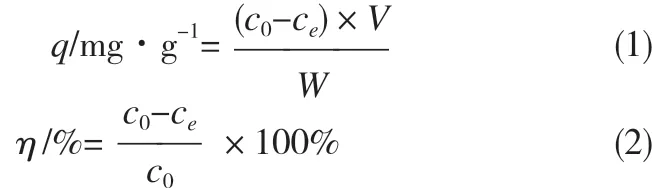
式中:V为阿莫西林溶液体积,L;W为生物炭的投加量,g;C0为阿莫西林的初始浓度,mg·L-1;Ce为吸附平衡时的阿莫西林浓度,mg·L-1。
本研究采用准一级和准二级的动力学模型对阿莫西林的吸附过程进行拟合,其线性计算公式如式(3)和式(4)所示。
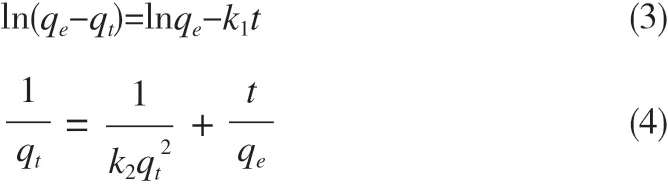
式中:t是吸附时间,min;qt是t时刻的吸附容量,mg·g-1;qe为饱和吸附容量,mg·g-1;k1是准一级动力学吸附常数,min-1;k2是准二级动力学吸附常数,g·(mg·min)-1。
吸附等温线的线性公式如式(5)~式(7)所示:
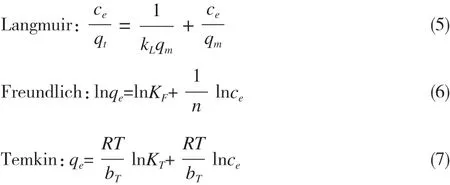
式中:qm为最大吸附量,mg·g-1;KL为Langmuir常数;KF为Freundlich 常数;n为吸附强度特征系数;R为理想气体常数,8.314J·(mol·K)-1;T为绝对温度,K;KT和bT为Temkin常数,其单位分别为L·g-1和J·mol-1。
2 结果与分析
2.1 生物炭的理化性质
2.1.1 生物炭的物理性质
生物炭的比表面积及孔径数据见表1。由表1可见,生物炭的比表面积为35.921 m2·g-1,相应的总孔体积和平均粒径为0.097 cm3·g-1和10.425nm。微孔表面积和体积仅占总比表面积和总孔体积的26.6%和4.1%,说明以脱水污泥为原料制备的活性炭的孔隙不发达。从SEM图(图1)也可以看出,生物炭的表面呈片状和块状结构,表面颗粒和孔隙相对较少。
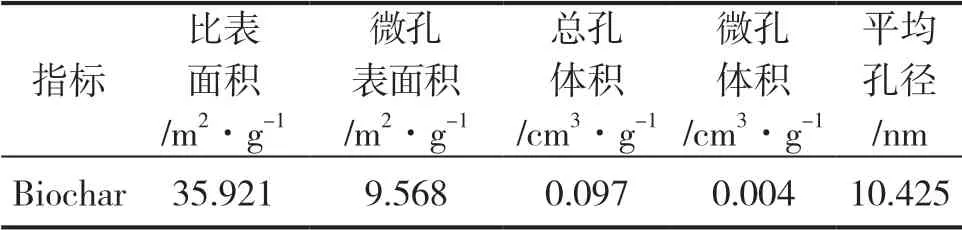
表1生物炭的孔隙结构参数Table 1 Hole structure parameters of biochar

图1生物炭的SEM图Fig.1 SEMimages of biochar
N2吸附脱附等温线如图2 所示。按照IUPAC分类,生物炭的N2吸附脱附等温线属于Ⅱ型,说明氮气吸附脱附过程是单一多层可逆吸附[14]。较低p/p0时的拐点表明,单分子层吸附量达到饱和,而在高p/p0时观察到的滞后环,则说明介孔结构中发生了毛细管凝聚。

图2生物炭的氮气吸附脱附等温线Fig.2 N2 adsorption desorption isotherm of biochar
2.1.2 生物炭的化学性质
众所周知,活性炭的吸附性能受表面官能团(如羧基、羰基、酚羟基和内酯基)的影响[15]。生物炭的FTIR 光谱如图3所示。3550 cm-1~3200cm-1处观察到的宽吸收峰为羧基和苯酚的O-H拉伸振动[16]。1685cm-1处的谱带为C=O键,与羧基和内酯相关[17]。1025cm-1和1383cm-1处的吸收峰分别来自醇和内酯基团的C-O键。此外,465cm-1处的吸收峰代表了C-H的拉伸振动[18]。由此可见,生物炭表面存在大量的含氧官能团,为阿莫西林的吸附提供了更多的结合点位。

图3生物炭的FTIR图谱Fig.3 FTIR curves of the biochar.
2.2 生物炭对阿莫西林的吸附研究
2.2.1 生物炭投加量的影响
在初始阿莫西林浓度为30 mg·L-1、pH=8.0、温度25℃、接触时间4h的条件下,生物炭对阿莫西林的吸附效果如图4 所示。当生物炭的投加量从2.0g·L-1升高到6.0g·L-1时,阿莫西林的去除率从27.22%快速提升至74.66%。继续增加生物炭的投加量未对去除率产生明显影响。去除率的升高归因于活性点位随生物炭的投加量增加而增加[19]。此外,从图4 也可以看出,生物炭的投加量与阿莫西林的吸附容量存在反比关系,吸附能力的下降,主要是高投加量的生物炭导致表面积和活性点位发生了聚集或重叠[20]。
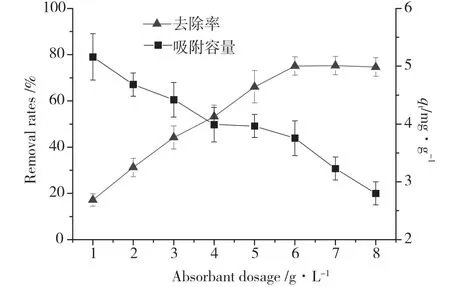
图4 生物炭的投加量对吸附效果的影响Fig.4 Effect of biochar dosage on amoxicillin removal performances
2.2.2 pH的影响
在初始阿莫西林浓度为30 mg·L-1、生物炭的投加量为6.0 g·L-1、温度25℃、接触时间4h的条件下,生物炭对阿莫西林的吸附效果如图5所示。由图5可见,阿莫西林的去除率随pH先升高后降低,最大去除率(75.80%)出现在pH=8时。这可能是因为pH会对生物炭或阿莫西林的表面电荷产生影响,从而改变了生物炭与阿莫西林分子或离子之间的静电作用。酸性条件下,阿莫西林以分子形式存在,与生物炭的吸附作用较强;但在强碱性条件下,阿莫西林的酚羟基和羧基因发生解离而带负电,与生物炭表面的-COOH等官能团相排斥[21]。
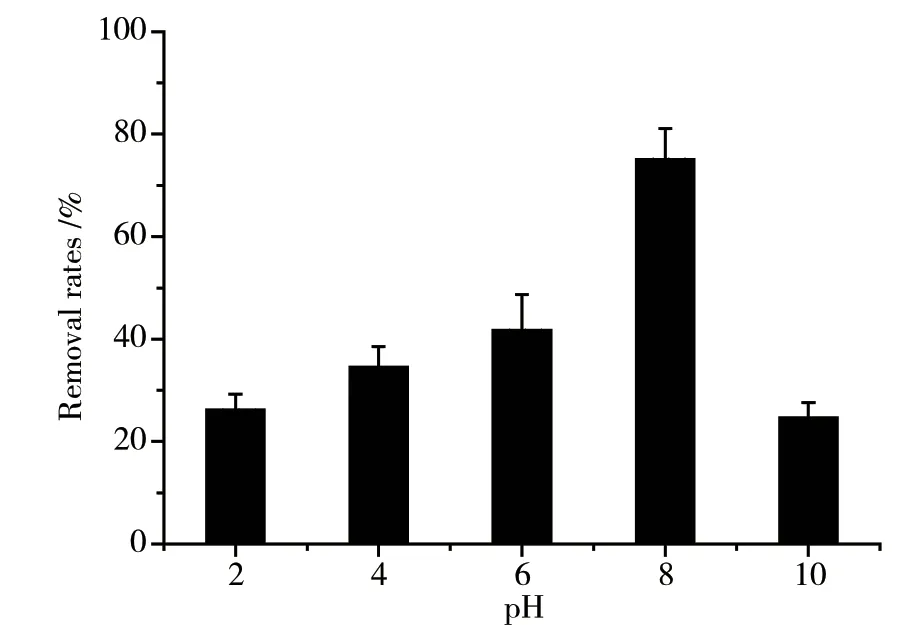
图5 pH 对阿莫西林去除率的影响Fig. 5 Effect of pH on amoxicillin removal rate
2.2.3 接触时间的影响
在初始阿莫西林浓度为30 mg·L-1、生物炭的投加量为6.0g·L-1、温度25℃、pH=8.0 的条件下,阿莫西林去除率随接触时间的变化如图6 所示。在前150 min 内,阿莫西林的去除率从69.7%升高到77.8%,而后维持相对的稳定。其变化趋势可能受两方面因素影响:1)初始阶段,生物炭的表面存在大量的活性点位;2)溶液与生物炭表面的阿莫西林浓度差较高,传质推动力较强。随着时间的推移,生物炭表面的活性点位被占据,吸附浓度梯度逐渐降低。
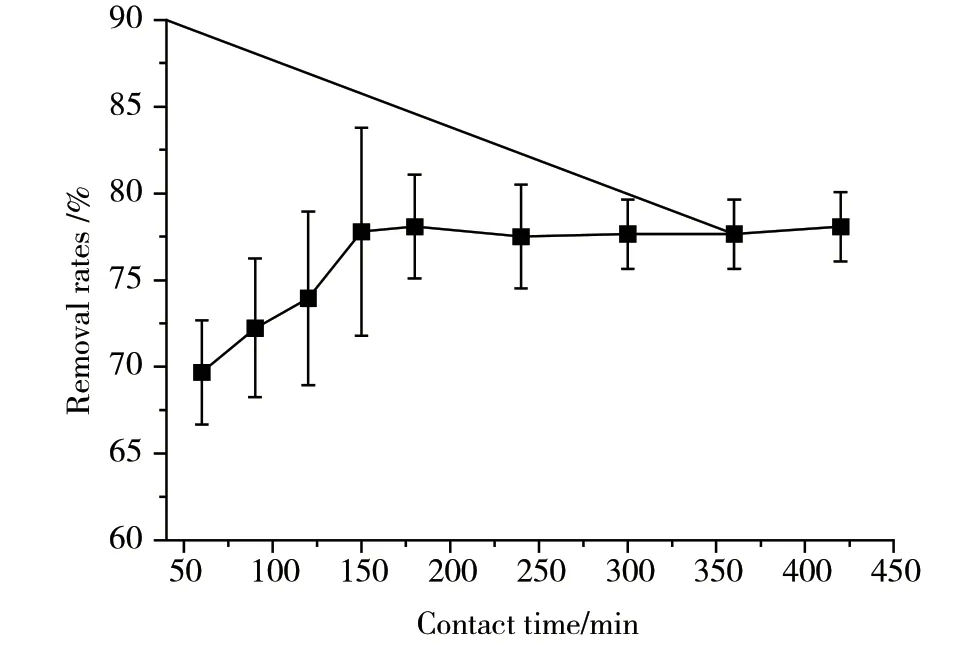
图6接触时间对去除率的影响Fig.6 Effect of contact time on amoxicillin removal.
2.2.4 温度的影响在初始阿莫西林浓度为30 mg·L-1、生物炭的投加量为6.0 g·L-1、pH=8.0、接触时间180 min的条件下,阿莫西林去除率随温度的变化如图7所示。阿莫西林的去除率先快速上升并在25℃时达到最高(78.7%),而后随着温度的进一步升高而下降。这可能是因为低温条件下,阿莫西林的动能较低,其与生物炭的碰撞接触较少;但温度过高时,阿莫西林分子的热运动加剧,超过了生物炭对阿莫西林的静电引力,导致被吸附的阿莫西林分子发生解析,去除率降低。
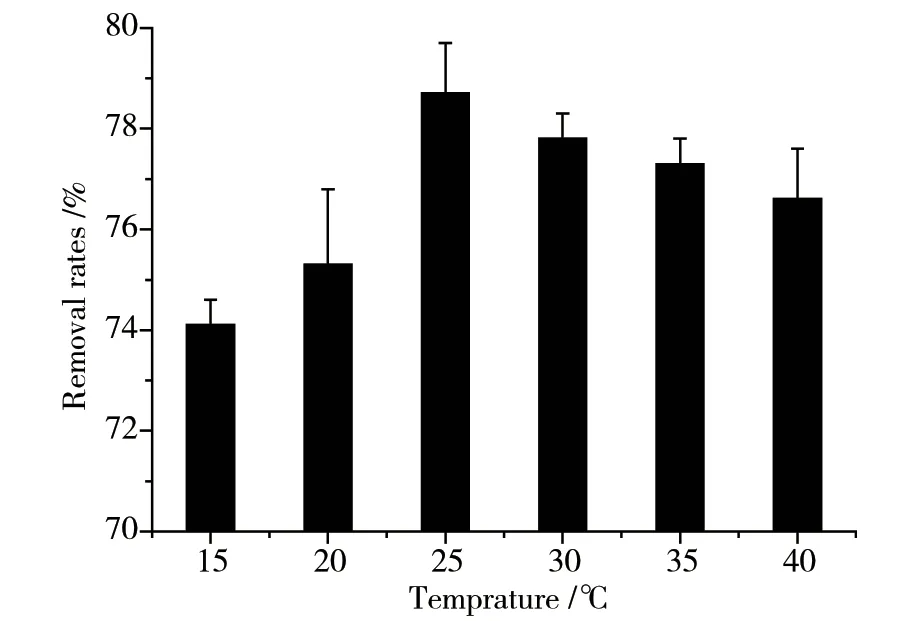
图7温度对阿莫西林去除率的影响Fig.7 Effect of temperature on amoxicillin removal
2.2.5 初始浓度的影响
在生物炭的投加量为6.0 g·L-1、pH=8.0、接触时间180min、温度25℃的条件下,考察初始浓度为10~90mg·L-1时,生物炭对阿莫西林的吸附效率,结果如图8所示。总体来说,生物炭对阿莫西林的去除率,随初始浓度增加,呈现先增加后降低的变化趋势,最大去除率出现在初始浓度30 mg·L-1时。这是因为在生物炭投加量一定的条件下,初始阿莫西林浓度较低时,生物炭的活性点位较多,可实现对阿莫西林的快速单层吸附;随着阿莫西林的不断增加,生物炭表面的活性点位相对减少,且对阿莫西林的吸附由单层吸附转为多层吸附,导致吸附速率逐渐减低。
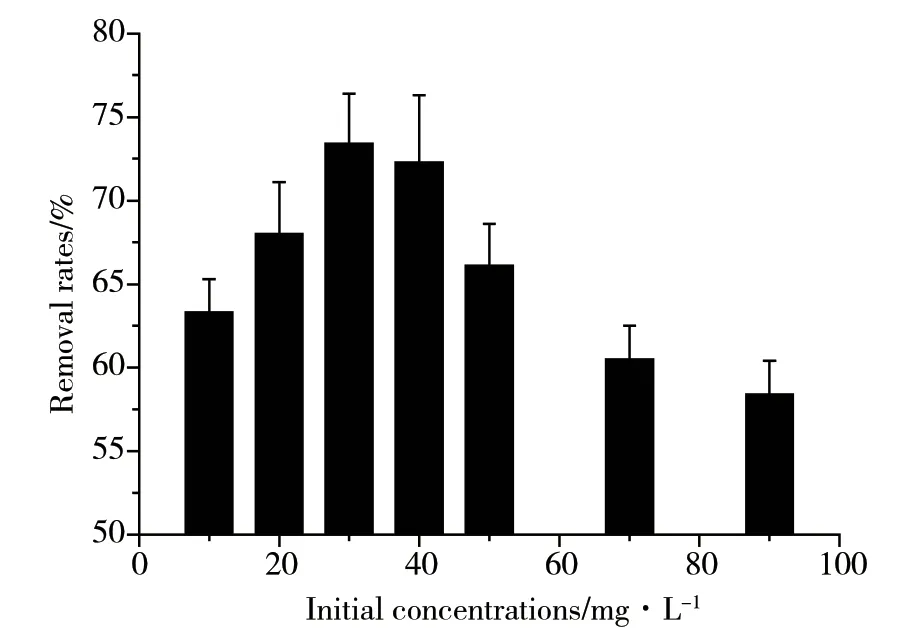
图8初始阿莫西林浓度对去除率的影响Fig.8 Effect of initial amoxicillin concentration on removal rate.
2.3 吸附动力学模型
准一级和准二级动力学模型对实验数据的拟合结果及相关参数如图9和表2 所示。结果表明,准二级动力学模型的相关系数(R2)比准一级模型更高,拟合的qe值更接近实验数据,说明准二级动力学模型更适合于描述生物炭对阿莫西林的吸附过程。此外,准二级动力学模型表明,阿莫西林在生物炭上的吸附以化学吸附为主。

表2生物炭对阿莫西林的吸附动力学参数Table 2 Kinetics parameters for the adsorption of amoxicillin onto surface of biochar.
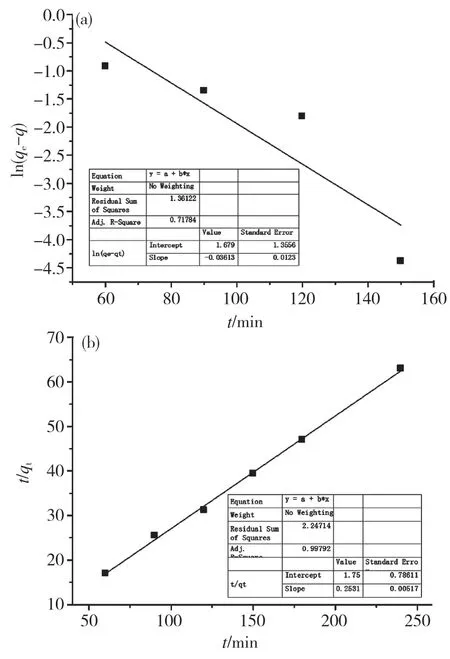
图9动力学模型Fig.9 Kinetics models of amoxicillin onto biaohar (a)pseudo-firstorder and(b)pseudo-second-order.
2.4 吸附等温线模型
实验数据与吸附等温线模型的拟合结果及相应的参数分别如图10和表3所示。由表3可见,3种热力学模型拟合的R2均在0.9以上,说明这3个模型都适合于描述阿莫西林在生物炭上的吸附过程,其中Freundlich 模型比Langmuir 和Temkin 模型的拟合度更高。同时,Freundlich 预测的n值大于1,表明生物炭对阿莫西林的吸附过程属于多层吸附,且可能发生在异质表面上。此外,根据Langmuir 等温线预测的qm为43.29 mg·g-1。
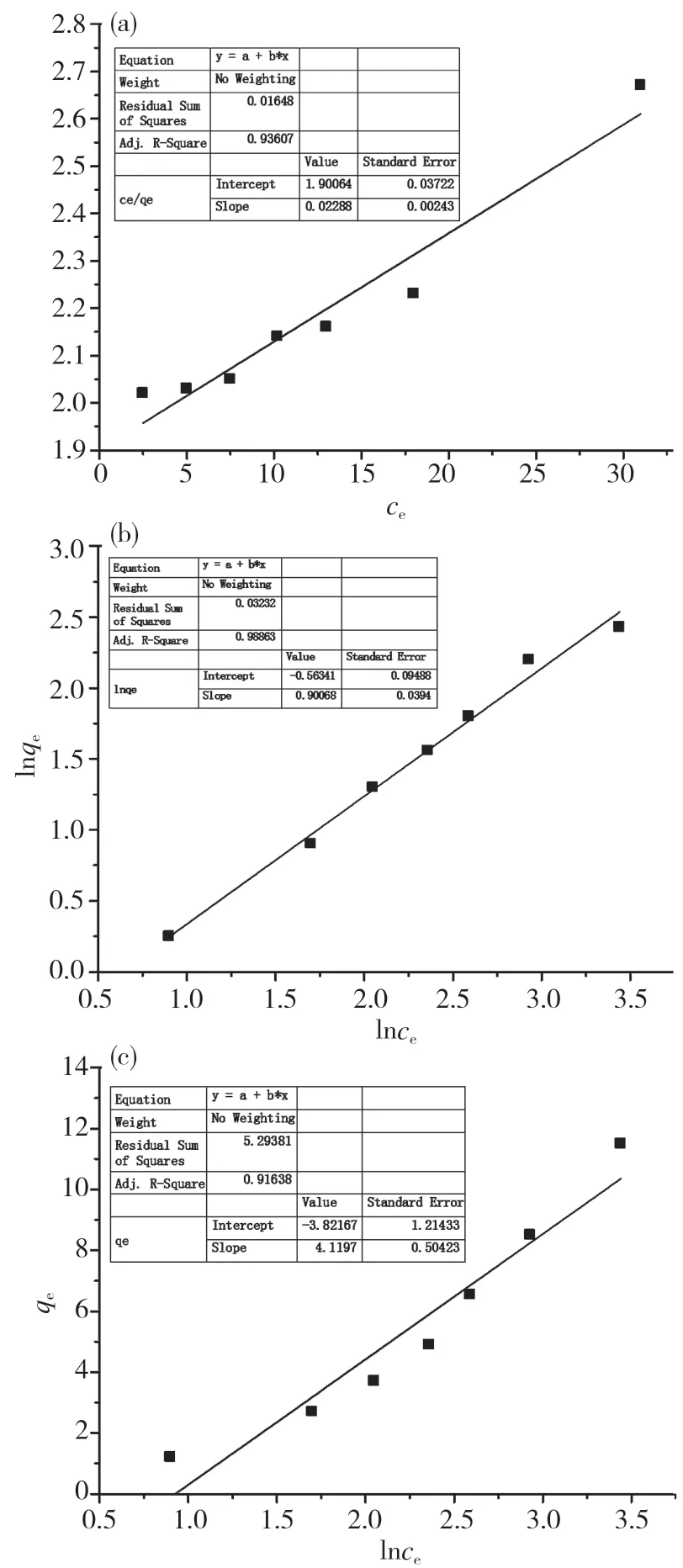
图10吸附等温线模型Fig.10 Adsorption isotherm models of (a) Langmuir isotherm model(b)Freundlich isotherm model (c)Temkin.

表3生物炭对阿莫西林的等温吸附模型参数Table 3 Adsorption isotherms parameters of amoxicillin onto the surface of biochar.
3 结论
生物炭对阿莫西林具有较好的吸附效果,最大去除效率可达到74.66%,最佳的吸附条件为:生物炭的投加量为6.0 g·L-1、阿莫西林初始浓度为30 mg·L-1、pH=8.0、接触时间150 min、温度25℃。生物炭对阿莫西林的吸附实验数据与准二级动力学模型拟合较好,说明生物炭的吸附主要通过化学吸附实现。尽管生物炭的比表面积为35.921m2·g-1,平均粒径为10.425nm,微孔结构发育较差,但其表面含有大量的含氧官能团,为化学吸附提供了大量的活性点位。此外,3种等温线模型均适合于描述阿莫西林在生物炭上的吸附过程,其中Langmuir 等温线预测的qm为43.29 mg·g-1。

